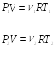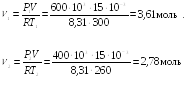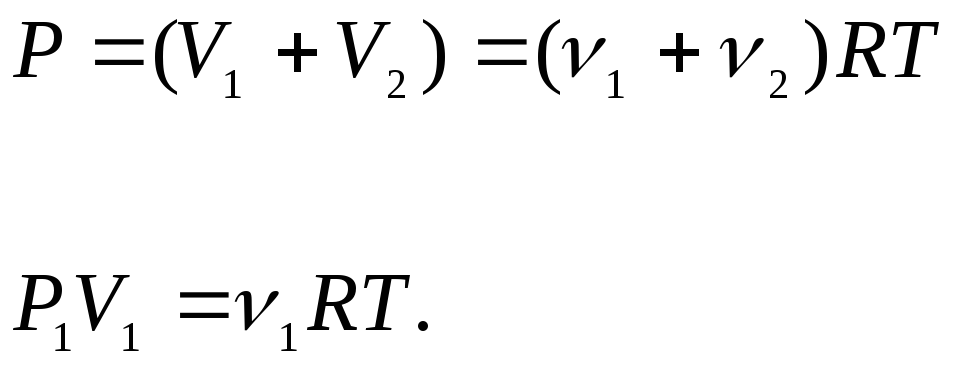- •Курс физики
- •Механика глава 1. Кинематика и динамика частицы § 1. Путь и перемещение
- •§ 2. Скорость и ускорение
- •§ 3. Сила и работа
- •Глава 2. Кинематика и динамика вращения твердого тела § 4. Угловая скорость и угловое ускорение
- •§ 5. Средняя скорость и среднее ускорение
- •§ 6. Момент силы
- •Глава 3. Законы сохранения § 7. Механическая энергия. Закон сохранения механической энергии
- •§ 8. Импульс. Закон сохранения импульса
- •§ 9. Момент импульса. Закон сохранения момента импульса
- •Глава 4. Механические колебания § 10. Гармонические колебания
- •§ 11. Затухающие колебания
- •§ 12. Вынужденные колебания
- •Глава 5. Механические волны § 13. Гармонические волны
- •§ 14. Плоская гармоническая волна
- •Экзаменационные вопросы 1
- •Контрольные задания 1 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Приложение а
- •Молекулярная физика глава 6. Кинетическая теория газов § 15. Уравнение состояния идеального газа
- •§ 16. Внутренняя энергия идеального газа
- •§ 17. Распределение Максвелла
- •§ 18. Барометрическая формула
- •§ 19. Распределение Больцмана
- •§ 20. Явления переноса
- •Глава 7. Термодинамика § 21. Термодинамическая система и термодинамический процесс
- •§ 22. Первый закон термодинамики
- •§ 23. Теплоемкость идеального газа
- •§ 24. Адиабатический процесс
- •§ 25. Энтропия
- •§ 26. Второй и третий законы термодинамики
- •Глава 8. Реальные газы § 27. Силы межмолекулярного взаимодействия в газах
- •§ 28. Агрегатное состояние вещества
- •§ 29. Уравнение Ван-дер-Ваальса
- •§ 30. Внутренняя энергия реального газа
- •Экзаменационные вопросы 2
- •Контрольные задания 2 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Приложение б
- •Электромагнетизм глава 9. Электрическое поле в вакууме § 31. Напряженность поля
- •§ 32. Поток вектора
- •§ 33. Теорема Гаусса для поля вектора
- •§ 34. Циркуляция вектора
- •§ 35. Потенциал поля
- •§ 36. Связь между φ и
- •Глава 10. Электрическое поле в диэлектрике § 37. Диполь в электрическом поле
- •§ 38. Поляризация диэлектрика
- •§ 39. Вектор
- •Глава 11. Энергия электрического поля § 40. Электроемкость
- •§ 41. Электроемкость плоского конденсатора
- •§ 42. Энергия электрического поля
- •Глава 12. Электрический ток § 43. Электрический ток
- •§ 44. Закон Ома для проводника
- •§ 45. Обобщенный закон Ома
- •§ 46. Закон Джоуля – Ленца
- •Глава 13. Магнитное поле в вакууме § 47. Магнитная индукция
- •§ 48. Закон Био – Савара
- •§ 49. Теорема Гаусса для поля вектора
- •§ 50. Теорема о циркуляции вектора
- •§ 51. Магнитное поле в соленоиде
- •§ 52. Закон Ампера
- •Глава 14. Магнитное поле в веществе § 53. Контур с током в магнитном поле
- •§ 54. Намагничивание магнетика
- •§ 55. Вектор
- •Глава 15. Энергия магнитного поля § 56. Индуктивность
- •§ 57. Электромагнитная индукция
- •§ 58. Энергия магнитного поля
- •Глава 16. Электромагнитные волны § 59. Вихревое электрическое поле
- •§ 60. Ток смещения
- •§ 61. Система уравнений Максвелла
- •§ 62. Электромагнитные волны
- •Глава 17. Волновая оптика § 63. Свет
- •§ 64. Интерференция света
- •§ 65. Дифракция света
- •§ 66. Поглощение света
- •§ 67. Рассеяние света
- •§ 68. Поляризация света
- •§ 69. Закон Малюса
- •§ 70. Вращение плоскости поляризации
- •Контрольные задания 3 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Экзаменационные вопросы 3
- •Приложение в
- •Квантовая физика глава 18. Квантовая оптика § 71. Тепловое излучение
- •§ 72. Закон Кирхгофа
- •§ 73. Законы теплового излучения черного тела
- •§ 74. Формула Планка
- •§ 75. Фотоэффект
- •§ 76. Формула Эйнштейна для фотоэффекта
- •§ 77. Фотон
- •§ 78. Эффект Комптона
- •Глава 19. Квантовая механика § 79. Волны де Бройля
- •§ 80. Волновая функция
- •§ 81. Соотношение неопределенностей Гейзенберга
- •§ 82. Уравнение Шредингера
- •§ 83. Микрочастица в потенциальном ящике
- •Глава 20. Атомная физика § 84. Атом водорода
- •§ 85. Излучение и поглощение света атомом водорода
- •§ 86. Пространственное квантование
- •§ 87. Принцип Паули
- •Глава 21. Зонная теория твердых тел § 88. Металлы, полупроводники и диэлектрики
- •§ 89. Электронно-дырочная проводимость полупроводников
- •§ 90. Примесные полупроводники
- •Глава 22. Ядерная физика § 92. Строение атомного ядра
- •§ 93. Энергия связи ядра
- •§ 94. Радиоактивность
- •Контрольные задания 4 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Экзаменационные вопросы 4
- •Приложение г
- •Оглавление
Молекулярная физика глава 6. Кинетическая теория газов § 15. Уравнение состояния идеального газа
Согласно кинетической теории, газ представляет собой большое число молекул, находящихся в непрерывном хаотическом тепловом движении. Свойства газов (например, давление и температура) являются суммарным результатом действия молекул.
Рассмотрим модель идеального газа. Согласно этой модели молекулы газа — это маленькие шарики, суммарный объем которых всегда пренебрежимо мал по сравнению с объемом сосуда, в котором они находятся. Шарики не взаимодействуют между собой на расстоянии, а только непрерывно упруго сталкиваются друг с другом, двигаясь до соудорения прямолинейно и равномерно.
Получим
уравнение состояния идеального газа —
уравнение, связывающее параметры
состояния газа
— давление P,
объем
![]() и температуру
и температуру
![]() (в кельвинах).
(в кельвинах).
Опыт показывает, что при небольших давлениях легкие газы, такие как водород и гелий, с хорошей точностью подчиняются уравнению
![]() (15.1)
(15.1)
называемому
уравнением Клапейрона. Следовательно,
уравнение (15.1) можно считать уравнением
состояния идеального газа. Постоянная
![]() зависит от химического состава и
количества газа.
зависит от химического состава и
количества газа.
Обозначим
через
![]() объема одного моля газа. Подставляя
объема одного моля газа. Подставляя
![]() где
где
![]() —
число молей газа, в уравнение (15.1), имеем
—
число молей газа, в уравнение (15.1), имеем
![]()
откуда
![]()
(15.2)
где
постоянная
![]() не зависит от количества газа. Кроме
того, так как, согласно закону Авогадро,
моли различных газов при одинаковых
давлениях и температурах имеют одинаковый
объем, постоянная
не зависит от количества газа. Кроме
того, так как, согласно закону Авогадро,
моли различных газов при одинаковых
давлениях и температурах имеют одинаковый
объем, постоянная
![]()
(15.3)
не зависит от химического состава газа, т. е. одинакова для всех газов. Поэтому ее принято называть универсальной газовой постоянной.
Найдем
численное значение
![]() .
Известно, что при нормальных условиях
.
Известно, что при нормальных условиях
![]() 1 атм
=
1 атм
=![]() Па,
Па,
![]() =273 К)
объем моля газа
=273 К)
объем моля газа
![]()
![]() Согласно соотношению (15.3)
Согласно соотношению (15.3)
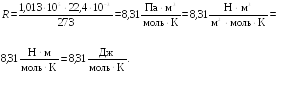
Подставляя
![]() в уравнение (15.1), получаем уравнение
состояния идеального газа
в уравнение (15.1), получаем уравнение
состояния идеального газа
![]()
![]() (15.4)
(15.4)
называемое уравнением Клапейрона – Менделеева.
Пример
15.1. В баллоне
вместимостью
![]() находится аргон под давлением
находится аргон под давлением
![]() и при температуре
и при температуре
![]() Когда из баллона было взято некоторое
количество газа, давление в баллоне
понизилось до
Когда из баллона было взято некоторое
количество газа, давление в баллоне
понизилось до
![]() а температура установилась
а температура установилась
![]() Определить массу
Определить массу
![]() аргона, взятого из баллона.
аргона, взятого из баллона.
|
Дано:
|
Решение
(Масса газа
газа;
.
.
.
|
|
|
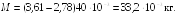
(см. Приложение Б).
Ответ: M = 33,2 г.
Пример
15.2. В баллонах
объемом
![]() и
и
![]() содержится газ. Давление в первом баллоне
содержится газ. Давление в первом баллоне
![]() во втором —
во втором —
![]() Определить давление
Определить давление
![]() после соединение баллонов, если
температура газа осталась прежней.
после соединение баллонов, если
температура газа осталась прежней.
|
Дано:
|
Решение
.
.
.
.
|
|
|
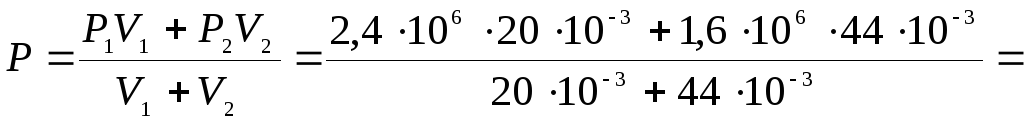
= 1,85·106 Па.
Ответ: P = 1,85·МПа.