- •Бийский технологический институт (филиал)
- •Р.Н. Питеркин, р.Ш. Просвирнин, е.А. Петров технология нитроэфиров и нитроэфирсодержащих промышленных вв
- •Содержание
- •Введение
- •Часть I. Нитроэфиры
- •1 Историческая справка о развитии промышленных способов производства нитроглицерина
- •2 Современные способы производства нитроэфиров
- •2.1 Оптимальные составы кислот и модули нитрации
- •2.2 Инжекторы для осуществления нитрационного
- •2.3 Холодильники для охлаждения эмульсии
- •2.4 Центробежные сепараторы для разделения эмульсии нитроэфир–отработанная кислота
- •2.5 Процесс и оборудование для стабилизации
- •2.6 Весовой дозатор-расходомер нитроэфиров
- •2.7 Насосы для транспортирования отработанных
- •2.8 Технологическая схема производства нитроэфиров в малогабаритном оборудовании
- •3 Вспомогательные стадии процесса производства нитроэфиров
- •3.1 Разложение нитротел в отработанных кислотах
- •3.2 Обезвреживание сточных вод производства
- •3.2.1 Адсорбционный способ обезвреживания
- •3.2.2 Автоклавный способ очистки сточных вод
- •3.2.3 Восстановление нитроэфиров
- •3.2.4 Электрохимический метод обезвреживания
- •3.2.5 Сверхкритическое водное окисление
- •3.3 Приборы для непрерывной оценки качества нитроэфиров
- •I, мA 0,1 % hno3 0,03 % hno3 0,01 % hno3
- •0,2 0,4 0,6 Содержание н2о, %
- •4 Свойства нитроэфиров
- •4.1 Физические свойства нитроэфиров
- •4.2 Взрывчатые свойства нитроэфиров
- •4.3 Поведение нитроэфиров в кислых средах
- •4.3.1 Стойкость кислых нгц, дндэг и их смеси
- •4.3.2 Стойкость кислых динитрата триэтиленгликоля, тринитрата нитроизобутилглицерина и динитрата
- •4.3.3 Влияние воды на стойкость кислых нитроэфиров
- •4.3.4 Влияние серной и азотной кислот
- •4.3.5 Влияние окислов азота
- •4.3.6 Стойкость нгц и дндэг с пониженной
- •4.3.7 Механизм разложения кислых нитроэфиров
- •4.3.8 Разложение нитроэфиров в отработанных
- •4.3.9 Разложение нитротел в слабых отработанных кислотах
- •4.4 Реакции нитроэфиров с основаниями
- •4.4.1 Гидролиз нитроглицерина
- •4.4.2 Гидролиз динитрата этиленгликоля (днэг)
- •4.4.3 Гидролиз динитрата диэтиленгликоля (дндэг)
- •4.5 Причины аварий на производствах нитроэфиров
- •Литература
- •Часть II. Нитроэфирсодержащие взрывчатые вещества
- •5 Технология производства нитроэфирсодержащих взрывчатых веществ
- •5.1 Современные направления развития
- •5.2 Разработка технологии и создание
- •Фаза подготовки компонентов
- •Фаза конечных операций
- •5.3 Автоматизация производства
- •5.4 Экологическая защита производства
- •5.4.1 Разработка эффективных методов
- •5.4.2 Технико-экономические показатели производства
- •6 Оптимизация и модернизация штатных рецептур нитроэфирсодержащих вв
- •6.1 Оптимизация угленита э-6
- •6.2 Исследование предохранительных свойств
- •6.3 Разработка и исследование угленита м – новой рецептуры вв V класса [15]
- •6.4 Модернизация детонита м
- •6.4.1 Разработка рецептуры модернизированного
- •6.4.2 Отработка технологии модернизированного
- •6.4.3 Промышленные испытания модернизированных детонитов [24]
- •7 Некоторые аспекты безопасности нитроэфирсодержащих вв
- •7.1 О химической стабильности и предельных сроках хранения нитроэфирсодержащих промышленных вв
- •7.2 О чувствительности нитроэфирсодержащих
- •7.3 О физической стабильности
- •Литература
- •Сокращения и обозначения
4.3.8 Разложение нитроэфиров в отработанных
кислотах
4.3.8.1 Разложение НГЦ в крепких отработанных кислотах
Состав отработанных кислот и их стойкость представлены в таблице 4.17. За показатель стойкости принимали время хранения до возрастания содержания окислов азота до 1 %.
Нитротела, растворённые в отработанных кислотах, содержат кроме нитроэфиров продукты их переэтерификации, гидролиза и окисления.
Концентрацию нитротел определяли методом окисления органических веществ бихроматом калия [52]. Для определения нитроэфиров автор работы использовал метод восстановления нитратных групп солями двухвалентного железа [52].
Таблица 4.17 – Состав отработанных кислот при получении НГЦ и их стойкость при 19–21 °C
|
Номер |
Состав отработанных кислот, % |
Состав нитроэфиров в нитротелах, % |
Стойкость кислоты в сутках | ||||||
|
HNO3 |
H2SO4 |
N2O4 |
нитротела |
нитроэфиры |
НГЦ |
ДНГ |
МНГ | ||
|
1 2 3 4 5 6 7 8 |
6,7 8,4 9,42 10,65 11,8 12,42 12,69 16,20 |
72,5 71,4 68,96 72,51 70,8 70,78 71,02 69,20 |
0,22 0,19 0,21 0,27 0,20 0,20 0,19 0,22 |
4,32 3,52 3,80 3,23 2,69 2,40 2,85 3,15 |
0,73 0,84 0,92 0,90 1,17 1,10 1,28 1,56 |
10 10 10 20 25 30 35 40 |
10 20 25 15 30 25 15 15 |
10 10 10 следы следы следы отсутст. отсутст. |
58 67 53 185 160 193 220 261 |
Состав нитроэфиров в нитротелах определялся методом тонкослойной хроматографии.
С ростом содержания азотной кислоты количество нитротел в отработанной кислоте снижается, а доля НГЦ в них возрастает. Кроме нитратов глицерина, в нитротелах содержатся смешанные сульфонитроэфиры различного состава. Их содержание снижается с повышением концентрации азотной кислоты и воды в отработанной кислоте.
Оптимальными отработанными кислотами при нитровании глицерина являются кислоты, содержащие 11–14 % HNO3 при мольном соотношении H2O:H2SO4 (1,1–1,2):1. В них содержится меньшее количество нитротел, и в нитротелах количество НГЦ максимальное. Стойкость таких отработанных кислот очень высокая.
Разложение нитротел в отработанных кислотах имеет автокаталитический характер. Сначала разложение идёт очень медленно без ускорения (индукционный период), после накопления около 1 % окислов азота процесс резко ускоряется и заканчивается полным окислением нитротел.
Содержание азотной кислоты снижается пропорционально росту содержания окислов азота. В кислотах с низким содержанием азотной кислоты последняя к концу разложения расходуется полностью на окислительные процессы. Количество серной кислоты несколько возрастает из-за снижения общего количества кислотной смеси вследствие улетучивания газообразных продуктов.
Рабочие нитрующие смеси в инжекторном способе нитрования глицерина представляют собой смеси свежей и отработанной кислоты с соотношением 1:1,2. Их стойкость значительно выше. Они без заметного разложения могут храниться более года. В них нитротела содержат в основном НГЦ, что подтверждается близкими результатами анализа бихроматным методом и методом восстановления сернокислым закисным железом.
Как и в кислых нитроэфирах в отработанных кислотах органические продукты окисляются окислами азота, постоянно регенерируемыми азотной кислотой. Отличительная особенность – отсутствие в продуктах разложения органических кислот.
Аналогичные по составу отработанные кислоты образуются при нитровании этиленгликоля и нитроизобутилглицерина. Они также отличаются высокой стойкостью (более 2-х месяцев).
4.3.8.2 Разложение ДНДЭГ в отработанных кислотах
В таблице 4.18 приведены составы отработанных кислот при получении ДНДЭГ и их стойкость.
Аналогично, как и у НГЦ, с ростом содержания HNO3 в отработанной кислоте снижается количество нитротел и возрастает содержание ДНДЭГ в нитротелах.
Стойкость кислот также возрастает, хотя она измеряется всего лишь в часах, а не в сутках. При введении в исходный диэтиленгликоль мочевины, удаляющей из кислот окислы азота, их стойкость резко возрастает.
Изменение содержания нитротел и ДНДЭГ при хранении отработанных кислот состава, отвечающего № 1, 4 и 5 в табли-це 4.18, представлено на рисунке 4.7.
Рисунок 4.7– Изменение содержания нитротел,
нитроэфиров и окислов азота в отработанных кислотах с ДНДЭГ: 1, 4, 5 – нитротела, 1’, 4’, 5 ’– нитроэфиры,
1”, 4”, 5” – окислы азота
Таблица 4.18 – Составы отработанных кислот и нитротел в производстве ДНДЭГ,
их стойкость при 18–20 °C
|
Номер |
Состав отработанных кислот, % |
Содержание в нитротелах, % |
Стойкость отработанной кислоты, часы–минуты | |||||
|
HNO3 |
H2SO4 |
N2O4 |
нитротела |
нитроэфиры |
ДНДЭГ |
МНДЭГ | ||
|
1 2 3 4 5 6 7 8 9 10 |
7,66 8,46 9,42 11,03 12,7 14,4 19,23 12,1 13,0 14,2 |
62,7 61,04 61,61 63,00 62,5 59,48 59,44 59,27 54,5 60,06 |
0,61 0,14 0,2 0,48 0,18 0,16 0,6 отс. отс. 0,2 |
7,8 7,56 6,47 6,3 6,35 5,54 5,6 5,45 6,1 5,35 |
2,38 - 3,25 3,46 4,0 4,2 5,34 - 2,57 - |
30 - 50 55 60 75 35 - 40 - |
20 - 20 5 отс. 5 отс. - 45 - |
2–05 3–45 7–35 3–15 9–15 11–40 70 52 * 49 * 92 ** |
|
* В ДЭГ 0,5 % мочевины ** В ДЭГ 0,7 % мочевины | ||||||||
Снижение содержания нитротел и нитроэфиров в их составе, за исключением начального периода, по времени совпадает с ростом содержания N2O4. Снижение содержания нитроэфиров в начальный период объясняется сульфированием ДНДЭГ. Равновесие между сульфо- и нитроэфирами достигается примерно в течение часа после окончания нитрации, далее идёт период медленного разложения нитротел, который переходит в автокаталитическое и заканчивается полным разложением нитротел.
Низкая стойкость отработанных кислот при получении ДНДЭГ по сравнению с кислотами при получении НГЦ связана не только с повышенным содержанием воды и нитротел, но и более лёгкой окисляемостью молекулы диэтиленгликоля и его эфиров. Органические кислоты в продуктах разложения не обнаружены.
Отработанные кислоты с производства ДНТЭГ ведут себя подобным же образом, но их стойкость ещё ниже из-за большей растворимости нитротел. 1 % мочевины в триэтиленгликоле способствует повышению стойкости до 8–24 часов.
Рабочие нитрующие смеси в инжекторном способе производства ДНДЭГ готовят смешением 4,5–5 массовых частей отработанной кислоты и 2,9–3,1 частей свежей нитросмеси. Они содержат 31–34 % HNO3, 4951 % H2SO4 и 3–4 % нитротел (в них 80–95 % ДНДЭГ). Их стойкость выше, чем стойкость отработанных кислот, но недостаточна для хранения в производственных условиях. Поэтому для повышения стойкости рекомендуется в диэтиленгликоль перед его нитрованием вводить до 2 % мочевины. Срок годности таких кислот (содержание окислов азота не более 0,3 %) составляет от 10 до 25 суток.
Отработанные кислоты при получении смесей НГЦ и ДНДЭГ нитрованием смесей глицерина и диэтиленгликоля с соотношением 58:42 и 43:57 содержат до 10–14 % HNO3, 65–67 % H2SO4 и до 4,5 % нитротел. Они имеют стойкость 5–10 суток. В инжекторном способе получения смесевого нитроэфира рекомендуется вводить в исходные спирты до 1 % мочевины.
На основании представленного экспериментального материала предложена следующая схема разложения нитроэфиров в отработанных кислотах.
О
,
кисление продуктов неполной нитрации и переэтерификации до альдегидов:
![]()
где X=H, NO, SO3H.
Гидратация альдегидов с образованием производных метиленгликоля и их нитритов:
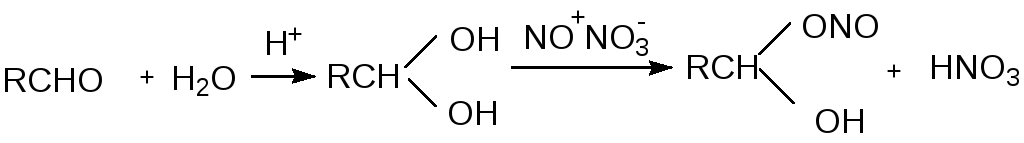
Нитриты могут образовываться также по реакциям:
![]()
Разложение нитрита
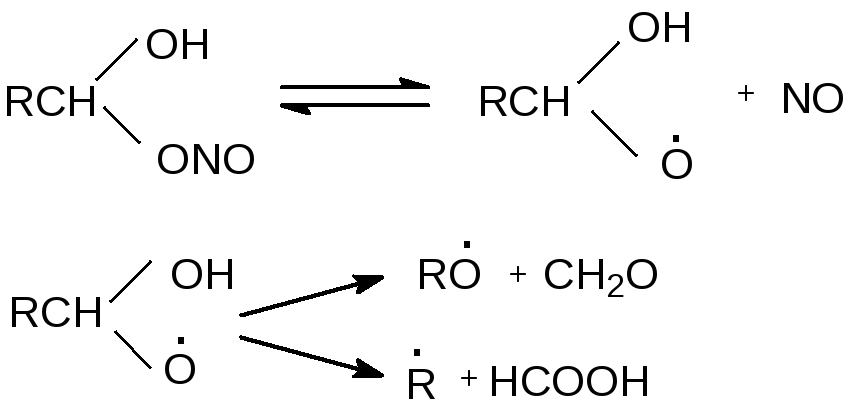
Радикалы
![]() и
и![]() разлагаются в зависимости от строения
исходного нитроэфира.
разлагаются в зависимости от строения
исходного нитроэфира.
Для
ДНЭГ: 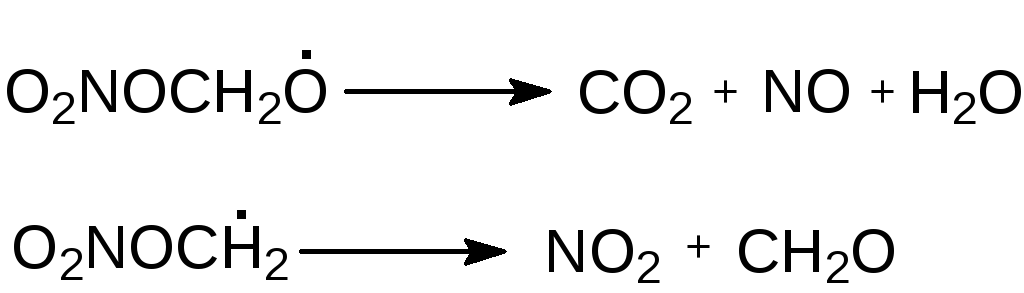
Для НГЦ:
Для ДНДЭГ: