
- •Бийский технологический институт (филиал)
- •Р.Н. Питеркин, р.Ш. Просвирнин, е.А. Петров технология нитроэфиров и нитроэфирсодержащих промышленных вв
- •Содержание
- •Введение
- •Часть I. Нитроэфиры
- •1 Историческая справка о развитии промышленных способов производства нитроглицерина
- •2 Современные способы производства нитроэфиров
- •2.1 Оптимальные составы кислот и модули нитрации
- •2.2 Инжекторы для осуществления нитрационного
- •2.3 Холодильники для охлаждения эмульсии
- •2.4 Центробежные сепараторы для разделения эмульсии нитроэфир–отработанная кислота
- •2.5 Процесс и оборудование для стабилизации
- •2.6 Весовой дозатор-расходомер нитроэфиров
- •2.7 Насосы для транспортирования отработанных
- •2.8 Технологическая схема производства нитроэфиров в малогабаритном оборудовании
- •3 Вспомогательные стадии процесса производства нитроэфиров
- •3.1 Разложение нитротел в отработанных кислотах
- •3.2 Обезвреживание сточных вод производства
- •3.2.1 Адсорбционный способ обезвреживания
- •3.2.2 Автоклавный способ очистки сточных вод
- •3.2.3 Восстановление нитроэфиров
- •3.2.4 Электрохимический метод обезвреживания
- •3.2.5 Сверхкритическое водное окисление
- •3.3 Приборы для непрерывной оценки качества нитроэфиров
- •I, мA 0,1 % hno3 0,03 % hno3 0,01 % hno3
- •0,2 0,4 0,6 Содержание н2о, %
- •4 Свойства нитроэфиров
- •4.1 Физические свойства нитроэфиров
- •4.2 Взрывчатые свойства нитроэфиров
- •4.3 Поведение нитроэфиров в кислых средах
- •4.3.1 Стойкость кислых нгц, дндэг и их смеси
- •4.3.2 Стойкость кислых динитрата триэтиленгликоля, тринитрата нитроизобутилглицерина и динитрата
- •4.3.3 Влияние воды на стойкость кислых нитроэфиров
- •4.3.4 Влияние серной и азотной кислот
- •4.3.5 Влияние окислов азота
- •4.3.6 Стойкость нгц и дндэг с пониженной
- •4.3.7 Механизм разложения кислых нитроэфиров
- •4.3.8 Разложение нитроэфиров в отработанных
- •4.3.9 Разложение нитротел в слабых отработанных кислотах
- •4.4 Реакции нитроэфиров с основаниями
- •4.4.1 Гидролиз нитроглицерина
- •4.4.2 Гидролиз динитрата этиленгликоля (днэг)
- •4.4.3 Гидролиз динитрата диэтиленгликоля (дндэг)
- •4.5 Причины аварий на производствах нитроэфиров
- •Литература
- •Часть II. Нитроэфирсодержащие взрывчатые вещества
- •5 Технология производства нитроэфирсодержащих взрывчатых веществ
- •5.1 Современные направления развития
- •5.2 Разработка технологии и создание
- •Фаза подготовки компонентов
- •Фаза конечных операций
- •5.3 Автоматизация производства
- •5.4 Экологическая защита производства
- •5.4.1 Разработка эффективных методов
- •5.4.2 Технико-экономические показатели производства
- •6 Оптимизация и модернизация штатных рецептур нитроэфирсодержащих вв
- •6.1 Оптимизация угленита э-6
- •6.2 Исследование предохранительных свойств
- •6.3 Разработка и исследование угленита м – новой рецептуры вв V класса [15]
- •6.4 Модернизация детонита м
- •6.4.1 Разработка рецептуры модернизированного
- •6.4.2 Отработка технологии модернизированного
- •6.4.3 Промышленные испытания модернизированных детонитов [24]
- •7 Некоторые аспекты безопасности нитроэфирсодержащих вв
- •7.1 О химической стабильности и предельных сроках хранения нитроэфирсодержащих промышленных вв
- •7.2 О чувствительности нитроэфирсодержащих
- •7.3 О физической стабильности
- •Литература
- •Сокращения и обозначения
4.3.6 Стойкость нгц и дндэг с пониженной
кислотностью
Такие нитроэфиры образуются при бессепарационном способе производства, когда нитроэмульсия разбавляется водой и только после этого разделяется, и в сепарационном способе производства после промывки кислого нитроэфира водой.
Нитроэфиры после разбавления нитромассы водой содержат не более 1 % кислот и до 1 % воды (в том числе 0,7–0,9 % заэмульгированной). Стойкость таких кислых нитроэфиров составляет 15–20 суток, а стойкость ДНДЭГ достигает даже 30 суток, что связано с малой склонностью его к гидролизу.
Нитроэфиры после промывки водой содержали около 0,1 % азотной кислоты и хранились без повышения содержания окислов азота в течение двух месяцев.
4.3.7 Механизм разложения кислых нитроэфиров
4.3.7.1 Разложение нитроглицерина
Изменение состава кислого НГЦ при длительном хранении представлено на рисунке 4.5. Содержание свободной серной кислоты в течение 2-х часов снижается почти в три раза из-за её расходования на образование сульфоэфиров. После установления равновесия между нитро- и сульфоэфирами идёт медленное разложение нитроэфира, что отражается ростом содержания окислов азота. Затем содержание нитроэфиров и азотной кислоты начинает снижаться.
%
своб. Н2SO4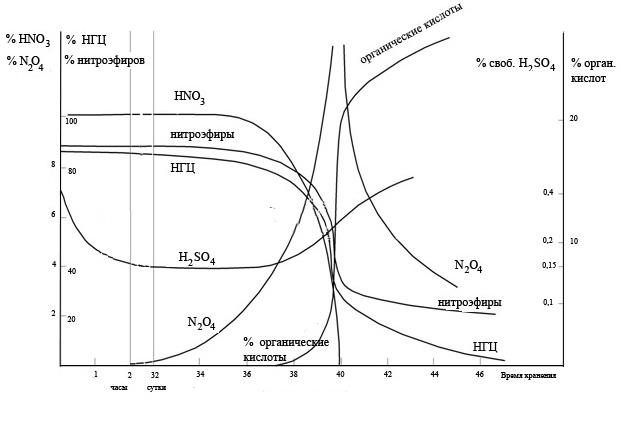
Рисунок 4.5 – Изменение состава кислого НГЦ при храненииПри достижении концентрации окислов азота около 0,1 % процесс принимает автокаталитический характер и резко ускоряется. Это ускорение продолжается до полного израсходования азотной кислоты. Содержание нитроэфиров (НГЦ+динитрат глицерина) падает от 90 до 30–40 %, содержание окислов азота повышается до 25–30 %, органических кислот до 20 %, содержание НГЦ снижается до 20 %. Органические кислоты содержат в основном глицериновую и гликолевую кислоты, в разлагающемся НГЦ содержатся также альдегиды и кетоны (нитраты глицеринового альдегида и диоксиацетона), которые далее выделяют углекислый газ, а также труднорастворимые NO и N2O3.
В конце автокаталитического разложения окраска кислого НГЦ изменяется от красно-бурого до тёмно-зелёного цвета (совместное присутствие N2O3 и N2O4). Снижение концентрации нитроэфиров и рост концентрации органических кислот замедляются. Общее содержание N2O4 и N2O3 снижается. Зелёная окраска постепенно переходит в синюю, что указывает на снижение количества N2O4 в этой смеси. В кислом продукте появляются кристаллы щавелевой кислоты, одного из конечных продуктов разложения НГЦ. При снижении концентрации окислов азота, которые находятся в виде N2O3, замедляется также снижение концентрации нитроэфиров, а концентрация НГЦ снижается быстрее из-за его гидролиза до α,β- и α,γ-ДНГ, частично до мононитрата глицерина.
Через 3–5 месяцев нитроэфиры постепенно исчезают. Из 1 моль НГЦ образуется, в конечном счёте, 0,5–0,7 моль щавелевой кислоты. Остаётся также небольшое количество недоокисленных органических альдегидов и кислот, которые при добавлении азотной кислоты окисляются до щавелевой кислоты и углекислого газа. От общей массы исходного кислого НГЦ остаётся 45 %, остальные 55 % газообразные продукты.
На начальных стадиях разложения определяющим является окисление спиртовой и сульфоэфирной групп четырёхокисью азота N2O4 до альдегидов:
![]()
Азотная кислота окисляет низшие окислы до N2O4, поставляя таким способом кислород для окисления:
![]()
При достаточном количестве N2O4 могут образовываться нитриты, которые легко гидролизуются и окисляются.
![]()
После израсходования свободной азотной кислоты содержание N2O4 начинает снижаться и процесс разложения замедляется. В составе окислов азота возрастает доля N2O3, которая интенсивно окисляет альдегиды до кислот:
![]()
Нитроглицерин сначала гидролизуется до динитратов глицерина, окисление спиртовых групп которых приводит к образованию динитратов глицеринового альдегида и диоксиацетона, которые с более высокими скоростями окисляются далее с образованием в конечном итоге щавелевой кислоты:
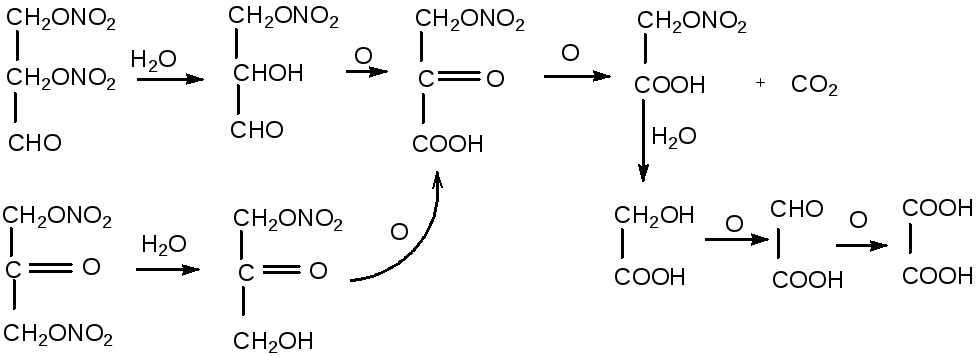
Приведённая схема не исключает возможность протекания других реакций, например, через образование нитритов. В пользу данной схемы говорят результаты исследования процессов разложения нитратов глицеринового альдегида, глицериновой и гликолевой кислот в среде азотной кислоты. В продуктах разложения обнаружены нитрат гликолевой кислоты, а в конце разложения выделена щавелевая кислота с выходом 50 % от теоретического.
Разложение кислых динитрата этиленгликоля и тринитрата нитроизобутилглицерина происходит аналогично разложению кислого НГЦ. Конечным продуктом разложения является щавелевая кислота, её выход составляет 1 моль на 1 моль нитроэфира.
4.3.7.2 Разложение динитрата диэтиленгликоля
Изменение состава кислого ДНДЭГ при хранении представлено на рисунке 4.6.
Р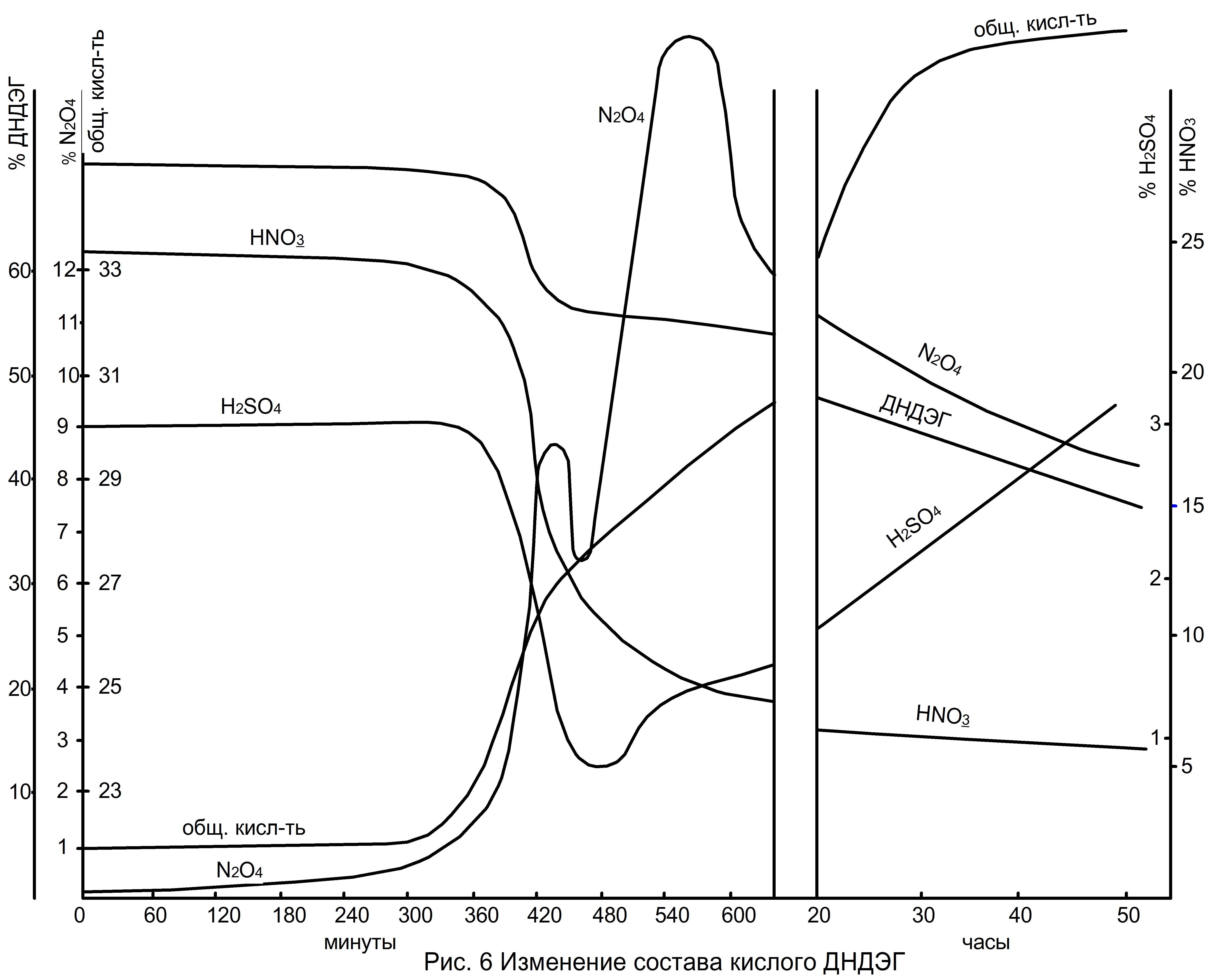 исунок
4.6 – Изменение состава кислого ДНЭГ
исунок
4.6 – Изменение состава кислого ДНЭГ
Процесс его разложения отличается по сравнению с НГЦ, ДНЭГ и НИБГТН. Во-первых, в первое время не снижается содержание серной кислоты, так как из-за большей склонности к сульфированию равновесие между нитро- и сульфо-эфирами достигается в процессе нитрации и сепарации при получении ДНДЭГ (15–20 мин). Во-вторых, при автокаталитическом разложении ДНДЭГ обнаруживаются только следы альдегидов, а количество мононитрата не превышает 10 % от ДНДЭГ. К концу автокаталитического разложения в ДНДЭГ содержится около 15 % нитрата диэтиленгликолевой кислоты (НДК) O2NOCH2CH2OCH2COOH, которая была выделена в виде натриевой соли и идентифицирована по ИК-спектру и по кислотности.
Содержание ДНДЭГ снижается от 70 до 55 %, азотная кислота расходуется примерно до 50 % от её исходного содержания. Далее процесс окисления замедляется.
Из-за выделения воды при окислении ДНДЭГ фактическая концентрация азотной кислоты снижается до 60 % и ниже и её окислительная способность также падает. Как и в случае с НГЦ окислы азота находятся в основном в виде N2O3. Из-за перехода N2O4 в N2O3 концентрация окислов азота несколько снижается, а затем наступает резкий рост из-за окисления промежуточных продуктов разложения ДНДЭГ.
Предположительно здесь играет роль образование нитритов и их окисление до кислоты:
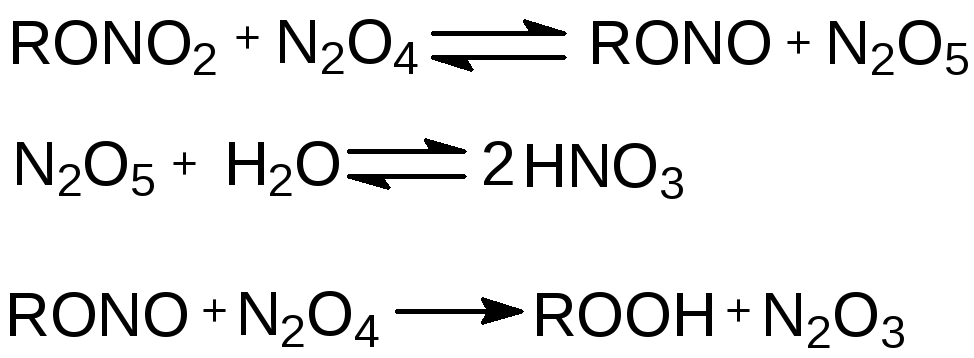
Содержание свободной серной кислоты падает до 1 % из-за сульфирования органических веществ, затем снова возрастает при разложении сульфированных продуктов.
Разложение ДНДЭГ после автокатализа продолжается и через несколько суток начинают выделяться кристаллы дигликолевой кислоты. Содержание окислов азота за это время медленно снижается, альдегиды до конца разложения не обнаруживаются. Через 2–3 месяца практически весь ДНДЭГ превращается в дигликолевую кислоту, углекислый газ почти не выделяется, щавелевой кислоты образуется около 0,5 %, её источником может быть этиленгликоль в исходном диэтиленгликоле.
Аналогично ДНДЭГ разлагается кислый ДНТЭГ до тригликолевой кислоты HOOCCH2OCH2CH2OCH2COOH, около 2 % обнаружено щавелевой и дигликолевой кислот.
Вышеописанные факты указывают на то, что в индукционный период идут реакции окисления мононитрата диэтиленгликоля (МНДЭГ), сульфо- и нитроэфиров до альдегидов.
В период автокаталитического разложения происходит образование сульфоэфиров, нитритов и окисление их четырёхокисью азота до альдегидов и органических кислот.
В конце автокатализа в период падения содержания окислов азота происходит окисление альдегидов, гидролиз нитритов, окисление их и продуктов гидролиза четырёхокисью азота до органических кислот и переход N2O4 в N2O3 вследствие разбавления азотной кислоты реакционной водой. В период вторичного быстрого повышения содержания окислов азота происходит окисление спиртов, альдегидов и продуктов переэтерификации ДНДЭГ трёхокисью азота до органических кислот и гидролиз нитроэфиров.
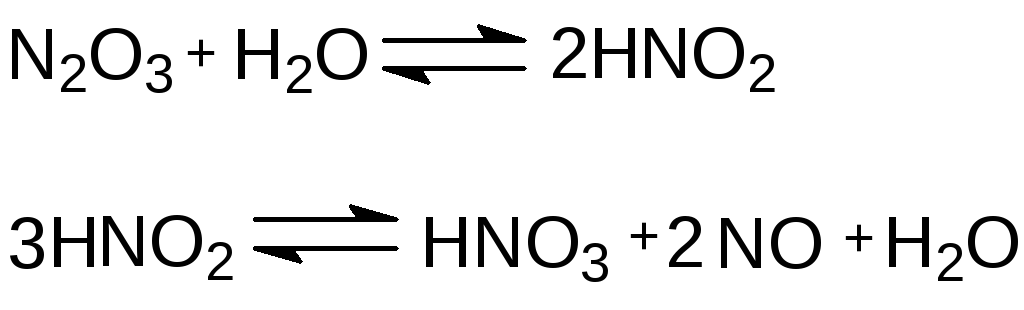
В период падения содержания окислов азота дополнительно к этим реакциям идёт распад N2O3.
В период медленного доразложения происходит гидролиз нитратов до спиртов и окисление последних до органических кислот.
