
- •Бийский технологический институт (филиал)
- •Р.Н. Питеркин, р.Ш. Просвирнин, е.А. Петров технология нитроэфиров и нитроэфирсодержащих промышленных вв
- •Содержание
- •Введение
- •Часть I. Нитроэфиры
- •1 Историческая справка о развитии промышленных способов производства нитроглицерина
- •2 Современные способы производства нитроэфиров
- •2.1 Оптимальные составы кислот и модули нитрации
- •2.2 Инжекторы для осуществления нитрационного
- •2.3 Холодильники для охлаждения эмульсии
- •2.4 Центробежные сепараторы для разделения эмульсии нитроэфир–отработанная кислота
- •2.5 Процесс и оборудование для стабилизации
- •2.6 Весовой дозатор-расходомер нитроэфиров
- •2.7 Насосы для транспортирования отработанных
- •2.8 Технологическая схема производства нитроэфиров в малогабаритном оборудовании
- •3 Вспомогательные стадии процесса производства нитроэфиров
- •3.1 Разложение нитротел в отработанных кислотах
- •3.2 Обезвреживание сточных вод производства
- •3.2.1 Адсорбционный способ обезвреживания
- •3.2.2 Автоклавный способ очистки сточных вод
- •3.2.3 Восстановление нитроэфиров
- •3.2.4 Электрохимический метод обезвреживания
- •3.2.5 Сверхкритическое водное окисление
- •3.3 Приборы для непрерывной оценки качества нитроэфиров
- •I, мA 0,1 % hno3 0,03 % hno3 0,01 % hno3
- •0,2 0,4 0,6 Содержание н2о, %
- •4 Свойства нитроэфиров
- •4.1 Физические свойства нитроэфиров
- •4.2 Взрывчатые свойства нитроэфиров
- •4.3 Поведение нитроэфиров в кислых средах
- •4.3.1 Стойкость кислых нгц, дндэг и их смеси
- •4.3.2 Стойкость кислых динитрата триэтиленгликоля, тринитрата нитроизобутилглицерина и динитрата
- •4.3.3 Влияние воды на стойкость кислых нитроэфиров
- •4.3.4 Влияние серной и азотной кислот
- •4.3.5 Влияние окислов азота
- •4.3.6 Стойкость нгц и дндэг с пониженной
- •4.3.7 Механизм разложения кислых нитроэфиров
- •4.3.8 Разложение нитроэфиров в отработанных
- •4.3.9 Разложение нитротел в слабых отработанных кислотах
- •4.4 Реакции нитроэфиров с основаниями
- •4.4.1 Гидролиз нитроглицерина
- •4.4.2 Гидролиз динитрата этиленгликоля (днэг)
- •4.4.3 Гидролиз динитрата диэтиленгликоля (дндэг)
- •4.5 Причины аварий на производствах нитроэфиров
- •Литература
- •Часть II. Нитроэфирсодержащие взрывчатые вещества
- •5 Технология производства нитроэфирсодержащих взрывчатых веществ
- •5.1 Современные направления развития
- •5.2 Разработка технологии и создание
- •Фаза подготовки компонентов
- •Фаза конечных операций
- •5.3 Автоматизация производства
- •5.4 Экологическая защита производства
- •5.4.1 Разработка эффективных методов
- •5.4.2 Технико-экономические показатели производства
- •6 Оптимизация и модернизация штатных рецептур нитроэфирсодержащих вв
- •6.1 Оптимизация угленита э-6
- •6.2 Исследование предохранительных свойств
- •6.3 Разработка и исследование угленита м – новой рецептуры вв V класса [15]
- •6.4 Модернизация детонита м
- •6.4.1 Разработка рецептуры модернизированного
- •6.4.2 Отработка технологии модернизированного
- •6.4.3 Промышленные испытания модернизированных детонитов [24]
- •7 Некоторые аспекты безопасности нитроэфирсодержащих вв
- •7.1 О химической стабильности и предельных сроках хранения нитроэфирсодержащих промышленных вв
- •7.2 О чувствительности нитроэфирсодержащих
- •7.3 О физической стабильности
- •Литература
- •Сокращения и обозначения
3.3 Приборы для непрерывной оценки качества нитроэфиров
Чистые нитроэфиры являются стойкими веществами и могут храниться без видимых изменений длительное время. Однако, в производственных условиях невозможно получить абсолютно чистые продукты. В них всегда содержатся незначительные количества примесей веществ, способных снизить стабильность полученных нитратов. Кроме кислот, не полностью удалённых из нитроэфиров в процессе стабилизации, причиной снижения стойкости может быть наличие в продукте повышенного содержания карбонильных соединений, органических и неорганических нитритов, источником которых являются процессы щелочного гидролиза нитроэфиров при промывке их растворами соды.
Контролю стойкости нитроэфиров с давних времён уделялось большое внимание.
Были разработаны различные стойкостные пробы, которые основаны на обнаружении двуокиси азота в газах, образующихся при термических воздействиях на нитроэфиры. Это получившая всеобщее распространение, в том числе в нашей стране, проба Абеля. Два миллилитра образца нитроэфира помещают в баню и выдерживают при 72 °C или при 82,2 °C. Над образцом подвешивают полоски стандартной бумаги, пропитанной KJ и крахмалом и смоченной на половину высоты 50 %-ным раствором глицерина. Определяют время, через которое на границе смоченной и сухой полоски появляется голубая окраска от выделяющегося йода, осаждающегося с крахмалом. Источником йода является двуокись азота, образующаяся при термическом разложении нитроэфира:
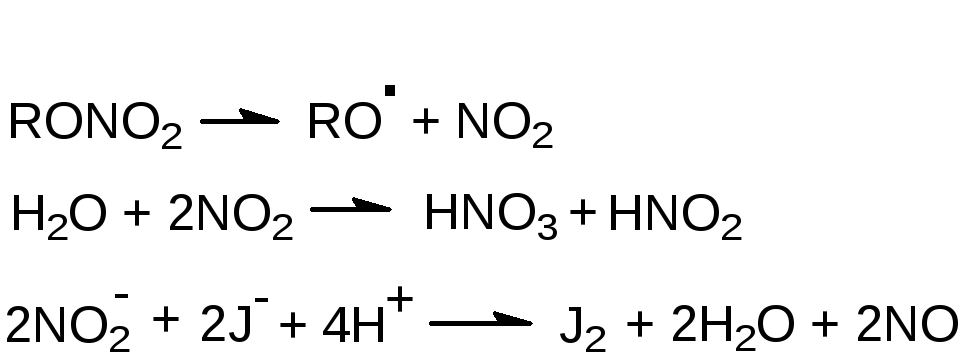
В СССР были установлены нормы времени до появления окраски йодокрахмальной бумажки при 72 °C, при которых нитроэфир считался стойким: для НГЦ – 30 мин, для ДНДЭГ – 15 мин, для смесевого нитроэфира – 20 мин.
Известны также и другие стойкостные пробы. Проба Гутмана (индикаторная бумага – бумага, смоченная водным сернокислым раствором дифениламина с небольшой добавкой глицерина, 70 °C), проба Муара (индикаторная бумага смочена смесью α-нафтиламина с сульфаниловой кислотой и глицерином), проба Спивака (бумага смочена солянокислым метафенилендиамином и раствором сахара, 66–67 °C), проба с йодцинккрахмальной бумагой (вместо KJ бумагу пропитывали ZnJ2 в смеси с ZnCl2, 80 °C), проба Хойтзема (определяют температуру, при которой в течение 15 мин не образуются продукты распада; газы удаляют током CO2 в сосуд со стеклянной ватой, смоченной раствором дифениламина в серной кислоте), проба Робертсона (газы, образующиеся при 90–130 °C, вытесняют струёй CO2 и пропускают над раскалённой медью, где окислы восстанавливаются до азота, объём которого измеряют), проба Меца (110 °C, продукты разложения поглощают водой и измеряют рН водного раствора), проба Васильева (потенциометрическое титрование).
Все предложенные стойкостные пробы требовали много времени на получение результата (это отбор пробы нитроэфира, доставка его в аналитическую лабораторию, собственно анализ в течение 40–60 мин). После освоения непрерывных процессов производства нитроэфиров результат анализа стойкости выдавался с большим опозданием, когда уже получены сотни килограммов нестабильного продукта. Кроме того, в пробу Абеля вносился субъективный фактор, связанный с опытом лаборанта, с тщательностью подготовки опыта.
Кроме того, многочисленные исследования указывали на значительно более высокую стабильность ДНДЭГа по сравнению с НГЦ, а по пробе Абеля он выглядел, как менее стойкий продукт.
Поэтому
перед исследователями постоянно стояла
проблема создания приборов, способных
непрерывно в потоке оценивать стабильность
нитроэфира. Например, в американском
патенте [21] от основного потока создают
отводной канал, где в НГЦ вводят реагент,
дающий окраску с
![]() .
Изменение окраски фиксируется
колориметром. Используются любые
реагенты – реагент Грисса 1-нафтиламин
и сульфаниловая кислота:
.
Изменение окраски фиксируется
колориметром. Используются любые
реагенты – реагент Грисса 1-нафтиламин
и сульфаниловая кислота:
а) диазотирование сульфаниловой кислоты
![]()
б) сочетание с 1-нафтиламином
![]()
Можно использовать оксалат 1-нафтиламина и сульфаниловую кислоту или N-(1-нафтил)-этилендиаминдигидрохлорид (реагент Зальцмана).
Здесь
определяют
![]() непосредственно в фазе нитроглицерина
без термического воздействия на него.
После стабилизации НГЦ всегда содержит
нитраты и нитриты. Содержание последних
колеблется от 0,36·10-4
до 70·10-4
%
при вполне нормальной стабильности
НГЦ. Поэтому предлагаемый способ оценки
стабильности НГЦ вызывает сомнения в
его объективности. Большой объём работ
начиная с 1949 г. был выполнен в одной
исследовательской организации по
разработке непрерывно действующей
установки контроля стойкости в первую
очередь нитроглицерина.
непосредственно в фазе нитроглицерина
без термического воздействия на него.
После стабилизации НГЦ всегда содержит
нитраты и нитриты. Содержание последних
колеблется от 0,36·10-4
до 70·10-4
%
при вполне нормальной стабильности
НГЦ. Поэтому предлагаемый способ оценки
стабильности НГЦ вызывает сомнения в
его объективности. Большой объём работ
начиная с 1949 г. был выполнен в одной
исследовательской организации по
разработке непрерывно действующей
установки контроля стойкости в первую
очередь нитроглицерина.
Их результат представлен в диссертациях Шарабри-ной М.Г. и Сафронова Н.И. Позже созданная ими установка использовалась на всех заводах СССР, связанных с получением нитроэфиров, и была введена в государственный стандарт на нитроэфиры в качестве замены пробы Абеля. Шарабрина М.Г. разработала установку, применяемую только к контролю НГЦ. Сафронов Н.И. на основе исследований скорости выделения азотной кислоты и оксидов азота при термическом разложении ДНДЭГ и смесей его с НГЦ, влияния температуры, влаги, азотной и серной кислот, нитритов, нитратов, перекиси водорода, мочевины и других возможных примесей подобрал условия осушки ДНДЭГ до влажности 0,1 % и температуру в реакторе для термического разложения ДНДЭГ. С участием специалистов СКБП СА (г. Тбилиси) работа установки АУСП-2 проходила в дистанционном и автоматическом режиме.
Принципиальная схема установки АУСП-2 представлена на рисунке 3.6.
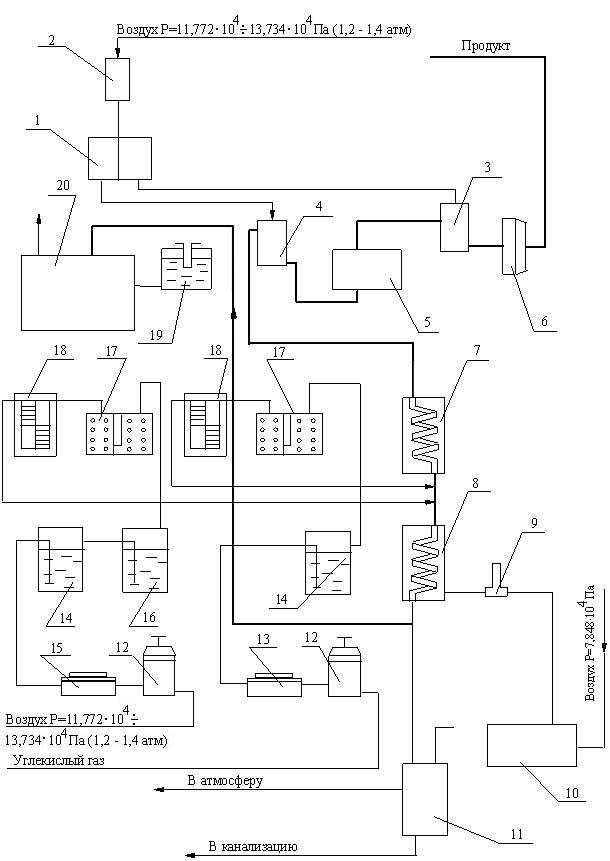
Рисунок 3.6 – Принципиальная схема установки АУСП-2
Установка состоит из следующих основных узлов:
пульта управления;
блока регулирования;
баков;
распределительного шкафа;
прибора для обезвреживания отработанного продукта;
термостата.
В блок дозирования входит узел термического разложения, в распределительный шкаф входит вторичный прибор, колориметр или спектрофотометр.
Принцип работы установки. Водная эмульсия нитроэфира, отфильтрованная от взвесей в фильтре 6, большим дозатором 3 подаётся в отстойник 5. Отделённый от воды продукт отбирается малым дозатором 4, поступает в осушитель 7, из которого стекает в реактор 8, в котором разлагается. Избыток эмульсии из отстойника 5 возвращается в рабочую магистраль. Горячая вода в рубашки осушителя и реактора подаётся термостатом.
Воздух к приводам дозаторов поступает из магистрали через фильтр 2 и распределитель 1. В осушитель воздух поступает через редуктор 12, регулятор расхода 15. Скорость подачи регулируется по изменению уровня воды в моностате 14 и контролируется по реометру 18.
Газообразные продукты разложения нитроэфиров потоком углекислого газа направляются в кювету фотоколориметра или спектрофотометра 20 с реактивом Грисса, который поступает из бачка 19. Остатки продукта сливают в прибор для обезвреживания 11, в который постоянно через ручной зажим стекает тройной объём дибутилфталата.
Через каждые 8 минут замеряют оптическую плотность, значение которой пропорционально стойкости продукта по пробе Абеля. Для НГЦ норма оптической плотности 0,320±0,005; для ДНДЭГ – 0,190±0,005; для НГЦ+ДНДЭГ – 0,270±0,005. Результат анализа фиксируется в условных минутах.
Технические характеристики установки:
Предел измерения 0–40 усл. мин.
Цена деления 1 мин.
Сигнал нестойкости 15, 20, 30 (ДНДЭГ, смесевой НГЦ, НГЦ).
Время установления нормального режима расслоения продукта, дозирования и термического разложения 5 мин (80–90 °С).
Давление воздуха для осушки 0,5–1,0 ати.
Расход CO2 3,6±0,2 л/мин.
Расход воздуха в осушитель 36±2 л/мин.
Производительность дозатора эмульсии 150 мл/мин.
Производительность дозатора нитроэфира 25 мл/мин.
Установка АУСП-2 размещается в здании, врезанном в вал здания дозирования нитроэфиров. Поток эмульсии нитроэфира в воде подаётся в это здание, собирается в лабиринте, и нитроэфир из него инжектором в виде эмульсии возвращается в здание дозирования. Как следует из описания принципа работы установки АУСП-2, она довольно сложна, требуется строительство отдельного здания для её размещения. Хотя цикличность измерений собственно установки невелика, но с учётом необходимости направления части потока эмульсии нитроэфира в воде от магистрали между зданиями нитрации и дозирования нитроэфиров значительно увеличивается время запаздывания измерений от момента получения нитроэфира.
Низкая чувствительность данного способа контроля стойкости к наличию остаточных кислот в нитроэфире вызвала необходимость дополнения системы контроля установкой контроля кислотности нитроэфиров. Это агрегат, проводящий автоматическую промывку пробы нитроэфира определённым количеством воды, содержащей смешанный индикатор (метиленовый синий с метиленовым красным), и последующим определением изменения интенсивности окраски раствора на фотоэлектроколориметре. Естественно, установка сложна, требует постоянного внимания со стороны обслуживающего персонала и длительного времени для подготовки её к работе.
Изучению механизма раcпада нитроэфиров и разработке способов контроля их стойкости посвящено большое число работ [22, 23, 24, 25]. Ускоренное термическое превращение НГЦ обусловлено гидролизом и окислением продуктов гидролиза. Скорость нейтрального гидролиза очень мала, щелочного и кислотного очень высока. Если в присутствии щелочного агента превращение постепенно замедляется, то при наличии кислоты самоускоряется. Основным объектом окисления в НГЦ являются примеси и первичные продукты превращения. Основным окисляющим агентом являются двуокись азота и азотная кислота.
Начальное содержание кислот даже в нестойком по пробе Абеля НГЦ очень мало (10-4 %). Чистый НГЦ такое количество азотной кислоты выделяет через 75 мин при 70 °C.
Кинетические
измерения показали, что термический
распад НГЦ сопровождается более высоким
содержанием
![]() ,
накопление
,
накопление![]() идёт значительно медленнее.
идёт значительно медленнее.
ДНДЭГ в силу особенностей механизма его распада [26, 27] даже при содержании 0,01–0,02 % кислот по стойкости не отличается от стойкости химически чистого. Такие количества кислот не ускоряют разложение ДНДЭГ, они относительно быстро исчезают за счёт соответствующих окислительных реакций и не успевают вновь образовываться за счёт гидролиза, склонность к которому у ДНДЭГ незначительна. Соответственно, не образуются легкоокисляемые продукты.
Из всего многообразия возможных примесей в технических нитроэфирах определяющее влияние на снижение их стабильности оказывают примеси минеральных кислот и в первую очередь азотной, азотистой и серной кислот, а также окислов азота и воды [28]. Поэтому привлекательной являлась задача создания прибора, способного в потоке нитроэфира непрерывно давать информацию о наличии в нём кислот. Предельным допускаемым содержанием кислот в нитроэфирах является 10-3 %. Продукт с содержанием кислот выше этого значения не должен допускаться к дальнейшему использованию.
Для этих целей пригоден электрохимический способ индикации кислотных продуктов. Впервые попытка его применения была предпринята Навальневым Н.С. в 1952 г. Но не найдя корреляции значений ЭДС между электродами из цинка и меди, помещённых в НГЦ, и пробой Абеля, от развития этого метода он отказался. Было отмечено, что ЭДС данной гальванической пары сильно зависит от содержания кислот в НГЦ. Этот факт заставил обратить внимание на возможность разработки прибора контроля кислотности нитроэфиров на основе гальванической пары, точнее коррозионного эффекта на основе элемента, состоящего из двух активных электродов, электролитом для которых служит анализируемый нитроэфир.
Металл электрода, который в данных условиях обладает наиболее электроотрицательным потенциалом, является анодом этого гальванического элемента и растворяется. Второй электрод в этом элементе является катодом, и на его поверхности протекают катодные процессы. Скорость коррозии анода тем больше, чем больше разность обратимых потенциалов катодной и анодной реакции. Она также находится в сложной зависимости от рH агрессивной среды, наличия окислителей и нейтральных солей, присутствия ПАВ. В общем виде скорость растворения анода характеризуется силой тока, протекающего между электродами.
В качестве анода предложено использовать цинк, так как цинк в области pH 8–12 пассивируется, а получение продукта с pH выше 12 в производственных условиях исключено. Его коррозия происходит только в кислой среде. В качестве катода целесообразно использовать медь, относящуюся к металлам с минимальным перенапряжением водорода.
На электрохимической ячейке с такими электродами были сняты поляризационные диаграммы с НГЦ. При совместном влиянии уменьшения pH среды и увеличения содержания окислителей, например, азотной кислоты, наблюдалось резкое возрастание коррозионного тока. При этом растворяется металл анода (цинк), а на катоде выделяется водород и удаляется за счёт восстановления кислоты. Сопротивление измерительной схемы должно быть не более 0,5 МОм, при этом изменение содержания нейтральных солей не оказывает влияния на коррозионный ток.
На рисунке 3.7 представлена схема измерения коррозионного тока, а на рисунке 3.8 зависимость показаний миллиамперметра от числа промывок ДНДЭГ и НГЦ.
При токе, равном 1 мА, наблюдается чёткий переход от кислого к нейтральному продукту как для НГЦ, так и для ДНДЭГ.
Минимальная концентрация кислот, регистрируемая измерительной системой, составляет 0,0004 %, что соответствует практически нейтральному продукту.
На показания мало влияет наличие в нитроэфире содового раствора и нейтральных солей.
Влияние кислот и влаги в нитроэфирах на величину коррозионного тока исследовано на опытном образце проточной ячейки (рисунки 3.9, 3.10).
При содержании азотной кислоты в НГЦ ниже 0,01 % влажность продукта практически не оказывает влияния на величину коррозионного тока. Инерционность системы измерения составляла 2 с, что равно времени однократного обмена продукта в ячейке.
Температура в пределах 12–32 °C и скорость протока нитроэфира в пределах 70–140 мл/мин слабо влияют на величину тока, особенно при низких содержаниях азотной кислоты.
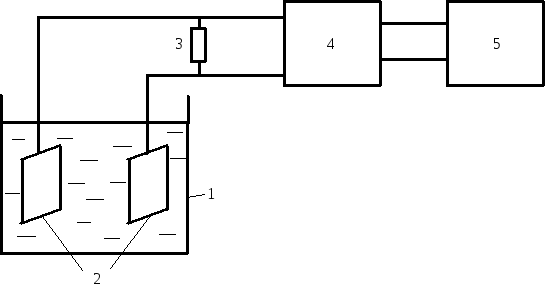
Рисунок 3.7 – Схема измерения коррозионного тока:
1 – электролитическая ячейка; 2 – электроды; 3 – R=13,4 кОм;
4 – усилитель; 5 – миллиамперметр

Рисунок 3.8 – Зависимость показаний миллиамперметра
от числа промывок нитроэфира: Δ – продукт кислый;
х – продукт щелочной; о – продукт нейтральный
