
- •Бийский технологический институт (филиал)
- •Р.Н. Питеркин, р.Ш. Просвирнин, е.А. Петров технология нитроэфиров и нитроэфирсодержащих промышленных вв
- •Содержание
- •Введение
- •Часть I. Нитроэфиры
- •1 Историческая справка о развитии промышленных способов производства нитроглицерина
- •2 Современные способы производства нитроэфиров
- •2.1 Оптимальные составы кислот и модули нитрации
- •2.2 Инжекторы для осуществления нитрационного
- •2.3 Холодильники для охлаждения эмульсии
- •2.4 Центробежные сепараторы для разделения эмульсии нитроэфир–отработанная кислота
- •2.5 Процесс и оборудование для стабилизации
- •2.6 Весовой дозатор-расходомер нитроэфиров
- •2.7 Насосы для транспортирования отработанных
- •2.8 Технологическая схема производства нитроэфиров в малогабаритном оборудовании
- •3 Вспомогательные стадии процесса производства нитроэфиров
- •3.1 Разложение нитротел в отработанных кислотах
- •3.2 Обезвреживание сточных вод производства
- •3.2.1 Адсорбционный способ обезвреживания
- •3.2.2 Автоклавный способ очистки сточных вод
- •3.2.3 Восстановление нитроэфиров
- •3.2.4 Электрохимический метод обезвреживания
- •3.2.5 Сверхкритическое водное окисление
- •3.3 Приборы для непрерывной оценки качества нитроэфиров
- •I, мA 0,1 % hno3 0,03 % hno3 0,01 % hno3
- •0,2 0,4 0,6 Содержание н2о, %
- •4 Свойства нитроэфиров
- •4.1 Физические свойства нитроэфиров
- •4.2 Взрывчатые свойства нитроэфиров
- •4.3 Поведение нитроэфиров в кислых средах
- •4.3.1 Стойкость кислых нгц, дндэг и их смеси
- •4.3.2 Стойкость кислых динитрата триэтиленгликоля, тринитрата нитроизобутилглицерина и динитрата
- •4.3.3 Влияние воды на стойкость кислых нитроэфиров
- •4.3.4 Влияние серной и азотной кислот
- •4.3.5 Влияние окислов азота
- •4.3.6 Стойкость нгц и дндэг с пониженной
- •4.3.7 Механизм разложения кислых нитроэфиров
- •4.3.8 Разложение нитроэфиров в отработанных
- •4.3.9 Разложение нитротел в слабых отработанных кислотах
- •4.4 Реакции нитроэфиров с основаниями
- •4.4.1 Гидролиз нитроглицерина
- •4.4.2 Гидролиз динитрата этиленгликоля (днэг)
- •4.4.3 Гидролиз динитрата диэтиленгликоля (дндэг)
- •4.5 Причины аварий на производствах нитроэфиров
- •Литература
- •Часть II. Нитроэфирсодержащие взрывчатые вещества
- •5 Технология производства нитроэфирсодержащих взрывчатых веществ
- •5.1 Современные направления развития
- •5.2 Разработка технологии и создание
- •Фаза подготовки компонентов
- •Фаза конечных операций
- •5.3 Автоматизация производства
- •5.4 Экологическая защита производства
- •5.4.1 Разработка эффективных методов
- •5.4.2 Технико-экономические показатели производства
- •6 Оптимизация и модернизация штатных рецептур нитроэфирсодержащих вв
- •6.1 Оптимизация угленита э-6
- •6.2 Исследование предохранительных свойств
- •6.3 Разработка и исследование угленита м – новой рецептуры вв V класса [15]
- •6.4 Модернизация детонита м
- •6.4.1 Разработка рецептуры модернизированного
- •6.4.2 Отработка технологии модернизированного
- •6.4.3 Промышленные испытания модернизированных детонитов [24]
- •7 Некоторые аспекты безопасности нитроэфирсодержащих вв
- •7.1 О химической стабильности и предельных сроках хранения нитроэфирсодержащих промышленных вв
- •7.2 О чувствительности нитроэфирсодержащих
- •7.3 О физической стабильности
- •Литература
- •Сокращения и обозначения
3.2.2 Автоклавный способ очистки сточных вод
Нитроэфиры в сточной воде гидролизуют содой при повышенных температурах и давлениях до остаточного содержания в воде НГЦ не более 150 мг/л, ДНДЭГ – не более 50 мг/л.
С такой концентрацией сточные воды можно направлять на биохимическую очистку в смеси с хозяйственно-бытовыми сточными водами.
НГЦ полностью разлагается за 10–12 мин при 120–130 °C в содовом растворе концентрацией 0,2–0,3 %. ДНДЭГ – за 15 мин при 150–160 °C в растворе соды концентрацией 1 %.
Исходя из кинетических данных по гидролизу ДНДЭГ, расчётное время пребывания в автоклаве должно быть:
при 160 °C – 17,8 мин;
при 170 °C – 9,8 мин;
при 180 °C – 5,5 мин.
За это время концентрация ДНДЭГ в 1 %-ном растворе соды снижается от 4000 до 50 мг/л.
Схема установки для обезвреживания сточной воды в автоклаве на одном из заводов приведена на рисунке 3.3.
Производительность её по сточной воде 3,2 м3/ч. Тепло обезвреженной воды здесь используется для предварительного нагрева сточной воды. Сточная вода из лабиринта 1 тарельчатым насосом 2 подаётся через подогреватель 3 в буферный реактор 4. Из него насосом-дозатором 5 вода нагнетается через подогреватель 6 в автоклав 7. Из автоклава вода с температурой 180 °C возвращается через подогреватель 6, буферный реактор 4 и подогреватель 3, из него при температуре 35–40 °C сбрасывается в канализацию. В подогревателе 3 и в реакторе 4 вода подогревается до 95–98 °C, затем в подогревателе 6 до 160 °C и в автоклаве 7 до 180 °C. Подогреватели 3 и 6 змеевикового типа. Змеевик из трубы 32×2 мм длиной 87 м.
В буферном реакторе обогрев идёт через змеевик водой, выходящей из автоклава, и через рубашку паром. Автоклав выполнен в виде трубы диаметром 159×6 мм длиной 28 м. Он разделён на зону нагрева и зону выдержки.
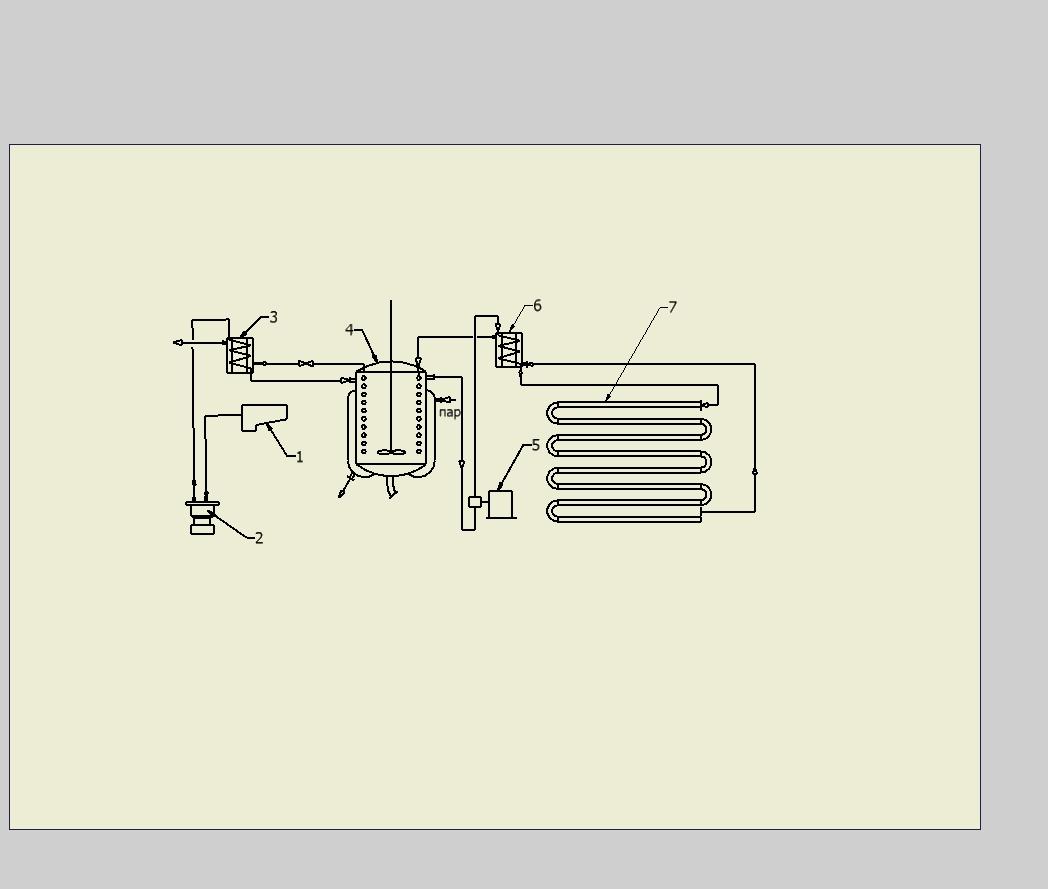
Рисунок 3.3 – Схема установки обезвреживания сточных вод в автоклаве
Зона нагрева – это намотанные на трубу гибкие ленточные электронагревательные элементы ЭНГЛУ 400-4,8/220-16, по 6 элементов в секции, всего три секции. В каждой секции их соединяют по схеме «Δ» (треугольника) по две штуки между фазами трёхфазного тока напряжением 380 В. Мощность одной секции 86,4 кВт. В зоне выдержки труба не обогревается, в ней время пребывания воды 4 минуты. Необходимое давление в системе поддерживается дроссельным клапаном, установленным на выходе обратного потока воды из змеевика буферного реактора.
Содержание ДНДЭГ в обезвреженной воде не превышает 50 мг/л, НГЦ гидролизуется полностью.
3.2.3 Восстановление нитроэфиров
чугунными стружками
Известен метод восстановления нитросоединений до аминов чугунными стружками. Обычно стружки и нитросоединения добавляют к водному раствору электролита (соли FeCl2, FeSO4, AlCl3, NH4Cl и др.) или на стружки действуют кислотами, получая электролит. Чугун содержит соединения углерода (феррит, графит, перлит), а также Mn, P, Si, S. Поэтому в нём возникают элементарные гальванические пары, где выделяющийся на аноде кислород содействует окислению железа. Электролит ускоряет коррозию железа вследствие увеличения проводимости, при этом сам он не расходуется. На катоде выделяется водород, 2–3 % которого от необходимого для восстановления нитроэфиров, теряется. Скорость реакции зависит от поверхности стружек, природы электролита и его концентрации. В результате восстановления образуется исходный спирт и аммиак, есть примеси N2 и NO.
RONO2 + 3Fe + 2H2O = ROH + Fe3O4 + NH3
На 2 кг НГЦ требуется с учётом потерь водорода 4,6 кг стружек, на 4 кг ДНДЭГ 7,1 кг стружек, что соответствует 1 м3 сточной воды.
Эксперименты показали, что при 100 °C и pH 1–2 полное восстановление НГЦ достигается за 30 мин, ДНДЭГ – за 60 мин. Значение pH не выше 2 поддерживали добавлением серной кислоты. Метод эффективен, но до реализации в промышленных условиях не доведен.
