
- •1. Основні положення та наукові основи курсу
- •2. Класифікація процесів та їх призначення
- •3. Основи раціональної побудови апаратів
- •1. Основні закономірності технологічних процесів
- •Закон збереження енергії
- •Де ра ,рв ,рс,рд ,ре – маса компонентів а,в,с,д,е.
- •Рівноважні та не рівноважні системи
- •2. Класифікація процесів та їх призначення
- •Під апаратом розуміють любий устрій, в якому протікає технологічний процес.
- •3. Основи раціональної побудови апаратів
- •Контрольні запитання:
- •2. Гідромеханічні та механічні процеси
- •2.1. Процеси подрібнення
- •1. Сутність і призначення процесу подрібнення
- •2. Основні способи подрібнення
- •Класифікація дроблення і помелу
- •Способи подрібнення
- •3. Апаратне забезпечення процесу подрібнення
- •( Дискового дезінтегратора)
- •Контрольні запитання:
- •2.2.Процеси сортування
- •1. Призначення та методи
- •2. Характеристика апаратів для сортування
- •П роцес триєрування виконується за допомогою триєрів, робочим органом яких є металевий циліндр, в якому виштампувано або висвердлено чашечки (рис.4).
- •Контрольні запитання:
- •2.3. Процеси пресування
- •1. Сутність і призначення пресування
- •2. Характеристика процесів пресування, апарати для пресування
- •3. Фактори, що впливають на процес пресування
- •Контрольні запитання:
- •2.4. Процеси перемішування
- •1.Суть процесу перемішування та його застосування
- •2. Способи перемішування, їх характеристика та апарати для перемішування
- •Р ис.1.Основні типи механічних мішалок:
- •- Однолопатева; 2 - багатолопатева; 3 - пропелерна; 4 - якірна;
- •Піноутворення та збивання заключаються в диспергуванні газів в рідині.
- •Р ис. 7. Схема збивального апарата
- •Перемішування пластичних мас
- •Р ис.9. Перемішувальні устрої для пластичних матеріалів
- •Потокове перемішування
- •Змішувачів
- •Р ис.15. Схема пристроїв для перемішування в потоці:
- •Контрольні запитання:
- •2.5. Процеси розділення неоднорідних систем
- •1. Характеристика дисперсних систем, їх класифікація
- •Класифікація дисперсних систем за ступенем дисперсності
- •2. Значення гідромеханічних процесів поділу дисперсних систем для охорони довкілля
- •Контрольні запитання:
- •2.6. Процеси осідання і фільтрування
- •1. Загальні відомості про процес осадження, апарати для осадження
- •2. Загальні відомості, класифікація фільтраційних процесів, апарати для фільтрування
- •Схеми затримання частинок осаду фільтрувальним шаром
- •Способи очищення газів
- •Контрольні запитання:
- •3. Теплові і масообмінні процеси
- •3.1. Загальні відомості про теплові процеси
- •1. Завдання, призначення та способи теплової обробки харчових продуктів.
- •2. Джерела теплової енергії та теплоносії.
- •3. Види теплообміну та їх характеристика.
- •П ередача тепла теплопровідністю крізь стінку
- •4. Основні типи теплообмінних апаратів
- •Схеми теплообмінних апаратів
- •Контрольні запитання:
- •3.2. Суть і способи нагрівання харчових продуктів
- •2. Поверхневе нагрівання
- •1. Вплив теплової обробки на якість кулінарної продукції
- •2. Поверхневе нагрівання
- •Нагрівання водяною парою
- •Нагрівання топковими газами
- •Нагрівання гарячими рідинами
- •Нагрівання електричним струмом
- •3 . Електрофізичні методи обробки харчових продуктів
- •Контрольні запитання:
- •3.3. Суть процесу варіння і його апаратурне оформлення
- •2. Зовнішній теплообмін при варінні продуктів
- •1. Класифікація процесів варіння
- •2. Зовнішній теплообмін при варінні продуктів
- •Динаміка коефіцієнта тепловіддачі під час варіння біфштекса січеного парою
- •Середньоінтегральні значення коефіцієнта тепловіддачі середовища до продукту при варінні різними способами
- •3. Теплофізичні закономірності процесу варіння
- •Розподіл вологи в біфштексі січеному під час варіння парою при атмосферному тискові
- •Поля температур по товщині біфштекса січеного під час варіння парою через 3(1), 6(2), 9 (3), 12 (4), 15 (5) хвилин від початку процесу
- •4. Фактори, що впливають на процес варіння
- •5.Основні типи варильних апаратів
- •Контрольні запитання:
- •2.Основи тепло – і масообміну під час смаження
- •3.Характеристика апаратів для смаження
- •4. Недоліки процесу смаження
- •Контрольні запитання:
- •Класифікація процесів смаження за технологічним принципом
- •3.5. Загальні відомості про масообмінні процеси
- •1. Основи масопередачі
- •2. Загальні ознаки масообміних процесів
- •Контрольні запитання:
- •3.6. Процеси випарювання і конденсації
- •1.Випарювання. Загальна характеристика процесу
- •С хеми багатокорпусних випарних установок
- •Принципова схема вакуум-випарної установки
- •2. Конденсація. Загальна характеристика процесу
- •Поверхневі конденсатори
- •Елементарний конденсатор холодильної установки
- •Конденсатори змішування
- •Барометричний конденсатор з протиточним рухом води і пару
- •Барометричний конденсатор з протиточним рухом води і пару Контрольні запитання:
- •3.7. Процес сушіння
- •1. Загальні відомості
- •Принципова схема сушки
- •2. Властивості матеріалів, кінетика процесу сушіння
- •3. Види і способи сушіння
- •4. Устаткування для процесу сушіння
- •Контрольні запитання:
- •3.8. Сорбційні процеси
- •1. Загальні відомості
- •2. Процес абсорбції
- •3. Процес адсорбції
- •С хема насадкового абсорбера Схема механічного абсорбера
- •Контрольні запитання:
- •3.9. Процеси перегонки і ректифікації
- •Сутність процесу та види перегонки
- •2. Апарати для перегонки та ректифікації
- •Простий кубовий апарат
- •3.10. Процеси екстракції
- •1.Суть процесу екстракції.
- •2. Фактори, що впливають на процеси екстракції.
- •3. Апарати для проведення процесу екстракції.
- •Контрольні запитання:
- •3.11. Процеси кристалізації і розчинення
- •1. Загальні відомості про процес кристалізації
- •Фізичні основи кристалізації із розчинів
- •Ріст кристалів
- •2. Апарати для проведення кристалізації
- •3. Фактори, що впливають на хід процесу кристалізації
- •4. Загальні відомості про процес розчинення
- •Контрольні запитання:
- •1.Призначення процесів охолодження і заморожування у громадському харчуванні. Охолодження як спосіб консервування кулінарної продукції
- •2.Закономірність процесів охолодження та заморожування
- •3.Суть та способи одержання холоду
- •4.Безмашинне охолодження
- •5.Машинне охолодження
- •6.Апарати для охолодження
- •С хема фризера періодичної дії
- •Патрубок для входу холодоагенту; 2 - оболонка; 3 - корпус апарата;
- •Контрольні запитання:
- •Використана література
- •Рецензія на навчальний посібник з дисципліни “Процеси і апарати харчових виробництв” для спеціальності 5. 05170101 “Виробництво харчової продукції”
Фізичні основи кристалізації із розчинів
Як будь-який фізико-хімічний процес, кристалізація характеризується статикою, кінетикою і динамікою.
Статика кристалізації визначає умови рівноваги між кристалами та міжкристальним розчином, а також зв'язок між початковими і кінцевими параметрами процесу.
Кінетика кристалізації визначає швидкість переходу речовини з рідкої фази у тверду за заданих умов.
Динаміка кристалізації визначає характер зміни параметрів системи протягом певного часу в разі змінення умов процесу (температури, концентрації, в'язкості тощо).
Кристалізація відбувається внаслідок обмеженої розчинності речовини в розчиннику. Рушійною силою кристалізації є різниця концентрацій розчиненої речовини в пересиченому розчині та на межі поділу фаз.
Якщо при деякій постійній температурі розчиняти будь-яку тверду речовину в будь-якому розчиннику (наприклад, цукор у воді), то за певного вмісту розчиненої речовини в розчині подальше її розчинення припиняється і настає динамічна рівновага між розчином і твердою фазою. Такий розчин називають насиченим. Концентрацію цієї речовини в насиченому розчині називають розчинністю. Розчин, концентрація якого менша за рівноважну, називають ненасиченим, а розчин, концентрація якого більша за рівноважну, - пересиченим.
Кристалоутворення
Кристалізація з розчинів відбувається навколо центрів кристалізації, що утворилися внаслідок пересичення розчину, або навколо подрібнених кристалів, внесених у пересичений розчин ззовні. Центрами кристалізації можуть бути не тільки кристалики речовини, що кристалізується, а й тверді частинки інших речовин, здатні адсорбувати на своїй поверхні молекули розчиненої речовини.
Центри кристалізації в розчинах утворюються внаслідок виникнення зародків нової фази. В пересичених розчинах ці зародки, приєднуючи молекули розчиненої речовини, досягають критичних розмірів і стають здатними до подальшого росту. Такі зародки називають центрами нової фази або центрами кристалізації. Після досягнення кристалічними зародками критичних розмірів починається стадія росту кристалів.
Ріст кристалів
Після утворення стійкого зародка відбувається нарощування кристалічної решітки цього кристала-зародка внаслідок відкладання на його поверхи: надлишку пересиченої речовини, що кристалізується із розчину. Тобто кристали ростуть.
Процес росту кристалів здійснюється в кілька основних послідовних стадій: дифузія речовини, що кристалізується, із об'єму пересиченого розчину до поверхні кристала, адсорбція молекул цієї речовини на поверхні кристала, міграція найпростіших частинок по поверхні, кристала та, останнє, вбудова їх у кристалічну решітку.
2. Апарати для проведення кристалізації
Схему кристалізатора, що працює за першим способом, наведено на рисунку. Він представляє собою резервуар з сорочкою і мішалкою, яка дозволяє прискорити охолодження розчину і перешкоджає осадженню кристалів на дно резервуара.
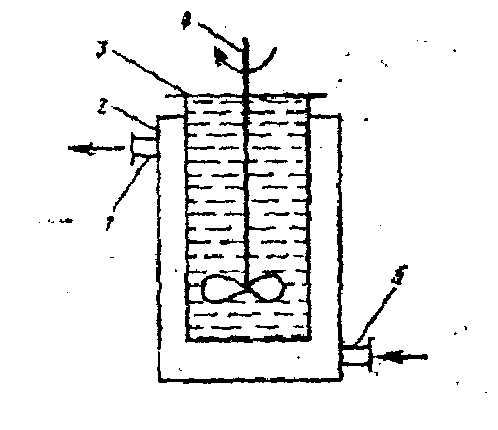
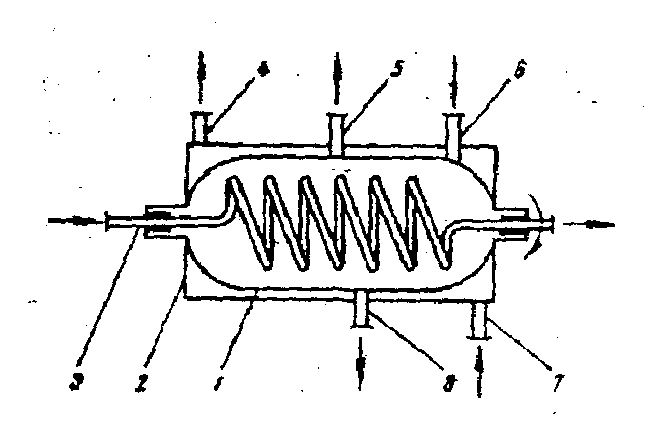
Схема кристалізатора з сорочкою Схема кристалізатора з системою
1 - патрубок для відведення холодної охолодження та вакуумування
води; 2 - сорочка; З – резервуар 1 - корпус кристалізатора;
апарата; 4 - вал із мішалкою; 5 – 2 - сорочка; 3 - змієподібна мішалка;
патрубок для подачі холодної води 4 -патрубок для виходу води;
5 - патрубок, що з'єднує кристалізатор
із конденсатором і вакуумнасосом;
б - патрубок для входу продукту; 7 –
патрубок для подачі води; 8 - патрубок
для випуску розчину і кристалів
Кристалізатор, що працює за третім способом, подано на рисунку. Всередині кристалізатора розміщена змієподібна мішалка, що одночасно є теплообмінником. Через нього рухається холодоагент (вода), який одночасно надходить у сорочку. Для видалення парів, що утворилися, кристалізатор зв'язаний з конденсатором і вакуум-насосом. У апарат надходить гарячий насичений розчин, що має температуру вищу температури її кипіння. В результаті цього виникає ефект самовипарювання, концентрація розчину зростає, він стає перенасиченим. Перенасиченість підсилюється охолодженням розчину.
