
- •Химия, ч. 2. Органическая химия
- •1. Информация о дисциплине
- •Предисловие
- •Место дисциплины в учебном процессе.
- •Содержание дисциплины и виды учебной работы
- •Содержание дисциплины по гос
- •Объем дисциплины и виды учебной работы
- •Раздел 1. Общие вопросы теоретической органической химии
- •1.2. Основные понятия органической химии
- •Раздел 2. Углеводороды
- •2.1. Алифатические углеводороды
- •2.2. Циклические углеводороды
- •Раздел 3. Важнейшие классы производных углеводородов (28 часов)
- •3.1. Гомофункциональные соединения
- •3.2. Гетероциклические и элементоорганические соединения
- •Раздел 4. Высокомолекулярные соединения
- •4.1. Общие представления о высокомолекулярных соединениях (вмс)
- •4.2. Методы синтеза высокомолекулярных соединений
- •4.3. Промышленные органические полимеры
- •Заключение
- •2.2. Тематический план дисциплины
- •2.2.1. Тематический план дисциплины для студентов очной формы обучения
- •2.2.2. Тематический план дисциплины
- •2.2.3. Тематический план дисциплины
- •При использовании информационно-коммуникационных технологий
- •2.5. Практический блок Лабораторные работы
- •3. Информационные ресурсы дисциплины
- •3.1. Библиографический список
- •3.2. Опорный конспект Введение
- •Раздел 1 Общие вопросы теоретической органической химии
- •Основные сырьевые источники органических соединений
- •1.2. Основные понятия органической химии
- •1. Циклоалканы
- •2. Циклоалкены, циклоалкины
- •Вопросы для самопроверки
- •Раздел 2
- •2.1. Алифатические углеводороды
- •Циклические углеводороды
- •Вопросы для самопроверки
- •Раздел 3 Важнейшие классы производных углеводородов
- •3.1. Гомофункциональные соединения
- •Свойства спиртов
- •Простые и сложные эфиры
- •Классификация аминов
- •3.2. Гетероциклические и элементоорганические соединения
- •Вопросы для самопроверки
- •Раздел 4 Высокомолекулярные соединения
- •4.1. Общие представления о высокомолекулярных соединениях
- •4.2. Методы синтеза высокомолекулярных соединений
- •4.3. Промышленные органические полимеры
- •Характеристика некоторых клеев и клеевых композиций представлена в разделе 4.1.1. (пример 7). Вопросы для самопроверки
- •Заключение
- •3.3. Глоссарий
- •3.4. Методические указания к выполнению лабораторных работ предисловие
- •3.4.1. Общие указания
- •3.4.2. Охрана труда и техника безопасности правила техники безопасности при работе в лаборатории оказание первой помощи при несчастных случаях
- •Первая помощь при ожогах и отравлениях
- •Растворители, применяемые для приготовления охлаждающих смесей с твердой углекислотой
- •Методы очистки и выделения органических соединений
- •Определение основных физических констант органических веществ
- •3.4.4. Лабораторные синтезы органических соединений
- •Отчет №
- •6. Выводы по работе. Синтезы азокрасителей
- •Получение полимеров реакцией полимеризации
- •Мономеры и вспомогательные вещества
- •Винилацетат (с4н6о2)
- •Пероксид бензоила (с14н10о4)
- •Получение полимеров реакцией поликонденсации
- •Мономеры и вспомогательные вещества
- •4. Блок контроля освоения дисциплины
- •4.1. Задания на контрольную работу и методические указания к ее выполнению
- •Распределение задач по шифрам для студентов специальности 150501.65
- •Контрольная работа
- •4.1.1. Примеры решения контрольных задач
- •Свойства отечественных полиэпоксидных смол
- •Свойства эпоксидных клеевых соединений в зависимости от природы отвердителя
- •4.2. Текущий контроль
- •Каменноугольная смола является источником…
- •Правильные ответы на тренировочный тест рубежного контроля
- •4.3. Итоговый контроль
- •Приложения
- •1. Основные сырьевые источники органических соединений
- •2. Углеводороды и радикалы (алкилы)
- •6. Краткая характеристика наиболее типичных полимеров, получаемых реакцией поликонденсации и методом полимераналогичных превращений
- •7. Полимерные композиционные материалы, свойства, области применения
- •О8. Свойства исходных соединений, применяемых в синтезах
Мономеры и вспомогательные вещества
С6Н5—ОН Фенол (С6Н6О)
Молекулярная масса94,1
Плотность d2020...1,0722
Показатель преломления пD21.…1,5509
Температура плавления, оС...…. 43,1
Температура кипения, оС….182
Бесцветные игольчатые кристаллы или сплавленная масса белого цвета. Под действием света и воздуха краснеет. Гигроскопичен. Растворимость в 100 г воды 8,2 г при 15 оС; при температурах выше 65 оС растворим неограниченно. Ядовит. Даже разбавленные растворы при действии на кожу вызывают долго не заживающие поражения. При попадании на кожу смывать тампоном, смоченным спиртом.
Н —С=О
Формальдегид
(СН2О)
—С=О
Формальдегид
(СН2О)
Н Молекулярная масса30,0
Температура плавления, оС. ...− 92
Температура кипения, оС.….−19,1
Газ с резким, трудно переносимым запахом. Применяется в виде формалина – 37 % водного раствора, содержащего также 6—15 % метанола и немного муравьиной кислоты. Относительная плотность формалина 1,08—1,11 (в зависимости от содержания метанола), рН 2,8—4,0. Формалин раздражаю-
ще действует на слизистые оболочки и дыхательные пути, может оказать вредное воздействие на центральную нервную систему и зрение. При попадании на слизистые оболочки или кожу следует промыть их водой, 2 % раствором соды и снова водой.
Работа 7. Получение новолачного олигомера
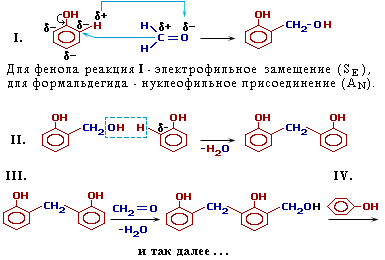
Ц е л ь: ознакомление с реакцией поликонденсации и синтез новолака –фенолформальдегидной смолы.
-
Загрузка реактивов:
фенол (кристаллический) – 9,4 г;
формалин (35-40 % раствор) – 4 мл;
соляная кислота (конц.) – 0,1 мл;
метиловый оранжевый.
Посуда:
колба круглодонная (100 мл);
холодильник обратный;
водяная баня;
чашка фарфоровая.
В круглодонной колбе емкостью 100 мл взбалтывают смесь фенола с формалином до полного растворения, затем добавляют 0,1 мл соляной кислоты, присоединяют к колбе обратный холодильник и нагревают на водяной бане при 90-100 оС в течение 20-40 минут. Реакция протекает с выделением тепла. При закипании смеси нагрев прекращают. Затем нагревание продолжают на кипящей водяной бане до разделения реакционной массы на два слоя: верхний - водный (обычно мутный) и нижний - густой, светло-желтый или светло-коричневый (в зависимости от качества фенола), который представляет собой продукт поликонденсации.
Содержимое колбы сливают в фарфоровую чашку. После охлаждения верхний слой отделяют. Оставшийся в чашке полимерный продукт промывают
теплой водой до нейтральной реакции по метиловому оранжевому и высушивают, постепенно нагревая до 200 оС.
Применение: для производства стеклопластиков; в качестве связующего при получении минеральной ваты, стекловаты, древесностружечных и древес-
новолокнистых плит, древеснослоистых пластиков; для керамических пресс-порошков; для покрытия металлов, керамики и бетона; для производства химически стойких мастик и замазок, для склеивания металла с керамикой.
С в о й с т в а н о в о л а ч н ы х о л и г о м е р о в.
Термопластичность. Небольшое количество твердого олигомера поме-
стить в металлическую ложечку и осторожно нагреть над электроплиткой до расплавления. Охладив расплав, убедиться, что олигомер вновь затвердевает. Повторить плавление и охлаждение 2-3 раза.
Растворимость. В заранее подготовленные чистые сухие пронумерован-
ные пробирки налить по 3 мл этанола, ацетона и 10 % раствора едкого натра. В каждую пробирку внести по 50-100 мг новолачного олигомера, убедиться в его растворимости.
Литература: [7], [17].
Работа 8. Получение резольных олигомеров
Ц е л ь: ознакомление с условиями синтеза и свойствами резольной смолы.
-
Загрузка реактивов:
фенол (кристаллический) – 2 г;
формалин (35-40 % раствор) – 5 мл;
аммиак (конц.) –1 мл.
Посуда:
пробирки – 3 шт.;
фарфоровая чашечка;
водяная баня.
В ы п о л н е н и е р а б о т ы. В пробирку вносят 2 г фенола, 5 мл
40 % раствора формалина и 1 мл концентрированного аммиака (аммиак вливать медленно!). При нагревании смеси на водяной бане (осторожно) она становится непрозрачной.
Полученную смолу охлаждают, сливают верхний водный слой, а оставшуюся вязкую массу нагревают в течение 1 часа в сушильном шкафу при 75 оС. Полученная резольная смола применяется для изготовления бакелита.
С в о й с т в а р е з о л ь н ы х о л и г о м е р о в.
Растворимость. В пронумерованные чистые сухие пробирки налить по 3 мл этанола, ацетона и 10 % водного раствора едкого натра, внести в каждую пробирку по 50100 мг резольного олигомера, убедиться в его растворимости.
Применение: используют для получения пресс-материалов, формовоч-
ных масс, литых изделий, лаковых и клеевых композиций, газонаполненных материалов.
Литература: [7], [17].
Работа 9. Поликонденсация фталевого ангидрида с глицерином
 n
С6Н4(СО)2О
+ m НОСН2−СНОН−СН2ОН
n
С6Н4(СО)2О
+ m НОСН2−СНОН−СН2ОН
фталевый ангидрид глицерин
• • •─ ООС (С6Н4)СОО − СН2− СН(ОСО)−СН2 −ООС (С6Н4)СОО ─ • • •
Ц е л ь: ознакомление с условиями синтеза полиэфирных полимеров (глифталевых полимеров).
-
Загрузка реактивов:
фталевый ангидрид - 11 г;
глицерин (безв.) - 8,5 г.
Посуда:
стакан фарфоровый (100 мл);
воронка стеклянная;
баня воздушная.
11 г фталевого ангидрида и 8,5 г безводного глицерина (если глицерин водный, навеску соотвотственно увеличивают) помещают в фарфоровый стакан, который плотно прикрывают опрокинутой стеклянной воронкой. Смесь быстро нагревают на воздушной бане до 180 оС и эту температуру поддерживают в течение 2 часов. Затем температуру повышают до 200-220 оС и нагревание продолжают до образования стеклообразной смолы, трудно растворимой в ацетоне - конечного продукта реакции.
Применение: для производства лаков, эмалей, клеев.
Литература: [7], [17].
