
- •Химия, ч. 2. Органическая химия
- •1. Информация о дисциплине
- •Предисловие
- •Место дисциплины в учебном процессе.
- •Содержание дисциплины и виды учебной работы
- •Содержание дисциплины по гос
- •Объем дисциплины и виды учебной работы
- •Раздел 1. Общие вопросы теоретической органической химии
- •1.2. Основные понятия органической химии
- •Раздел 2. Углеводороды
- •2.1. Алифатические углеводороды
- •2.2. Циклические углеводороды
- •Раздел 3. Важнейшие классы производных углеводородов (28 часов)
- •3.1. Гомофункциональные соединения
- •3.2. Гетероциклические и элементоорганические соединения
- •Раздел 4. Высокомолекулярные соединения
- •4.1. Общие представления о высокомолекулярных соединениях (вмс)
- •4.2. Методы синтеза высокомолекулярных соединений
- •4.3. Промышленные органические полимеры
- •Заключение
- •2.2. Тематический план дисциплины
- •2.2.1. Тематический план дисциплины для студентов очной формы обучения
- •2.2.2. Тематический план дисциплины
- •2.2.3. Тематический план дисциплины
- •При использовании информационно-коммуникационных технологий
- •2.5. Практический блок Лабораторные работы
- •3. Информационные ресурсы дисциплины
- •3.1. Библиографический список
- •3.2. Опорный конспект Введение
- •Раздел 1 Общие вопросы теоретической органической химии
- •Основные сырьевые источники органических соединений
- •1.2. Основные понятия органической химии
- •1. Циклоалканы
- •2. Циклоалкены, циклоалкины
- •Вопросы для самопроверки
- •Раздел 2
- •2.1. Алифатические углеводороды
- •Циклические углеводороды
- •Вопросы для самопроверки
- •Раздел 3 Важнейшие классы производных углеводородов
- •3.1. Гомофункциональные соединения
- •Свойства спиртов
- •Простые и сложные эфиры
- •Классификация аминов
- •3.2. Гетероциклические и элементоорганические соединения
- •Вопросы для самопроверки
- •Раздел 4 Высокомолекулярные соединения
- •4.1. Общие представления о высокомолекулярных соединениях
- •4.2. Методы синтеза высокомолекулярных соединений
- •4.3. Промышленные органические полимеры
- •Характеристика некоторых клеев и клеевых композиций представлена в разделе 4.1.1. (пример 7). Вопросы для самопроверки
- •Заключение
- •3.3. Глоссарий
- •3.4. Методические указания к выполнению лабораторных работ предисловие
- •3.4.1. Общие указания
- •3.4.2. Охрана труда и техника безопасности правила техники безопасности при работе в лаборатории оказание первой помощи при несчастных случаях
- •Первая помощь при ожогах и отравлениях
- •Растворители, применяемые для приготовления охлаждающих смесей с твердой углекислотой
- •Методы очистки и выделения органических соединений
- •Определение основных физических констант органических веществ
- •3.4.4. Лабораторные синтезы органических соединений
- •Отчет №
- •6. Выводы по работе. Синтезы азокрасителей
- •Получение полимеров реакцией полимеризации
- •Мономеры и вспомогательные вещества
- •Винилацетат (с4н6о2)
- •Пероксид бензоила (с14н10о4)
- •Получение полимеров реакцией поликонденсации
- •Мономеры и вспомогательные вещества
- •4. Блок контроля освоения дисциплины
- •4.1. Задания на контрольную работу и методические указания к ее выполнению
- •Распределение задач по шифрам для студентов специальности 150501.65
- •Контрольная работа
- •4.1.1. Примеры решения контрольных задач
- •Свойства отечественных полиэпоксидных смол
- •Свойства эпоксидных клеевых соединений в зависимости от природы отвердителя
- •4.2. Текущий контроль
- •Каменноугольная смола является источником…
- •Правильные ответы на тренировочный тест рубежного контроля
- •4.3. Итоговый контроль
- •Приложения
- •1. Основные сырьевые источники органических соединений
- •2. Углеводороды и радикалы (алкилы)
- •6. Краткая характеристика наиболее типичных полимеров, получаемых реакцией поликонденсации и методом полимераналогичных превращений
- •7. Полимерные композиционные материалы, свойства, области применения
- •О8. Свойства исходных соединений, применяемых в синтезах
Первая помощь при ожогах и отравлениях
При термических ожогах необходимо быстро сделать примочку раство-
ром марганцевокислого калия (перманганата) и покрыть обожженное место мазью от ожогов.
1. При ожогах кислотами обожженное место сначала хорошо промывают водой, а затем раствором гидрокарбоната натрия.
2. При ожогах сухими щелочами обожженное место промывают водой, а затем 1 % раствором уксусной кислоты.
3. При попадании на кожу разъедающих органических веществ необ-
ходимо быстро смыть вещество подходящим растворителем, например, спиртом.
4. При попадании в глаз кислоты или щелочи необходимо промыть глаз водой, а затем 2 % раствором борной кислоты в случае попадания щелочи или 1 % раствором гидрокарбоната натрия в случае попадания кислоты.
ОБЩИЕ СВЕДЕНИЯ О РАБОТЕ В ЛАБОРАТОРИИ ОРГАНИЧЕСКОГО СИНТЕЗА
ОБОРУДОВАНИЕ И ТЕХНИКА ЛАБОРАТОРНЫХ РАБОТ
В химической лаборатории наиболее употребительным материалом для изготовления приборов и аппаратов является стекло. Посуда из стекла устойчива к воздействию большинства химических реагентов (за исключением HF и расплавленных щелочей и их концентрированных растворов), легко моется и поддается термической обработке, прозрачна.
При сборке стеклянных приборов отдельные их части обычно соединяют с помощью корковых или резиновых пробок, либо при помощи стеклянных шлифов.
Стандартные шлифы. Большинство лабораторных приборов имеет стандартные взаимозаменяемые конические шлифы. Под словом «шлиф» понимают равномерно отшлифованную поверхность. Две притертые друг к другу отшлифованные стеклянные поверхности представляют собой соединение на шлифах, наиболее употребительные из которых изображены на рис. 6, 7.
Рис. 8. Переход от
нормального НШ 26 к НШ 12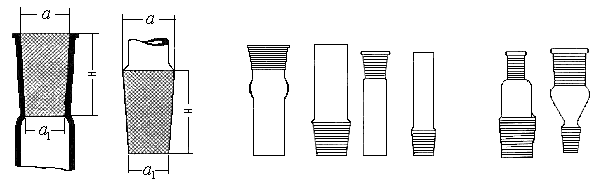
Рис. 6. Конусность
нормального шлифа
Рис.
7. Нормальные шлифы
Соединение на шлифах осуществляется при помощи шлифа-муфты (внешний шлиф) и шлифа-керна (внутренний шлиф). Для точной характеристики указывают максимальный и минимальный диаметры (иногда длину) шлифа, которые обозначаются соответствующими цифрами, например, НШ 29/32, НШ 29/42, НШ 14,5/23, НШ 40/45 и т.д. Обычно достаточно указать меньший диаметр.
Наиболее распространены шлифы малых размеров (НШ 14,5) и больших размеров (НШ 29). Шлифы разных диаметров можно соединить при помощи переходных муфт (рис. 8), смазав их вазелином.
Химическая посуда. Стаканы. В стаканах выполняют вспомогательные работы с водными растворами. Для работы с органическими жидкостями их применяют реже. Они могут служить в качестве сосудов для проведения реакций при температуре не выше 100 оС, которые не нужно изолировать от доступа воздуха и влаги.
Колбы. В лаборатории органического синтеза используют плоскодонные и круглодонные колбы. В плоскодонных колбах Эрленмейера, в основном, хранят и готовят растворы. Их нельзя применять при работах, связанных с высокими температурами и особенно при работе в вакууме. Выше 100 С пользуются круглодонными колбами (рис. 9).

Рис.9. Приборы для проведения синтезов: а – трехгорлая колба с обратным холодильником, мешалкой и капельной воронкой; б – трехгорлая колба с мешалкой, термометром и двурогим форштосом, к которому присоединены обратный холодильник и капельная воронка; в – добавление твердого компонента
Они могут быть снабжены холодильниками, насадками, дефлегматорами, ректификационными колонками и другими вспомогательными деталями, например, хлоркальциевой трубкой и термометром (рис. 10, а - г).

Рис.10. Насадки на шлифах: а – осушительная хлоркальциевая трубка; б – угольник для перегонки; в–насадка Вюрца; г – термометр
Для более сложных операций, в которых одновременно с нагреванием необходимо, например, равномерно перемешивать смеси, постоянно добавлять
один из компонентов по каплям (рис. 9, а) или вводить твердый компонент в определенный момент (рис. 9, в), используют колбы, имеющие 2 – 4 горла. Если нет таких колб, применяют круглодонные колбы со специальными насадками – форштосами (рис. 9, б). Для перегонки при атмосферном давлении применяют колбы Вюрца, снабженные отводной трубкой.
Холодильники. Во избежание потерь низкокипящих компонентов реак-
ционные сосуды снабжают обратными холодильниками, где пары охлаждают-
ся и конденсат возвращается в сосуд. При перегонке конденсатотводят с помо-
щью нисходящих холодильников. Типы наиболее часто рименяемых холодиль
ников изображены на рис. 11 [2]. Простейшим холодильником является обратный воздушный холодильник (рис. 11, а), представляющий собой полую стеклянную трубку и применяемый только при работе с высококипящими жидкостями (Т. кип. больше 150 С). В качестве обратных более эффективны воздушные шариковые холодильники (рис. 11, б).
Холодильник Либиха (рис. 11, в) используется, как правило, в качестве нис-ходящего до 160 С. При перегонке жидкостей с температурой кипения менее 120 С в рубашку этого холодильника подается проточная вода, а в интервале 120…160 С – непроточная.
Шариковый холодильник (рис.11, г) используется только как обратный. Поскольку этот холодильник имеет шаровидные расширения, ток паров в нем
становится турбулентным. Охлаждающее действие такого холодильника значительно выше, чем у холодильника Либиха.
Змеевиковый холодильник (рис. 11, д) никогда не используется как обратный, так как конденсат, который недостаточно хорошо стекает по сгибам змеевика, может быть выброшен из холодильника и послужить причиной
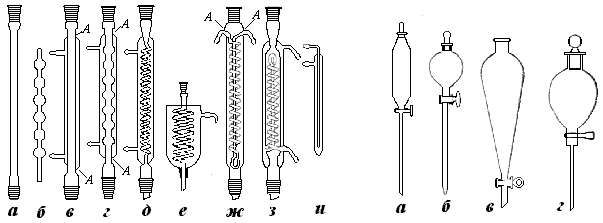
Рис.11. Типы холодильников Рис.12. Капельные (а, б) и делительные
(в, г) воронки
несчастного случая. Змеевиковый холодильник, установленный вертикально, является наиболее эффективным нисходящим холодильником, особенно для низкокипящих веществ. Змеевиковый, так же как и шариковый, холодильник нельзя употреблять в качестве наклонно поставленных холодильников, так как при наклонном положении происходит накапливание конденсата в спирали змеевика или шариках.
Хлоркальциевые трубки. Для предохранения содержимого приборов от доступа влаги из воздуха применяют трубки, заполненные прокаленным хлори-дом кальция или другим поглощающим водяной пар веществом (рис. 10, а).
Капельные и делительные воронки. Для приливания жидкости к реакционной смеси служат капельные воронки – цилиндрические, шарообра-
зные (рис. 12, а, б) или грушевидные, обычно небольшого размера, но снабженные длинной трубкой. Воронки такой же формы, но с более короткой трубкой, изготовленные из толстого стекла, применяют для разделения несмешивающихся жидкостей и для экстракции; они называются делительными воронками (рис. 12, в, г) [2]. В отличие от капельных эти воронки имеют более толстые стеклянные стенки и меньшую длину трубки.
Эксикаторы ─ емкости из толстостенного стекла ─ предназначены для высушивания твердых веществ. Вещество, которое подвергают сушке, на часовом стекле или в чашке Петри помещают в эксикатор на фарфоровую подставку. В качестве осушающего агента применяют безводные хлорид кальция, сульфат магния, сульфат натрия, натронную известь, гидроксид натрия, оксид фосфора (V) и др. Концентрированную серную кислоту также используют для поглощения влаги, остатков спирта, эфира, ацетона, анилина и пиридина.
Сборка приборов. Приборы собирают в соответствии с условиями реакции, а также свойствами исходных и конечных продуктов. Как правило, их обычно собирают из отдельных частей со стандартными шлифами. В тех случаях, когда реакция проводится при нагревании реакционной смеси до кипения, следует пользоваться круглодонными колбами как более прочными и устойчивыми по отношению к температурным воздействиям и толчкам, часто сопровождающим кипение жидкости. Чтобы жидкость равномерно кипела, в колбу кладут «кипелки» – кусочки необожженного фарфора. «Кипелки» можно вносить только в холодную жидкость, так как, попав в жидкость, нагретую до температуры кипения, они вызывают бурное и обильное парообразование, которое может привести к выбросу жидкости из колбы, пожару, несчастному случаю.
Реакционные
колбы заполняют не более, чем на
![]() их объема.
их объема.
Приступая к работе, необходимо убедиться в чистоте химической посуды, которая считается чистой, если на ее стенках вода образует равномерную пленку. Иногда приходится прибегать к химическим методам очистки посуды. Если ее невозможно отмыть водой и органическими растворителями (спирты, ацетон, бензин и др.), то для мытья посуды чаще всего применяют хромовую смесь (бихромат калия, растворенный в концентрированной серной кислоте). Вымытую хромовой смесью посуду ополаскивают водой и сушат.
Измельчение. Проводя химические реакции, вещества следует максима-льно измельчать, так как скорость растворения прямо пропорциональна по-верхности растворяемого вещества.
Методы, используемые при измельчении материалов (дробление, размалы-вание, растирание, просеивание), выбирают в зависимости от механических и химических свойств материала.
Перемешивание. При проведении многих реакций перемешивание применяют, когда постепенно прибавляемое вещество нужно равномерно распределить по всему объему (перевести в раствор или взвесь), или если местное разогревание за счет теплоты реакции может вызвать распад нестойких продуктов. В гетерогенных реакциях (несмешивающиеся друг с другом жидкости или жидкость – твердое вещество) перемешивание необходимо для лучшего протекания процесса, ибо для этих случаев скорость реакции зависит от величины поверхности контактирования веществ.
Встряхивание. Применяют в тех случаях, когда реакционную смесь не требуется нагревать или охлаждать, а также для процессов с участием твердых или жидких веществ, реагирующих без выделения газов или паров.
Нагревание. Нагревание используют для ускорения большинства органических реакций, при выделении и очистке веществ (перегонка, возгонка, растворение, плавление, сушка), при определении физических констант веществ (Т. кип., Т. пл. и т. д.). Большинство органических реакций протекает сравнительно медленно. Для того чтобы достигнуть максимального выхода, увеличивают продолжительность реакции или повышают температуру холо-
реакции. Часто реакционную массу кипятят в колбе, снабженной обратным дильником, при этом температура в процессе реакции остается приблизительно
постоянной.
Прямой нагрев стеклянных сосудов пламенем горелки Бунзена, Теклю или Мекера [2], которая сама всасывает необходимое количество воздуха, применяют редко ввиду малой устойчивости стекла к резким изменениям температуры. По соображениям безопасности прямое пламя не применяют для нагревания горючих жидкостей.
Электрические нагреватели, особенно закрытые электроплитки, также используют для прямого нагрева. Широко используются колбонагреватели, по форме соответствующие нагреваемой колбе.
Нагревательные бани. Бани применяют во всех случаях, когда необхо-димо вести нагревание в течение длительного времени при определенной температуре.
В зависимости от типа теплоносителя различают бани воздушные, паро-
вые, жидкостные (водяные, масляные, глицериновые, силиконовые, парафино-
вые), металлические, солевые, песчаные и т.д. [2].
Воздушные бани используют для нагревания сосудов, содержащих металлический натрий или калий.
Паровые бани очень удобны для перегонки жидкостей, кипящих не выше 80 С.
Жидкостные бани. Водяные бани применяют для нагревания веществ почти до 100 и для перегонки жидкостей, кипящих не выше 80С. Воду в бане можно нагревать газом, электричеством или паром.
Необходимо различать 2 типа нагрева на водяной бане: когда колба погружена в воду (таким путем достигается температура 100 С) и когда колба воды не касается и нагревается только водяным паром (температура при этом немного ниже).
Масляные и парафиновые бани. Масляные бани применяют для нагрева до 250 С, а парафиновые – до 150…200 С. Масло и парафин при температу-рах выше 200 С начинают сильно дымить, поэтому нагревание на таких банях проводят под тягой.
Глицериновые бани можно нагревать не выше 200…220 С, так как при этой температуре глицерин начинает разлагаться с образованием акролеина.
Серная кислота также используется в качестве жидкости для бань (в приборах для определения температуры плавления). Ее можно нагревать до 250…280 С [5].
Песчаная баня представляет собой железную чашку, дно которой покрыто тонким слоем мелкозернистого песка. Баню нагревают либо газом, либо совмещают с закрытой электроплиткой. Песчаные бани прогреваются неравномерно, вследствие чего при работе с ними очень трудно поддерживать даже приблизительно постоянную температуру. Вместо песка можно использо-
вать железные опилки и чешуйчатый графит, который хорошо проводит тепло и не царапает колбы.
Выбор бань определяется свойствами нагреваемого вещества или реакционной смеси, а также температурой, необходимой для их нагревания.
Охлаждение [2]. Для охлаждения до комнатной температуры чаще всего применяют воду. Если не требуется быстро охлаждать, то достаточно погрузить реакционную колбу или стакан в большой сосуд, через который непрерывно протекает холодная вода. В случае сильно экзотермических реакций вода даже при перемешивании не в состоянии отобрать достаточное количество тепла, поэтому ее следует заменить другим охлаждающим агентом.
Для охлаждения до 0 С пользуются льдом. Залогом хорошего охлажде-
ния является тесный контакт охлаждающей поверхности с охлаждающим средством, поэтому лед надо сильно измельчать. Если вещество необходимо охладить до температуры ниже температуры замерзания воды, то обычно используют смеси льда и различных электролитов (табл. 3).
Таблица 3
Охлаждающие смеси со льдом или снегом
Вещество |
Относительное количество |
Предельно низкая температура,С |
|
льда (снега) |
вещества |
||
Na2CO3·10 H2O KCl NH4Cl NaCl NaN03+NH4NO3 NH4Cl+NaNO3 KNO3+KCNS NaNO2 CaCl2·6 H2O |
100 100 100 100 100 100 100 100 49 70 |
20 30 25 33 55+52 13+38 2+112 50 100 100 |
-2 -11 -15 -21,3 -26 -31 -34 -18 -19,7 -54,9 |
Доступным охлаждающим средством является твердая углекислота («сухой лед»), которая используется в смесях с различными органическими растворителями (табл. 4).
Таблица 4
