
- •Химия, ч. 2. Органическая химия
- •1. Информация о дисциплине
- •Предисловие
- •Место дисциплины в учебном процессе.
- •Содержание дисциплины и виды учебной работы
- •Содержание дисциплины по гос
- •Объем дисциплины и виды учебной работы
- •Раздел 1. Общие вопросы теоретической органической химии
- •1.2. Основные понятия органической химии
- •Раздел 2. Углеводороды
- •2.1. Алифатические углеводороды
- •2.2. Циклические углеводороды
- •Раздел 3. Важнейшие классы производных углеводородов (28 часов)
- •3.1. Гомофункциональные соединения
- •3.2. Гетероциклические и элементоорганические соединения
- •Раздел 4. Высокомолекулярные соединения
- •4.1. Общие представления о высокомолекулярных соединениях (вмс)
- •4.2. Методы синтеза высокомолекулярных соединений
- •4.3. Промышленные органические полимеры
- •Заключение
- •2.2. Тематический план дисциплины
- •2.2.1. Тематический план дисциплины для студентов очной формы обучения
- •2.2.2. Тематический план дисциплины
- •2.2.3. Тематический план дисциплины
- •При использовании информационно-коммуникационных технологий
- •2.5. Практический блок Лабораторные работы
- •3. Информационные ресурсы дисциплины
- •3.1. Библиографический список
- •3.2. Опорный конспект Введение
- •Раздел 1 Общие вопросы теоретической органической химии
- •Основные сырьевые источники органических соединений
- •1.2. Основные понятия органической химии
- •1. Циклоалканы
- •2. Циклоалкены, циклоалкины
- •Вопросы для самопроверки
- •Раздел 2
- •2.1. Алифатические углеводороды
- •Циклические углеводороды
- •Вопросы для самопроверки
- •Раздел 3 Важнейшие классы производных углеводородов
- •3.1. Гомофункциональные соединения
- •Свойства спиртов
- •Простые и сложные эфиры
- •Классификация аминов
- •3.2. Гетероциклические и элементоорганические соединения
- •Вопросы для самопроверки
- •Раздел 4 Высокомолекулярные соединения
- •4.1. Общие представления о высокомолекулярных соединениях
- •4.2. Методы синтеза высокомолекулярных соединений
- •4.3. Промышленные органические полимеры
- •Характеристика некоторых клеев и клеевых композиций представлена в разделе 4.1.1. (пример 7). Вопросы для самопроверки
- •Заключение
- •3.3. Глоссарий
- •3.4. Методические указания к выполнению лабораторных работ предисловие
- •3.4.1. Общие указания
- •3.4.2. Охрана труда и техника безопасности правила техники безопасности при работе в лаборатории оказание первой помощи при несчастных случаях
- •Первая помощь при ожогах и отравлениях
- •Растворители, применяемые для приготовления охлаждающих смесей с твердой углекислотой
- •Методы очистки и выделения органических соединений
- •Определение основных физических констант органических веществ
- •3.4.4. Лабораторные синтезы органических соединений
- •Отчет №
- •6. Выводы по работе. Синтезы азокрасителей
- •Получение полимеров реакцией полимеризации
- •Мономеры и вспомогательные вещества
- •Винилацетат (с4н6о2)
- •Пероксид бензоила (с14н10о4)
- •Получение полимеров реакцией поликонденсации
- •Мономеры и вспомогательные вещества
- •4. Блок контроля освоения дисциплины
- •4.1. Задания на контрольную работу и методические указания к ее выполнению
- •Распределение задач по шифрам для студентов специальности 150501.65
- •Контрольная работа
- •4.1.1. Примеры решения контрольных задач
- •Свойства отечественных полиэпоксидных смол
- •Свойства эпоксидных клеевых соединений в зависимости от природы отвердителя
- •4.2. Текущий контроль
- •Каменноугольная смола является источником…
- •Правильные ответы на тренировочный тест рубежного контроля
- •4.3. Итоговый контроль
- •Приложения
- •1. Основные сырьевые источники органических соединений
- •2. Углеводороды и радикалы (алкилы)
- •6. Краткая характеристика наиболее типичных полимеров, получаемых реакцией поликонденсации и методом полимераналогичных превращений
- •7. Полимерные композиционные материалы, свойства, области применения
- •О8. Свойства исходных соединений, применяемых в синтезах
4.2. Методы синтеза высокомолекулярных соединений
Основные методы получения полимеров. Синтетические полимеры получают из низкомолекулярных продуктов (мономеров) по реакциям полиме-
ризации, поликонденсации, а также путем химиических превращений других природных и синтетических полимеров.
Полимеризация ─ реакция соединения молекул мономера, протекающая за счет разрыва кратных связей и не сопровождающаяся выделением низкомолекулярных продуктов, т.е. не приводящая к изменению элементарного состава мономера.
В реакцию полимеризации вступают в основном ненасыщенные моно-меры, у которых двойная связь находится между углеродными атомами (этилен → полиэтилен; винилхлорид → поливинилхлорид) или между углеродом и любым другим атомом (формальдегид → полиметиленоксид). В первом случае образуются карбоцепные полимеры, во втором - гетероцепные.
Ускоряется процесс полимеризации веществами, легко распадающимися на свободные радикалы, – инициаторами, а тормозится соединениями, быстро реагирующими с радикалами, - ингибиторами (замедлителями). Ингибиторы применяются для предотвращения самопроизвольной полимеризации некото-рых мономеров в процессе их хранения, например при хранении стирола.
В качестве примера нами приведена реакция полимеризации сопря-женного диенового углеводорода (бутадиен -1,3), которая, как и у олефинов (см. стр. 33), осуществляется под влиянием катализаторов или инициаторов.
Дивинил (бутадиен -1,3) – легко сжижающийся газ с характерным непри-ятным запахом. Является одним из важнейших мономеров для производства синтетических каучуков и латексов, пластмасс и других органических соеди-нений.
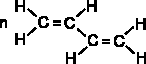
Диены отличаются высокой реакционной способностью (по сравнению с мономерами, содержащими изолированные двойные связи) и их молекулы присоединяются преимущественно в положение 1,4 с образованием длинных неразветвленных макромолекул:

Реакция полимеризации бутадиена -1,3 с образованием продукта 1,4 - присоединения представлена ниже :
|
→ |
|
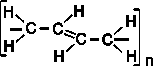
бутадиен -1,3 полибутадиен
Однако наиболее ценные в практическом отношении продукты получаются при стереорегулярной полимеризации диеновых углеводородов по схеме 1,4- присоединения с образованием цис- конфигурации полимерной цепи, т.е. цис-полибутадиена. |
цис-полибутадиен |
Мономером для получения синтетического каучука является изопрен или
2- метилбутадиен -1,3 (см. стр. 34) – летучая бесцветная жидкость с Ткип.= 34,1 оC. Изопрен также является основной структурной единицей природного (натурального) каучука.
Натуральный каучук получают из млечного сока (латекса) каучуконо-сного дерева гевеи, растущего в тропических лесах Бразилии. При нагревании без доступа воздуха каучук распадается с образованием диенового углеводо-рода – 2- метилбутадиена-1,3 или изопрена.
Каучук – это стереорегулярный полимер, в котором молекулы изопрена соединены друг с другом по схеме 1,4- присоединения с цис- конфигурацией полимерной цепи :
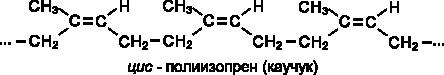
Молекулярная масса натурального каучука колеблется в пределах от 7.104 до 2,5.106.
транс- Полимер изопрена также встречается в природе в виде гуттаперчи.
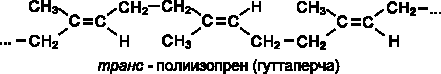
Натуральный каучук обладает уникальным комплексом свойств: высокой текучестью, устойчивостью к износу, клейкостью, водо- и газонепроницаемо-стью.
В 1932 году С.В. Лебедев разработал способ синтеза синтетического каучука на основе бутадиена, получаемого из спирта. И лишь в пятидесятые го-
ды отечественные ученые осуществили каталитическую стереополимеризацию
диеновых углеводородов и получили стереорегулярный каучук, близкий по свойствам к натуральному каучуку. В настоящее время в промышленности выпускают каучук, в котором содержание звеньев изопрена, соединенных в положении 1,4, достигает 99 %, тогда как в натуральном каучуке они составляют 98%. Кроме того, в промышленности получают синтетические каучуки на основе других мономеров, таких как изобутилен и хлоропрен (см. стр. 33, 37), и натуральный каучук утратил свое монопольное положение.
Поликонденсация - процесс образования полимеров химическим взаимо-действием молекул мономеров, сопровождающийся выделением низкомолеку-лярных веществ (воды, хлороводорода, аммиака, спирта и т.д.).
В отличие от реакции полимеризации состав элементарных звеньев поликонденсационных полимеров не соответствует составу исходного мономера.
В реакции участвуют мономеры, содержащие функциональные группы или активные атомы (например, в фенолах), способные взаимодействовать между собой (─ОН, ─СООН, ─NН2, галогены и др.). При наличии в молекуле мономера двух функциональных групп, способных реагировать между собой, образуется гомополимер линейного строения, реакция в этом случае называется гомополиконденсацией:
nH2N─ R─СООН → Н─ [─HN─ R─СО─]n─ОН + (n-1) H2O.
аминокислота полиамид
В случае разнотипных мономеров имеет место гетерополиконденсация. Например, волокно нейлон получается из продукта взаимодействия адипино-вой кислоты с гексаметилендиамином в метаноле, причем на первой стадии ре-акции образуется соединение с той же функциональностью:
H2N(CH2)6NH2 + HOOC(CH2)4COOН →
гексаметилен- адипиновая
диамин кислота
→ H2N(CH2)6NHOC(CH2)4COOH + H2O
димер
При дальнейшей поликонденсации происходит взаимодействие между отдельными фрагментами будущего полимера с образованием в итоге поли-амида:
H2N─(CH2)6─NHOC─(CH2)4─COOH + H2N─(CH2)6─NHOC─(CH2)4─COOH →
→ [─NH(CH2)6NH–OC(CH2)4CO–] n + nH2O
полиамид
Увеличение числа функциональных групп хотя бы в одном из реагиру-ющих соединений до трех и более приводит к образованию полимеров про-странственного строения, поликонденсация в этом случае называется про-странственной.
Особенностью реакции поликонденсации является ее обратимый ха-рактер – скорость образования полимера на каждой стадии взаимодействия мономеров равна скорости его деструкции (разрушения) при достижении со-стояния равновесия. Для получения полимеров с большой молекулярной масс-сой необходимо удалять выделяющиеся в процессе реакции низкомолеку-лярные продукты. Для этого или повышают температуру реакционной среды, что приводит к понижению вязкости реакционной смеси ( в ходе реакции поликонденсации вязкость естественно увеличивается), или процесс ведут при пониженном давлении, а значит, при более низкой температуре, при которой полимер не разрушается.
Продукты реакции поликонденсации в итоге представляют собой слож-ную смесь, в состав которой могут входить фракции полимергомологов, низ-комолекулярные соединения, некоторое количество остаточного мономера и даже побочные продукты.
По реакции поликонденсации получают фенолоальдегидные смолы, по-лиамиды, простые и сложные полиэфиры и другие полимеры. Наиболее изучена и имеет практическое значение реакция фенолов с формальдегидом (первые продукты конденсации фенола с формальдегидом были получены в 1878 г. А. Байером в кислой среде). Исключительно большое влияние на свойства образующихся полимеров оказывают такие факторы как тип альдегида, функциональность использованного фенола, рН реакционной среды и мольное соотношение исходных веществ. Например, если в кислой среде количество формальдегида не превышает эквимолекулярного по отношению к фенолу, образуются термопластичные смолообразующие олигомеры линейного стро-ения – новолаки. Если же формальдегид взят хотя бы в небольшом избытке и реакцию проводят в щелочной среде, образуются резолы – сильно развет-вленные термореактивные олигомеры.
При создании определенных условий резольное и новолачное состояния взаимообратимы.
Классификация и особенности химических реакций полимеров.
Методом химических превращений полимеров получают новые высоко-молекулярные соединения из готовых полимеров. Этот способ особенно удо-бен в тех случаях, когда синтез нового полимера непосредственно из низко-молекулярных веществ невозможен, или не существует мономера заданного строения, или когда синтезировать новый полимер технологически удобнее, изменив структуру уже имеющегося полимера. Различают следующие наиболее типичные химические реакции полимеров:
реакции функциональных групп или полимераналогичные превращения;
реакции сшивания (структурирования) – макромолекулярные реакции;
реакции деструкции.
Краткое описание этих процессов дано в разделе 4.1.1 (пример 6).

 .
.