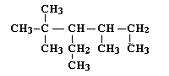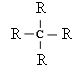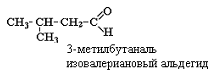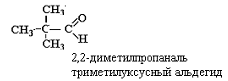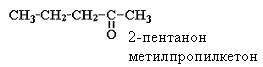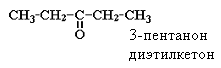- •Химия, ч. 2. Органическая химия
- •1. Информация о дисциплине
- •Предисловие
- •Место дисциплины в учебном процессе.
- •Содержание дисциплины и виды учебной работы
- •Содержание дисциплины по гос
- •Объем дисциплины и виды учебной работы
- •Раздел 1. Общие вопросы теоретической органической химии
- •1.2. Основные понятия органической химии
- •Раздел 2. Углеводороды
- •2.1. Алифатические углеводороды
- •2.2. Циклические углеводороды
- •Раздел 3. Важнейшие классы производных углеводородов (28 часов)
- •3.1. Гомофункциональные соединения
- •3.2. Гетероциклические и элементоорганические соединения
- •Раздел 4. Высокомолекулярные соединения
- •4.1. Общие представления о высокомолекулярных соединениях (вмс)
- •4.2. Методы синтеза высокомолекулярных соединений
- •4.3. Промышленные органические полимеры
- •Заключение
- •2.2. Тематический план дисциплины
- •2.2.1. Тематический план дисциплины для студентов очной формы обучения
- •2.2.2. Тематический план дисциплины
- •2.2.3. Тематический план дисциплины
- •При использовании информационно-коммуникационных технологий
- •2.5. Практический блок Лабораторные работы
- •3. Информационные ресурсы дисциплины
- •3.1. Библиографический список
- •3.2. Опорный конспект Введение
- •Раздел 1 Общие вопросы теоретической органической химии
- •Основные сырьевые источники органических соединений
- •1.2. Основные понятия органической химии
- •1. Циклоалканы
- •2. Циклоалкены, циклоалкины
- •Вопросы для самопроверки
- •Раздел 2
- •2.1. Алифатические углеводороды
- •Циклические углеводороды
- •Вопросы для самопроверки
- •Раздел 3 Важнейшие классы производных углеводородов
- •3.1. Гомофункциональные соединения
- •Свойства спиртов
- •Простые и сложные эфиры
- •Классификация аминов
- •3.2. Гетероциклические и элементоорганические соединения
- •Вопросы для самопроверки
- •Раздел 4 Высокомолекулярные соединения
- •4.1. Общие представления о высокомолекулярных соединениях
- •4.2. Методы синтеза высокомолекулярных соединений
- •4.3. Промышленные органические полимеры
- •Характеристика некоторых клеев и клеевых композиций представлена в разделе 4.1.1. (пример 7). Вопросы для самопроверки
- •Заключение
- •3.3. Глоссарий
- •3.4. Методические указания к выполнению лабораторных работ предисловие
- •3.4.1. Общие указания
- •3.4.2. Охрана труда и техника безопасности правила техники безопасности при работе в лаборатории оказание первой помощи при несчастных случаях
- •Первая помощь при ожогах и отравлениях
- •Растворители, применяемые для приготовления охлаждающих смесей с твердой углекислотой
- •Методы очистки и выделения органических соединений
- •Определение основных физических констант органических веществ
- •3.4.4. Лабораторные синтезы органических соединений
- •Отчет №
- •6. Выводы по работе. Синтезы азокрасителей
- •Получение полимеров реакцией полимеризации
- •Мономеры и вспомогательные вещества
- •Винилацетат (с4н6о2)
- •Пероксид бензоила (с14н10о4)
- •Получение полимеров реакцией поликонденсации
- •Мономеры и вспомогательные вещества
- •4. Блок контроля освоения дисциплины
- •4.1. Задания на контрольную работу и методические указания к ее выполнению
- •Распределение задач по шифрам для студентов специальности 150501.65
- •Контрольная работа
- •4.1.1. Примеры решения контрольных задач
- •Свойства отечественных полиэпоксидных смол
- •Свойства эпоксидных клеевых соединений в зависимости от природы отвердителя
- •4.2. Текущий контроль
- •Каменноугольная смола является источником…
- •Правильные ответы на тренировочный тест рубежного контроля
- •4.3. Итоговый контроль
- •Приложения
- •1. Основные сырьевые источники органических соединений
- •2. Углеводороды и радикалы (алкилы)
- •6. Краткая характеристика наиболее типичных полимеров, получаемых реакцией поликонденсации и методом полимераналогичных превращений
- •7. Полимерные композиционные материалы, свойства, области применения
- •О8. Свойства исходных соединений, применяемых в синтезах
4.1.1. Примеры решения контрольных задач
Пример 1 (к задачам 1-10). Назвать по рациональной и ИЮПАК номенклатурам углеводород. Написать уравнения реакций дегидрирования данного углеводорода с отщеплением одной молекулы водорода. На примере одного из алкенов написать формулы пространственных (геометрических) изомеров. Какой из алкенов не имеет геометрических изомеров?
|
В основе названия разветвленного алкана лежит название входящего в его конструкцию нормального алкана с наиболее длинной углерод-ной цепью. При этом углеводород с разветвлен- ной цепью pассматpивают как продукт замеще- ния атомов водоpода в ноpмальном алкане угле- |
водоpодными pадикалами.
Порядок построения названия разветвленного алкана:
1). Выбрать в молекуле главную углеродную цепь. Во-первых, она долж-на быть самой длинной. Во-вторых, если имеются две или более одинаковые по длине цепи, то из них выбирается наиболее разветвленная. Например, в моле-куле есть 2 цепи с одинаковым числом (7) атомов С:

В случае (а) цепь имеет 1 заместитель, а в (б) – 2. Поэтому следует выб-рать вариант (б).
2). Пронумеровать атомы углерода в главной цепи так, чтобы атомы С, связанные с заместителями, получили возможно меньшие номера. Поэтому ну-мерацию начинают с ближайшего к ответвлению конца цепи. Например:

3). Назвать все радикалы (заместители), указав впереди цифры, обозна-чающие их местоположение в главной цепи. Если есть несколько одинаковых заместителей, то для каждого из них через запятую записывается локант – (ци-фра, обозначающая местоположение заместителя). Количество заместителей указывается приставками ди-, три-, тетра-, пента- и т.д. (например, 2,2-диметил или 2,3,3,5-тетраметил).
4). Названия всех заместителей расположить в алфавитном порядке (так установлено последними правилами ИЮПАК). 5). Назвать главную цепь углеродных атомов, т.е. соответствующий нормальный алкан. |
|
|
|
По рациональной номенклатуре углеводороды с развет-вленной углеродной цепью рассматривают как производные ро-доначальника ряда, в молекуле которого один или несколько атомов водорода замещены на радикалы. |
|
В ряду алканов, к которому относит-ся данный углеводород (все связи простые), родоначальником ряда является метан СН4. Поэтому в основе названия будет слово «метан», перед которым приписывают наз-вания заместителей, т.е. радикалов. |
|
Выбрав в соединении наиболее замещенный атом углерода (под цифрой 3 – в этом случае все радикалы нам знакомы), можно определить с какими радикалами он связан. У третьего атома углерода три заместителя (этил-, втор.бутил- и трет.бутил-). Перечисляют радикалы по мере их усложнения, простейшие содержат меньшее число углеродных атомов и имеют цепочку нор-мального строения. Количество одинаковых заместителей указывается приставками ди-, три-, тетра-.
Таким образом, по рациональной номенклатуре углеводород будет называться как этилвтор.бутилтрет.бутилметан.
Реакции дегидрирования этилвтор.бутилтрет.бутилметана приводят к образованию алкенов и могут быть представлены следующими уравнениями:

Из трех возможных алкенов первый (3,5,5-триметил-4-этилгексен-1) не имеет стереоизомеров, так как в нем у одного из двоесвязанных углеродных атомов имеются одинаковые заместители (два атома водорода); для двух дру-гих этот вид изомерии имеет место.
Следовательно формулы пространственных изомеров для симм.метил-диэтилтрет.бутилэтилена (рациональная номенклатура) будут иметь следую-щий вид:
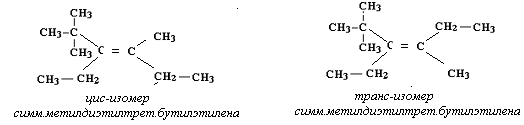
Пример 2 (к задачам 11-20). Напишите структурные формулы всех возможных изомеров карбонильных соединений с общей формулой С5C10О. На-зовите эти соединения.
К карбонильным соединениям относятся альдегиды и кетоны, которые имеют в своем составе одинаковую функциональную группу =С=О. Для альдегидов и кетонов характерна структурная изомерия.
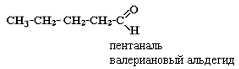
Решать эту задачу начнем с написания углеродных цепочек. Постепенно укорачивая главную цепь углеродных атомов и нумеруя атомы углерода, кото-рые входят в состав главной цепи, получим для класса альдегидов четыре вида углеродных цепей, содержащих пять углеродных атомов, для кетонов – три вида углеродных цепочек.
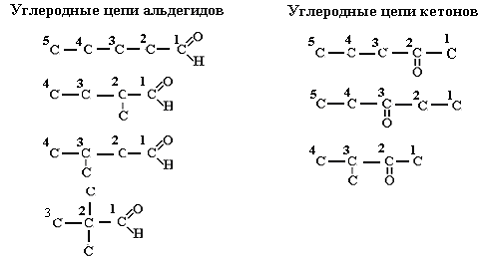
На следующем этапе к каждому атому углерода приписываем необходимое количество водородных атомов (вспомним, что валентность углерода в органических соединениях постоянна и равна четырем) и в результате получим формулы структурных изомеров альдегидов и кетонов, отличающихся строением углеродного скелета: |
|
||
|
для альдегидов: |
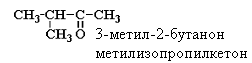
для кетонов: |
|
|
|
|
|
Кроме изомерии углеродного скелета в ряду альдегидов и кетонов наблюдается межклассовая изомерия с кетонами (пентаналь и пентанон-2), а для класса кетонов имеет место изомерия по положению карбонильной группы (начиная c C5):
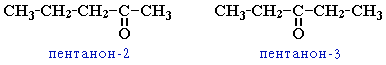
Пример 3 (к задачам 21-30). Изобразить в уравнениях реакций химиче-ские превращения. Дать названия всем соединениям и назвать реакции, которыми Вы воспользовались при решении данного перехода:
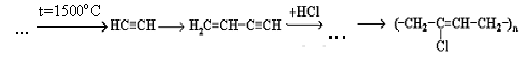
Зная о методах переработки природных газов и обратив внимание на условия, в которых получается ацетилен, используем реакцию пиролиза метана (t=1500 оС) – это один из промышленных способов получения ацетилена:
2СН4 → СН≡СН + 3Н2.
Следующей будет реакция димеризации ацетилена, которая протекает под действием водно-аммиачного раствора CuCl:
Винилацетилен является важным промежуточным продуктом в произ-
водстве масло- и бензостойкого синтетического хлоропренового каучука. Присоединение галогеноводорода к винилацетилену осуществляется по прави-
лу Марковникова, т.е. водород присоединяется к наименее гидрогенизирован-
ному атому углерода тройной связи, образуя при этом хлоропрен – мономер в реакции синтеза хлоропренового каучука. При полимеризации хлоропрена получаем хлоропреновый каучук или полихлоропрен.
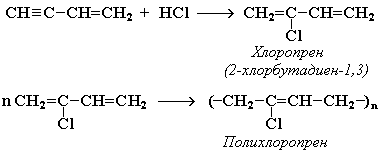
Пример 4 (к задачам 31 - 40). Какие углеводороды образуются при алки-лировании бензола пропиленом и хлористым метилом? Напишите уравнения реакций, укажите условия протекания данных реакций.
Алкилирование бензола осуществляют в присутствии кислот Льюиса (хлоридов алюминия и цинка, трифторида бора и др.). В качестве алкилирую-
щих агентов используют спирты или алкены, как видно из реакции взаимодей=
ствия бензола с пропиленом, приведенной ниже:
Процесс алкилирования бензола хлористым метилом представлен следующим уравнением:
Метилбензол
В лаборатории алкилирование по Фриделю-Крафтсу имеет ограниченное применение, так как обычно при этой реакции образуются смеси продуктов.
Пример 5 (к задачам 41-50). Получить диэтилкарбинол из этана, используя в заданном порядке следующие реакции: бромирование, дегидробро-мирование, оксосинтез, магнийорганический синтез. Назвать основные продукты реакций.
Бромирование этана – реакция радикального замещения атомов водорода на галоген (SR):

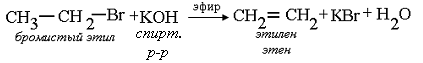
Дегидробромирование (элиминирование) бромистого этила – реак-ция отщепления галогенводородов от галогенпроизводных алканов (Е):
Оксосинтез – один из основных промышленных методов получения альдегидов в газовой или жидкой фазе в присутствии кобальтовых катализато-ров при температуре 100-200 оС и давлении 10,13-20,26 МПа:
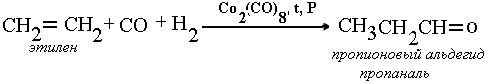
Магнийорганический синтез (см. прил. 4).
а). Получение «реактива Гриньяра» (RMgX) взаимодействием металлического магния с алкилгалогенидами в среде безводных растворителей (эфир, петролейный эфир, третичные амины):
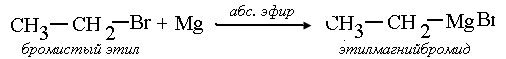
Реактивы Гриньяра – чрезвычайно активные реагенты, легко вступающие в реакцию соединениями, содержащими активный водород (вода, спирт, амми-ак, первичные и вторичные амины и пр.), в их числе и альдегиды.
б). Взаимодействие «реактива Гриньяра» с альдегидом с образованием промежуточных продуктов реакции (алкоголяты спиртов общей формулы R-OMgBr):
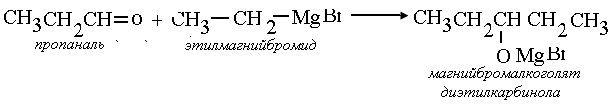
в). Гидролиз магнийбромалкоголята заканчивается образованием вторичного спирта – диэтилкарбинола:

Реакция магнийорганических соединений с карбонильными представляет собой способ синтеза первичных, вторичных и третичных спиртов (в зависимости от строения исходного альдегида или кетона).
Пример 6 (к задачам 51 - 70). Реакции функциональных групп. Полимер-аналогичные превращения полимеров - метод синтеза ВМС. Напишите примеры реакций. Виды деструкции полимеров и их стабилизация.
Различают следующие наиболее типичные химические реакции полимеров:
реакции функциональных групп или полимераналогичные превращения;
реакции сшивания (структурирования) – макромолекулярные реакции;
реакции деструкции.
Полимераналогичные превращения (реакции элементарных звеньев по-лимерной цепи).
Особое значение приобрел синтез полимеров из высокомолекулярных соединений, содержащих реакционноспособные группы. Этот способ получе-ния полимеров применяют в тех случаях, когда исходные мономера неизве-стны, или они не полимеризуются.
Химические превращения, при которых происходит изменение химиче-ского состава без изменения формы и длины макромолекулярной цепи поли-мера, т.е. без изменения степени полимеризации, называют полимер-аналогичными превращениями или реакциями элементарных звеньев полимер-ной цепи.
В реакции полимераналогичных превращений могут вступать соедине-ния с самыми разнообразными функциональными группами: –СОН; –СОСl; –СОNН2; –SО3Н; –SОСl и пр. На этом методе основаны промышленные способы получения эфиров целлюлозы (ацетат целлюлозы, нитрат целлюлозы и др.) пу-тем ее этерификации. При этом гидроксильные группы целлюлозы замещаются на –ОСОСН3 и –ОNО2.
Кислотным или щелочным омылением поливинилацетата, например, по-лучают поливиниловый спирт:
 ∙∙∙
– СН2
– СН – СН2
– СН – СН2
– СН – ∙∙∙ ОН-
∙∙∙
– СН2
– СН – СН2
– СН – СН2
– СН – ∙∙∙ ОН-
│ │ │
ОСОСН3 ОСОСН3 ОСОСН3
∙∙∙ – СН2 – СН – СН2 – СН – СН2 – СН – ∙∙∙
│ │ │
ОН ОН ОН
Поливиниловый спирт используют для получения довольно прочных пленок и волокон. Поливиниловый спирт пластифицируют гидроксилсодержа-
щими соединениями (этиленгликоль, глицерин), получая при этом высокоэла-
стичный материал в виде каучукоподобных листов, которые в течение долгого времени остаются гибкими в широком диапазоне теператур. При обработке поливинилового спирта масляным альдегидом получают поливинилбутираль, основным применением которого является изготовление безосколочного стекла: тонкий слой пластифицированного полимера склеивает два листа стекла. Эластичный и плотный поливинилбутираль, обладающий высокой адгезией к стеклу, хорошо служит для этой цели.
Макромолекулярные реакции.
Если при химических превращениях полимеров изменяется степень по-лимеризации (а иногда и структура основной цепи полимера), то такие реакции называют макромолекулярными. Большинство этих реакций ведет к образо-ванию пространственных структур с одновременным возрастанием молекуляр-ной массы полимера (межмолекулярные реакции).
В процессе полимеризации или поликонденсации обычно получают по-лимеры линейного или разветвленного строения, а при изготовлении из таких полимеров изделий специально проводят реакции сшивания (структуриро-вания) – реакции образования поперечных (мостиковых) связей между макро-молекулами, приводящие к получению полимеров сетчатого, пространст-венного строения. В резиновой промышленности эти реакции называются вулканизацией, в промышленности пластических масс – отверждением. Образо-вание поперечных химических связей в полимерах между атомами углерода соседних макромолекул возможно как без добавления других веществ, так и при помощи соединений, специально вводимых в систему. Такие вещества называются вулканизирующими агентами или отвердителями. В качестве вулканизирующего агента обычно используется сера, с этой же целью можно применять селен, теллур и даже кислород воздуха.
При небольшом числе поперечных связей (редкая сетка) получаются мяг-кие эластичные продукты; по мере увеличения мостиковых связей жесткость полимерного материала повышается. К получению совершенно твердого мате-риала приводит образование очень частой сетки.
Процесс вулканизации каучука, например, проводят при нагревании с се-рой до 130-140 оС, при этом синтетический каучук приобретает необходимые физико-механических свойства: высокую прочность, эластичность, стойкость к действию растворителей и агрессивных химических сред. Атомы серы в про-цессе вулканизации присоединяются по месту разрыва некоторых двойных связей и линейные молекулы каучука "сшиваются" в более крупные трехмер-ные молекулы с образованием резины, которая по прочности значительно превосходит невулканизированный каучук:
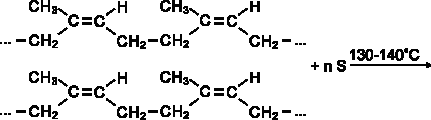

Наполненные активной сажей каучуки в виде резин используют для изго-товления автомобильных шин и других резиновых изделий.
Реакции деструкции.
Реакциями деструкции называются реакции разрыва химических связей в главной цепи макромолекулы.
В зависимости от природы агента, вызывающего разрыв связей в цепи, различают физическую и химическую деструкцию. Физическая деструкция, в свою очередь, подразделяется на термическую, механическую, фотохимии-ческую и деструкцию, вызванную влиянием ионизирующих излучений. Химическая деструкция протекает под действием различных химических агентов.
В процессе переработки и при эксплуатации изделий из полимерных ма-териалов они подвергаются различным видам деструкций одновременно. По-этому можно назвать процесс нагревания полимера, сопровождающийся одно-временным окислением, термоокислительной деструкцией, а реакцию химической деструкции, протекающей на свету, – фотоокислительной деструкцией.
Термическая деструкция. Химические реакции полимеров при повы-шенных температурах протекают как с разрывом, так и без разрыва связей гла-вной цепи макромолекулы. Это зависит от природы полимера. Так, например, полиэтилен, полистирол, полиметилметакрилат при нагревании деструкти-руются, а при нагревании поливинилхлорида отщепляются молекулы газо-образного хлористого водорода с образованием либо поливинилена – линей-ного продукта с системой сопряженных связей:
∙∙∙ – СН = СН – СН = СН – ∙∙∙ ,
либо нерастворимого продукта пространственного строения.
Стойкость полимеров к химическому разложению, проходящему под действием энергии теплового движения, называют термостойкостью (термо-стабильностью, термоустойчивостью). Термостойкость не следует отождест-влять с теплостойкостью. Так как при нагревании могут разрываться хими-ческие связи, то важнейшим фактором, определяющим термостойкость поли-мера, является энергия связи между атомами в главной цепи. Наиболее устой-чивой к термическим воздействиям является углерод–углеродная связь.
На прочность связи С–С влияет степень разветвленности полимеров и, конечно, заместители в макромолекулярной цепочке. Разветвленные полимеры менее термостойки, чем неразветвленные, так как у разветвленных полимеров связи С–С между боковыми цепями и главной цепью менее прочны, чем связи
С–С в главной цепи. Увеличение числа заместителей в цепи способствует уменьшению энергии связи С–С, поэтому полиэтилен является по сравнению с полипропиленом более термостойким материалом. Так температура, при кото-рой полимер теряет половину своей первоначальной массы в течение первых 30 минут при нагревании (по данным Мадорского и Страуса) у полипропилена – 387 оС, у полиэтилена она несколько выше – 404 оС.
Отсюда следует, что наименее термостойкими карбоцепными полиме-рами будут полиизопрен (325 оС), полиметилметакрилат (327 оС), полиизо-бутилен (348 оС). Более термостойким по сравнению с этими соединениями будет полистирол (364 оС) и еще в большей степени – полиэтилен. Гетеро-цепные высокомолекулярные соединения, содержащие в цепи связи С–О, на-пример целлюлоза и ее эфиры (ацетат целлюлозы, нитрат целлюлозы, этил-целлюлоза), имеют невысокую термостойкость.
К нетермостойким полимерам относятся поливинилхлорид и полиакри-лонитрил, однако продукты, образующиеся при их термической обработке и имеющие систему сопряженных связей, являются термо- и огнестойкими.
Механическая деструкция – это разрыв цепи, протекающий под влия-нием различных механических воздействий, которым полимер подвергается при переработке (измельчение, вальцевание и пр.) и при эксплуатации изделий. Например, при интенсивном механическом измельчении целлюлозы, крахмала, полистирола и других полимеров, а также при течении расплавов и растворов имеет место снижение молекулярной массы полимера. Механическая деструк-ция полимеров обусловлена флуктуациями внутренней энергии, т.е. откло-нениями внутренней энергии от равномерного распределения. Накопленные флуктуации обеспечивают направленность процесса разрыва химических свя-зей в главной цепи полимера.
Большую роль при переработке и эксплуатации изделий играют механо-химические реакции – реакции превращения механической энергии в химии-ческую. С ними связаны явления усталости полимерных материалов, получе-ние привитых и блоксополимеров и т.д.
Фотохимическая деструкция – процесс деструкции, протекающий под действием излучений. Процесс облучения некоторых полимеров УФ-светом при повышенных температурах, сопровождающийся деполимеризацией с выде-лением мономера, называется фотолизом. Под действием излучений высокой энергии, например при действии рентгеновских лучей, радиоактивных излуче-ний и пучков электронов, полимеры претерпевают различные химические пре-вращения, что нужно учитывать при ренгеноструктурном и электронографи-ческом исследовании полимеров.
Химическая деструкция протекает под действием различных хими-ческих агентов, таких, как вода, кислоты, амины, спирты, кислород воздуха и др. Наиболее важными видами химической деструкции являются окисли-тельная деструкция и деструкция под действием протоносодержащих веществ (гидролиз, ацидолиз, аминолиз и т.д.).
Стойкость полимера к действию окислителей зависит от его строения и от наличия легкоокисляющихся групп и связей в макромолекуле. Энергичным окисляющим агентом является озон, под действием которого на свету натуральный каучук подвергается сильнейшей деструкции. Эту особенность каучука необходимо учитывать при хранении и эксплуатации изделий из данного полимера. Более стойкими к окислению являются карбоцепные насыщенные полимеры (полиэтилен, полистирол, полиизобутилен). При комнатной температуре они практически не окисляются, деструкция возможна только при нагревании.
В наибольшей степени подвержены окислительной деструкции гетеро-цепные соединения и соединения, имеющие ацетильные связи, например целлюлоза, которая деструктируется под действием кислорода воздуха.
Гидролиз – деструкция, протекающая под действием воды или водных растворов кислот и солей и сопровождающаяся присоединением воды по месту разрыва связи.
По степени подверженности гидролизу соединения, содержащие ацетальные (целлюлоза), амидные(белки), эфирные связи, располагаются в следующий ряд:
│ │ │
– СН – О – > – С – NН – > – С – О – С – > – С – О – С –
│ ║ ║ │ │ │
О – О О
ацетальная амидная сложная эфирная простая эфирная
Ацидолиз– деструкция под действием карбоновых кислот с образованием более низкомолекулярных продуктов:
∙∙∙–HN–(CH2)n –NH–CО– (CH2)m –CO–∙∙∙ + НООС–(CH2)4 –СООН →
→ ∙∙∙–HN–(CH2)n –NHCО– (CH2)4 –COОН + НООС–(CH2) m –СО–∙∙∙
Аминолиз– деструкция, протекающая под действием аминов. Примером может служить взаимодействие полиамидов при нагревании с гексаметиленди-
амином:
∙∙∙–HN–(CH2)n –NH–CО– (CH2)m –CO–∙∙∙ + NH2 –(CH2)6 – NH2 →
→ ∙∙∙–HN–(CH2)n –NH2 + NH2 –(CH2)6 – NH–CО– (CH2)m –CO–∙∙∙
Пример 7 (к задачам 51 - 70). Клеи. Компоненты клеевых композиций, их назначение. Технология склеивания. Адгезия и когезия.
Клеи (адгезивы)- композиции на основе веществ, способных соединять (склеивать) различные материалы, благодаря образова-нию между их поверхностями и клеевой прослойкой прочных адгезионных связей.
Соединение материалов при помощи клея обусловлено адгезией и когезией.
Адгезиея – способность клея связываться со склеиваемой поверхностью и прочно на ней удерживаться.
Когезия – сила взаимодействия между частицами клея, определяющая его прочность в сухом состоянии.
Процесс адгезии является довольно сложным и в настоящее время имеет ряд теоретических представлений, которые по-разному рассматривают сущ-ность адгезии. Условно процессы адгезии объясняются следующими теориями: химической, электрической, диффузионной и механической.
Взаимодействие склеиваемого материала и клея можно рассматривать как суммарный эффект всех видов адгезии.
Клеи могут содержать отвердители и добавки, например, наполнители, растворители, стабилизаторы, пластификаторы, эластификаторы. Добавками модифицируют свойства клея – липкость, вязкость, скорость отверждения, сохранность и жизнеспособность.
По типу основы клеи подразделяются на органические и неорганические. Они могут быть жидкие (растворы, эмульсии, суспензии), пастообразные или твёрдые.
Клеи, полученные на основе клеящих полимеров, относятся к группе природных. В качестве примера можно назвать животные (на основе материалов, обогащенных коллагеном) или казеиновые клеи (на основе казеина или продуктов его переработки). Природные клеи, как и другие типы клеев, могут содержать модифицирующие добавки, растворители, антисептики, стабилизаторы, смолы, повышающие липкость, например канифоль.
Широкое распространение, благодаря возможности легкого и напра-вленного изменения свойств, получили синтетические клеи, изготовленные на основе синтетических мономеров, олигомеров, полимеров или их смесей.
Синтетические клеи делят на термореактивные и термопластичные. В первой группе клеев при склеивании изменяется их химическая структура, и они из пластического состояния необратимо переходят в стеклообразное или эластическое в результате протекания химической реакции (полимеризации или поликонденсации). У второй группы клеев изменений в химической струк-туре при склеивании не наблюдается; они затвердевают в результате удаления растворителя или застывания расплава.
Технология склеивания заключается в возможности прочно соеди-нять между собой различные материалы, сохраняя при этом их свойства. То об-стоятельство, что при склеивании материалы сохраняют свои свойства, являет-ся уникальным достоинством этого способа соединения. Но к особенностям технологии склеивания следует отнести не только способность прочно соеди-нить две детали между собой, но и придать клеевому соединению особые свойства, например, антикоррозийность. Клей может выполнять роль электро-изолятора в месте соединения двух металлов, или клеевое соединение может оказаться полезным в борьбе с вибрацией конструкции, благодаря тому, что оно способно поглотить или отфильтровать колебания определённой частоты.
Благодаря исключительно интересному сочетанию свойств нашли широ-кое применение во многих отраслях промышленности клеящие материалы на основе различных эпоксидных смол.
Эпоксидные смолы представляют собой олигомеры или индивидуальные низкомолекулярные продукты, превращающиеся в процессе отверждения в эпоксидные сшитые полимеры. Они утверждаются с небольшими усадками как при обычных, так и при повышенных температурах без выделения побочных веществ, образуя продукты с хорошими физико-механическими и диэлектриче-скими характеристиками и высокой адгезией к металлам и многим неметал-лическим материалам.
Первые сведения об эпоксидных смолах появились в 1943 г., но лишь в
1946 г. швейцарская фирма «Ciba» выпустила эпоксидный клей Аральдит 1. В настоящее время известны многочисленные эпоксидные клеевые композиции, пригодные для работы в широком интервале температур, обладающие высокой прочностью, длительным сроком службы и удобной технологией применения.
Эпоксидные клеи пригодны для соединения большого числа различных материалов в строительстве, в автомобильной, авиационной, судостроитель-ной, электро- и радиотехнической промышленности, машиностроении, при-боростроении и многих других отраслях народного хозяйства.
Интересны работы по применению эпоксидных клеев для соединения живых тканей. Первые реальные попытки применить клей для этих целей при-вели к созданию препарата «остеопласт» на основе эпоксидной смолы. В на-стоящее время остеопласт находит применение для лечения переломов длин-ных трубчатых костей и в костнопластических операциях. Проведены иссле-дования по использованию остеопласта при фиксации позвоночника и при костносуставном туберкулезе. Предложен пломбировочный материал для кли-нической стоматологии на основе эпоксидных смол.
Осуществлен выпуск «универсальных» клеящих материалов, способных склеивать материалы разной природы, кроме полиэтилена, органического стек-ла, фторопластов, лавсана, причем без применения нагревания. Такие клеи выпускаются не только для технических, но и для бытовых целей.
Все эпоксидные клеи разделены на две основные группы: клеи холодного отверждения и клеи горячего отверждения. Такое деление в известной мере условно, так как не требующие нагревания композиции могут отверждаться и при повышенных температурах, что во многих случаях приводит к повышению их прочностных характеристик и улучшению других свойств. Однако основное различие между клеями этих двух групп состоит в том, что клеи горячего от-верждения применяются преимущественно в качестве конструкционных клеев повышенной теплостойкости при склеивании силовых изделий ответственного назначения из металлов и неметаллических материалов. Клеи холодного отверждения используют главным образом для склеивания неметаллических материалов (пластмассы, резины, ткани, фарфор, керамика, бумага и др.) и при-клеивания их к различным металлам.
Большинство клеевых эпоксидных смол получают из эпихлоргидрина и дифенилолпропана в среде органического растворителя (толуол, ксилол, их смеси с бутанолом или циклогексаноном). Сначала конденсацией фенола с ацетоном в присутствии кислотного катализатора получают дифенилолпропан:
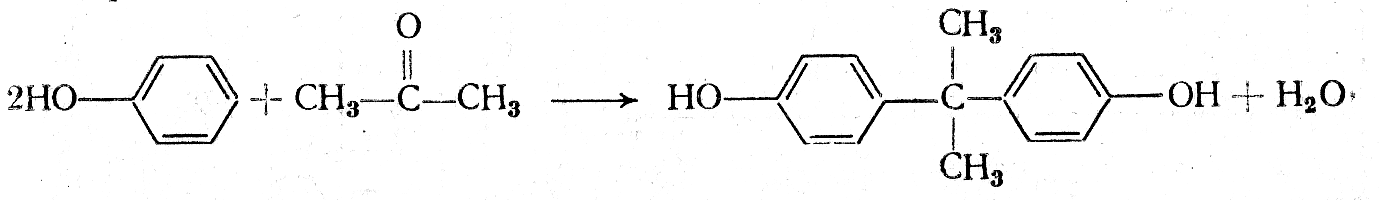
Фенол Ацетон Дифенилолпропан
4,4'-Диоксидифенил-2,2-пропан
Реакция получения смолы протекает по следующей схеме:
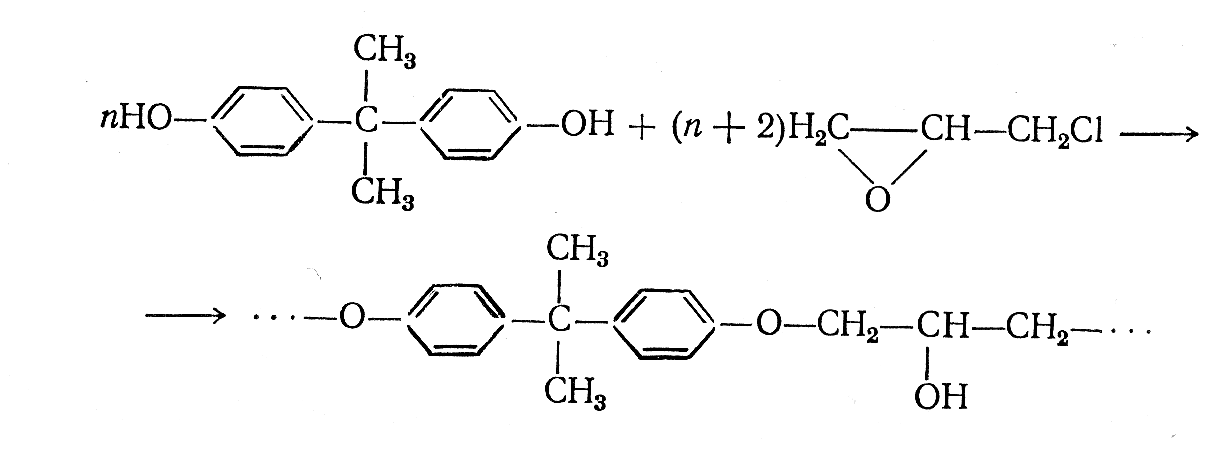
Некоторые характеристики отечественных полиэпоксидных смол приве-дены в таблице 6.
При использовании эпоксидных смол в клеевых композициях в их состав добавляют отвердители. Отверждение эпоксидных смол может происходить как в результате поликонденсации эпоксида с полифункциональным соедине-
нием — отвердителем (полиамины, низкомолекулярные полиамиды, изоциана-
ты,
Таблица 6