
- •Свойства металлов и сплавов, их измерители
- •Строение металлов и сплавов, их кристаллизация
- •§ 2. Производство и характеристика чугунов Исходное сырье для выплавки чугуна
- •Классификация, ассортимент и маркировка чугунов
- •Чугунные отливки и трубы
- •Ферросплавы
- •§ 3. Производство и характеристика сталей Сырьевые материалы для выплавки стали и способы ее производства
- •Химический состав стали
- •Строение стального слитка и металлургические методы повышения его качества
- •Виды термической и химико-термической обработки стали
- •Классификация и ассортимент стали
- •§ 4. Стальной прокат и металлические изделия Общие сведения и классификация продукции прокатного производства
- •Сортамент стального проката
- •Сортамент металлоизделий промышленного назначения
- •Условия хранения и транспортирования стального проката и металлоизделий
- •§ 5. Цветные металлы и сплавы на их основе
- •Легкие металлы
- •Тяжелые металлы
- •Тугоплавкие металлы
- •Драгоценные металлы
- •§ 6. Неорганические и металлические порошковые материалы и изделия на их основе Значение и применение порошковых материалов и изделий
- •Способы получения и характеристики металлических порошков
- •Aсортимент и маркировка металлических и неорганических порошков
- •Методы получения изделий порошковой металлургии
- •§ 1. Общие сведения о строительных материалах
- •Свойства строительных материалов и изделий
- •§ 2. Природные каменные материалы Значение и классификация природных каменных материалов
- •Классификация и основные свойства важнейших горных пород
- •Материалы и изделия из природного камня
- •Условия хранений и транспортирования материалов и изделий из природного камня
- •§ 3. Стекло и стеклоизделия Общие сведения о стекле и стеклоизделиях
- •Листовые стенломатериалы
- •Троительные изделия из стекла
- •Условия хранения и транспортирования стекла и стеклоизделий
- •§ 4. Керамические материалы и изделия Общие сведения о керамических материалах и их классификация
- •С тоновые керамические материалы
- •Керамические изделий для облицовки и отделки
- •Керамические материалы и изделия различного назначения
- •Условия хранения и трас"ортирования керамических материалов и изделий
- •§ 5. Минеральные вяжущие вещества и материалы на их основе
- •Материалы и изделия на основе минеральных вяжущих веществ
- •Условия хранения и траспортирования минеральных вяжущих веществ и материалов на их основе
- •6. Органические вяжущие вещества и материалы на их основе Состав, свойства и основные виды органических вяжущих веществ
- •§ 7. Лесные и бумажные материалы Значение, состав и свойства древесины
- •Классификация лесных материалов
- •Круглые лесоматериалы
- •Пиломатериалы
- •1 А & л и ц а 14. Маркировка пиломатериалов
- •Изделия и конструкции из древесшны
- •Сырье, полуфабрикаты и производство бумажной продукции
- •Классификация и ассортимент бумажной продукции
- •3.2. Показатели качества товаров
- •3.3. Требования, предъявляемые к товарам
- •3.4. Факторы и условия, влияющие на качество товаров
- •2.3. Ассортимент товаров
- •2.4. Артикулы и прейскурантные номера товаров
- •Глава 2. Классификация и ассортимент товаров
- •Глава 3.
- •3.4. Факторы и условия, влияющие на качество товаров
- •Глава 5. Основные свойства материалов и изделий
- •§ 1. Неорганические кислоты, щелочи и соли
- •Ассортимент, применение, хранение и перевозка кислот
- •§ 2.Пластмассы Общие сведения о полимерах 9) /
- •Сырьевые пластмассы
- •Пленочные полимерные материалы
- •Листовые пластмассы
- •Газонаполненные пластмассы
- •Условия хранения и транспортирования пластмасс
- •§ 3. Каучуки, резина и резиновые
- •Классификация, ассортимент и маркировка резиновых технических изделий
- •Условия хранения и транспортирования каучуков и резиновых технических изделий
- •§ 4. Текстильные волокна и материалы Классификация текстильных волокон и нитей
- •Характеристики текстильных волокон и нитей, их измерители
- •Важнейшие виды натуральных волокон
- •§ 5. Лакокрасочные материалы Назначение, состав и классификация лакокрасочных материалов
- •Условные обозначения лакокрасочных материалов и покрытий
- •Основные лакокрасочные материалы
- •Вспомогательные и подсобные лакокрасочные материалы
- •Условия хранения и транспортирования лакокрасочных материалов
Строение металлов и сплавов, их кристаллизация
"V/ о ' Внутренним строением металлов называется строение
и взаимное расположение их атомов, а также более крупная структура, видимая в микроскоп или невооруженным глазом.
Металлы по внутреннему строению представляют собой совокупность нейтральных атомов, положительно или отрицательно заряженных ионов и свободных электронов, образующих так называемый «электронный газ». Наличие «электронного газа» обусловливает высокую электро- и теплопроводность металлов, а взаимосвязь свободных электронов между собой и с ионами создает прочную связь, называемую металлической. Специфика металлической связи делает металлы пластичными (ковкими).
Кроме природы атомов на свойства металлов влияют характер связи между атомами, расстояние между ними и порядок их расположения.
Все металлы в твердом состоянии имеют кристаллическое строение, т. е. их атомы (ионы) расположены в строгом, периодически повторяющемся порядке, образуя ,'в пространстве атомно-кристаллическую решетку (в противоположность аморфным твердым телам, атомы которых расположены в пространстве хаотично).
Порядок расположения атомов у различных металлов неодинаков. Обычно он определяется простыми ха-
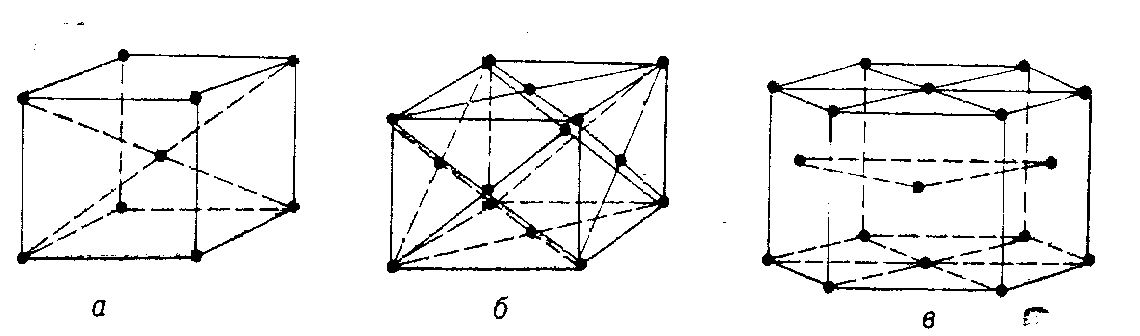
Рис. 6. Порядок расположения атомов в простых реше-ках:
а—объемно-центрированной кубической (9 атомов); б—гранецентрирован-ной кубической (14 атомов); в —гексагональной плотноупакованной (17 атомов).
рактерными для большинства металлов (рис. 6) или сложными кристаллическими решетками. Линии на рис. 6 условные. Атомы 'в действительности колеблются возле положений равновесия, т. е. в узлах кристаллической решетки. Расстояние между атомами в кристаллической решетке измеряется в ангстремах (1А==10~9 нм). У большинства металлов расстояние между атомами находится в пределах 0,28—6,8 нм.
Наименьший объем кристалла, дающий представление об атомной структуре металла во всем объеме, называется элементарной кристаллической ячейкой.
Получаемые обычным способом металлы представляют собой поликристаллические тела, состоящие из множества элементарных ячеек, ориентированных относительно друг друга самым различным образом. Ячейки имеют неправильную форму и называются кристаллитами, или зернами. Если сочетание элементарных ячеек правильное, по расположению атомов повторяющее элементарную ячейку, то образовавшееся тело называется монокристаллом.
Металлические сплавы, как и металлы, имеют кристаллическое строение. При этом в зависимости от взаимодействия компонентов они подразделяются на твердые растворы, химические соединения и механические смеси.
Твердые растворы образуются тогда, когда при сплавления атомы одного элемента в разных количествах входят в кристаллическую решетку другого элемента, не изменяя в значительной мере ее формы. Элемент, сохранивший форму своей решетки, называется растворителем, а элемент, атомы которого вошли в эту решет- • ку,—растворенным. По размещению атомов растворенного элемента в решетке растворителя различают твер-
дые растворы замещения (атомы растворенного элемента располагаются в узлах решетки растворителя) и твердые растворы внедрения (атомы растворенного элемента находятся между атомами растворителя и узлами его решетки).
Если входящие в состав твердого раствора замещения компоненты имеют близкое строение решеток и атомов, то такие элементы могут образовывать непрерывный ряд твердых растворов, т. е. количество замещенных атомов может изменяться от 0 до 100 %.
При этом считается, что растворителем является тот элемент, содержание которого в сплаве более 50 %.
Растворы внедрения образуются элементами, сильно отличающимися строением решетки и размерами атомов.Твердые растворы являются гомогенными (однородными) сплавами, так как их структура представляет собой одинаковые по составу и свойствам зерна. Свойства твердых растворов ib значительной степени могут отличаться от свойств входящих в него компонентов. Все металлы в той или иной степени могут растворяться один в другом, образуя твердые растворы.
Химические соединения образуются при химическом взаимодействии атомов компонентов сплава, сопровождающемся значительным тепловым эффектом. При этом кристаллическая решетка химического соединения и все его свойства могут резко отличаться от решетки и свойств компонентов. В огличие от твердых растворов химические соединения обычно образуются между компонентами, имеющими большое различие в электронном строении атомов. Типичными примерами химических соединений являются соединения магния с оловом, свинцом, сурьмой, висмутом, серой, селеном, теллуром и др. По своей структуре они гомогенны.
Химические соединения металлов называются интерметаллическими (интерметаллидами), а соединения металлов с неметаллами (нитридами, гидридами, борида-ми, карбидами), обладающие металлической связью,— металлическими соединениями.
Механические смеси образуются тогда, когда при затвердении расплава атомы его компонентов не перемешиваются, а кристаллизуются в характерную каждому решетку. Структура таких сплавов гетерогенна (неоднородна) и представляет собой смесь кристаллов компонентов сплава, сохранивших свою структуру.
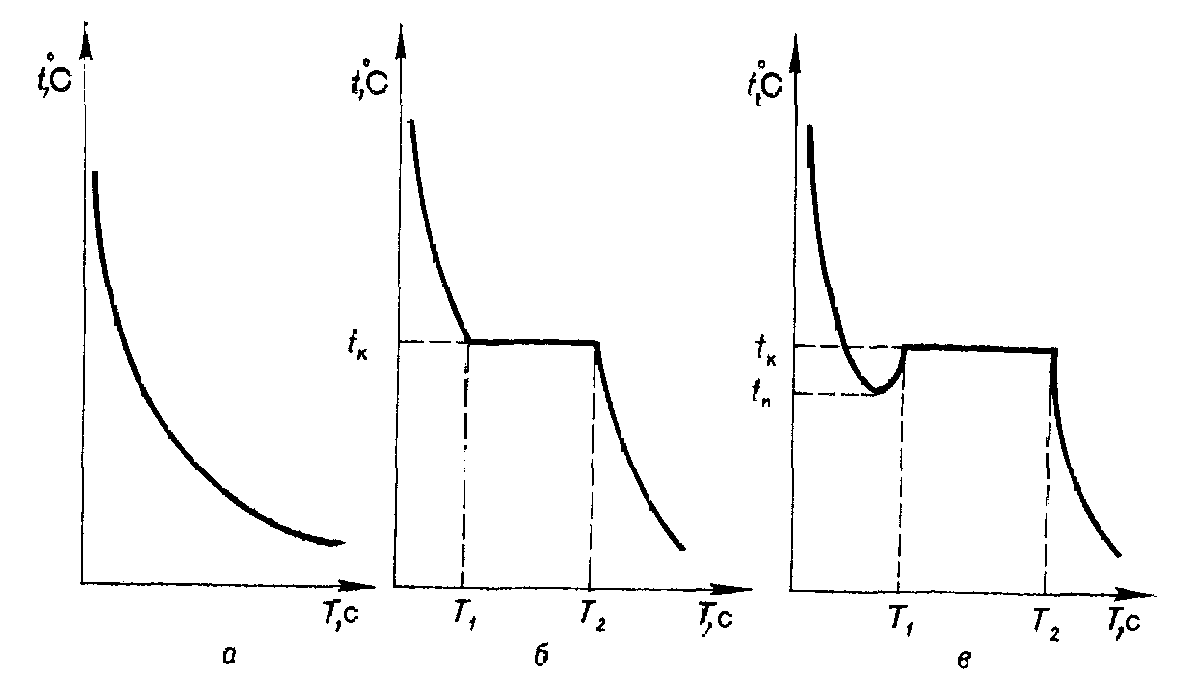
Рис. 7. Кривые охлаждения аморфного (а), кристаллического тела (б) и металлов (в), где /„ fn—температура кристаллизации и переохлаждения, "С; (Ti—Та) —время кристаллизации, с.
Строение кристаллического тела обусловливает следующие особенные их свойства по сравнению с аморфными:
различие свойств монокристаллов в различных направлениях, т. е. анизотропность, или векториальность, свойств;
наличие плоскостей скольжения, приложение внешних сил приводит к скольжению (сдвигу) одной плоскости относительно другой;
•существование критической температуры при затвердевании или плавлении, при которой происходит переход из жидкого (расплавленного) состояния в твердое или наоборот.
Переход металла из жидкого состояния в твердое называется кристаллизацией, а из твердого в жидкое — плавлением. Если образование кристаллов происходит из жидкости при ее охлаждении, то этот процесс называется первичной кристаллизацией, если образование кристаллов идет в твердом состоянии тела,—вторичной кристаллизацией.
Процессы кристаллизации графически изображают кривыми, строящимися в координатах температура — время (рис. 7).
Явление переохлаждения в кристаллизующемся металле объясняется тем, что в период затвердевания про-
исходит резкие снижение подвижности атомов, вследствие чего скачкообразно изменяется его внутренняя энергия. Это сопровождается выделением тепла, которое подогревает жидкую ванну и некоторое время (7'!—Тч) удерживает ее температуру постоянной, пока жидкость полностью не закристаллизуется.
Степень переохлаждения тем больше, чем больше скорость охлаждения.
Русский ученый-металлург Д. К. Чернов в 1878 г. установил, что процесс кристаллизации состоит из нескольких стадий. Первая стадия — образование зародышей (центров) кристаллизации. На последующих стадиях из этих центров образуются дендриты (древовидные образования), которые, срастаясь, образуют зерна (кристаллиты). При этом они не имеют правильной геометрической формы, так как в местах соприкосновения растущих кристаллов рост граней прекращается.
Величина зерна металла — важнейшая характеристика, которая определяет все основные его свойства. Мелкозернистый металл имеет более высокие характеристики твердости, прочности, ударной вязкости, но у него пониженная электропроводность, хуже магнитные свойства.
Размер зерна зависит от количества центров кристаллизации и скорости роста кристаллов (скорости охлаждения). Чем больше центров кристаллизации и меньше скорость их роста, тем меньше будет зерно.
Образование центров кристаллизации может происходить самопроизвольно или на имеющихся в жидком металле частицах примесей, что используется при модифицировании — введении в жидкий металл примесей (модификаторов).
На образование центров кристаллизации, а следовательно, и величину зерна влияет степень переохлаждения tv—i-n (см. рис. 7). Чем больше степень переохлаждения, тем больше центров кристаллизации и мельче образующееся зерно.
_ s. Способы изменения структуры и свойств металлов У в твердом состоянии
Изменение структуры и свойств металлов производят и без его расплавления. Для этого используют три характерных для металлических веществ явления: аллотропию, пластическую деформацию и рекристаллизацию.
Аллотропия (полиморфизм)—способность металлов
в твердом состоянии иметь различное кристаллическое строение (вид решетки). Процесс перехода одного вида решетки в другой называется аллотропическим, или полиморфным, превращением. Определенный тип решетки, характерный для металла в твердом состоянии и существующий в определенном интервале температур и давления, называется модификацией (аллотропической формой). Модификации металлов обозначают начальными буквами греческого алфавита: а, |3, у и др.
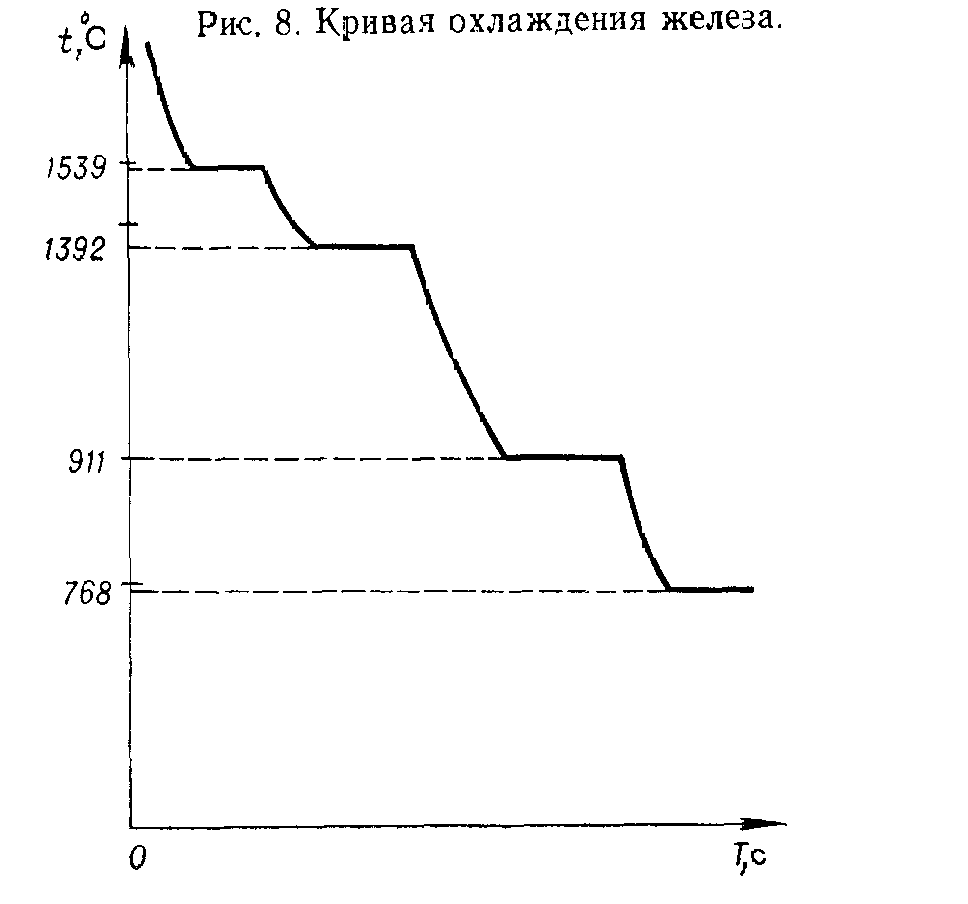
Известны модификации железа, кобальта, титана, олова, марганца, лития и др. Для железа характерны два аллотропических превращения: Fea^Fey. При температуре менее 910 °С и в интервале от 1392 до 1539 °С железо имеет объемно центрированную решетку (Ред), а в интервале температур от 911 до 1392 °С — гранецент-рированную решетку (Fey). На рис. 8 переход железа из одной модификации в другую отмечен соответствующими горизонтальными площадками. При температуре 768 °С аллотропических изменений не происходит. Ниже этой температуры железо магнитно, выше — немагнитно. Температуры 768 °С, 911°С, 1392 °С и 1539 °С называются критическими.
При нагревании железа и переходе Pea в Fey происходят зарождение и рост новых зерен другой формы и размера. Как правило, при этом получаются более мелкие, равноосные зерна, которые при охлаждении, т. е. превращении Fey в Fea, сохраняют свою форму и размеры. Металл получается с более мелкими и равномерными по размеру зернами. Следовательно, при постоянном давлении стоит только нагреть металл до такой температуры, при которой осуществляется переход из одной модификации в другую, а затем охладить его, как атомы, перестроившись из одной решетки в другую, придадут новую форму и размеры зернам.
Процессы, связанные с аллотропическими превращениями железа, широко используются при термической обработке стали и чугуна.
В некоторых случаях аллотропические превращения могут приводить и к разрушению металла. Например, олово при охлаждении ниже температуры —18 °С превращается в порошок, известный под названием «оловянная чума».
Аллотропические превращения можно искусственно затормозить или вовсе не допустить путем быстрого охлаждения металла или добавки в него других элементов.
Пластическая деформация—это изменение размеров и формы металлов под действием приложенных сил и сохранение их после прекращения воздействия (в противоположность упругой деформации, устраняющейся после прекращения действия внешних сил).
В результате пластической деформации металл становится более прочным, твердым и менее пластичным. Происходит это вследствие нарушения строения кристаллической решетки, что затрудняет дальнейшую пластическую деформацию. Явление упрочения металла при пластическом деформировании называется наклепом.
Пластическая деформация сопровождается также изменением и более крупной структуры — формы и размеров зерен. При деформировании в одном направлении (например, при прокатке) зерна получаются вытянутыми. Такую структуру называют волокнистой. Это явление в ряде случаев нежелательно, так как делает тело анизотропным, т. е. свойства его вдоль волокон отличаются от свойств поперек их.
Волокнистость устраняется нагревом (для устранения наклепа до температуры 300—400 °С). При этом обра
зуются новые, отличительные от исходных, равновесные зерна металла. Такой процесс называется рекристаллизацией, а температура его протекания — температурой рекристаллизации.I Методы исследования структуры металлов и сплавов
Внутреннее строение, или структуру, металлов и их дефекты изучают с помощью макроструктурного, микроструктурного, магнитного, люминесцентного, ультразвукового, рентгеновского н ^-Дефектоскопического методов анализа.
Макроструктура—это строение металла, видимое невооруженным глазом или при небольшом увеличении с помощью лупы. Макроструктурный анализ используют для выявления формы и расположения зерен в литом металле, направления волокон в поковках и штамповках, местонахождения, размеров и форм нарушения сплошности, дефектов сварки, оценки толщины поверхностного слоя в изделиях, подвергнутых специальной поверхностной обработке, и др. Его осуществляют просмотром отшлифованной, отполированной и протравленной поверхности металлического изделия или макрошлифа (вырезанного из заготовки или металлоизделия темплета), поверхность которого шлифуют и протравливают.
Микроструктурный анализ — это исследование структуры металлов и сплавов с помощью микроскопов с увеличением от 1500 до 100000. Его осуществляют посредством изучения микрошлифов — вырезанных из металлоизделия или заготовки образцов, поверхность которых шлифуют, полируют и подвергают травлению специальными реактивами. При использовании электронных микроскопов рассматривают тонкий прозрачный слепок с микрошлифа — фольгу, или реплику.
В последнее время для исследования структуры и свойств металлов широко применяются методы фракто-графии, позволяющие исследовать строение изломов, т. е. поверхностей, образующихся в результате разрушения металлоизделий или заготовок. Изломы изучают посредством макро- и микроструктурного анализа.
Магнитный метод (магнитная дефектоскопия) применяется для выявления трещин, волосовин, раковин и других дефектов, находящихся на поверхности (или близко около нее) изделий из ферромагнитных материалов. Сущ-
ность метода заключается в намагничивании изделия. Затем на поверхность наносится магнитный порошок окиси железа или его суспензия в керосине. Частицы порошка под действием магнитного потока, рассеивающегося в месте расположения дефекта, ориентируются по силовым линиям. В результате отчетливо выделяются даже самые мелкие дефекты.
Люминесцентный метод (люминесцентная дефектоскопия) используется для выявления поверхностных дефектов изделий (микротрещин). Он основывается на свойстве некоторых органических веществ светиться под действием ультрафиолетовых лучей. Сущность метода заключается в нанесении на поверхность изделия специального флуоресцирующего раствора и ее освещении ультрафиолетовым светом. Проникающий в микротрещины раствор под действием лучей светится, тем самым позволяя их выявить.
С помощью ультразвукового метода (ультразвуковая дефектоскопия) выявляют дефекты, расположенные глубоко в толще металла. Для этого используются ультразвуковые дефектоскопы, с помощью которых через толщу металла пропускают пучок ультразвуковых волн и контролируют их прохождение. Любая несплошность металла нарушает нормальное распространение волн, что можно увидеть на экране имеющегося в приборе осциллографа.
Рентгеновский метод (рентгеновская дефектоскопия) применяется для контроля литых, кованых и штампованных деталей, а также сварных соединений. Он заключается в просвечивании деталей рентгеновским излучением и фиксировании выходящего излучения на специальной светочувствительной пленке. При этом темные места на пленке свидетельствуют о наличии дефектов в исследуемых деталях.
Разновидностью рентгеновского метода является у-де-фектоскопия.
Од Коррозия и методы защиты от нее
•^6 ^ Коррозией называется разрушение металла вследст-J-- вие его взаимодействия с окружающей средой.
Если металл корродирует сильно, то его называют активным, если слабо,— пассивным.
В зависимости от механизма разрушений коррозию

подразделяют на химическую и электрохимическую. Химической коррозией называют процессы разрушения металла, происходящие в среде сухих газов или жидкостей, не проводящих электрический ток (масло, бензин, керосин). Химическая коррозия характеризуется только окислительными процессами. Электрохимическая коррозия происходит в жидкостях, проводящих электрический ток,— электролитах. В этом случае процесс коррозионного разрушения обусловлен прохождением электрического тока.
По виду агрессивной среды коррозию подразделяют на атмосферную, морскую, речную, почвенную, коррозию в электролитах (кислотах, щелочах, солях) и др. Определяют коррозию и по характеру разрушения металла (рис. 9). При этом сплошная коррозия характерна только для однородных металлов.
Различают также коррозию под напряжением, возникающую в результате действия коррозионной среды и напряжения растяжения.
Для защиты металлов от коррозии применяют ряд методов. Различают активную и пассивную защиту. К методам активной защиты металлов от коррозии относятся легирование, протекторная защита, рациональное конструирование, ингибитирование, удаление компонентов, стимулирующих коррозию, и другие, к методам пассивной защиты — нанесение защитных металлических и неметаллических покрытий.
Так, легирование стали коррозионно-стойкими металлами позволяет значительно сократить потери, сохранить ее качественные характеристики. Известно, что нелегированные стали кородируют практически при любых климатических условиях, причем скорость коррозии — 140— 1200 г/(м2.год).
Протекторная защита заключается в присоединении к защищаемому металлу другого металла с более низ-
ким электрохимическим потенциалом (чаще всего магния или цинка). Как протектор металл ускоренно корро-дирует, сохраняя в неприкосновенности защищаемое изделие. Этот метод особенно эффективен для защиты труб, проложенных под землей.
Рациональное конструирование изделий с целью защиты их от коррозии предполагает уменьшение поверхности и особенно горизонтальных плоскостей, где скопляется влага, сокращение количества соединений и др. Здесь, особенно на болтах или заклепках, металл корро-дирует особенно сильно.
Ингибитирование—это метод, предполагающий использование веществ, подавляющих коррозию. Такие вещества путем физической абсорбции или химических реакций, блокируют поверхность металла или создают на нем защитный слой. Наиболее широко ингибиторы применяются на нефтеперерабатывающих предприятиях для снижения коррозионной активности охлаждающих жидкостей (воды, антифризов). При хранении и транспортировании чувствительных приборов, сверхточного инструмента ингибиторы насыщают своими парами находящийся внутри упаковки воздух и осаждаются на металлы в виде тончайшей пленки.
Металлические защитные покрытия используются для защиты стали. Их наносят гальваническим осаждением, металлизацией, распылением, погружением в расплав, напылением в вакууме, диффузией. Для покрытий изделий и деталей применяют цинк, кадмий, алюминий, олово, свинец, никель, хром, медь, а также латунь и бронзу. Погружая такие детали в горячие подкисленные растворы хроматов калия и натрия, производят пассивирование покрытий. В результате замедляется их коррозия. Такие покрытия переливаются всеми цветами, что является типичным признаком высококачественной антикоррозионной защиты.
Разновидностью металлических защитных покрытий является также наложенный на поверхность детали лист металла (меди, алюминия), имеющего более высокие антикоррозионные свойства. Наложение такого металла осуществляется прокаткой, а процесс называется плакированием.
Для создания неметаллических защитных покрытий наиболее широко используются лакокрасочные материалы. Их доля среди средств пассивной защиты составляет
70—80%. Они отличаются универсальностью применения, простотой использования. Однако необходима тщательная предварительная подготовка поверхности.
К неметаллическим защитным покрытиям относятся также окисные и фосфатные пленки. Окисные пленхи получают оксидированием (кипячением детали в водном растворе сильного окислителя). При этом детали приобретают синий или черный цвет. Фосфатные пленки получают обработкой деталей смесями фосфорной кислоты и ее солей.
Кроме того, в качестве неметаллических защитных покрытий широко используются пластмассы, смазочные материалы, смолы, полимерные пленки, резина, соединения кремния и др.
Если наряду с защитой от коррозии покрытие служит и для декоративных целей, его называют защитно-декоративным.
