
- •Биохимия
- •Москва, 2011
- •Введение в биохимию
- •Раздел I. Биохимия обмена веществ в организме человека
- •Глава 1. Химический состав организма человека
- •1.1. Химические элементы, входящие в состав организма человека
- •1.2. Вещества, образующие организм человека
- •Примерное процентное содержание важнейших веществ в организме человека
- •Вопросы и задания для самоконтроля
- •Глава 2. Общие закономерности обмена веществ
- •2.1. Обмен веществ как основа жизнедеятельности живых организмов
- •2.2. Ассимиляция и диссимиляция – две стороны обмена веществ
- •2.3.Этапы обмена веществ
- •2.4. Изменения обмена веществ
- •2.4.1. Возрастные изменения обмена веществ
- •2.4.2. Изменчивость обмена веществ как основа приспособляемости живых организмов
- •2.5. Взаимосвязь обменных процессов с клеточными структурами
- •2.5.1. Строение клетки
- •Вопросы и задания для самоконтроля
- •Глава 3. Биоэнергетика
- •3.1. Источники энергии для организма человека
- •Важнейшие источники энергии организма человека
- •3.2. Биологическое окисление как основной путь получения энергии
- •3.3. Аэробное биологическое окисление
- •3.4. Адениловая система
- •3.5. Биохимические механизмы аэробного биологического окисления
- •3.6. Энергетический эффект биологического окисления.
- •Окислительно-восстановительный потенциал промежуточных переносчиков и изменение свободной энергии при переносе электронов в дыхательной цепи
- •3.7. Субстратное фосфорилирование.
- •3.8. Регуляция скорости аэробного окисления.
- •3.9. Свободное окисление.
- •3.10. Анаэробное окисление.
- •Образование свободных радикалов.
- •Вопросы и задания для самоконтроля
- •Глава 4. Общие принципы регуляции обмена веществ в организме
- •4.1. Концентрация реагирующих веществ (доступность субстратов) как фактор регуляции обменных процессов
- •4.2. Ферменты – биологические катализаторы
- •4.2.1. Строение ферментов
- •4.2.2. Свойства ферментов
- •4.2.3. Механизм действия ферментов
- •4.2.4. Классификация и номенклатура ферментов
- •4.3. Витамины.
- •4.3.1. Номенклатура витаминов
- •4.3.2. Функции витаминов
- •4.3.3. Жирорастворимые витамины Витамины группы а
- •Витамин d (кальциферол)
- •Витамин е (токоферол)
- •Витамин к
- •4.3.4. Водорастворимые витамины Витамин в1 (тиамин)
- •Витамин в2 (рибофлавин)
- •Витамин в3 (пантотеновая кислота)
- •Витамин рр (в5, никотиновая кислота и никотинамид)
- •Витамин в6 (пиридоксин)
- •Витамин в12 (цианокобаламин)
- •Витамин Вс (фолиевая кислота, фолацин)
- •Витамин с (аскорбиновая кислота)
- •Витамин р (рутин)
- •Витамин н (биотин)
- •Витамин u (метилметионинсульфоний)
- •4.3.5. Витаминоподобные вещества
- •4.4.Гормоны
- •Сведения о железах внутренней секреции, секретируемых ими гормонах, их химической природе и регулирующем влиянии
- •4.4.1. Гормоноподобные вещества
- •4.4.2. Химическая природа гормонов
- •4.4.3. Химические превращения гормонов
- •4.4.4. Механизм действия гормонов
- •4.4.5. Взаимодействие между железами внутренней секреции
- •4.4.6. Нервная регуляция деятельности желез внутренней секреции
- •Вопросы и задания для самоконтроля
- •Глава 5. Обмен углеводов
- •5.1. Общие сведения об углеводах
- •5.2. Пищеварение углеводов
- •Крахмал → высоко молекулярные → низко молекулярные → декстрины декстрины
- •5.3. Пути использования продуктов пищеварения углеводов в организме
- •5.4. Синтез гликогена
- •5.5. Использование углеводов в качестве источника энергии
- •5.5.1. Анаэробная фаза превращений углеводов
- •5.5.2. Аэробная стадия превращений углеводов
- •Вопросы и задания для самоконтроля
- •Глава 6. Обмен липидов
- •6.1. Общие сведения о липидах
- •6.2. Жиры (триглицериды)
- •6.3. Стероиды
- •6.4. Пищеварительные превращения липидов
- •6.5. Транспорт и депонирование липидов
- •6.6. Диссимиляция липидов
- •6.6.1. Окисление глицерина
- •6.6.2. Окисление жирных кислот
- •6.6.3. Мобилизация жиров из жировых депо
- •6.6.4. Образование и превращения кетоновых тел
- •6.7. Превращения холестерола и фосфолипидов
- •6.8. Синтез липидов из продуктов углеводного и белкового обмена
- •Вопросы и задания для самоконтроля
- •Глава 7. Обмен белков
- •7.1. Общие сведения о белках
- •7.2. Свойства белков
- •7.3. Роль белков в организме человека
- •7.4. Превращения белков в организме человека
- •7.4.1. Пищеварительные превращения белков
- •7.4.2. Пути использования аминокислот в организме
- •7.4.2. 1. Синтез белков
- •7.4.2.2. Декарбоксилирование аминокислот
- •7.4.2.3. Трансаминирование аминокислот
- •7.4.2.4. Дезаминирование аминокислот
- •7.4.3. Устранение аммиака из организма
- •Вопросы и задания для самоконтроля
- •Глава 8. Обмен воды и минеральных соединений
- •8.1. Содержание и роль воды в организме человека
- •8.2. Потребность в воде
- •8.3. Содержание и роль минеральных веществ в организме человека
- •8.3.1. Содержание и роль минеральных кислот
- •8.3.2. Содержание и роль солей в организме
- •Возрастные изменения минерального и органического компонентов костной ткани.
- •8.3.3. Содержание и роль ионов в организме человека
- •8.3.4. Минеральные буферные системы организма человека
- •8.4. Регуляция обмена воды и минеральных веществ в организме
- •8.5. Особенности обмена воды и минеральных соединений при занятиях физической культурой и спортом
- •Вопросы и задания для самоконтроля
- •Раздел II. Биохимические основы мышечной деятельности
- •Глава 9. Биохимия мышц и мышечного сокращения
- •9.1. Химический состав мышечной ткани
- •9.2. Строение мышечной ткани
- •9.2.1. Строение мышечного волокна
- •9.3. Типы мышечных волокон
- •9.4. Механизм и химизм мышечного сокращения
- •9.4.1. Механизм мышечного сокращения
- •9.4.2. Химические превращения, обеспечивающие сокращение и расслабление мышцы
- •Вопросы и задания для самоконтроля
- •Глава 10. Энергетика мышечной деятельности
- •10.1. Роль атф при мышечной работе
- •10.2. Пути ресинтеза атф при работе
- •10.2.1. Креатинфосфокиназная реакция
- •10.2.2. Ресинтез атф в процессе гликолиза
- •10.2.3. Миокиназная реакция
- •10.2.4. Аэробный ресинтез атф
- •10.2.5. Соотношение различных путей ресинтеза атф при работе
- •Вопросы и задания для самоконтроля
- •Глава 11. Биохимические изменения в организме под влиянием мышечной работы
- •11.1. Срочные биохимические изменения
- •11.2. Отставленные изменения
- •11.3. Кумулятивные (накопительные) биохимические изменения
- •11.4. Зависимость срочных биохимических изменений от особенностей выполняемой тренировочной работы
- •11.4.1. Влияние мощности и продолжительности выполняемых упражнений на характер и глубину срочных биохимических изменений
- •11.4.2. Характеристика упражнений зоны максимальной мощности
- •11.4.3. Характеристика упражнений зоны субмаксимальной мощности
- •11.4.4. Характеристика биохимических изменений при выполнении упражнений зоны большой мощности
- •11.4.5. Характеристика биохимических изменений при выполнении упражнений зоны умеренной мощности
- •11.4.6. Характеристика различных метаболических состояний организма
- •11.4.7. Влияние продолжительности интервалов отдыха между повторными упражнениями на срочные биохимические изменения
- •11.4.8. Зависимость срочных биохимических изменений от режима деятельности мышц
- •11.4.9. Зависимость срочных биохимических изменений от количества участвующих в обеспечении работы мышц
- •Вопросы и задания для самоконтроля
- •Глава 12. Биохимия утомления
- •12.1. Понятие и общая характеристика утомления
- •12.2. Современные представления о природе и механизмах утомления
- •12.3. Биохимические изменения, вызывающие утомление при выполнении упражнений зоны максимальной мощности
- •12.4. Биохимические изменения, вызывающие утомление при выполнении упражнений зоны субмаксимальной мощности
- •12.5. Биохимические изменения, вызывающие утомление при выполнении упражнений зоны большой и умеренной мощности
- •Вопросы и задания для самоконтроля
- •Глава 13. Биохимические превращения в период отдыха после мышечной работы
- •13.1. Гетерохронность восстановительных процессов
- •13.2. Пути ускорения восстановительных процессов
- •13.3. Явление суперкомпенсации
- •Вопросы и задания для самоконтроля
- •Глава 14. Закономерности биохимической адаптации под влиянием систематической тренировки
- •14.1. Понятие о срочной и долговременной адаптации
- •14.2. Биохимические предпосылки основных принципов спортивной тренировки
- •14.3. Эффект повторной работы, выполняемой в период недовосстановления после предыдущей.
- •14.4. Эффект повторной работы, выполняемой в период суперкомпенсации, вызванной предыдущей работой
- •Вопросы и задания для самоконтроля
- •Глава 15. Биохимические основы скоростно-силовых качеств
- •15.1. Биохимические факторы, определяющие проявление силы и быстроты
- •15.2. Биохимическое обоснование методики совершенствования силовых и скоростных способностей.
- •Вопросы и задания для самоконтроля
- •Глава 16. Биохимические основы выносливости
- •16.1. Биохимические факторы, определяющие проявление алактатного компонента выносливости
- •16.2. Биохимические факторы, определяющие проявление гликолитического компонента выносливости
- •16.3. Биохимические факторы, определяющие проявление аэробного компонента выносливости
- •16.4. Специфичность различных компонентов выносливости
- •16.5. Методы оценки алактатного компонента выносливости
- •16.6. Методы оценки гликолитического компонента выносливости
- •16.7. Методы оценки аэробного компонента выносливости
- •16.8. Биохимическая характеристика средств и методов совершенствования различных компонентов выносливости
- •16.8.1. Тренировка алактатного компонента выносливости
- •16.8.2. Совершенствование гликолитического компонента выносливости
- •16.8.3. Биохимическое обоснование средств и методов совершенствования аэробного компонента выносливости
- •Вопросы и задания для самоконтроля
- •Глава 17. Биохимическое обоснование особенностей методики занятий физическими упражнениями и спортом с лицами разного возраста
- •17.1. Биохимические особенности растущего организма
- •Относительное потребление кислорода детьми и подростками в состоянии покоя
- •17.2. Биохимические особенности стареющего организма
- •Вопросы и задания для самоконтроля
- •Глава 18. Биохимический контроль в процессе занятий физической культурой и спортом
- •18.1. Объекты биохимических исследований
- •18.2. Тесты, используемые в биохимическом контроле в процессе занятий физической культурой и спортом
- •18.3. Химические исследования выдыхаемого воздуха
- •18.3.1. Максимальное потребление кислорода (мпк)
- •18.3.2. Дыхательный коэффициент (дк)
- •18.3.3. Неметаболический «излишек» со2
- •18.3.4. Кислородный долг.
- •18.4. Биохимические исследования крови
- •18.4.1. Определение кислотно-щелочного равновесия крови
- •18.4.2. Определение содержания молочной кислоты в крови
- •18.4.3. Определение содержания мочевины в крови
- •18.4.4. Определение количества и активности ферментов в крови
- •18.5. Исследование мышечной ткани
- •18.6. Выбор биохимических показателей
- •Вопросы и задания для самоконтроля
- •Глава 19. Биохимические основы рационального питания при занятиях физической культурой и спортом
- •19.1. Сбалансированность важнейших компонентов питания
- •19.2. Суточные энерготраты организма человека
- •19.3. Суточная потребность в углеводах, жирах, белках
- •19.4. Белковый компонент питания
- •19.5. Липидный компонент питания
- •19.6. Углеводный компонент питания
- •19.7. Обеспечение потребности в витаминах
- •19.8. Удовлетворение потребности в минеральных соединениях
- •19.9. Потребность в воде и пути ее удовлетворения
- •19.10. Специфические функции питания
- •19.11. Биологически активные пищевые добавки
- •19.11.1. Адаптогены
- •19.11.2. Ноотропы
- •19.11.3. Препараты энергетического и пластического действия
- •19.11.4. Антиоксиданты и антигипоксанты
- •19.11.5. Витамины и витаминные комплексы
- •19.11.6. Стимуляторы кроветворения
- •19.12. Режим питания
- •Вопросы и задания для самоконтроля
- •Список литературы
- •На последнюю страницу обложки
3.5. Биохимические механизмы аэробного биологического окисления
Транспорт высокоэнергетических электронов и протонов от окисляемого субстрата на кислород осуществляет система, состоящая из окислительно-восстановительных ферментов, локализованная на внутренней мембране митохондрий. В состав этой системы входят:
- пиридиновые дегидрогеназы, у которых в качестве коферментов выступают НАД (никотинамидадениндинуклеотид) или НАДФ (никотинамидадениндинуклеотидфосфат);
- флавиновые дегидрогеназы (флавиновые ферменты), роль небелковой части у которых выполняют ФАД (флавинадениндинуклеотид) или ФМН (флавинмононуклеотид);
- убихинон (кофермент Q);
- цитохромы.
Пиридиновые дегидрогеназы. Строение НАД и НАДФ представлено на рис. 4.

Никотинамидаденин- Никотинамидаденинди-
динуклеотид (НАД) нуклеотидфосфат (НАДФ)
Рис. 4. Строение НАД и НАДФ
НАД и НАДФ являются динуклеотидами, нуклеотиды которых связаны пирофосфатной связью (через два соединенных между собой остатка фосфорной кислоты). В состав одного нуклеотида входит амид никотиновой кислоты (витамин РР), другой нуклеотид представлен адениловой кислотой. В молекуле НАДФ имеется дополнительный остаток фосфорной кислоты, присоединенный ко второму углеродному атому рибозы, связанной с адениловой кислотой.
НАД и НАДФ являются коферментами большого числа специфических для разных субстратов окисления дегидрогеназ. Связь между ними и белковой частью непрочная, они объединяются только непосредственно в момент реакции.
Некоторые пиридиновые дегидрогеназы локализованы в матриксе митохондрий. НАД-зависимые дегидрогеназы передают электроны и протоны в дыхательную цепь, НАДФ-зависимые дегидрогеназы служат источником восстановительных эквивалентов для реакций биосинтеза
Активной частью НАД и НАДФ является витамин РР. При взаимодействии с восстановленным субстратом пиридиновое кольцо витамина РР связывает два электрона и протон, второй протон остается в среде ( рис. 5).
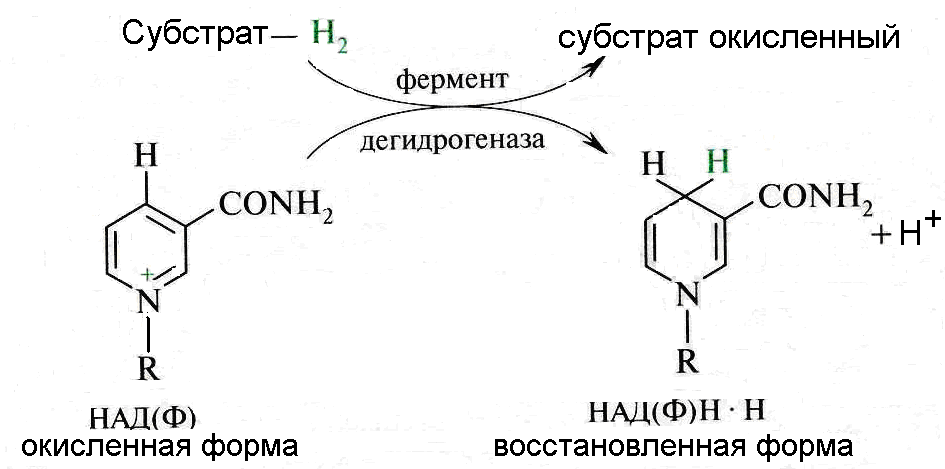
Рис. 5. Окисление субстрата пиридиновыми дегидрогеназами
Флавиновые ферменты. В отличие от НАД и НАДФ, простетические группы флавиновых ферментов (ФАД и ФМН) прочно связаны с белковой частью. Обе простетические группы содержат метаболически активную форму рибофлавина (витамина В2), к которой в процессе их восстановления присоединяются атомы водорода (рис.6).
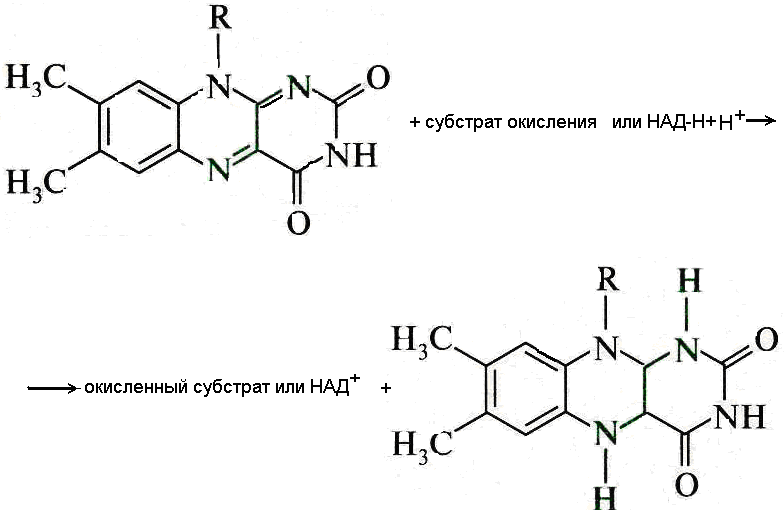
Рис. 6. Окисление субстратов активной частью (витамин В2) простетической группы флавиновых ферментов
ФАД - содержащие флавиновые ферменты выполняют функцию, аналогичную пиридиновым ферментам – являются первичными акцепторами электронов и протонов. Они непосредственно окисляют некоторые субстраты, например сукцинат (янтарную кислоту) или ацил-КоА (активную форму любой жирной кислоты).
ФМН-зависимая дегидрогеназа выполняет роль промежуточного переносчика электронов и протонов между НАД и убихиноном, т.е. является непосредственным участником дыхательной цепи.
Убихинон (кофермент
Q).
Убихинон является производным бензохинона
с длинной боковой цепью. Его строение
представлено на рис.7.

Рис. 7. Строение кофермента Q (убихинона)
Кофермент Q играет роль промежуточного переносчика электронов и протонов в дыхательной цепи, непосредственно окисляя флавиновые ферменты. Место присоединения протонов и электронов – атомы кислорода в кольце бензохинона (рис. 8):

Рис. 8. Механизм переноса протонов молекулой кофермента Q (убихина)
Цитохромы. Цитохромы относятся к классу хромопротеинов. В их состав входит железосодержащий гем, по своему строению аналогичный гему гемоглобина. Различные цитохромы отличаются строением боковых цепей в структуре гема, структурой белковых компонентов, способом соединения гема с белковым компонентом. Функция цитохромов связана с переносом электронов от убихинона к кислороду. Они локализованы в дыхательной цепи в определенной последовательности:
Цит.b →цит.с1 → цит.с → цит.аа3
Цитохромы b, с1 и с выполняют функцию промежуточных переносчиков электронов, а комплекс цитохромов а и а3, называемый цитохромоксидазой, является терминальным дыхательным ферментом, непосредственно взаимодействующим с кислородом. Этот комплекс состоит из шести субъединиц, каждая из которых содержит геминовую группу и атом меди. Две субъединицы из шести составляют цитохром а, а остальные четыре образуют цитохром а3.
Перенос цитохромами электронов непосредственно связан с присутствием в их составе ионов железа. Окисленная форма цитохромов содержит Fе3+. Принимая электроны от убихинона или другого цитохрома, Fe3+ переходит в восстановленное состояние (Fе2+), а передавая электроны другому цитохрому или кислороду, Fe2+ вновь переходит в окисленное состояние (F3+).
Кислород, принимая электроны от цитохромоксидазы, переходит в активное (ионизированное) состояние, затем принимает два протона из окружающей среды. В результате образуется молекула воды.
Схематично систему переноса электронов и протонов по дыхательной цепи можно представить следующим образом (рис. 9):

Рис. 9. Последовательность расположения переносчиков электронов и протонов в дыхательной цепи
