- •8.4. Мозжечок
- •8.6. Базальные ганглии
- •8.8. Методы исследования цнс
- •8.9. Особенности физиологии цнс развивающегося организма
- •Глава 9 вегетативная нервная система
- •9.1. Функциональные особенности внс и ее отделы
- •9.2. Симпатическая нервная система
- •9.4. Парасимпатическая нервная система
- •9.6. Интраорганная нервная система и тканевые рецепторы
- •9.8. Взаимодействие между отделами внс
- •9.9. Центры вегетативной нервной системы
- •9.10. Афферентные пути вегетативной нервной системы
- •9.11. Дуга вегетативного рефлекса
- •9.12. Тонус вегетативных центров
- •9.14. Особенности вегетативной нервной системы детей
- •Глава 10
- •10.1. Общая характеристика эндокринных желез и гормонов
- •10.2. Регуляция образования гормонов
- •10.3. Методы изучения функций желез внутренней секреции
- •10.4. Гипофиз
- •10.5. Эпифиз (шишковидная железа)
- •2. Установлена определенная зависимость между содержанием йода и гормонообразова-
- •Глюкагон
- •10.10. Надпочечники
- •10.11. Половые железы
- •10.12. Гормоны плаценты. Понятие о тканевых гормонах и антигормонах
- •10.13. Особенности эндокринной системы детей
- •10.14. Эндокринная система стареющего организма
- •Глава 11
- •11.1. Кровь как внутренняя среда организма
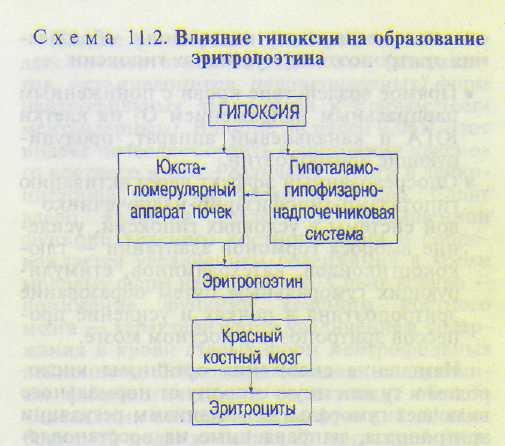
- •11.3. Регуляция эритропоэза
- •11.4. Физиология лейкоцитов
- •11.5. Регуляция лейкопоэза
- •11.6. Система регуляции агрегатного состояния крови (pack)
- •Глава 12
- •12.1. История. Понятия. Роль системы дыхания
- •12.2. Внешнее дыхание
- •12.8. Система дыхания старкющего организма
- •Глава 13
- •13.2. Цикл сердечной деятельности
- •13.3. Особенности свойств сердечной мышцы
- •1. Параметры потенциала покоя и пд.
- •13.4. Особенности энергетического обеспечения сердечной мышцы
- •13.6. Методы исследования деятельности сердца
Глава 11
СИСТЕМА КРОВИ
Система крови — совокупность органов кроветворения, периферической крови, органов кроверазрушения и нейрогуморального аппарата регуляции (Г.Ф.Ланг). ~
11.1. Кровь как внутренняя среда организма
11.1.1. ПОНЯТИЯ, ОБЩАЯ ХАРАКТЕРИСТИКА КРОВИ. ФИЗИКО-ХИМИЧЕСКИЕ КОНСТАНТЫ
Внутренняя среда организма — это совокупность жидкостей, включающая кровь, лимфу, тканевую и цереброспинальную жидкости. Значение внутренней среды организма состоит в том, что из нее ткани получают все необходимое для своей жизнедеятельности и отдают в нее метаболиты (продукты обмена веществ).
Состав крови. Кровь — жидкая ткань организма. Она состоит из плазмы (жидкая часть крови) и форменных элементов — эритроцитов, лейкоцитов, тромбоцитов. Плазмы содержится 55—60 %, форменных элементов — 40—45 %'. Соотношение плазмы и форменных элементов определяется при помощи прибора гематокрита. Гематокритное чис-ло_— это количество форменных элементов крови в процентах от общего объема крови (в норме оно равно 40—45).
Количество крови в организме человека составляет 5—9 % от массы тела, т.е. у человека массой 65—70 кг количество крови 4,5-— 6 л. В организме в состоянии покоя до 45— 50 % всей массы крови находится в кровяных депо (селезенке, печени, легких и подкожном сосудистом сплетении), являющихся резервуарами крови. В селезенке кровь может быть почти полностью выключена из циркуляции, а в печени и сосудистом сплетении кожи кровь циркулирует в 10—20 раз медленнее, чем в других сосудах.
Функции крови: 1) транспортная — доставка тканям различных веществ; за счет
этого выполняются функции: а) дыхательная; б) питательная; в) экскреторная; г) регуляции постоянства температуры тела; д) регуля-торная — участие в гуморальной регуляции многих функций организма; 2) защитная -участие в фагоцитозе, образовании антител.
Физико-химические свойства крови. Кровь обладает тремя свойствами: а) суспензионными; б) коллоидными; в) электролитными. Суспензионные и коллоидные свойства крови зависят от количества белков и от соотношения их различных фракций (альбумины, глобулины). Белки удерживают жидкую часть крови в кровяном русле. Электролитные свойства крови обусловлены содержанием в ней разнообразных солей. Они обеспечивают осмотическое давление крови, которое в норме составляет 6,6—7,6 атм. Кровь имеет слабощелочную реакцию, ее рН 7,35—7,45.
Одним из показателей состояния внутренней среды организма является величина осмотического давления плазмы крови. Функции клеток организма могут осуществляться при относительном постоянстве этого показателя. Так, например, эритроциты, помещенные в раствор хлорида натрия, имеющий одинаковое с кровью осмотическое давление, не изменяют ни своей формы, ни размера. Раствор, имеющий одинаковое осмотическое давление с кронью, называется изотоническим (0,85—0,9 % раствор натрия хлорида). Раствор с более высоким осмотическим давлением, чем осмотическое давление крови, называется гипертоническим, а имеющий более низкое давление — гипотоническим. Часть осмотического давления, создаваемого белками плазмы, называют онкотическим давлением (25—30 мм рт.ст.).
Кислотно-основное состояние (КОС) организма является одним из важнейших и наиболее стабильных параметров постоянства внутренней среды. От соотношения водородных и гидроксильных ионов во внутренней среде организма зависят активность ферментов, интенсивность и направленность окис-
206
яительно-восстановительных реакций, процессы обмена белков, углеводов и лилидов, функции различных органов и систем, проницаемость биологических мембран. Активность реакции среды влияет на способность гемоглобина связывать кислород и отдавать его тканям. Активную реакцию среды оценивают показателем рН, отражающим содержание в жидкостях ионов водорода. Величина рН является одним из самых «жестких» параметров крови и колеблется у человека в норме в очень узких пределах — 7,35—7,45. Более значительные изменения рН крови связаны с патологическими нарушениями обмена веществ. В других биологических жидкостях и в клетках рН может отличаться ог рН крови. Так, в эритроцитах рН составляет 7.18—7,20. Сдвиг рН крови даже на 0,1 за указанные границы обусловливает нарушение функций сердечно-сосудистой, дыхательной и других систем; сдвиг на 0,3 может вызвать коматозные состояния, а на 0,4 — зачастую несовместим с жизнью. Кислотно-основное состояние (КОС) поддерживается буферными системами крови, а регулируется с помощью легких, желудочно-кишечного тракта, почек.
Буферной системой называют смеси, которые обладают способностью препятствовать изменению рН среды при внесении в нее кислот или оснований. Буферными свойствами обладают смеси, которые состоят из слабой кислоты и ее соли, содержащей сильное основание, или из слабого основания и соли сильной кислоты. Наиболее емкими буферными системами крови являются бикар-бонатная, фосфатная, белковая и гемоглоби-новая. Первые три системы особенно важную роль играют в плазме крови, а гемоглобиновый буфер, самый мощный, действует в эритроцитах,
Бикарбонатный буфер состоит из слабой угольной кислоты Н2СО3 и бикарбонатов: NaHCOj в плазме и КНСО3 в клетках. В нормальных условиях (при рН крови около 7,4) в плазме бикарбоната в 20 раз больше, чем углекислоты. При образовании в плазме избытка кислореагирующих продуктов ионы водорода соединяются с анионами бикарбоната (НСОз). Бикарбонатный буфер способен нейтрализовать и избыток оснований. В этом случае ионы ОН"" связываются углекислотой и вместо самого сильного основания OI-Г образуется менее сильное НСО^, избыток которого в виде бикарбонатных солей выделяется почками. До тех пор пока количество угольной кислоты и бикарбоната натрия изменяется пропорционально и между ними сохра-
няется соотношение 1:20, рН крови остается в пределах нормы, поэтому содержание составных частей бикарбонатного буфера является важнейшим показателем кислотно-основного состояния организма.
Фосфатный буфер представлен солями одно- (NaH2PO4) и двузамещенных (Na2HPO4) фосфатов. Фосфатная буферная система является основной буферной системой клеток. Механизм коррекции сводится к образованию подвижных фосфатов в клетке и фосфорных солей мочи. При нормальном рН в плазме соотношение одно- и двузамещенных фосфатных солей составляет 1:4. Этот буфер участвует в почечной регуляции КОС, а также в регуляции реакции некоторых тканей. В крови же его действие главным образом сводится к поддержанию постоянства и воспроизводства бикарбонатного буфера. Так, при избытке в крови Н^СОз происходит обменная реакция: Н2СО3 + Na2HPO4 - NaHCQa + NaH2PO4, т.е. избыток Н2СО3 устраняется, а концентрация NaHCO3 увеличивается, поддерживая постоянство отношений компонентов бикарбонатного буфера.
Белковая буферная система является довольно мощной. Белки плазмы крови содержат достаточное количество кислых и основных радикалов. Поэтому они могут взаимодействовать с основаниями и кислотами,
Гемоглобиновый буфер является самой емкой буферной системой. На его долю приходится до 75 % всей буферной емкости крови. Гемоглобин, как и другие белки, является амфолигом. Свойства буферной системы гемоглобину придает главным образом его способность постоянно находиться в виде двух форм — восстановленного (редуцированного) гемоглобина ННЬ, связывающего ионы Н+, и окисленного (оксигемоглобина) КНЬО2, отдающего ионы Н+ (см. раздел 12.3.2).
Гемоглобиновый буфер уменьшает закис-ление среды также и с помощью образования карбаминовой связи с СО2: ННЬСО2 (см. раздел 12.3.2).
Буферные системы стабилизируют рН крови лишь на молекулярном уровне, но не обеспечивают выведения из организма основных или кислых элементов. Регулируют рН различные органы и системы, главными из которых являются легкие и почки.
11.1.2. СОСТАВ ПЛАЗМЫ И ЗНАЧЕНИЕ ЕЕ ЭЛЕМЕНТОВ
Плазма — жидкая часть крови, остающаяся
после удаления из нее форменных элементов. В ее состав входят неорганические (около

1. Б е л к и (67—75 г/л), среди них альбуминов — 37—41 г/л, глобулинов — 30—34 г/л, фибриногена 3,0—3,3 г/л. Значение белков:
1) обеспечивают коллоидно-осмотическое (онкотическое) давление (25—30 мм рт.ст.);
2) образуют иммунные антитела; 3) участву ют в процессе свертывания крови (фибрино ген и другие плазменные факторы свертыва ния крови); 4) обеспечивают вязкость крови;
-
регулируют рН крови (белковый буфер);
-
выполняют транспортную функцию. Альбумины составляют 50—60 % от общего
количества белков плазмы крови, образуются в печени и костном мозге. Они обладают высокой гидрофильностью, играют главную роль в создании онкотического давления крови, выполняют транспортную функцию за счет большого числа в них активных полярных диссоциированных групп (связывают и переносят различные вещества, в частности гормоны, лекарства), выполняют также питательно-пластическую функцию, так как являются резервным белком при голодании.
Глобулины составляют 35—40 % от общего количества белков. С помощью электрофореза на бумаге из глобулинов выделяют а,-, а2-, Р- и у-фракции, а в агаровом геле обнаруживают 7—8 фракций, в крахмальном или поли-акриламидном геле — до 16—17 фракций, а при иммуноэлектрофорезе получают до 30 фракций глобулинов. В состав глобулинов входят: 1) липоидный компонент — липопро-теиды (а- и р-глобулины); 2) углеводный компонент — гликопротеиды (а,- и а2-гло-
булины); 3) металлы — металлопротеиды. К ним относятся трансферрин (р-глобулин) и церулоплазмин (агглобулин). Значение глобулинов состоит в том, что они выполняют защитную функцию, р- и у-глобулины являются источником образования иммунных антител, образующихся в ответ на поступление в организм чужеродных белков.
-
Азотсодержащая часть плаз мы небелковой природы — это промежуточные продукты обмена белка. Они составляют остаточный азот. Основными компонентами остаточного азота являются азот мочевины, аминокислот (в основном глутамина и глутаминовой кислоты), моче вой кислоты. Содержание остаточного азота в крови составляет 14,3—28,6 ммоль/л. При некоторых патологических состояниях содер жание остаточного азота в крови повышает ся — развивается азотемия. В зависимости от причин она подразделяется на ретенционную и продукционную. Ретенционная азотемия наступает в результате недостаточного выде ления с мочой азотсодержащих продуктов при нормальном поступлении их в кровяное русло. Продукционная азотемия возникает при избыточном поступлении азотсодержа щих продуктов в кровь как следствие усилен ного распада тканевых белков, например, из злокачественной опухоли. Функция почек при этом, как правило, не нарушена.
-
Безазотистые органические вещества — глюкоза, содержание ко торой в крови 3,3—5,5 ммоль/л, или 80— 120 мг%; молочная, пировиноградная кисло ты, липиды (фосфолипиды, жирные кисло ты, лецитин). Концентрация глюкозы в арте риальной крови выше, чем в венозной. Это обусловлено непрерывным использованием глюкозы клетками тканей и органов. Молоч ная кислота является продуктом гликолиза
208
(расщепления углеводов) и гликогенолиза (расщепления гликогена). Увеличение концентрации молочной кислоты в крови связано в основном с усилением ее продукции в мышцах, а также с понижением способности печени превращать молочную кислоту в глюкозу и гликоген. То же относится и к пирови-ноградной кислоте. Содержание липидов в крови колеблется в довольно широких пределах и зависит от характера пищи. Значительная часть липидов в плазме крови представлена в форме липопротеидов, связанных главным образом с а- и р-глобулинамй.
4. В состав органических веществ плазмы крови входят также биологически активные вещества — ферменты, витамины и гормоны.
11.2. ФИЗИОЛОГИЯ ЭРИТРОЦИТОВ
11.2.1. СТРУКТУРНО-ФУНКЦИОНАЛЬНАЯ ХАРАКТЕРИСТИКА
Эритроциты — самые многочисленные клеточные элементы крови; в зависимости от размеров различают нормоциты, микроциты и макроциты. У человека и других млекопитающих эритроциты не имеют ядра, митохондрий, белоксинтезируюЩеТГВистемы. Для эритроцитов характерны гомогенная цитоплазма и наличие в ней гемоглобина. На долю белка гемоглобина приходится 34 % общей и 90—95 % сухой массы эритроцитов.
Исследование эритроцитов в сканирующем электронном микроскопе позволило определить наличие их различных (в зависимости от поверхностной архитектоники) форм в периферической крови. Около 85 % всех эритроцитов составляют щ&шижш» имеющие форму двояковогнутого диска, что обеспечивает некоторые диффузионные преимущества, необходимые для выполнения эритроцитами их основной функции — пере-носа дыхательных газов крови (рис. ИЛ). При такой форме эритроцитов" значительно увеличивается их диффузионная поверхности которая у взрослого человека составляет суммарно около 3800 м2. Остальные 15 % эритроцитов имеют различную форму, размеры и отростки на поверхности клетки.
В структуре эритроцитов различают стро-му, которая состоит из остова клетки, и поверхностного слоя — мембраны. Строение клеточной мембраны эритроцитов имеет сходство с мембранами ядерных клеток. Помимо белка спектрина, в мембране и цито-скелете эритроцитов обнаружены рецептор-

Рис. ИЛ. Зрелые эритроциты.
ные белки — гликопротеиды, каталитические белки — ферменты, играющие роль в транспорте ионов и образующие каналы в мембране. Одним из важных гликопротеидов является гликофорин, содержащийся как на внешней, так и на внутренней поверхностях мембран эритроцитов. Гликофорин содержит большое количество сиаловой кислоты и обладает значительным отрицательным зарядом. В мембране он располагается неравномерно, образует выступающие из мембраны участки, которые являются носителями иммунологических детерминант, т.е. служат рецепторами для вирусов и местами для прикрепления агглютининов.
В отличие от мембран всех других клеток организма мембрана эритроцитов легкопроницаема для анионов HCOj, СГ, а также для О2, СО2, Н+, ОН", в то же время малопроницаема для катионов К+ и Na+. Проницаемость для анионов примерно в 1 млн раз выше, чем для катионов. Толщина мембраны эритроцитов, по данным разных авторов, колеблется от 1 до 2 нм. Транспорт веществ через мембрану эритроцитов осуществляется, как и в других клетках (см. раздел 2.5).
Гиалоплазма эритроцита при электронной микроскопии выглядит электронно-плотной, содержит многочисленные гранулы гемоглобина размером 4—5 нм. Касаясь содержимого эритроцитов, необходимо отметить в нем до 60 % воды и 40 % сухого остатка, причем, как указывалось выше, 90—95 % сухого остатка приходится на гемоглобин и 5—10 % составляют различные белки, глюкоза, липиды и минеральные вещества. Другие клетки организма содержат значительно больше воды — примерно 80 % и более.
Особенности строения эритроцитов, их форма обусловливают различные физиологические и физико-химические свойства эритроцитов.
209
1. Пластичность эритроцитов — это их способность к обратимой деформации при прохождении через микропоры и узкие изви тые капилляры диаметром до 2,5—3 мкм. Свойство пластичности выражено у дискоид- ных эритроцитов; размеры нормального дис- коидного эритроцита составляют W7,2— 7,5 мкм. Пластичность эритроцита во многом определяется особенностями строения ци- тоскелета эритроцитов, расположением и со стоянием белковых молекул цитоскелета. FIcl мере старения эритроцитов их способность к деформации снижается, а превращение их в сфероциты (имеющие форму шара) за счет изменения цитоскелета приводит к тому, что они не могут проходить через капилляры диаметром до 3 мкм и задерживаются крас ной пульпой селезенки. Такие эритроциты не способны пройти в синус селезенки и фаго цитируются клетками мононуклеарной фаго цитирующей системы. Считают, что в про цессе старения эритроцитов возникает необ ратимая агрегация спектрина и гемоглобина, что обусловливает нарушение структуры и пластических свойств эритроцитов. Пластич ность эритроцитов зависит также от содержа ния и соотношения различных фракций ли- пидов в мембрдые..клеток, причем очень важ ным является соотношение фосфолипидов и холестерина, которое определяет свойство текучести мембраны эритроцитов и других клеток. Данное соотношение выражается в виде липолитического коэффициента (ЛК). В норме
= холестерин J1^ лецитин 'у'
Липиды в мембранах эритроцитов находятся почти исключительно в форме бислоя. При увеличении количества лецитина возрастает проницаемость мембран эритроцитов. При снижении количества холестерина, изменении его положения в мембране происходит снижение стойкости эритроцитов, меняются свойства текучести их мембран.
2. Осмотическая стойкость эритроцитов. Осмотическое давление в эритроцитах не сколько выше, чем в Плазме крови, что обес печивает тургор клеток. Это создается высо кой внутриклеточной концентрацией белков по сравнению с плазмой крови. При этом со держание низкомолекулярных веществ в эри троцитах значительно ниже, чем в плазме крови.
При помещении эритроцитов в гипотоническую среду может наступить осмотический, или коллоидно-осмотический, гемолиз. Последний обусловлен тем, что вода поступает в
эритроциты до того момента, когда мембрана разрывается и гемоглобин выходит в окружающую среду. В умеренно гипотонической среде эритроциты приобретают сферическую форму. Резистентность, или устойчивость эритроцитов может резко снижаться при различных формах врожденных или приобретенных гемолитических анемий. Изучение осмотической резистентности эритроцитов у взрослого здорового человека показало, что примерно 50 % их гемолизируется в 0,43 % растворе хлорида натрия. При помещении эритроцитов в гипертоническую среду происходит их сморщивание, что связано с потерей ими воды.
-
Обеспечение креаторных связей эритро цитами. В настоящее время установлено, что эритроциты, помимо транспорта дыхатель ных газов крови, обеспечивают идеальный перенос различных веществ. Это позволяет эритроцитам осуществлять межклеточные взаимодействия. Обеспечение креаторных свя зей эритроцитами облегчается за счет боль шой суммарной поверхности и их постоян ного движения по организму. В эксперимен тальных исследованиях было убедительно по казано, что при повреждении структуры пе чени у крыс эритроциты начинают усиленно транспортировать из костного мозга в печень нуклеотиды, пептиды, аминокислоты, спо собствуя восстановлению структуры органа.
-
Способность эритроцитов к оседанию. Удельный_в£с_э_1жгло.1щтов П j)96) выше, чем плазмы крови (1,027), поэтому "эритроциты в пробирке с кровыоТ лишенной возможности свертываться, способны медленно оседать на дно. В условиях физиологической нормы ско рость оседания эритроцитов невысока, что обусловлено преобладанием в плазме крови белков альбуминовой фракции. Альбумины являются лиофильными коллоидами, создают вокруг эритроцитов гидратную оболочку и удерживают их во взвешенном состоянии. Глобулины представляют собой лиофобные коллоиды, способствуют уменьшению гидрат- ной оболочки вокруг эритроцитов и отрица тельного поверхностного заряда их мембран, что ведет к усилению агрегации эритроцитов.
Сопротивление таких агрегатов трению меньше, чем отдельных эритроцитов, агрегаты быстрее оседают. В связи с этим важная роль в обеспечении скорости оседания эритроцитов (СОЭ) отводится соотношению альбуминовых и глобулиновых фракций крови, т.е. белковому коэффициенту (БК)- В норме
1,5-1,7.
[альбумины] [глобулины]
210
При нормальном белковом коэффициенте СОЭ составляет у мужчин 1 — 10 мм/ч, у женщин — 2—15 мм/ч. При некоторых патологических процессах и заболеваниях СОЭ повышается, так как увеличивается количество белков глобулиновой фракции (гаптоглоби-на, церулоплазмина, липопротеидов, пара-протеинов, фибриногена), получивших название агломеринов.
-
Агрегация эритроцитов. При замедле нии движения крови и повышении ее вязкос ти эритроциты образуют агрегаты, обуслов ливая развитие феномена реологических рас стройств при различных критических и тер минальных состояниях организма, в частнос ти при травматическом шоке, постинфаркт ном коллапсе, перитоните, острой кишечной непроходимости, остром панкреатите, ожогах и других патологических состояниях. Внача ле агрегация эритроцитов носит обратимый характер, при этом образуются ложные агре гаты, или монетные столбики. В случае бы строго восстановления кровотока они распа даются на полноценные клетки с сохранен ными мембраной и внутриклеточной струк турой. При более длительном нарушении кровотока образуются истинные агрегаты. При этом возникает микротромбообразова- ние, нарушается микроциркуляция, появля ются выраженные метаболические и функци ональные расстройства в различных органах и системах.
-
Деструкция эритроцитов. Продолжи тельность жизни эритроцита в кровяном русле составляет около 120 .дней. В этот пе риод развивается физиологическое старение клетки, которое характеризуется постепен ным увеличением метаболических сдвигов и функциональных расстройств. Около 3 0 % эритроцитов в норме подвергается разруше нию в сосудистом русле. В костном мозге на ряду с процессами эритропоэза также воз можно и разрушение эритрокариоцитов и эритроцитов, усиливающееся при патологи ческих процессах в печени и селезенке.
11.2.2. МЕТАБОЛИЗМ ЭРИТРОЦИТОВ
Зрелые эритроциты человека отличаются не только своим упрошенным строением, но и более ограниченным количеством метаболических реакций. Как известно, в процессе трансформации ретикулоцита в зрелый эритроцит в течение 1—3 сут происходят существенные изменения в обмене веществ клетки. Прекращается значительная часть синтетических процессов: утрачивается способность
к синтезу белка, тема, липидов, фосфолипи-дов, резко снижается содержание нуклеиновых кислот и АТФ. Почти полностью утрачивается способность к дыханию в связи с инактивацией флавиновых ферментов и ци-тохромоксидазы, нарушается цикл трикарбо-новых кислот.
Эритроциты в отличие от ретикулоцитов и эритрокариоцитов не способны синтезировать пурины, нуклеиновые кислоты, порфи-рины. Изменение обмена веществ сочетается с изменением морфологии клетки по мере ее созревания: исчезает ядро, разрушаются рибосомы и митохондрии при действии протеаз и липаз. В зрелых эритроцитах сохраняется способность к гликолизу и утилизации небольшого количества глюкозы в пентозном цикле.
Как известно, основная (кислородтран-спортная) функция эритроцитов не является энергозависимой. Тем не менее для поддержания ряда других функций и стабильности мембраны эритроцитов важное значение имеет способность клеток к синтезу АТФ, а также соединений с высокой восстанавливающей способностью, в частности НАДН, НАДФН. Энергетическое обеспечение клетки осуществляется за счет утилизации глюкозы в результате анаэробного гликолиза, причем установлено, что в условиях нормы эритроциты утилизируют в реакциях гликолиза только глюкозу и при ее отсутствии энергетическое обеспечение эритроцитов нарушается.
Характерной особенностью анаэробного расщепления углеводов в безъядерных эритроцитах является существование побочного пути гликолиза, в результате которого 1,3-дифосфоглицерат (1,3-ДФГ) превращается не только в 3-фосфоглицерат, но и в 2,3-ДФГ. В энергетическом отношении образование 2,3-ДФГ менее эффективно, так как приводит к образованию лишь одной молекулы АТФ вместо двух молекул, накапливающихся при основном пути гликолиза. Однако роль 2,3-ДФГ не ограничивается участием в резервном механизме ресинтеза АТФ. Основное значение этого соединения заключается в регуляции сродства гемоглобина к кислороду. При увеличении концентрации 2,3-ДФГ в эритроците уменьшается степень сродства гемоглобина к кислороду; при этом большее количество кислорода освобождается из оксигемоглобина и передается тканям. При-уменьшении концентрации 2,3-ДФГ сродство гемоглобина к кислороду увеличивается, и при данном РО2 из оксигемоглобина извлекается меньше кис-
211
лорода. Уровень 2,3-ДФГ увеличивается при заболеваниях, связанных с гипоксией, а также при стрессе, что проявляется в уменьшении сродства гемоглобина к кислороду и ограничении гипоксии.
АТФ также уменьшает сродство гемоглобина к кислороду, однако в результате значительно большего содержания 2,3-ДФГ в эритроците (примерно в 4 раза) АТФ отводится значительно меньшая роль в этом процессе.
П.2.3. КОЛИЧЕСТВО ЭРИТРОЦИТОВ И ИХ ФУНКЦИИ
Количество эритроцитов у мужчин колеблется в пределах 4,5—5,5хЮ12/л, у женщин — 3,7—4,7x1012/л. Количественные изменения эритроцитов могут носить физиологический, компенсаторный или патологический характер, проявляться в виде увеличения или уменьшения числа эритроцитов в периферической крови.
Эритроцитоз — состояние, характеризующееся увеличением количества эритроцитов в периферической крови. В соответствии с механизмами развития этого состояния различают относительный и абсолютный эритроцитоз. Относительный э^шцррдитоз возникает в том случае, когда увеличивается количество эритроцитов в единице объема крови в связи со сгущением, крови, но эри-Xpori^^jie.JfaKTjiBMpyeTCH. Относительный эритроцитоз может иметь место при физической нагрузке, а также ржогах, когда возникает выраженная плазмопотеря через раневую поверхность, при неукротимой рвоте в случае кишечной непроходимости, токсикозе беременности, при диареях, сопровождающих холеру, дизентерию и другие кишечные инфекции.
Абсолютный эритроцитоз — состояние, характеризующееся увеличением количества эритроцитов в периферической крови вследствие усиления эритропоэза. Абсолютный эритроцитоз бывает двух видов. 1. Компенсаторный, обеспечивающий развитие компенсаторно-приспособительных реакций в условиях патологии, например при сердечной недостаточности или у здоровых лиц — жителей высокогорных районов в связи с хронической гипоксией и стимуляцией эри-тропоэза. 2. Патологический эритроцитоз, не обеспечивающий адаптационных реакций, имеет место при опухолевом поражении почек, надпочечников^ гипофиза, что сопровождается усилением продукции гумо-
ральных и гормональных стимуляторов эри-тропоэза.
Эритропения— состояние, характеризующееся уменьшением количества эритроцитов в крови. В соответствии с механизмами развития эритропении могут носить абсолютный или относительный характер. Относительная эритропения обусловлена увеличением поступления жидкости в организм, разжижением крови, что приводит к уменьшению количества эритроцитов в единице объема крови при сохраненном эритролоэзе, Абсолютная эритропения связана с различными патогенетическими факторами: подавлением эритропоэза, усилением разрушения эритроцитов или с усиленной кровопотерей, что приводит к уменьшению содержания эритроцитов в периферической крови.
Основные функции эритроцитов. 1. Транспорт О2 и СО2, аминокислот, пептидов, нук-леотидов к различным органам и тканям, что способствует обеспечению репаративно-реге-нераторных процессов. 2. Детоксицирующая функция обеспечивается благодаря способности адсорбировать токсичные продукты эндогенного, экзогенного, бактериального и небактериального происхождения и их инак-тивировать. 3. Важнейшей функцией эритроцитов является участие в регуляции кислотно-основного состояния организма за счет гемоглобина, обеспечивающего до 70 % всей буферной емкости крови. 4. Эритроциты принимают непосредственное участие в процессах свертывания крови и фибринолиза за счет адсорбции на их мембране разнообразных ферментов этих систем. 5. Участие в иммунологических реакциях организма — реакциях агглютинации, преципитации, лизиса, опсонизации, реакциях цитотоксического типа. Это обусловлено наличием в мембране эритроцитов комплекса специфических полисахаридно-аминокислотных соединений, обладающих свойствами антигенов (агг-лютиногенов).
Помимо зрелых эритроцитов, в периферической крови циркулируют ретикулоциты, число которых в норме составляет 1—2%. Рлгпикулоциты —■ молодые безъядерные клетки — образуются на последнем этапе созре"-вания, предшествующем образованию эритроцита. Количество ретикулоцитов в периферической крови позволяет судить об интенсивности эритропоэза, компенсаторно-приспособительных реакциях в условиях нормы и патологии. При усилении эритропоэза возникает ретикулоцитоз, характеризующийся увеличением количества ретикулоцитов в крови.
212
11.2.4, СОЕДИНЕНИЯ ГЕМОГЛОБИНА И ЕГО ФУНКЦИИ
А. Структурная характеристика гемоглобина.
Гемоглобин (от греческого haema — кровь и латинского giobus — шарик) относится к числу важнейших дыхательных белков, осуществляющих транспорт О2 и СОа. Гемоглобин — основной компонент эритроцитов крови всех позвоночных и некоторых беспозвоночных животных. В каждом эритроците содержится около 28 млн молекул гемоглобина. Гемоглобин — сложный протеин, относится к классу так называемых хромопротеидов (гемопроте-идов), состоит из железосодержащих групп r/ема и белкового остатка глобина. На долю гема приходится. 4 % и на белковую часть — 96 %. Молекулярная масса гемоглобина составляет 64 500 Д. Динамическое взаимодействие гема с глобином придает гемоглобину уникальные свойства, необходимые для обратимого процесса транспорта кислорода.
Г е м — это комплексное соединение про-топорфирина IX с железом. Он крайне неустойчив и легко превращается либо в гематин с окислением двухвалентного железа до трехвалентного и присоединением к последнему ОН", либо в гемин, содержащий вместо ОН"" ионизированный хлор. Структура гема идентична для гемоглобина всех видов животных. Различия в свойствах гемоглобина обусловлены различиями белкового компонента. Как известно, молекула гемоглобина представляет собой тетрамер, состоящий из двух пар полипептидных цепей, каждая из которых соединена с гемом. Совокупность четырех попарно одинаковых полипептидных цепей образует белковую часть молекулы гемоглобина — глобин. В крови взрослого человека содержатся НЬА (95—98 %, его обозначают как HbAi), а также НЬА2 (2-2,5 %), HbF (0,1—2 %). Молекула НЬА включает две а- и две р-полипептидные цепи, НЬА2 — две а- и две 5-полипептидные цепи. У мужчин содержание гемоглобина в среднем составляет 130—160 г/л, у женщин — 120—140 г/л. Эритроциты, нормально насыщенные гемоглобином, получили название нормохромных, со сниженным количеством — гипохромных, а с повышенным содержанием гемоглобина — гиперхромных.
Б. Соединения гемоглобина. Важнейшими соединениями гемоглобина являются оксиге-моглобин и восстановленный (редуцированный) гемоглобин. В составе этих соединений гемоглобина сохраняется двухвалентное железо, а следовательно, не изменяется способность гемоглобина к связи с О2. При воздействии
на гемоглобин окислителей (перекисей, супероксидного анион-радикала, нитритов, нитропроизводных органических веществ — хининов) происходит истинное окисление гемоглобина с отнятием электрона, превращением железа гемоглобина из двухвалентного в трехвалентное. В связи с этим образуется метгемоглобин, который не способен вступать в обратимую реакцию с О2. В венозной крови содержится соединение гемоглобина с СО2 — карбогемоглобин.
Из тканей различных органов, особенно кишечника, постоянно поступают в кровь вещества, вызывающие образование метгемо-глобина в условиях нормы, однако в очень небольших количествах. Это связано с наличием в эритроцитах антиоксидантов, в частности глутатиона и аскорбиновой кислоты, препятствующих образованию метгемоглоби-на или обеспечивающих его восстановление при участии фермента НАДН—метгемогло-бинредуктазы. Восстановление метгемогло-бина в гемоглобин в эритроцитах происходит в процессе ферментативных реакций с участием дегидрогеназ и соответствующих субстратов — молочной кислоты, глюкозы, глю-козо-6-фосфата.
Карбоксигемоглобин — соединение гемоглобина с угарным газом — окисью углерода (СО). Закономерности насыщения гемоглобина окисью углерода такие же, как и для насыщения гемоглобина кислородом. Разница заключается в том, что сродство СО к гемоглобину в* 300 раз выше, чем О2 к гемоглобину; распад карбоксигемоглобина происходит в 10 000 раз медленнее, чем окси-гемоглобина. Высокое сродство гемоглобина к СО обусловливает высокую ядовитость угарного газа. Примесь даже 0,1 % СО в окружающем воздухе приводит к тому, что почти 80 % гемоглобина оказывается связанным с угарным газом и выключается из функции переноса кислорода.
Мио глобин — вещество, близкое по структуре гемоглобину, оно находится в мышцах.
В. Функции гемоглобина. Главными функциями гемоглобина являются дыхательная и буферная. Выполнение указанных функций гемоглобином возможно лишь при сохранении целостности эритроцитов, так как при гемолизе эритроцитов и выходе гемоглобина в плазму крови он быстро выводится из организма за счет фагоцитоза клетками мононук-леарной фагоцитирующей системы, а также в силу быстрого удаления через почки.
Один моль гемоглобина может связать до 4 молей кислорода, а 1 г гемоглобина —
213
1,345 мл кислорода. Кислородная емкость крови — это максимальное количество кислорода, которое может быть связано 1 мл крови. Насыщение гемоглобина кислородом составляет 96—98 %. Связывание кислорода происходит в процессе так называемой оксигена-ции, а не истинного окисления. Железо в ок-сигемоглобине остается двухвалентным. При выполнении дыхательной функции молекула гемоглобина изменяет свои размеры подобно дышащей грудной клетке. Это послужило основанием для того, чтобы назвать гемоглобин «дышащей молекулой, или молекулярными легкими». Соотношение между количеством гемоглобина и оксигемоглобина определяется в значительной степени парциальным напряжением кислорода в крови, хотя при этом и не соблюдается линейная зависимость. Это соотношение выражается в виде кривой диссоциации оксигемоглобина. Участие гемоглобина в регуляции рН крови (буферная функция) связано с его ролью в транспорте кислорода и углекислого газа, а также со свойствами его как белка, являющегося амфолитом.
Г. Поступление железа в организм и синтез гемоглобина. Синтез гемоглобина осуществляется путем синхронной продукции тема и полипептидных цепей глобина с последующим образованием законченной молекулы. Синтез гемоглобина начинается в нормоцитах. По мере дальнейшего созревания эритроидной клетки, уменьшения количества полисом в цитоплазме снижается и синтез гемоглобина. В ретикулоцитах еще возможен синтез гемоглобина на рибосомально-цитоплазматичес-ком уровне. Зрелые эритроциты не синтезируют гемоглобин. Процесс синтеза гемоглобина при эритропоэзе связан с потреблением эндогенного железа. Важную роль в обмене эндогенного железа играют следующие соединения белковой природы: трансферрин (сидеро-филин), ферритин и гемосидерин.
Трансферрин — специфический белок, содержащийся в плазме крови, представляет собой р-глобулин с молекулярной массой около 80 000 Д. Он выполняет транспортную функцию, обеспечивая перенос железа из слизистой оболочки кишечника и синусов паренхимы селезенки в костный мозг, где утилизируется в процессе эритропоэза.
Ферритин — водорастворимый комплекс гидроокиси железа с белком апоферритином. Молекулярная масса ферритина составляет около 460 000 Д, содержание железа — примерно 2 % от его массы.
Гемосидерин близок по составу к феррити-ну, содержание железа в нем составляет
около 30 % от общей массы молекулы. Основными местами депонирования гемосиде-рина являются костный мозг, печень и селезенка. В организме здорового взрослого человека содержится в целом около 3—5 г эндогенного железа, причем в фонде эритро-на — около 60—70 %; железо запасов (ферритина и гемосидерина внутренних органов) составляет 30—40 %. В составе трансферри-тина содержится около 3—4 мг железа, в ферментах различных органов и тканей имеется еще около 150 мг железа.
Содержание эндогенного железа в организме в значительной мере определяется постоянством поступления экзогенного железа, Однако этот процесс строго лимитирован; количество железа, всасываемого из пищи в течение суток даже при резко возросшей потребности в. нем, не превышает 2,0—2,5 мг, Важное значение имеет не только количество железа в данном продукте, но и форма его и соответственно возможность его всасывания из данного продукта. Железо находится во многих продуктах как растительного, так и животного происхождения. Много железа в мясе, печени, почках, бобовых культурах, сушеных абрикосах, черносливе, изюме, рисе, хлебе, яблоках. Однако из риса всасывается не более 1 % железа, из фруктов — не более 3 %. Много железа всасывается из говядины, особенно телятины, — до 22 %, из рыбы — до 11 %.
Пишевые продукты могут содержать различные формы железа, входящего в состав тема, ферритина, гемосидерина, комплексных соединений с оксалатами, фосфатами. Железо, входящее в состав гемсодержащщ соединений, всасывается значительно лучше, чем из ферритина и гемосидерина. Основным местом депонирования железа является печень, а формами депонирования — ферритин и гемосидерин.
Содержание железа в сыворотке крови имеет большой диапазон колебаний в условиях нормы — от 70 до 170 мкг% (12,5-30,4 мкмоль/л). Железосвязывающая способность сыворотки крови в норме колеблется от 30,6 до 84,6 мкмоль/л (70—470 мкг%). Под железосвязывающей способностью сыворотки крови понимают то количество железа, которое может связаться с трансферрином. Потери железа из организма происходят различными путями: с калом, мочой, потом, эпителием кожи, причем с мочой теряется около 0,1 г железа, с эпителием кожи и потом — около 0,2—0,3 мг, с калом — около 0,4 мг/сут. Известно, что железо, теряемое с калом, включает в себя железо слущивающе-
214