
- •Глава 1. Развитие представлений о природе теплоты
- •§ 1.1. Физика и механика
- •Что дает механика Ньютона?
- •Физика во времена Ньютона
- •Механическая картина мира
- •Крах механической картины мира
- •Тепловые и электромагнитные явления
- •§ 1.2. Тепловые явления
- •Роль тепловых явлений
- •Свойства тел и температура
- •Тепловые процессы и строение вещества
- •Тепловые явления в технике
- •§ 1.3. Краткий очерк развития представлений о природе тепловых явлений
- •Воззрения древних
- •Зарождение научной теории тепла
- •Теория теплорода
- •Крах теории теплорода
- •§ 1.4. Термодинамика и молекулярно-кинетическая теория Термодинамика
- •Молекулярно-кинетическая теория
- •Термодинамика и статистическая механика
- •Глава 2. Основы молекулярно-кинетической теории
- •§ 2.1. Основные положения молекулярно-кинетической теории
- •Доказательства существования молекул
- •Туннельный микроскоп
- •Размеры атомов и молекул
- •Число молекул
- •§ 2.2. Масса молекул. Постоянная Авогадро
- •Масса молекулы воды
- •Относительная молекулярная масса
- •Количество вещества
- •Постоянная Авогадро
- •Молярная масса
- •§ 2.3. Броуновское движение
- •Тепловое движение молекул
- •Модель броуновского движения
- •Наблюдение броуновского движения
- •Объяснение броуновского движения
- •Броуновское движение и измерительные приборы
- •§ 2.4. Силы взаимодействия молекул
- •Молекулярные силы
- •Электромагнитная природа молекулярных сил
- •Ориентационные силы
- •Индукционные (поляризационные) силы
- •Дисперсионные силы
- •Силы отталкивания
- •График зависимости молекулярных сил от расстояния между молекулами
- •Происхождение сил упругости
- •Атомно-силовой микроскоп
- •§ 2.5. Потенциальная энергия взаимодействия молекул
- •Зависимость потенциальной энергии от расстояния между молекулами
- •Главная задача
- •Движение частицы в пространстве с заданной потенциальной энергией
- •§ 2.6. Строение газообразных, жидких и твердых тел
- •Жидкости
- •Твердые тела
- •§ 2.7. Примеры решения задач
- •Упражнение 1
- •Глава 3. Температура. Газовые законы
- •§ 3.1. Состояние макроскопических тел в термодинамике
- •Макроскопические параметры
- •Давление газа в молекулярно-кинетической теории
- •§ 3.2. Температура. Тепловое равновесие
- •Субъективные представления о температуре
- •Происхождение терминов «температура» и «градус»
- •Первые термометры
- •Современные термометры
- •Тепловое равновесие
- •Температура
- •Молекулярно-кинетическое истолкование температуры
- •§ 3.3. Уравнение состояния
- •§ 3.4. Равновесные (обратимые) и неравновесные (необратимые) процессы
- •§ 3.5. Газовые законы. Закон Бойля-Мариотта
- •Газовые законы
- •Закон Бойля—Мариотта
- •Молекулярно-кинетическое истолкование закона Бойля—Мариотта
- •§ 3.6. Закон Гей-Люссака. Идеальный газ
- •Закон Гей-Люссака
- •Экспериментальное определение зависимости объема газа от температуры
- •Изобары
- •Идеальный газ
- •Газовая шкала температур
- •§ 3.7. Абсолютная температура
- •Абсолютный нуль температуры
- •Шкала Кельвина
- •Зависимость объема от абсолютной температуры
- •§ 3.8. Законы Авогадро и Дальтона
- •Закон Авогадро
- •Закон Дальтона
- •§ 3.9. Уравнение состояния идеального газа
- •Уравнение состояния
- •Изменение состояния газа
- •Вывод уравнения состояния идеального газа
- •Универсальная газовая постоянная
- •Уравнение Менделеева—Клапейрона
- •§ 3.10. Закон Шарля. Газовый термометр
- •Закон Шарля
- •Газовый термометр постоянного объема
- •§ 3.11. Применение газов в технике
- •Управление давлением газа
- •Большая сжимаемость газов
- •Зависимость объема газа от температуры
- •Разреженные газы
- •§ 3.12. Примеры решения задач
- •Разделив почленно уравнение (3.12.4) на уравнение (3.12.5), получим
- •При этом
- •Упражнение 2
- •Глава 4. Молекулярно-кинетическая теория идеального газа
- •§ 4.1. Системы с большим числом частиц и законы механики. Статистическая механика
- •Термодинамические параметры с микроскопической точки зрения
- •Системы из большого числа частиц и законы механики
- •Статистическая механика
- •Средние по времени и статистические средние
- •Два этапа становления статистической механики (молекулярно-кинетической теории)
- •§ 4.2. Идеальный газ в молекулярно-кинетической теории
- •Идеальный газ
- •Значение столкновений между молекулами
- •§ 4.3. Среднее значение скорости теплового движения молекул
- •Средние значения
- •Среднее значение квадрата скорости
- •§ 4.4. Основное уравнение молекулярно-кинетической теории
- •Столкновение молекулы со стенкой
- •Число соударений со стенкой молекул, скорости которых близки к VIX
- •Импульс средней силы, действующий на стенку со стороны всех молекул
- •Давление газа
- •§ 4.5. Температура— мера средней кинетической энергии молекул
- •Постоянная Больцмана
- •Физический смысл постоянной Больцмана
- •Зависимость давления газа от концентрации его молекул и температуры
- •§ 4.6. Распределение максвелла
- •Вероятность случайного события
- •Распределение молекул по скоростям — распределение Максвелла
- •Распределение модулей скоростей молекул
- •Наиболее вероятная скорость молекул
- •Роль быстрых молекул
- •§ 4.7. Измерение скоростей молекул газа
- •Средняя скорость теплового движения молекул
- •Экспериментальное определение скоростей молекул
- •Средняя скорость броуновской частицы
- •§ 4.8. Внутренняя энергия идеального газа
- •Внутренняя энергия молекулярных газов
- •§ 4.9. Примеры решения задач
- •Упражнение 3
- •Глава 5. Законы термодинамики
- •§ 5.1. Работа в термодинамике
- •Работа в механике и термодинамике
- •Вычисление работы
- •Геометрическое истолкование работы
- •§ 5.2. Количество теплоты
- •Калориметрические опыты
- •Количество теплоты. Уравнение теплового баланса
- •Теплоемкость
- •§ 5.3. Эквивалентность количества теплоты и работы
- •Опыты Джоуля
- •Механический эквивалент теплоты
- •§ 5.4. Закон сохранения энергии. Внутренняя энергия
- •Закон сохранения энергии
- •Внутренняя энергия
- •Зависимость внутренней энергии от макроскопических параметров
- •§ 5.5. Первый закон термодинамики
- •Первый закон термодинамики
- •Суть первого закона термодинамики
- •Невозможность создания вечного двигателя
- •Работа и количество теплоты — характеристики процесса изменения энергии
- •§ 5.6. Теплоемкости газа при постоянном объеме и постоянном давлении
- •Теплоемкость газа при постоянном объеме Найдем молярную теплоемкость газа при постоянном объеме. Согласно определению теплоемкости
- •Теплоемкость газа при постоянном давлении
- •Теплоемкость идеального газа при изотермическом процессе
- •§ 5.7. Адиабатный процесс
- •Теплообмен в замкнутой системе
- •§ 5.8. Необратимость процессов в природе
- •§ 5.9. Второй закон термодинамики
- •§ 5.10. Статистическое истолкование необратимости процессов в природе
- •Противоречие между обратимостью микропроцессов и необратимостью макропроцессов
- •Житейский пример необратимости
- •Микроскопическое и макроскопическое состояния
- •Вероятность состояния
- •Переход системы к наиболее вероятному состоянию
- •Расширение «газа» из четырех молекул
- •Необратимость расширения газа с большим числом молекул
- •Стрела времени
- •Границы применимости второго закона термодинамики
- •«Демон Максвелла»
- •§ 5.11. Тепловые двигатели
- •Простейшая модель тепловой машины
- •Принципы действия тепловых двигателей
- •Роль холодильника
- •Кпд теплового двигателя
- •Применение тепловых двигателей
- •Тепловые двигатели и охрана природы
- •§ 5.12. Максимальный кпд тепловых двигателей
- •Идеальная тепловая машина Карно
- •Идеальная холодильная машина
- •Тепловой насос
- •Максимальный кпд тепловых машин (теорема Карно)
- •Кпд реальных тепловых машин
- •§ 5.13. Примеры решения задач
- •Вычитая почленно из второго уравнения первое, получим
- •Упражнение 4
- •Глава 6. Взаимные превращения жидкостей и газов
- •§ 6.1. Испарение жидкостей
- •Испарение
- •Молекулярная картина испарения
- •Конденсация пара
- •Охлаждение при испарении
- •Испарение твердых тел
- •§ 6.2. Равновесие между жидкостью и паром
- •Насыщенный пар
- •Ненасыщенный пар
- •§ 6.3. Изотермы реального газа
- •Давление насыщенного пара
- •Семейство изотерм реального газа
- •Зависимость давления и плотности насыщенного пара от температуры
- •§ 6.4. Критическая температура. Критическое состояние
- •Критическая температура
- •Критическое состояние
- •Плотность жидкости и ее насыщенного пара при критической температуре
- •Экспериментальное исследование критического состояния
- •Диаграмма равновесных состояний газа и жидкости
- •§ 6.5. Кипение
- •Зависимость температуры кипения жидкости от давления
- •Различие температур кипения жидкостей
- •§ 6.6. Теплота парообразования
- •Зависимость удельной теплоты парообразования от температуры
- •§ 6.7. Сжижение газов
- •Установки для сжижения газов
- •Хранение жидких газов
- •Применение сжиженных газов
- •Значение сжижения газов для научных исследований
- •§ 6.8. Влажность воздуха
- •Парциальное давление водяного пара
- •Абсолютная влажность
- •Относительная влажность
- •Точка росы
- •Гигрометр
- •Волосной гигрометр
- •Психрометр
- •Значение влажности
- •§ 6.9. Примеры решения задач
- •Упражнение 5
- •Глава 7. Поверхностное натяжение в жидкостях
- •§ 7.1. Поверхностное натяжение
- •Поверхностные эффекты
- •Поверхность жидкости стремится к сокращению
- •§ 7.2. Молекулярная картина поверхностного слоя
- •Происхождение сил поверхностного натяжения
- •Молекулярная картина поверхностного слоя
- •§ 7.3. Поверхностная энергия
- •Поверхностное натяжение
- •§ 7.4. Сила поверхностного натяжения
- •Измерение силы поверхностного натяжения
- •От чего зависит сила поверхностного натяжения?
- •Измерение коэффициента поверхностного натяжения
- •Зависимость поверхностного натяжения от примесей
- •§ 7.5. Смачивание и несмачивание
- •Явления на границе жидкость — твердое тело
- •Значение смачивания
- •§ 7.6. Давление под искривленной поверхностью жидкости
- •Влияние кривизны поверхности на давление внутри жидкости
- •Избыточное давление под сферической поверхностью жидкости
- •§ 7.7. Капиллярные явления
- •Высота поднятия жидкости в капиллярных трубках
- •Капиллярные явления в природе, быту и технике
- •§ 7.8. Примеры решения задач
- •Упражнение 6
- •Глава 8. Твердые тела и их превращение в жидкости § 8.1. Кристаллические тела
- •Кристаллы
- •Монокристаллы и поликристаллические тела
- •Форма и размеры кристаллов
- •Полиморфизм
- •Анизотропия кристаллов
- •§ 8.2. Кристаллическая решетка
- •Четыре типа кристаллов
- •Молекулярные кристаллы
- •Ковалентные кристаллы
- •Ионные кристаллы
- •Металлические кристаллы
- •Строение кристалла объясняет его свойства
- •§ 8.3. Аморфные тела
- •Сходство аморфных тел с жидкостями
- •Переход аморфных тел в кристаллические
- •Ближний порядок
- •Объяснение свойств аморфных тел
- •§ 8.4. Жидкие кристаллы
- •Молекулы жидких кристаллов
- •Нематические жидкие кристаллы
- •Смектические жидкие кристаллы
- •Холестерические* жидкие кристаллы
- •Применение жидких кристаллов
- •§ 8.5. Дефекты в кристаллах
- •Точечные дефекты
- •Дислокации
- •Винтовая дислокация
- •Рост кристаллов
- •§ 8.6. Объяснение механических свойств твердых тел на основании молекулярно-кинетической теории
- •Механизм пластических деформаций
- •Дислокации и прочность твердых тел
- •§ 8.7. Плавление и отвердевание
- •Плавление кристаллических тел
- •Плавление аморфных тел
- •Отвердевание кристаллических и аморфных тел
- •Объяснение плавления и отвердевания на основании молекулярно-кинетической теории
- •Переохлаждение жидкости
- •§ 8.8. Теплота плавления
- •Удельная теплота плавления
- •Теплота кристаллизации
- •Роль теплоты плавления льда и кристаллизации воды в природе
- •Сопло космической ракеты
- •Фазовые переходы. Сублимация
- •§ 8.9. Изменение объема тела при плавлении и отвердевании. Тройная точка
- •Объяснение «странного» поведения льда и воды
- •Вода и лед в природе
- •Зависимость температуры плавления от давления
- •Тройная точка
- •§ 8.10. Примеры решения задач
- •На плавление льда пошло количество теплоты
- •Следовательно, согласно закону сохранения энергии
- •Упражнение 7
- •Глава 9. Тепловое расширение твердых и жидких тел
- •§ 9.1. Тепловое расширение тел
- •Молекулярная картина теплового расширения
- •§ 9.2. Тепловое линейное расширение
- •§ 9.3. Тепловое объемное расширение
- •Связь между коэффициентами линейного и объемного расширения
- •Зависимость плотности вещества от температуры
- •Пользуясь формулой (9.3.3), можно записать
- •Пренебрегая выражением (αΔt)2по сравнению с единицей, получим
- •Тепловое расширение жидкостей
- •Особенности расширения воды
- •§ 9.4. Учет и использование теплового расширения тел в технике
- •Учет теплового расширения тел
- •Использование теплового расширения в технике
- •Терморегулятор
- •§ 9.5. Примеры решения задач
- •Образовавшийся зазор между пробкой и горлышком составит
- •Подставляя числовые значения величин, найдем
- •Упражнение 8
- •Ответы к упражнениям
- •Содержание
§ 3.11. Применение газов в технике
Газы обладают рядом свойств, которые делают их незаменимыми в очень большом числе технических устройств. Все особенности поведения газов, позволяющие использовать их на практике, можно установить с помощью уравнения состояния (3.9.9).
Газ — сжатое упругое тело
Как следует из уравнения состояния, давление, оказываемое газом на стенки сосуда, равно
![]() (3.11.1)
(3.11.1)
Это давление исчезает лишь при т → 0 (газа почти нет) или V → ∞ (газ неограниченно расширился), а также при Т→ 0 (молекулы газа не движутся).
Сила давления газа на стенки F = pS, представляет собой частный вид силы упругости. Газ подобен пружине, которая всегда сжата. Важно, что газ малой массы способен создавать сравнительно большое давление.
Управление давлением газа
Давление газа можно менять, изменяя его объем или температуру. Кроме того, силу давления газа легко регулировать и не меняя его объема или температуры. Газ — это сжатая «пружина», «жесткость» которой можно быстро изменить, используя прямо пропорциональную зависимость давления газа от его массы (см. формулу (3.11.1)). Увеличивая массу газа в любом замкнутом пространстве, мы можем увеличить давление. Так и поступают, например, накачивая автомобильную шину или футбольный мяч воздухом. Выпуская часть газа из сосуда, уменьшают его давление.
Большая сжимаемость газов
Газы, особенно при давлениях, близких к атмосферному, по сравнению с жидкостями и твердыми телами легко сжимаются. Это означает, что небольшое изменение давления заметно меняет их объем. И наоборот, значительное изменение объема не приводит к большому изменению давления.
Благодаря большой сжимаемости газа сила его давления мало меняется при расширении или сжатии. Поэтому газ, толкая поршень, совершает значительную работу на большом отрезке пути.
Хорошая сжимаемость газов позволяет запасать их в больших количествах в баллонах, удобных для хранения. Сжатый природный газ транспортируется по трубам на расстояния в тысячи километров.
Зависимость объема газа от температуры
Объем газов значительно увеличивается при увеличении температуры. При нагревании на 1 °С объем газа при постоянном давлении увеличивается в сотни раз больше, чем объем жидких и твердых тел.
Все перечисленные свойства газов используются в технике.
Газ — амортизатор
Свойство газа не сохранять свою форму, малая его плотность и возможность регулировки давления делают газ одним из самых совершенных амортизаторов.
Вот как работает автомобильная или велосипедная шина. Когда колесо наезжает на бугорок, шина с находящимся в ней воздухом деформируется (рис. 3.16) и толчок, получаемый осью колеса, значительно смягчается. Если бы шина была жесткой, то ось подпрыгнула бы вверх на высоту бугорка или Рис .3.16 еще больше.
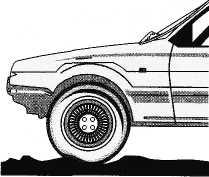
Рис. 3.16
Газ — рабочее тело двигателей
Большая сжимаемость газов и ярко выраженная зависимость их давления и объема от температуры делают газ «удобным» рабочим телом в двигателях, работающих на сжатом газе, и в тепловых двигателях.
В двигателях, работающих на сжатом газе, в частности на сжатом воздухе, газ (воздух) при расширении вследствие хорошей сжимаемости совершает работу почти при постоянном давлении. Сжатый воздух, оказывая давление на поршень, открывает двери в автобусах, поездах метро и электричках. Сжатым воздухом приводят в движение поршни воздушных тормозов железнодорожных вагонов и грузовиков. Пневматический молоток и другие пневматические инструменты приводятся в движение сжатым воздухом.
Даже на космических кораблях имеются небольшие реактивные двигатели, работающие на сжатом газе — гелии. Они ориентируют корабль нужным образом.
В двигателях внутреннего сгорания на автомобилях, тракторах, самолетах и в реактивных двигателях в качестве рабочего тела, приводящего поршень, турбину или ракету в движение, используют газы высокой температуры.
При сгорании горючей смеси в цилиндре (например, паров бензина и воздуха) температура резко увеличивается, давление на поршень растет и газ, расширяясь, совершает работу на всей длине рабочего хода поршня (рис. 3.17).
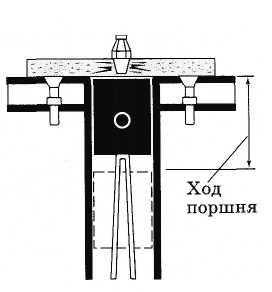
Рис. 3.17
Практически только газ можно эффективно использовать в качестве рабочего тела в двигателях. Нагревание жидкого или твердого тела до такой же температуры, как и газа, вызвало бы лишь незначительное перемещение поршня.
Любое огнестрельное оружие в сущности является тепловой машиной. Рабочее тело здесь тоже газ — продукты сгорания взрывчатых веществ. Сила давления газа выталкивает пулю из канала ствола или снаряд из дула орудия. И существенно, что эта сила совершает работу на всей длине канала. Поэтому скорости пули и снаряда оказываются огромными: сотни метров в секунду.
