
- •Под редакцией профессора э. В. Недашковского
- •Отв. Редактор - проф. Э.Недашковский
- •Оглавление
- •Раздел 1. Вопросы общей анестезиологии
- •Раздел 2. Вопросы частной анестезиологии
- •Раздел 3. Регионарная анестезия, лечение боли
- •Раздел 4. Вопросы интенсивной терапии
- •Раздел 5. Общая информация
- •Раздел 6. Актуальные аспекты респираторной терапии
- •Раздел 1. Вопросы общей анестезиологии
- •Медикаментозное лечение интраоперационной ишемии миокарда
- •Принципы риска и безопасность
- •Раздел 1. Смерть младенца вследствие трудных родов
- •Раздел 2. Проблема оказания помощи
- •Участие ррак в переносе сигнальной информации и апоптозе
- •Ингибиторы ренин-ангиотензиновой системы и анестезия
- •Методы определения глубины анестезии
- •Анализ электроэнцефалограммы
- •Гипертрофическая обструктивная кардиомиопатия
- •Гемодинамические цели при митральной регургитации
- •163061, Архангельск, пр. Троицкий, 51, каб.330.
- •Одиночные или множественные подергивания?
- •Роль послеоперационной анальгезии при амбулаторных хирургических вмешательствах
- •Литература
- •Лечение хронических болевых синдромов детского возраста
- •Лекарства и плацента
- •Физиологические изменения фармакологии при беременности Сердечно-сосудистая система
- •2. Факторы, влияющие на плацентарный транспорт
- •2.1 Маточные факторы
- •2.2 Плацентарные факторы
- •2.3 Факторы плода
- •3. Анестезиологические препараты и трансплацентарный транспорт
- •3.1 Внутривенные препараты
- •3.2 Закись азота и галогенные анестетики
- •3.3 Миорелаксанты
- •3.4 Опиоиды ,
- •3.5 Местные анестетики и регионарная анестезия
- •Применение ларингеальной маски в акушерстве
- •Анестезиологический осмотр в акушерстве
- •24 Часов
- •I. Нужна ли госпитализация?
- •II. Тяжелые ожоги: что должно быть сделано до перевода в ожоговый центр?
- •1) Как поступить: охлаждать ожоги или согревать пациента?
- •2) Подготовка к дальнейшему лечению
- •3) Количество и состав сред инфузионной терапии
- •4) Анальгезия и седация '
- •5) Респираторная поддержка
- •6) Особые случаи
- •1. Мониторный контроль состояния кардио-респираторной системы и жидкостных секторов организма
- •1. Патогенез
- •1.1. Методика дилюционной тромбоцитопении и коагулопатии
- •1.2. Диссеминированное внутрисосудистое свертывание (двс)
- •1.3. Гипотермия
- •2.1. Профилактические компоненты терапии
- •2.2. Можем ли мы полагаться на клинические данные?
- •2.3. Можем ли мы полагаться на данные исследований гемостаза?
- •2.4. Дополнительные подходы
- •Вопрос 1: как пользоваться компасом в лесу информации?
- •Вопрос 3: насколько интересно название статьи? кто авторы? насколько различается профиль ваших лечебных учреждений?
- •Вопрос 4: четко ли изложены выводы работы в тезисах статьи?
- •Вопрос 5: надежда и вера: где гипотеза?
- •Вопрос 6: какие методы используются для сбора данных? насколько подробно они описаны?
- •Вопрос 7: как представлены средние величины?
- •Вопрос 8: были ли представлены наиболее важные клинические параметры и исходы?
- •Вопрос 9: достоверны ли результаты статистически? насколько они важны с клинической точки зрения?
- •Вопрос 10: верю ли я результатам прочитанной работы?
Анализ электроэнцефалограммы
Сжатый спектральный ряд (массив)
Метод сжатого спектрального ряда (ССР, англ: CSA - compressed spectral array) направлен на измерение распределения сигналов ЭЭГ по их мощности. Производиться запись дискретных периодов ЭЭГ (в течение 2 или 8 секунд), которые далее подвергаются быстрой трансформации Фурье, что позволяет разделить суммарную мощность импульсов в зависимости от их частоты. Значение мощности импульсов определенной частоты может быть отображено графически в виде последовательности, состоящей из плато и пиков. В то же время математический анализ ССР дает возможность математического извлечения одинарных численных значений, которые могут в свою очередь использоваться в качестве показателя центрального эффекта анестетиков.
Спектральной границе соответствует уровень частоты ЭЭГ-сигналов, ниже которого находится 95% суммарной мощности ССР: данный показатель пытаются применить для измерения верхней границы спектрального распределения мощности. Было продемонстрировано постепенное снижение спектральной границы на фоне увеличения концентрации анестетиков, но четкой корреляции между ее значением и глубиной анестезии обнаружено не было. Анализ ССР дает средневзвешенную частоту (СЧ), которая представляет собой срединное значение распределения спектрального ряда. СЧ представляет собой значение частоты, ниже и выше которого лежит 50% суммарной мощности импульсов ЭЭГ. Было выдвинуто предположение, что значение средневзвешенной частоты является точным показателем глубины анестезии. В то же время попытка исследования системы мониторинга, основанной на принципе «замкнутой петли» и использовании данного показателя при анестезии пропофолом, не дала положительных результатов. Достигнутая глубина анестезии не соответствовала условиям, в которых возможно начало и выполнение хирургического вмешательства, так как потеря роговичного рефлекса отмечалась не у всех добровольцев [5].
Биспектральный показатель
Биспектральный анализ – более новый метод анализа ЭЭГ, основанный на обработке фазовых межчастотных связей ЭЭГ [6]. Биспектральный показатель (БП, англ. BIS – bispectral index) представляет собой средневзвешенное значение измерения, анализирующего фазовые и частотные связи между тремя составляющими частотами ЭЭГ (схема 1)
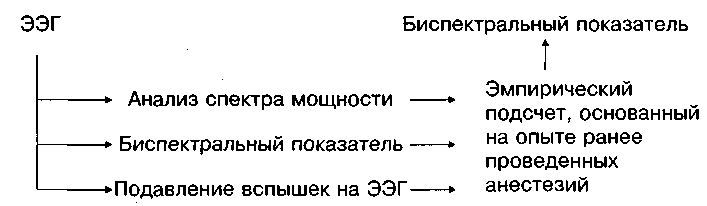
Схема 1. Как рассчитывается биспектральный показатель
БП оказался более точным показателем, чем другие типы анализа, например CCPJ но и он может претерпевать определенные межпоказательные отклонения [7]. При и&[ следовании пациентов на фоне анестезии закисью азота или фентанилом [8, 9] можно не обнаружить изменений на ЭЭГ при переходе от бодрствования ко сну. Кроме того, малопоказательно применение данного показателя у многих пациентов при анестезии изофлюраном [10].
Слуховые вызванные потенциалы
Изучение ССГТ (соматосенсорные потенциалы) является альтернативной методикой определения глубины анестезии. На фоне передачи звуковых стимулов (щелчков) через наушники производится запись ЭЭГ. Электроды расположены на волосистой части головы. Происходит запись, обработка и усреднение от сотен до тысяч импульсов ЭЭГ, в результате чего рассчитывается ССП (рисунок 2а и 2b). Имеются сообщения о том, что ССП надежно отражают уровень анестезии в течение различных этапов хирургического вмешательства [11].
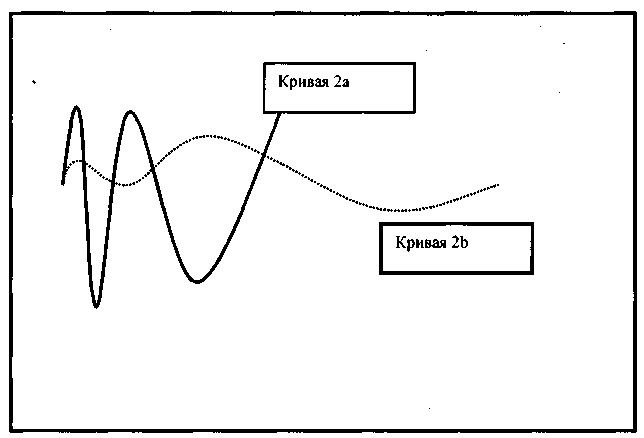
Рисунок 2
Кривая 2а - типичная форма кривой ССП, записанных у пациентов в сознании.
Кривая 2b - типичная форма кривой ССП во время анестезии. Видно увеличение сглаженности пиков и снижение их амплитуды.
Единственный показатель, являющийся производным от ССП - Ехссп> четко коррелирует с клиническим состоянием пациентов при серийном многократном переходе от состояния сна к бодрствованию [1, 12]. Данный показатель отличается меньшей вариабельностью, чем БП [12, 13]. При исследованиях, проведенных на фоне гипотермии и искусственного кровообращения, устойчивое значение показателя было в пределах 30-40, в то время как БП варьировал от 10 до 90 ед. [14]. БП рассматривался как индикатор глубины анестезии, но он не позволял предугадать реакции больного. Индекс ССП позволяет предугадать движения пациента во время введения ларингеальной маски на фоне индукции пропофолом [15] и при разрезе во время анестезии севофлюраном [16].
Методика «замкнутой петли» в мониторинге глубины анестезии
Последним требованием к измерению глубины анестезии является автоматическое определение скорости поступления анестетика для развития адекватной анестезии на фоне спонтанного дыхания. Любые, действующие по принципу замкнутой петли системы мониторинга должны быть точными, надежными и быстродействующими. Необходимо быстрое реагирование подобных систем на изменение характера входящих сигналов.
Применение показателя систолического артериального давления в качестве входного сигнала системы замкнутой петли отвечало за изменение количества ингаляционных анестетиков, а также позволяло производить дополнительное введение морфина [17]. Однако применение системы имело место только после развития адекватной анальгезии и на фоне интраоперационной миорелаксации. У трех пациентов не удалось достигнуть адекватного контроля над течением анестезии.
Средневзвешенная частота сжатого спектрального ряда также применялась для контролируемого введения внутривенных анестетиков, но не исследовалась у пациентов с сохранением во время оперативного вмешательства спонтанного дыхания [5]. Дальнейшее развитие метод замкнутой петли получил при контролированной седации пропофолом на фоне эпидуральной анестезии, при этом в качестве входного сигнала был использован биспектральный показатель [18]. Система функционировала удовлетворительно, но в то же время в данной клинической ситуации уровень хирургической стимуляции представляется минимальным.
Вызванные слуховые потенциалы (ВСП) были использованы в роли входного сигнала системы замкнутой петли при управлении дозированием пропофола во время хирургических вмешательств, производимых на фоне спонтанного дыхания [2]. Извлечение сигнала СВП из кривой волны производилось каждые три секунды, при этом качество анестезии поддерживалось на приемлемом уровне под контролем ответа симпатической нервной системы и двигательной реакции. Метод с применением СВП был использован для отображения фармакодинамической потребности в пропофоле и обеспечения непредвзятой оценки пропофол-сберегающих эффектов ремифентанила [19].
Сон и анальгезия
Изучение пропофол-сберегающих эффектов ремифентанила продемонстрировало существование взаимосвязи между состоянием сна, анальгезией и стимуляцией и показало, что развитие адекватной анестезии не у всех пациентов зависит только от отдельно взятой концентрации анестетика. Действительно, в каждом отдельном случае потребность в анестетике значительно варьирует и зависит от выраженности хирургической стимуляции и качества анальгезии в любой определенный момент времени. Показатель СВП способен предоставить информацию, объединяющую в себе уровень гипнотического эффекта, качество анальгезии и выраженности хирургической стимуляции (схема 3).
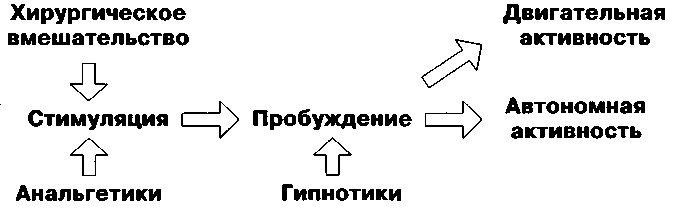
Схема 3: Отношения между хирургической стимуляцией, анальгезией и сном. Анальгетики подавляют стимулирующее влияние хирургического вмешательства и снижают потребность в гипнотиках [20].
Применение низких доз анальгетиков требует создания относительно высокой концентрации гипнотических препаратов. В противоположность этому, при введении анальгетиков в высоких дозах, адекватная анестезия может поддерживаться и формироваться при использовании меньших доз гипнотических препаратов. Наиболее ясно последнюю взаимосвязь демонстрирует проведение хорошей премедикации и формировании адекватного местного блока еще до доставки в операционную. В этих обстоятельствах, на фоне потенциального отсутствия хирургической стимуляции потребность в анестетиках может быть снижена до крайне низких значений.
Заключение
Предложено много новых разработок, объединенных общей целью – предоставить анестезиологу надежный метод контроля глубины анестезии. Для каждого из этих методов должны быть предъявлены определенные требования. В таблице 2 представлены тесты, предложенные для определения состоятельности и надежности той или иной методики определения глубины анестезии.
Литература:
1. Davies FW, Mantzaridis H, Kenny GNC, Fisher AC. Middle latency auditory evoked potentials during repeated transitions from consciousness to unconsciousness. Anesthesia 1996; 51:107-113.
2. Kenny GN, Mantzaridis H. Closed-loop control ofpropofol anesthesia. Br J Anaesth 1999; 83(2): 223-228.
3. Sandin RH, Enlund G, Samuelsson P, Lennmarken C. Awareness during anesthesia: a prospective case study. Lancet 2000; 355(9205): 707-711.
4. Russel IF. Midazolam-alfentanil: an anesthetic? An investigation using the isolated forearm technique. Br] Anaesth 1993; 70: 42-46.
5. Schwilden H, Stoeckel H, Schutler J. Closed loop feedback control of propofol anesthesia by quantitative EEC analysis in humans. BrJ Anaesth 1989; 62:290-296.
6. Ramp// IJ. A primer for EEC signal processing in anesthesia. Anesthesiol 1998; 89(4): 980-1002.
7. Vernen JM, Lang E, Sebel PS, Manberg P. Prediction of movement using bispectral EEC analysis during propofol/alfentanil or isoflurane/alfentanil anesthesia. Anesthesia & Analgesia 1995; 80(4)-.780-785.
8. Barr G, Jakobsson JG, Owall A, Anderson RE. Nitrous oxide does not alter bispectral index: study with nitrous oxide as sole agent and as adjunct to i.v. anesthesia. BrJ Anaesth 1999; 82(6): 827-830.
9. Barr G, Anderson RE, Owall A. Jakobsson JG. Effect of the bispectral index during medium-high dose fentanyl induction with or without propofol supplement. Acta Anesthesiol Scand 2000; 44(7): 807-811.
10. Detsch O, Scheneider G, Kochs E, Hapfelmeier G, Werner C. Increasing isoflurane concentration may cause paradoxical increases in the EEC bispectral index in surgical patients. BrJ Anaesth 2000; 84(1): 33-37.
11. Thornton C, Konieczko K, Jones JG? Jordan C, Dore CJ, Heneghan CP. Effect of surgical stimulation on the auditory evoked response. BrJ Anaesth 1988; 60:372-378.
12. Gajraj RJ, Do/ M, Mantzaridis H, Kenny GN. Analysis of the EEC bispectrum, auditory evoked potentials and the EEC power spectrum during repeated transitions from consciousness to unconsciousness. BrJ Anaesth 1998; 80: 46-52.
13. Do/ M, Gajraj RJ, Mantzaridis H, Kenny GNC. Relationship between calculated blood concentration of propofol and electrophysiological variables during emergence from anesthesia: a comparison of bispectral index, spectral edge frequency, median frequency and auditory evoked potentials index. BrJ Anaesth 1997; 78(2): 180-184.
14. Do/ M, Gajraj RJ, Mantzaridis H, Kenny GN. Effect of cardiopulmonary bypass and hypothermia on EEC variables. Anesthesia 1997; 52:1048-1055.
15. Do/ M, Gajraj RJ, Mantzaridis H, Kenny GN. Prediction of movement at laryngeal mask airway insertion: comparison of auditory evoked response index, bispectral index, spectral edge frequency, and median frequency. Br J Anaesth 1999; 82: 203-207.
16. Kurita T, Do/ M, K, oh T, Kenny GN, Sato K. Auditory evoked potentials index predicts movement in response to skin incision during sevoflurane anesthesia. Anesthesiology 91, A501-A501.1999.
17. Robb HM, Asbury AJ, Gray WM, Linkens DA. Towards a standardized anesthetic state using isoflurane and morphine. Br J Anaesth 1993; 71:366-369.
18. Mortair E, Strays M, De ST, Versihelen L, Roily J. Closed loop controlled administration ofpropofol using bispectral analysis. Anesthesia 1998; 53(8): 749-754.
19. Milne SE, Kenny GN. Increasing the remifentanil target blood concentration reduces closed loop propofol administration. BrJ Anaesth 82 (suppl.), 119-119. 19-99.
20. Do/ M, Gajraj RJ, Mantzaridis H, Kenny GN. Comparison of bispectral EEC analysis and auditory evoked potentials for monitoring depth of anesthesia during propofol anesthesia. BrJ Anaesth 1999; 82(5): 672-678.
АНЕСТЕЗИЯ У БОЛЬНЫХ С ЗАБОЛЕВАНИЯМИ КЛАПАНОВ СЕРДЦА ПРИ НЕКАРДИАЛЬНЫХ ОПЕРАЦИЯХ
В. Шлак (Дюссельдорф, Германия)
Анестезия у больных с поражением клапанов сердца может представлять определенные трудности. Периоперационный риск зависит от степени и прогрессирования заболевания. Целью анестезии является сохранение больного сердца в «оптимально рабочем состоянии». Однако в зависимости от вида поражения это состояние меняется.
В лекции приводится патофизиологические особенности каждого вида поражения, предоперационная оценка, цели управления гемодинамикой и методы лечения. Рекомендации по профилактике эндокардита приведены в приложении.
Понятие кривой «давление-объем»
Кривая «давление-объем» помогает понять гемодинамические особенности различных видов поражения клапанов. На рисунке 1 представлено соотношение между давлением и объемом в левом желудочке (ЛЖ) во время сердечного цикла в норме. В момент А открывается митральный клапан и заполняется левый желудочек. Давление в ЛЖ нарастает с увеличением в нем объема крови (линия АВ). Эта линия отражает пассивное отношение (покоя) давление-объем в левом желудочке, которое в основном зависит от податливости («жесткости») желудочка. В момент В ЛЖ начинает сокращаться и митральный клапан закрывается. Увеличивается изоволемическое давление (линия ВС) до точки С, в этот момент давление в левом желудочке превышает давление в аорте и открывается аортальный клапан. Начинается фаза изгнания (линия CD), давление увеличивается дальше, а объем крови уменьшается. В момент D аортальный клапан закрывается и наступает изоволемическая релаксация (при постоянном желудочковом объеме быстро снижается желудочковое давление (линия DA)). Зона кривой давление-объем равна внешней работе, выполняемой сердцем в течение одного цикла.
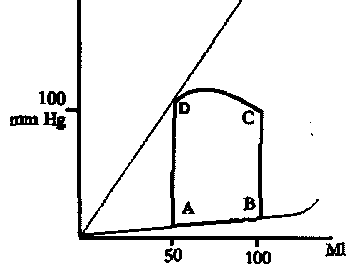
Рис. 1. Нормальная кривая давление-объем.
Положительное инотропное влияние усиливает работу сердца (рис. 2). При том же конечном диастолическом объеме (объем в момент В) создается более высокое давление и больший объем изгоняется из желудочка. На следующих рисунках для сравнения с патологией при поражении клапанов нормальная кривая давление-объем показана в виде пунктирной линии. Анализ кривой давление-объем поможет объяснить цели анестезиологического пособия для поддержания гемодинамической стабильности у больных с заболеваниями клапанов.
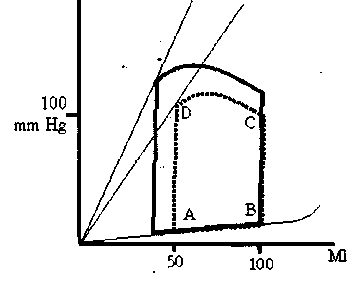
Рис. 2. Влияние инотропной стимуляции на кривую давление-объем (пунктирная линия норма).
Аортальный стеноз
Аортальный стеноз представляет собой препятствие изгнанию объема левого желудочка через аортальный клапан. В норме площадь аортального клапана 2-3 см2. Гемодинамически значимым является уменьшение площади менее 1,5 см2, а если она становится меньше 0,4 см2 или градиент давления больше 50 mm Hg, стеноз является критическим. Основные причины стеноза аорты – врожденная патология клапанов (двустворчатый клапан), кальциноз и ревматическое поражение сердца. При современной антибактериальной терапии большинство аортальных стенозов вызваны калыдификацией двустворчатого аортального клапана (двустворчатый аортальный клапан встречается в 2% случаев).
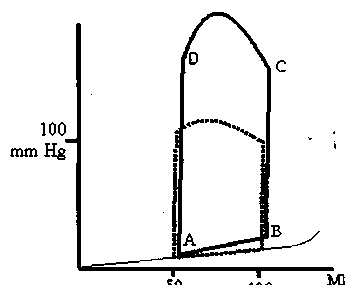
Рис. 3. Сравнение кривой давление-объем при аортальном стенозе по сравнению с нормой (пунктирная линия).
На рисунке 3 показана типичная кривая давление-объем при аортальном стенозе. Обструкция оттока требует создания высокого давления в левом желудочке для изгнания крови, работа сердца усиливается, что отражается в увеличении площади кривой давление-объем. Сердце адаптируется к работе при повышенном давлении с помощью концентрической гипертрофии, т.е. увеличения мышечной массы ЛЖ при его нормальном объеме. Гипертрофия стенки желудочка приводит к увеличению количества миофибрилл. Увеличение толщины стенки при нормальном объеме левого желудочка сохраняет ее напряжение на нормальном уровне несмотря на увеличенное давление. К сожалению, увеличение мышечной массы ЛЖ не сопровождается увеличением количества капилляров, поэтому часто при нагрузке возникают признаки ишемии миокарда, а на поздних стадиях у 50% больных наблюдается стенокардия даже при отсутствии поражения коронарных артерий. Кривая давление-объем показывает уменьшение комплайнса левого желудочка (линия" АВ). Чтобы достичь необходимый конечный диастолический объем в «жестком» желудочке, требуется гораздо большее давление заполнения. Высокое конечное диасто-лическое давление увеличивает риск развития ишемии миокарда, которая, в свою очередь, нарушает расслабление ЛЖ. Низкий комплайнс ЛЖ («плотный желудочек») приводит к усилению роли предсердий в заполнении желудочка. В норме сокращение предсердия обеспечивает 15-20% желудочкового наполнения, а в условиях аортального стеноза способствует наполнению на 40%. Это значит, что внезапное нарушение синусового ритма может быть катастрофическим. В противоположность другим вариантам патологии сердечная недостаточность в условиях аортального стеноза является не результатом необратимого нарушения насосной функции сердца, а истощения резервов компенсации преднагрузки. Несмотря на достаточную сократимость, «плотный» желудочек заполняется недостаточно. Высокое давление заполнения отражается на легочном кровообращении.
К клиническим симптомам аортального стеноза относятся:
• стенокардия;
• сердечная недостаточность;
• синкопальные состояния;
• внезапная смерть.
Если не используется хирургическое лечение, продолжительность жизни после возникновения симптомов сокращается до 2-5 лет. С другой стороны, не у всех больных с тяжелым аортальным стенозом наблюдаются соответствующие симптомы. Если при физическом обследовании выявлены симптомы аортального стеноза (типичный систолический шум), определить тяжесть поражения может помочь эхокардиография.
Главной целью во время анестезии является уменьшение работы желудочка на оптимальном уровне - для проталкивания крови через стеноз лучшим вариантом является низкая частота и высокий ударный объем. Необходимо избегать тахикардии (интубаци-онная реакция, хирургическая стимуляция) с помощью углубления анестезии и дополнительного введения опиоидов. В то же время гипертрофированный миокард требует большой преднагрузки для заполнения ЛЖ, поэтому также необходимо поддержание синусового ритма и достаточное инфузионная терапия.
В противоположность нормальному состоянию низкое периферическое давление не уменьшает работу желудочков, т.к. не оно определяет давление в левом желудочке, а стеноз. Низкое артериальное давление уменьшает коронарное перфузионное давление, т.к. коронарные артерии лежат перед стенозом. Низкое коронарное давление, в свою очередь, может вызвать ишемию миокарда, потому что давление внутри левого желудочка остается высоким. Следовательно, для предотвращения падения артериального давления необходимо быстро применять вазопрессоры. Спинальная анестезия, уменьшающая пред- (наполнение желудочка) и постнагрузку (давление коронарной перфузии), неблагоприятна для больных с тяжелым аортальным стенозом. Большинство анестезиологов не используют катетер Свана-Ганца, т.к. при возникновении вентрикулярной фибрилляции шанс успешной сердечной реанимации значительно уменьшается.
Гемодинамические цели при аортальном стенозе
• нормальная (низкая) частота сердечных сокращений;
• поддержка синусового ритма;
• адекватная волемическая нагрузка;
• нормальное периферическое сопротивление.
