
- •В.Н. Захарченко Курс физической химии Москва
- •Часть 2. Электрохимические системы и электрохимические процессы
- •Термодинамика гальванического элемента
- •Гальванический элемент
- •Термодинамика гальванического элемента
- •Электродный потенциал. Электродные реакции
- •Основные типы электродов
- •Классификация электродов
- •Электроды 1-го рода
- •Электроды 2-го рода
- •Окислительно-восстановительные электроды
- •Газовые электроды
- •Ионоселективные электроды
- •Ионы в растворах электролитов
- •Классическая теория электролитической диссоциации
- •Взаимодействие растворяемого вещества с растворителем
- •Межионное взаимодействие в растворах
- •Термодинамика растворов электролитов
- •Формальные представления об активности ионов в растворах электролитов
- •Экспериментальные данные по коэффициентам активности
- •Явления переноса в растворах электролитов
- •Диффузия в растворах электролитов
- •Диффузионный потенциал
- •Электрическая проводимость растворов электролитов
- •Электрохимическая поляризация
- •Эдс поляризации и электродная поляризация
- •Теории электродной поляризации
- •Характеристика электрохимических цепей
- •Основные принципы классификации электрохимических цепей
- •Физические электрохимические цепи
- •Гравитационные цепи
- •Аллотропические цепи
- •Концентрационные цепи
- •Химические электрохимические цепи
- •Простые химические цепи
- •Сложные химические цепи
- •Химические источники тока
- •Эталонные гальванические элементы
- •Первичные гальванические элементы
- •Элемент Лекланше
- •Ртутнооксидный элемент
- •Индийсодержащие элементы
- •Элементы с твердыми электролитами
- •Резервные элементы
- •Вторичные гальванические элементы
- •Свинцовый аккумулятор
- •Щелочной аккумулятор
- •Серебряный аккумулятор
- •Часть 3. Химическая кинетика и катализ
- •Формальная кинетика
- •Основные понятия
- •Классификация химических реакций по их кинетике
- •Необратимая реакция первого порядка
- •Необратимая реакция второго порядка
- •Два случая бимолекулярной реакции
- •2A Продукты реакции,
- •Необратимая реакцияn-ого порядка
- •Методы определения порядка реакции
- •Дифференцирование кинетической кривой
- •Кинетика сложных реакций
- •Параллельные реакции
- •Обратимая реакция
- •Последовательные реакции
- •Влияние температуры на скорость химических реакций
- •Эмпирические закономерности влияния температуры на скорость реакций
- •Уравнение Аррениуса
- •Элементарные акты химических превращений
- •Теория активных столкновений
- •Механизм мономолекулярных реакций по теории активных столкновений (схема Линдемана)
- •Теория переходного состояния (теория активного комплекса)
- •Химическая индукция
- •Фотохимические процессы
- •Основные законы фотохимии
- •Механизм фотохимических реакций
- •Цепные реакции
- •Общие сведения о цепных реакциях
- •Зарождение цепи и методы обнаружения свободных радикалов
- •Развитие и обрыв цепи
- •Катализ
- •Общие сведения
- •Гомогенный катализ
- •Кислотно-основной катализ
- •Ферментативный катализ
- •Гетерогенный катализ
- •Предметный указатель
- •Оглавление
Газовые электроды
Газовые электроды представляют собой разновидность окислительно-восстановительных электродов, на которых протекают реакции с участием газов. Наибольший интерес из этой группы представляют водородный и кислородный электроды.
Водородный электрод. Этот электрод содержит платинированную платину, погруженную в водный раствор и одновременно контактирующую с пузырьками водорода. Платинированная платина (используются другие названия: черненная платина, серая платина) покрыта электролитическим способом мельчайшими частицами платины, имеет высокую удельную поверхность и обладает каталитическими свойствами, что ускоряет наступление равновесия реакции с участием газообразного водорода.
На водородном электроде протекает реакция:
2H+ + 2e = H2.
Условно водородный электрод записывается следующим образом:
H+H2, Pt или H+H2 (Pt).
Замечательной особенностью водородного электрода является то, что по предложению В.Нернста стандартный водородный электрод был принят в качестве стандартного электрода сравнения. Следовательно, стандартный потенциал водородного электрода равен 0. Напомним, что стандартным условиям отвечают: активность ионоводорода равна 1 и давление водорода, рассматриваемого как идеальный газ, равно 1 атм или 1,01325105 Па. Следовательно, если давление водорода выражать в атмосферах, то выражение для электродного потенциала принимает следующий вид:
 .
(2 - 7)
.
(2 - 7)
Если же давление выражается в Паскалях, то формула для расчета электродного потенциала может быть записана так:
 .
.
При постоянном давлении водорода потенциал водородного электрода зависит только от водородного показателя среды:
= bpH.
В связи с этим водородный электрод является главным рН‑ метрическим электродом.
Кислородный электрод. Существуют два варианта рассмотрения кислородного электрода. Первому из них отвечают следующие характеристики:
1/2O2 + H2O + 2e = 2OH,
OHO2, Pt,
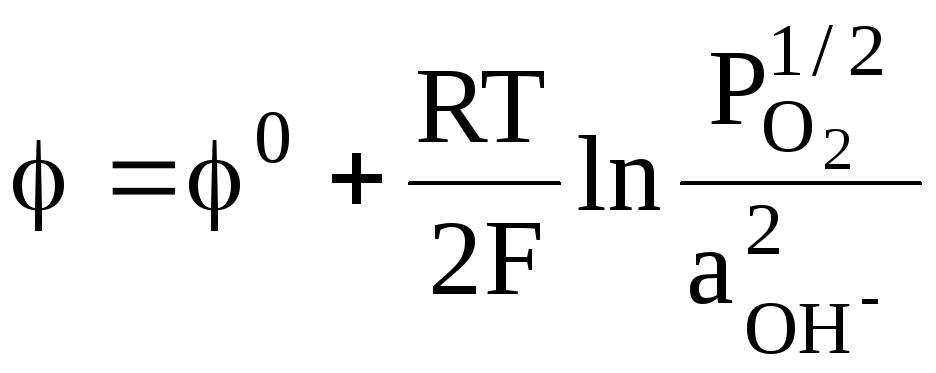 ,
,
0 = + 0,401 В,
а второй характеризуется следующим:
1/2O2 + 2H+ + 2e = H2O,
H+O2, Pt,
![]()
0 = +1,228 B.
Кроме приведенных реакций на кислородном электроде могут протекать реакции с образованием пероксида водорода и пероксид-ионов. В связи с этим воспроизводимый кислородный электрод реализовать не удается.
Ионоселективные электроды
Электроды этого типа содержат мембрану, обладающую ионообменными свойствами. Твердая мембрана может быть изготовлена из однородного материала или из частиц ионообменного вещества в твердом связующем, чаще всего в пластической массе. На границе мембраны с раствором могут протекать процессы:
Mz+(раствор) = Mz+(мембрана)
или
Аz+(раствор) = Ax−(мембрана),
где Mz+(раствор) или Аz+(раствор) – катионы или анионы, содержащиеся в растворе, Mz+(мембрана) или Ax−(мембрана) - те же ионы, содержащиеся в мембранах.
Равновесному отношению активностей в растворе и мембране отвечает скачок потенциала. Так как скачок потенциала зависит от определенного сорта ионов, то поверхность мембран рассматривается подобно электроду, обладающему избирательными свойствами по отношению к ионам, и называется ионоселективным электродом.
В частности, потенциал поверхности, зависящий от активности катионов Mz+, можно выразить следующим образом:
 (2
- 8)
(2
- 8)
Самым распространенным ионоселективным электродом является стеклянный электрод, к изучению которого мы приступаем.
Стеклянный электрод представляет собой стеклянную мембрану, разделяющую два раствора, в одном из которых поддерживается постоянной концентрация водородных ионов, а в другом растворе необходимо определить водородный показатель. Потенциал на границе раствор – стеклянная поверхность, на которой протекает процесс:
H+ = H+(ст),
где H+ и H+(ст) означают ионы водорода в растворе и в стекле, может быть выражен формулой:
 .
.
Способ нахождения отношения активностей ионов водорода в растворе и стекле был предложен Б. П. Никольским на основе представлений об ионном обмене.
Электродное стекло содержит ионы щелочного металла M+, которые могут замещаться ионами водорода. Ионному обмену
M+(ст) +H+ = M+ + H+(ст)
отвечает константа равновесия

Предполагается, что замещаться могут ионы во всех доступных местах данной мембраны и число замещаемых мест всегда остается постоянным:
![]()
Из двух последних равенств следует

и
![]() .
(2 - 9)
.
(2 - 9)
Если
константа ионного обмена очень мала,
что обеспечивается подбором состава
стекла, то выполняется условие:
![]() .
Для такого образца стекла выражение
для электродного потенциала приобретает
вид:
.
Для такого образца стекла выражение
для электродного потенциала приобретает
вид:
![]() ,
,
где
![]() .
.
Для проведения рН-метрических измерений стеклянный электрод из натриевого стекла (содержит SiO2, Na2O и CaO) выдувают из трубки в виде шарика с очень тонкой стенкой (около 0,1 мм). Шарик и частично трубку заполняют внутренним раствором, который часто представляет собой 0,1 М раствор HCl. Во внутренний раствор погружают серебряную проволоку, покрытую AgCl, и трубку тщательно герметизируют, обеспечивая постоянство состава внутреннего раствора. Затем стеклянный электрод погружают в испытуемый раствор, который через солевой мостик контактирует с серебрянохлоридным электродом. Образуется цепь:
Ag, AgCl Cl−, H+ стекло H+x Cl− AgCl, Ag
внутренний испытуемый
(1) раствор раствор (2)
1 2 3 4
Скачки потенциала в цепи на границах внутреннего электрода сравнения и внутреннего раствора 1, внутреннего растворастекло 2, во внешнем электроде сравнения 4 остаются постоянными. Поэтому ЭДС, равная разности потенциалов между точками (2) и (1), должна определяться только активностью ионов водорода H+x испытуемого раствора.
Диапазон значений рН, измеряемых стеклянным электродом, очень велик (приблизительно от 0 до 13 единиц). На стеклянный электрод не действуют соли тяжелых металлов. Он очень удобен для измерений рН в непрозрачных и окрашенных средах.
Стеклянный электрод повсеместно используется в аналитической химии, в промышленности и в биологических исследованиях. Для медицинских целей выпускаются миниатюрные конструкции стеклянного электрода, который можно вводить в вену или артерию для прямых измерений водородного показателя крови.
Стеклянный электрод может быть использован для определения активности ионов щелочных металлов, Ag+, Tl+, NH4+ и некоторых органических катионов. Для этого в стекольную массу вводят оксиды алюминия, бора и др.
Катионная
функция (для ионов металлов ее называют
металлической функцией) стеклянного
электрода объясняется увеличением
константы Кобм.
В этом случае может быть достигнуто
соотношение
![]() и выражение для электродного потенциала
примет следующий вид:
и выражение для электродного потенциала
примет следующий вид:
![]() .
.
Избирательность ионоселективных электродов достигает больших величин. Например, содержащий Al2O3 стеклянный электрод позволяет определять активность ионов натрия при 1000-кратном избытке ионов калия.
Мембраны из полимеров и частиц труднорастворимых солей металлов используются для определения в растворах анионов, входящих в состав соли.
Монокристаллы LaF3 были использованы для изготовления лантанфторидных электродов, позволяющих определять содержание фторид-ионов в различных средах, включая слюну.
