
- •Москва 2010 Оглавление
- •1. Введение.
- •2. Структура твёрдых тел.
- •2.1. Механизм кристаллизации.
- •2.2. Термодинамика кристаллизации.
- •2.3. Правило фаз Гиббса, фазовые диаграммы.
- •2.4. Процессы структурообразования.
- •2.5. Надмолекулярная структура полимеров.
- •3. Основные свойства материалов.
- •3.1. Механические свойства материалов.
- •3.1.1. Особенности структуры и свойств полимерных материалов.
- •3.2. Теплофизические свойства материалов.
- •3.2.1. Теплоёмкость.
- •3.2.2. Теплопроводность.
- •3.2.3. Температуропроводность
- •3.2.4. Тепловое расширение.
- •3.2.5.Температуры фазовых переходов.
- •3.3. Электрические свойства.
- •3.3.1. Проводники, полупроводники и диэлектрики.
- •3.3.2. Основные электрические характеристики материалов.
- •Эта величина носит название температурный коэффициент диэлектрической проницаемости.
- •3.4. Магнитные свойства материалов.
- •4. Металлические материалы.
- •4.1. Сплавы железо – углерод
- •4.2. Легированные стали.
- •4.3. Термическая и химико-термическая обработка металлов.
- •4.3. Металлические проводниковые материалы.
- •4.3.1. Материалы высокой проводимости.
- •4.3.2. Материалы высокого удельного сопротивления.
- •Металлические материалы для приборов измерения температуры, основанных на тепловом расширении веществ.
- •4.4. Сверхпроводники и криопроводники.
- •4.5. Металлические магнитные материалы.
- •5. Диэлектрические материалы.
- •5.1. Стёкла, ситаллы.
- •5.2. Ситаллы.
- •5.3. Техническая керамика.
- •6.1. Традиционная электротехническая керамика.
- •6.2. Оксидная керамика
- •6.2.1. Керамика на основе ВеО (брокерит, броммелитовая керамика).
- •6.2.2. Керамика на основе МgО (периклазовая керамика).
- •6.2.3. Керамика из оксида алюминия – корундовая керамика.
- •6.2.4. Кварцевая керамика.
- •6.2.5. Керамика из диоксида циркония ZrO2
- •6.2.6. Керамика из оксида иттрия y2o3.
- •6.3. Керамика из бескислородных соединений.
- •6.3.1. Карбиды и карбидная керамика
- •6.3.1.1. Керамика на основе карбида кремния.
- •6.3.1.2. Карбид бора в4с.
- •6.3.1.3. Керамика на основе карбидов d – элементов.
- •6.3.2. Нитридная керамика.
- •6.3.2.2. Нитрид алюминия.
- •6.3.2.3. Керамика на основе нитрида кремния Si3n4
- •6.3.3. Боридная керамика.
- •6.3.4. Силицидная керамика.
- •6.4. Конденсаторная керамика - на основе диоксида титана, титанатов, цирконатов и других соединений с подобными свойствами.
- •6.5. Магнитная керамика
- •7. Полимерные материалы
- •7.1. Термопластичные полимеры.
- •7.1.1. Полиэтилен (пэ).
- •7.1.3. Полистирол (пс)
- •7.1.4. Полиметилметакрилат (пмма).
- •7.1.5. Поливинилхлорид (пвх).
- •7.1.6. Фторопласты.
- •7.1.9. Полиуретаны (пу).
- •7.1.10. Полиимиды (пи).
- •7.1.11. Эфиры целлюлозы (этролы, целлулоид).
- •7.2. Термореактивные полимеры – реактопласты.
- •7.2.1 Фенопласты.
- •7.2.2. Аминопласты (карбамидные пластики).
- •7.2.3. Эпоксидные смолы.
- •7.2.4. Ненасыщенные полиэфирные смолы (пн).
- •7.2.5. Эластомеры (каучуки и резины).
- •7.3. Герметики
- •7.3.1. Вулканизирующиеся, отверждаемые герметики (ог).
- •7.3.2. Высыхающие герметики (вг).
- •7.4. Тепло- и термостойкие полимеры.
- •7.4.1. Карбоциклические полимеры и связующие.
- •7.4.2. Гетероциклические полимеры и связующие.
- •7.5. Полимерные композиционные материалы (пкм).
- •7.6. Полимеры со специфическими свойствами
- •7.6.1. Полимеры со специфическими электрическими свойствами
- •7.6.1.1. Антистатические полимерные материалы.
- •7.6.1.2. Полимерные электреты.
- •7.6.1.3. Полимерные полупроводники и проводники.
- •7.6.2. Флуоресцирующие полимеры.
- •7.6.3. Оптические полимеры.
- •7.6.4. Светочувствительные полимерные материалы.
- •7.6.5. Ионнообменные полимеры.
- •7.6.6. Биодеструктируемые полимеры.
- •7.6.7. Полимерные материалы триботехнического назначения.
- •8. Углеродные материалы и композиции.
- •8.1. Углеродные волокна (ув).
- •8.2. Углепластики (уп).
- •8.3. Композиционные материалы на основе ув и углеродной матрицы
- •9. Полупроводниковые материалы.
- •9.1. Элементарные полупроводники.
- •9.2. Полупроводниковые соединения.
- •10. Технология конструкционных материалов.
- •10.1. Технология металлических материалов.
- •10.1.1. Характеристика литейного произвдства.
- •10.1.2. Обработка металлов давлением (омд).
- •10.1.2.1. Виды обработки металлов давлением.
- •10.1.3. Сварка и пайка металлов и сплавов.
- •10.2. Переработка полимерных материалов
- •10.3. Технология стеклянных материалов.
- •10.3.1. Вытягивание.
- •10.3.2. Прокат.
- •10.3.3. Растекание (флоат – способ).
- •10.3.4. Выдувание.
- •10.3.5. Прессование.
- •10.3.6. Центробежное формование.
- •10.4. Технология керамических материалов.
- •10.4.1. Прессование на механических прессах.
- •10.4.2. Гидростатическое прессование.
- •10.4.3. Литьё в пористые формы.
- •10.4.4 Формование способом выдавливания (пластический способ).
8. Углеродные материалы и композиции.
Материалы этого типа с одной стороны относятся к неорганическим, а с другой стороны, искусственно получают их из органического сырья. Таким образом, они являются как бы переходными от органических к неорганическим материалам.
В природе углерод встречается в виде алмаза, графита и саж. Искусственно получены ещё несколько форм углерода: карбин, фуллерены, нанотрубки. Углерод в алмазе, графите и карбине имеет различный типа гибридизации. В алмазе наблюдается sp3- гибридизация, в графите sp2-гибридизация и в карбине sp –гибридизация. Наряду с чистыми аллотропными формами углерод образует большое число промежуточных соединений, содержащих комбинации атомов с различными типами гибридизации.
Кристаллическая решётка алмаза относится к атомному типу. Элементарная ячейка представляет собой тетраэдр, в центре и четырёх вершинах которого расположены атомы углерода. Координационное число решётки алмаза равно 4, все атомы углерода в кристаллической решётке расположены друг от друга на одинаковом расстоянии 1,54 Å. Каждый из них связан друг с другом неполярной ковалентной связью. Любой кристалл алмаза, следовательно, можно рассматиривать как гигантскую молекулу. Решётка алмаза, не имеющая искажённых валентных углов, сильно сопротивляется любым видам деформации. По этой причине алмазу свойственны высокая твёрдость (наибольшая из всех известных веществ), высокая прочность, заметная хрупкость, тугоплавкость (он возгоняется при 3700 оС). Плотность алмаза 3510 кг/м3.

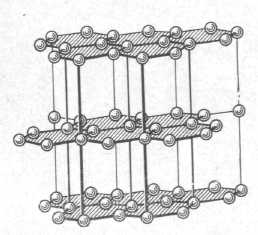
Рис. 8.1.Кристаллические решётки алмаза и графита.
В природе алмазы образовались от 1750 . 106 до 90. 106 лет тому назад на большой глубине (около 150 – 200 км) в мантии земли, где стабильные давление (Р ³ 45 ГПа) и температура (900 – 1400 оС), а затем магмой были вынесены в земную кору. Искусственное получение алмазов было осуществлено в 1897 году Муассеном путём насыщения расплава железа углеродом (графитом) и резким охлаждением слитка. Такая технология имитировала природные условия образования алмазов. С 1955 года алмазы получают в промышленных масштабах из графита при ~ 3000 оС и давлениях 10 ГПа. В настоящее время разработаны технологии синтеза не только изолированных кристаллов, но и поликристаллических блоков алмазов (алмазитов) при более мягких условиях (Р ³ 7,5 ГПа, Т = 1500 - 2000 оС, катализатор). Искусственные алмазы имеют небольшие размеры – 0,2 – 20 мкм и применяются как абразивный материал при изготовлении полировочных паст, отрезных дисков, режущего инструмента и т.д. Есть пути синтеза алмазов, не требующие экстремальных условий: это осаждение на поверхности затравочного кристалла из углеродсодержащего газа (например, метана), а также плазмохимический метод. В зависимости от природы поверхности затравочного кристалла можно получать поликристаллические слои или тонкие монокристаллические плёнки. В последнем случае электрической проводимостью можно управлять, просто добавляя в плазму атомы бора, которые служат в кристалле дырками.
Графит – более устойчивая форма, чем алмаз. При нагревании до высокой температуры в отсутствии воздуха алмаз превращается в графит. Природный графит имеет вид землистой или слоистой тёмно-серой массы с металлическим блеском, холодной и жирной на ощупь. Графит имеет гексагональную кристаллическую решётку, атомы углерода расположены в параллельных слоях (базисных плоскостях). В направлении, перпендикулярном базисным плоскостям, связь в 6 раз слабее, чем в слоях. Из-за этого отдельные слои легко скользят относительно друг друга и это свойство используется при создании антифрикционных материалов. Другой особенностью графита является высокая электропроводность (однако, ниже, чем у металлов и сплавов), значительная теплопроводность и стойкость к воздействию неблагоприятных климатических факторов. Эти свойства обусловили применение графита в электро - и радиотехнике.
Известен ряд способов получения искусственного графита путём термической перекристаллизации углей при температуре 2200 – 2500 оС. Благодаря испарению зольных примесей искусственные графиты более чистые, чем природные.
Путём термического разложения паров углеводородов в вакууме или в среде инертного газа при температуре ³ 900 оС получают пиролитический углерод. По своим свойствам и структуре пиролитический углерод приближается к графиту. Расстояние между слоями с/2 несколько больше, чем у графита и достигает 3,7 Å. Наоборот, расстояния между атомами в слоях меньше, чем у графита и составляет 1,39 Å. Плёнки пиролитического углерода имеют сравнительно высокое электрическое сопротивление и применяются для получения резисторов поверхностного типа.
Сажи – это продукт неполного сгорания или термического разложения углеродсодержащих веществ. В зависимости от исходного сырья и метода получения сажи подразделяются на газовые (канальную, печную, термическую, специальную), ацетиленовую, антраценовую, форсуночную, ламповую и др. Существенной особенностью саж является их малый объёмный вес. Так, например, 1 л канальной сажи ДГ-100 весит от 50 до 150 г. Это объясняется высокой дисперсностью частиц сажи, которую обычно оценивают по величине удельной поверхности саж. Удельной поверхностью называется общая поверхность частиц в единице веса (1г) или объёма. Для сажи ДГ-100 удельная поверхность (геометрическая) составляет 92 – 100 м2/г. Первичная частица сажи состоит из нескольких тысяч более мелких частиц, называемых кристаллитами. Структура кристаллита представляет собой деформированную, искажёную решётку графита.
Сажи применяют в качестве пигментов в лакокрасочной промышленности, для окрашивания в массе полимеров, перерабатываемых через расплав, в качестве основного усилителя резиновых смесей, в качестве проводящего компонента в композиционных резистивных материалах и для изготовления электроугольных изделий.
В 70-х годах ХХ столетия в СССР была синтезирована ещё одна аллотропная форма углерода – карбин, имеющий линейную структуру
- С º С – С º С - или = С = С = С = С = , в которых проявлялась высокая электропроводность за счёт перекрывания p-электронов в системе сопряжения кратных связей.

Рис.8.2. Структура частиц сажи: а – плоская углеродная решётка сажевого кристаллита; б – расположение углеродных решёток в кристаллите; в – первичная частица сажи; г – цепочечная структура сажи.
В 1985 году была открыта ещё одна форма углерода – фуллерены, а в 1991 году была открыта следующая форма - нанотрубки. Фуллерены и нанотрубки – это обширные классы интереснейших наноструктур, т.е. структур, имеющих размеры порядка 10-9м. Фуллерены – это сферические, похожие на футбольный мяч, молекулы, образованные атомами углерода. Фулеренов синтезировано уже очень много, от малых (С20, С28) до гигантских (С240, С1840), даже многослойных, типа шарик в шарике (луковица). Из четырёхслойных фуллеренов С60 – С240 – С540 – С960 даже получают алмазы. Уже можно составить своего рода периодическую систему феллереновых элементов, из которых формируются многие «фуллереновые вещества». Синтезированы фуллереновые полимеры, плёнки, кристаллы (фуллериты), допированые кристаллы (фуллериды) как с собственными структурами, так и повторяющие строение обычных кристаллов. Например, фуллерен С28 имеет ту же валентность, что и атом углерода и образует устойчивый кристалл со структурой алмаза – гипералмаз.
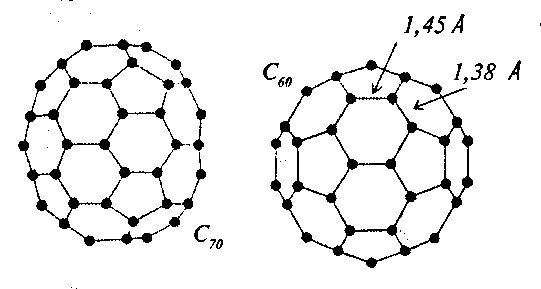
Рис 8.3. Структура фуллеренов С60 и С70. Стенки пятичленных циклов, образующих фуллереновые шарики, состоят из одинарных связей, а у шестичленных циклов встречаются и двойные связи.
Другой большой класс наноструктур – углеродные и неорганические однослойные и многослойные нанотрубки. Синтезировано множество разнообразных нанотрубок, существуют их ассоциаты – «жгуты», кристаллы и т.п. Из нанотрубок получают очень интересные материалы, например, уникальной прочности нанобумагу, представляющую собой плотные плёнки из переплетённых, подобно растительным волокнам, жгутов нанотрубок. Недавно китайские специалисты научились прясть нанотрубки и получать таким образом углеродные нити. Если же фуллерен запихнуть в нанотрубку, то получится ещё один класс углеродных структур – пипод.

(а)
(б)
Рис.8.4. Нанотрубки, свёрнутые под углом 0о (а) и под углом 30о (б)
В пиподах обнаружен эффет температурного р-п перехода. При комнатной температуре пипод – полупроводник, с понижением температуры он становится проводником. На сегодня пиподы – интересные и перспективные материалы для микро- и наноэлектроники, аккумуляторов водорода, высокотемпературных сверхпроводников.


а б
Рис 8.5 (а) Сценарий формирования пипоидов: диффузия фуллеренов через открытый конец (1) или через дефект стенки нанотрубки (2); (б) Модель смешанного пипоида Тi8С12&ВN-HT.
К сожалению, пока синтез нанотрубок и фулеренов – довольно сложное и дорогое дело, тем не менее производство фулеренов и нанотрубок с каждым годом увеличивается. А расходы на исследования по нанотехнологии растут опережающими темпами. Так, за 4 года, с 1998 по 2001, общие (без России) расходы на нанотехнологии возрасли с 434 млн. дол. США до 1267 млн. дол. США. Будем надеяться, что грандиозные ожидания, связанные с развитием этого нового направления науки, оправдаются.
И, наконец, в 2003 году эмигрировавшими в Европу нашими учёными Андреем Геймом и Константином Новосёловым был открыт новый углеродный материал графен, представляющий собой один слой кристаллической решётки графита толщиной в один атом. Графен обладает высокой прочностью и интересными электрическими свойствами. Предполагается, что он найдёт широкое применение в микроэлектронике. Авторы этого открытия получили Нобелевскую премию по физике за 2010 год.
