
- •Дмитрів а. М., Стецьків а. О., Сав’як о. Л. Фізична хімія Навчальний посібник
- •Івано-Франківськ – 2013
- •Передмова
- •Загальні правила роботи у лабораторії фізичної і колоїдної хімії
- •Правила техніки безпеки при виконанні робіт у лабораторії фізичної та колоїдної хімії
- •Основні правила надання першої допомоги при нещасних випадках
- •Розділ 1 Хімічна термодинаміка
- •Перший закон термодинаміки
- •1. Ізотермічний процес:
- •2. Ізохорний процес:
- •3. Ізобарний процес:
- •Термохімія
- •Залежність ентальпії реакції від температури. Рівняння кірхгофа
- •Приклади розв'язування задач
- •Заняття №1
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення теплового ефекту нейтралізації Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Заняття №2
- •Теоретична частина другий закон термодинаміки. Ентропія
- •Статистичний характер другого закону термодинаміки
- •Обчислення ентропії. Зміна ентропії у різних процесах
- •Третій закон термодинаміки. Абсолютне значення ентропії
- •Характеристичні функції
- •Термодинаміка хімічної рівноваги хімічний потенціал
- •Закон дії мас та константи рівноваги
- •Рівняння ізотерми хімічної реакції
- •Залежність константи рівноваги від температури. Рівняння ізохори та ізобари хімічної реакції
- •Приклади розв'язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Дослідження рівноваги оборотної хімічної реакції Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Вміст колб № 1-6
- •Питання для самоконтролю
- •Розділ 2 фазові рівноваги
- •Приклади розв'язування задач
- •Заняття №3 Тема: Термічний аналіз. Фазові перетворення в одно- і дво компонентних системах. Розподіл речовини між двома рідинами. Екстракція. Побудова діаграми стану бінарної системи.
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Побудова діаграми стану бінарної системи нафталін-фенол
- •Експериментальна частина
- •Методичні вказівки
- •Склад зразків
- •Питання для самоконтролю
- •Розділ 3 розчини
- •ОсМотичний тик розчинів. Зниження температури замерзання і підвищення температури кипіння розбавлених розчинів неелектролітів
- •Приклади розв'язування задач
- •Заняття №4 Тема: Колігативні властивості розчинів. Визначення молярної маси розчиненої речовини методом кріоскопії.
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення молярної маси розчиненої речовини методом Раста Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Заняття №5 Тема: Електрична провідність розчинів електролітів. Кондуктометричне титрування. Визначення ізотонічного коефіцієнту розчину електроліту.
- •Теоретична частина
- •Приклади розв'язування задач
- •Електропровідність розчинів електролітів
- •Приклади розв'язування задач
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Перелік питань, які виносяться на змістовий модуль 1
- •Лабораторна робота Визначення ізотонічного коефіцієнту розчину електроліту Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Розділ 4 електрохімія
- •Заняття №6 Тема: Електродні потенціали та електрорушійна сила гальванічних елементів. Окисно-відновні електроди. Потенціометричне визначення рН розчину.
- •Теоретичні відомості
- •Гальванічні елементи, їх класифікація
- •Приклади розв’язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Потенціометричне визначення рН водних розчинів Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Результати вимірювань ерс хлорсрібно-скляного кола
- •Питання для самоконтролю
- •Поясніть, чому потенціал хлорсрібного електрода при даній концентрації кСl є сталим?
- •Заняття №7
- •Теоретичні відомості
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Розділ 5 хімічна кінетика і каталіз
- •Методи визначення порядку реакції
- •Приклади розв’язування задач
- •Заняття № 8
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення константи швидкості реакції йодування ацетону
- •Експериментальна частина
- •Методика виконання роботи
- •Вивчення швидкості реакції йодування ацетону
- •Використовуючи рівняння (8.2) та значення Сац,0, сн,0, Сx і τ розраховують константу швидкості k.
- •Питання для самоконтролю
- •Заняття № 9
- •Теоретична частина вплив температури на швидкість реакції
- •Рівняння Арреніуса
- •Каталіз
- •Характерні особливості каталізаторів
- •Гомогенний каталіз
- •Кислотно-основний каталіз
- •Ферментний каталіз
- •Гетерогенний каталіз
- •Приклади розв’язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Перелік питань, які виносяться на змістовий модуль 2
- •Самостійна робота на занятті
- •Експериментальна частина
- •Методичні вказівки
- •Питання, які виносяться на модуль 1 «фізична хімія»
- •Банк тестів з фізичної хімії
- •1. Хімічна термодинаміка
- •2. Фазові рівноваги
- •3. Загальна характеристика розчиНів
- •4. Електрохімія
- •5. Хімічна кінетика
- •Засоби контролю знань студентів
- •Значення найважливіших фундаментальних сталих
- •Кріоскопічні та ебуліоскопічні константи деяких розчинників
- •Константи дисоціації деяких слабких електролітів при 25 °с
- •Стандартні ентальпії утворення ∆н0298, ентропії ∆s0298 та енергії Гіббса ∆g0298 деяких речовин при 298 к
- •Стандартні електродні потенціали деяких металів у водних розчинах
- •Перелік літератури Основна література
- •Додаткова література
Питання для самоконтролю
Чому в методі Раста для вимірювань температури замерзання (плавлення) можна використовувати звичайний термометр?
Як впливає швидкість нагрівання в методі Раста на спостережуване значення температури плавлення твердої речовини.
Чи залежить точність кріоскопічних вимірювань від природи розчиненої речовини?
Чому в методі Раста як розчинник доцільно використовувати камфору?
Заняття №5 Тема: Електрична провідність розчинів електролітів. Кондуктометричне титрування. Визначення ізотонічного коефіцієнту розчину електроліту.
Актуальність: Водні розчини електролітів широко використовують у фармації для приготування лікарських препаратів. Знання закономірностей поведінки електролітів у водних розчинах необхідне для правильного їх використання як основи фармацевтичних препаратів. Методи фізико-хімічного дослідження, що ґрунтуються на вимірюванні електричної провідності розчинів (кондуктометрія) широко використовують в фармації, медико-біологічних дослідженнях.
Навчальні цілі:
Знати:
основи теорії Арреніуса, закон розбавлення Оствальда;
основи протолітичної теорії Бренстеда-Лоурі;
сучасні теорії дисоціації слабких електролітів Льюїса, Ізмайлова;
визначення понять: “термодинамічна константа дисоціації”, “активність та коефіцієнт активності”, “йонна сила розчину”;
основні положення електростатичної теорії сильних електролітів Дебая-Гюккеля;
закон Кольрауша, поняття про йонну провідність розчинів;
визначення понять: рухливість йонів та число переносу йонів;
основи методу кондуктометрії та його використання.
Вміти:
записати та проаналізувати математичний вираз закону розбавлення Оствальда;
дати визначення поняттям кислота та основа, виходячи з позицій теорій Бренстеда-Лоурі та Льюїса;
обчислити рН розчинів слабких і сильних кислот та основ;
провести кріоскопічні вимірювання та обчислити ізотонічний коефіцієнт даного електроліту в розчині;
визначати кондуктометричну сталу комірки приладу, використовуючи стандартні розчини KCl;
визначати питому провідність досліджуваних розчинів, користуючись кондуктометром;
побудувати криву кондуктометричного титрування і визначити точки еквівалентності.
Теоретична частина
Електроліти – це речовини, які в розчиненому (чи розплавленому стані) проводять електричний струм. Розчини електролітів володіють електропровідністю, яка обумовлена тим, що молекули електролітів у воді і деяких інших розчинниках дисоціюють на йони – частинки, які несуть електричні заряди.
Електроліти можна поділити на 2 типи: сильні і слабкі.
При дисоціації слабких електролітів встановлюється йонна рівновага, що характеризується константою рівноваги. Для бінарного електроліту цю рівновагу схематично можна виразити рівнянням:
АВ = А+ + В–.
За законом дії мас константу рівноваги К визначають за співвідношенням:
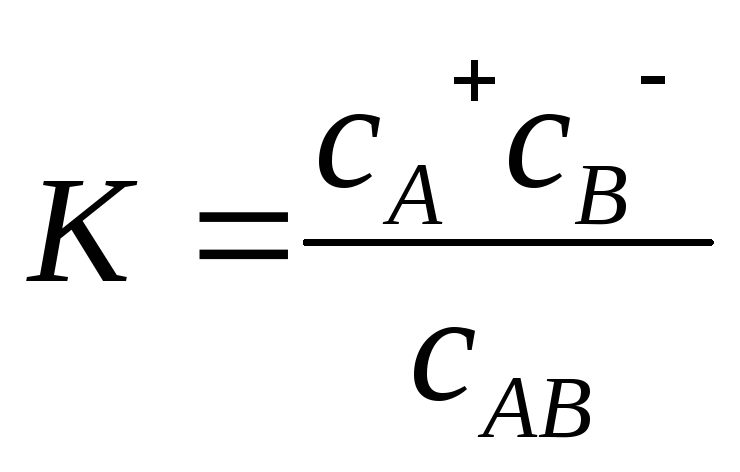 ,
,
де
сА+
і
сВ–
– відповідно концентрації йонів А+
і
В–;
сАВ
–
концентрація недисоційованих молекул
АВ.

 Якщо
один моль електроліту міститься у V
літрах
розчину,
а ступінь дисоціації його дорівнює α,
то концентрації
йонів А+
і
В–
відповідно
дорівнюватимуть
Якщо
один моль електроліту міститься у V
літрах
розчину,
а ступінь дисоціації його дорівнює α,
то концентрації
йонів А+
і
В–
відповідно
дорівнюватимуть
сА+ = сВ– = α/V.
Частина молекул, що не розпадаються на йони, становить 1 – α, тоді:
![]() .
.
Підставляючи
визначені значення сА+,
сВ-,
сАВ
в
рівняння
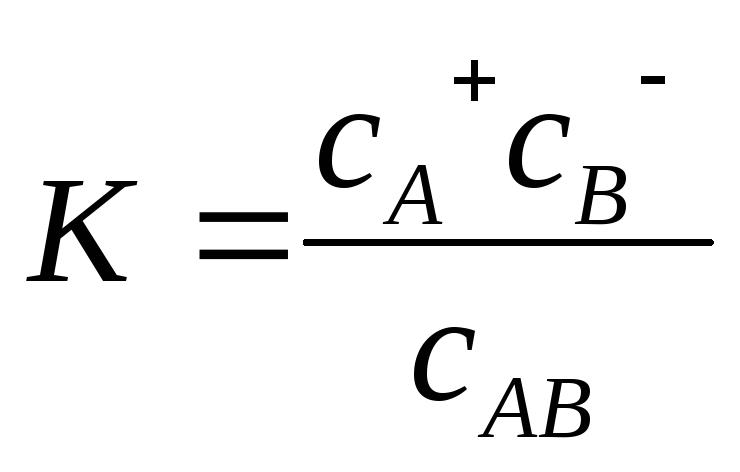 одержимо:
одержимо:
![]() .
.
Замінюючи V на 1/с, знайдемо:
![]() .
.
Це рівняння дістало назву закону розбавлення Оствальда. Воно зв'язує між собою константу дисоціації розчиненого електроліту, ступінь його дисоціації та концентрацію.
Константа дисоціації при сталій температурі в одному й тому самому розчиннику має стале значення лише для слабких електролітів у сильно розбавлених розчинах. Ступінь електролітичної дисоціації речовини, розчиненої в даному розчиннику, залежить (при сталій температурі) від природи і концентрації речовини. Ці кількісні характеристики розчинів слабких електролітів можна визначати різними способами, зокрема методом електропровідності.
Для
слабких кислот і основ значення α дуже
мале і
ним у знаменнику рівняння
![]() можна знехтувати.
Тоді рівняння матиме вигляд:
можна знехтувати.
Тоді рівняння матиме вигляд:
![]() звідки
звідки
![]() .
.
Силу основ і кислот зручніше характеризувати константою дисоціації, оскільки ступінь дисоціації електроліту змінюється залежно від концентрації розчину.
Електроліти, ступінь дисоціації яких перевищує 30 %, умовно відносять до сильних електролітів. Для кількісного описування таких розчинів застосувати рівняння класичної теорії електролітичної дисоціації, не припустивши великих похибок, неможливо. Тому для розчинів сильних електролітів загальну концентрацію замінюють ефективною (тобто такою, що проявляє себе в дії), яка інакше називається активністю електроліту, або активністю його йонів і позначається буквою а.
Активність бінарного електроліту записують рівнянням:
а = а+а–.
Отже, активність а виражає ефективну концентрацію дисоційованої частини електроліту в розчині, що відображає сумарну дію двох факторів – неповної дисоціації молекул (якщо вона має місце) і взаємне притягання різнойменних йонів.
Ефективна концентрація в f разів більша від загальної концентрації, тобто:
a = f c.
Активність катіонів і аніонів у розчині можна записати:
а+ = f+ с+; а– = f– с–.
де f+ і f– – відповідно коефіцієнти активності катіонів і аніонів; с+ і с– відповідно концентрації катіонів і аніонів.
Практично можна визначити лише середній коефіцієнт активності всього електроліту, тому і активності катіонів і аніонів електроліту також будуть середніми активностями:
а+ = f±c+; а– = f ±с- ; а± = f±c.
Середній коефіцієнт активності для сильно розбавлених розчинів залежить від загальної концентрації йонів усіх розчинених електролітів і від їхніх валентностей. Тому для характеристики залежності активності електроліту від концентрації всіх йонів, що знаходяться в розчині, Льюїс і Рендель ввели поняття про йонну силу І.
І = 1/2(с1z12 + с2z22 + с3z32 + ... сіzі2),
де сі – концентрації відповідних йонів; zі – їх валентності.
Коефіцієнт активності даного електроліту в розбавлених розчинах сильних електролітів має стале значення, якщо ці розчини мають однакові йонні сили.
Згідно з теорією сильних електролітів, залежність між середнім коефіцієнтом активності електроліту і йонною силою для розбавлених водних розчинів, йонна сила не перевищує 0,01 (при 298 К), виражається формулою:
![]() ,
,
де z1 і z2 – заряди йонів; І – йонна сила розчину. Це рівняння називають рівнянням Дебая – Гюккеля.
Розчини електролітів замерзають при нижчій і киплять при вищій температурі, ніж розчини неелектролітів, однакові за молярною концентрацією, що є відхиленням від законів Рауля. Розчини електролітів мають вищий осмотичний тиск, ніж це випливає з закону Вант-Гоффа для неелектролітів. Тому в рівняння, що описують властивості розчинів неелектролітів, Вант-Гофф ввів поправочний множник і, який назвав ізотонічним коефіцієнтом. Це дало можливість застосовувати такі рівняння до розчинів електролітів:
π = iCмRT;
ΔТзам = іkкрСm;
ΔТкип = іkебСm;
![]() .
.
Отже, ізотонічний коефіцієнт показує, у скільки разів зниження тиску пари і температури замерзання та підвищення температури кипіння і осмотичного тиску, визначені експериментально для розчинів електролітів, більші, ніж обчислені за мольними концентраціями останніх.
Буферними системами називають розчини, які здатні зберігати стале значення рН середовища при розбавленні або при додаванні до них невеликих кількостей сильної кислоти чи лугу, а також при їх концентруванні. Найпоширенішими є водні кислотно-основні буферні розчини, які містять слабку кислоту і поєднану з нею основу. До біологічних буферних систем організму належать чотири типи буферних розчинів: гідрогенкарбонатний, фосфатний, гемоглобіновий та білковий. Вони характеризуються різною буферною ємністю та неоднаковим вмістом у фізіологічних рідинах.
рН для даного складу буферного розчину є величина постійна, однак змінюючи співвідношення концентрації кислоти і солі, можна одержувати в кожному випадку інше значення рН буферної системи, яке може коливатися в деяких певних межах.
Для
розрахунку рН кислотного буферного
розчину використовують формулу:
![]() звідки зарівнянням
Гендерсона – Гассельбаха:
звідки зарівнянням
Гендерсона – Гассельбаха:
![]() або
або
![]() ,
,
а для основних буферних розчинів:
![]() .
.
Здатність буферних розчинів протидіяти зміні рН називають буферною дією. Буферна ємність (В) – це розрахункова величина, яка визначається числом грам-еквівалентів сильної кислоти або сильної основи, яку треба додати до 1 дм3 буферного розчину, щоб змінити значення рН на одиницю.
![]() .
.
