
- •Дмитрів а. М., Стецьків а. О., Сав’як о. Л. Фізична хімія Навчальний посібник
- •Івано-Франківськ – 2013
- •Передмова
- •Загальні правила роботи у лабораторії фізичної і колоїдної хімії
- •Правила техніки безпеки при виконанні робіт у лабораторії фізичної та колоїдної хімії
- •Основні правила надання першої допомоги при нещасних випадках
- •Розділ 1 Хімічна термодинаміка
- •Перший закон термодинаміки
- •1. Ізотермічний процес:
- •2. Ізохорний процес:
- •3. Ізобарний процес:
- •Термохімія
- •Залежність ентальпії реакції від температури. Рівняння кірхгофа
- •Приклади розв'язування задач
- •Заняття №1
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення теплового ефекту нейтралізації Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Заняття №2
- •Теоретична частина другий закон термодинаміки. Ентропія
- •Статистичний характер другого закону термодинаміки
- •Обчислення ентропії. Зміна ентропії у різних процесах
- •Третій закон термодинаміки. Абсолютне значення ентропії
- •Характеристичні функції
- •Термодинаміка хімічної рівноваги хімічний потенціал
- •Закон дії мас та константи рівноваги
- •Рівняння ізотерми хімічної реакції
- •Залежність константи рівноваги від температури. Рівняння ізохори та ізобари хімічної реакції
- •Приклади розв'язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Дослідження рівноваги оборотної хімічної реакції Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Вміст колб № 1-6
- •Питання для самоконтролю
- •Розділ 2 фазові рівноваги
- •Приклади розв'язування задач
- •Заняття №3 Тема: Термічний аналіз. Фазові перетворення в одно- і дво компонентних системах. Розподіл речовини між двома рідинами. Екстракція. Побудова діаграми стану бінарної системи.
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Побудова діаграми стану бінарної системи нафталін-фенол
- •Експериментальна частина
- •Методичні вказівки
- •Склад зразків
- •Питання для самоконтролю
- •Розділ 3 розчини
- •ОсМотичний тик розчинів. Зниження температури замерзання і підвищення температури кипіння розбавлених розчинів неелектролітів
- •Приклади розв'язування задач
- •Заняття №4 Тема: Колігативні властивості розчинів. Визначення молярної маси розчиненої речовини методом кріоскопії.
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення молярної маси розчиненої речовини методом Раста Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Заняття №5 Тема: Електрична провідність розчинів електролітів. Кондуктометричне титрування. Визначення ізотонічного коефіцієнту розчину електроліту.
- •Теоретична частина
- •Приклади розв'язування задач
- •Електропровідність розчинів електролітів
- •Приклади розв'язування задач
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Перелік питань, які виносяться на змістовий модуль 1
- •Лабораторна робота Визначення ізотонічного коефіцієнту розчину електроліту Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Розділ 4 електрохімія
- •Заняття №6 Тема: Електродні потенціали та електрорушійна сила гальванічних елементів. Окисно-відновні електроди. Потенціометричне визначення рН розчину.
- •Теоретичні відомості
- •Гальванічні елементи, їх класифікація
- •Приклади розв’язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Потенціометричне визначення рН водних розчинів Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Результати вимірювань ерс хлорсрібно-скляного кола
- •Питання для самоконтролю
- •Поясніть, чому потенціал хлорсрібного електрода при даній концентрації кСl є сталим?
- •Заняття №7
- •Теоретичні відомості
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Розділ 5 хімічна кінетика і каталіз
- •Методи визначення порядку реакції
- •Приклади розв’язування задач
- •Заняття № 8
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення константи швидкості реакції йодування ацетону
- •Експериментальна частина
- •Методика виконання роботи
- •Вивчення швидкості реакції йодування ацетону
- •Використовуючи рівняння (8.2) та значення Сац,0, сн,0, Сx і τ розраховують константу швидкості k.
- •Питання для самоконтролю
- •Заняття № 9
- •Теоретична частина вплив температури на швидкість реакції
- •Рівняння Арреніуса
- •Каталіз
- •Характерні особливості каталізаторів
- •Гомогенний каталіз
- •Кислотно-основний каталіз
- •Ферментний каталіз
- •Гетерогенний каталіз
- •Приклади розв’язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Перелік питань, які виносяться на змістовий модуль 2
- •Самостійна робота на занятті
- •Експериментальна частина
- •Методичні вказівки
- •Питання, які виносяться на модуль 1 «фізична хімія»
- •Банк тестів з фізичної хімії
- •1. Хімічна термодинаміка
- •2. Фазові рівноваги
- •3. Загальна характеристика розчиНів
- •4. Електрохімія
- •5. Хімічна кінетика
- •Засоби контролю знань студентів
- •Значення найважливіших фундаментальних сталих
- •Кріоскопічні та ебуліоскопічні константи деяких розчинників
- •Константи дисоціації деяких слабких електролітів при 25 °с
- •Стандартні ентальпії утворення ∆н0298, ентропії ∆s0298 та енергії Гіббса ∆g0298 деяких речовин при 298 к
- •Стандартні електродні потенціали деяких металів у водних розчинах
- •Перелік літератури Основна література
- •Додаткова література
Характеристичні функції
За зміною ентропії можна визначити напрямок і межу перебігу самодовільного процесу лише в ізольованих системах. Однак на практиці доводиться мати справу й з іншими системами. Для характеристики перебігу процесів у цих системах були введені інші термодинамічні функції. Функцією стану називають характеристичною, якщо на її основі та на основі її похідних можна явно виразити термодинамічні властивості системи і дають змогу визначити напрям і межу того чи іншого спонтанного процесу. Характеристичними функціями є:
Ентальпія: H = U + PV;
Вільна енергія (енергія Гелмгольца або ізохорно-ізотермічний потенціал): F = U – TS;
Термодинамічний потенціал (енергія Гіббса або ізобарно-ізотермічний потенціал):
G = U – TS + PV = H – TS.
Після диференціювання цих виразів одержимо:
dH = dU + PdV + VdP, враховуючи, що dU = ТdS – PdV, тоді
dH = ТdS + VdP; Н = f(S, P), U = f(S, V);
dF = – PdV – SdT; F = f(V, T);
dG = – SdT + VdP = VdP – SdT; G = f(P, T).
Як видно з вибраних форм характеристичних функцій, термодинамічний потенціал Гіббса є найбільш вигідний, оскільки визначається зміною температури і тиску. Якраз ці величини є найбільш простими і зручними для вимірювання. Функції ∆U i ∆H також є термодинамічними потенціалами, бо їх зменшення при відповідних сталих дорівнює максимальній корисній роботі.
Ізохорний і ізобарний потенціали є функціями стану, і їх використовують для вирішення питання напрямку процесу в умовах термодинамічної рівноваги. Якщо ∆F і ∆G дорівнюють нулю, то система перебуває в рівновазі, якщо ∆F < 0 і ∆G < 0, то процес відбувається самодовільно з перетворенням енергії у корисну роботу. У випадку, коли ∆F > 0 і ∆G > 0, процес несамочинний, зміна стану системи відбувається тільки при використанні зовнішньої роботи. Так само як енергія Гельмгольца так і енергія Гіббса характеризують працездатність системи і визначають ту частину енергії, яка в ізохорно-ізотермічному та ізобарно-ізотермічному процесах перетворюється у роботу.
Для розрахунку зміни функцій Гіббса і Гельмгольца в результаті хімічних реакцій найчастіше застосовують рівняння Гіббса-Гельмгольца в вигляді:
ΔG = ΔН – TΔS;
ΔF = ΔU – TΔS.
Для обчислень за останніми рівняннями використовують табличні значення стандартних ентальпій утворення та згоряння речовин, а також їх абсолютних ентропій.
Термодинаміка хімічної рівноваги хімічний потенціал
Часткові похідні від інших термодинамічних потенціалів (при відповідних сталих) дорівнюють хімічному потенціалу компонента:
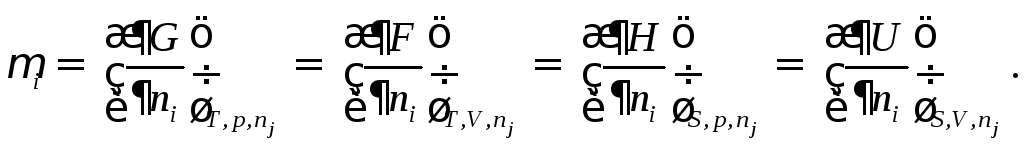
Таким чином, хімічний потенціал даної речовини рівний частинній похідній від будь-якого термодинамічного потенціалу даної фази до числа молів даної речовини при умові, що інші термодинамічні параметри і число молів решти речовин залишаються сталими.
Хімічний потенціал компонента залежить від температури, природи компонента та його вмісту в системі.
Для 1 моль ідеального газу за Т = const маємо:
![]()
Інтегруючи це рівняння, отримуємо:
G = RT ln p + const.
За стандартних умов const = G°, де G° – стандартна енергія Гіббса. Отже:
G = G0 + RT ln p.
Для компонента суміші ідеальних газів:
µі=µ0і+ RT lnрi ,
де µ0і – стандартний хімічний потенціал, а рi – парціальний тиск компонента і.
Для ідеальних розчинів:
µі=µ0і+ RT lnсi,
де сi – концентрація компонента в розчині.
Для реальних розчинів концентрацію замінюють активністю:
µі=µ0і+ RT lnаi.
Поняття про активність було введено Льюїсом. Активність – це величина, підстановка якої замість концентрації у термодинамічні рівняння робить їх справедливими для реальних систем.
Активність дорівнює добутку концентрації на коефіцієнт активності:
ai = ci ∙ yi або ai = ci ∙ γi,
де уi і γi – відповідно молярний і моляльний коефіцієнти активності.
Хімічний потенціал є функцією, що визначає напрямок і межі довільного переходу даного компонента з однієї фази в іншу при відповідних перетвореннях (шляхом випаровування, розчинення, кристалізації і взаємодії).
Загальною умовою можливого перебігу довільного процесу є нерівність
![]() ,
,
а стану рівноваги відповідає рівність
![]() ,
,
де µ – хімічний потенціал; dn – зміна кількості молів речовини.
