
- •Дмитрів а. М., Стецьків а. О., Сав’як о. Л. Фізична хімія Навчальний посібник
- •Івано-Франківськ – 2013
- •Передмова
- •Загальні правила роботи у лабораторії фізичної і колоїдної хімії
- •Правила техніки безпеки при виконанні робіт у лабораторії фізичної та колоїдної хімії
- •Основні правила надання першої допомоги при нещасних випадках
- •Розділ 1 Хімічна термодинаміка
- •Перший закон термодинаміки
- •1. Ізотермічний процес:
- •2. Ізохорний процес:
- •3. Ізобарний процес:
- •Термохімія
- •Залежність ентальпії реакції від температури. Рівняння кірхгофа
- •Приклади розв'язування задач
- •Заняття №1
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення теплового ефекту нейтралізації Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Заняття №2
- •Теоретична частина другий закон термодинаміки. Ентропія
- •Статистичний характер другого закону термодинаміки
- •Обчислення ентропії. Зміна ентропії у різних процесах
- •Третій закон термодинаміки. Абсолютне значення ентропії
- •Характеристичні функції
- •Термодинаміка хімічної рівноваги хімічний потенціал
- •Закон дії мас та константи рівноваги
- •Рівняння ізотерми хімічної реакції
- •Залежність константи рівноваги від температури. Рівняння ізохори та ізобари хімічної реакції
- •Приклади розв'язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Дослідження рівноваги оборотної хімічної реакції Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Вміст колб № 1-6
- •Питання для самоконтролю
- •Розділ 2 фазові рівноваги
- •Приклади розв'язування задач
- •Заняття №3 Тема: Термічний аналіз. Фазові перетворення в одно- і дво компонентних системах. Розподіл речовини між двома рідинами. Екстракція. Побудова діаграми стану бінарної системи.
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Побудова діаграми стану бінарної системи нафталін-фенол
- •Експериментальна частина
- •Методичні вказівки
- •Склад зразків
- •Питання для самоконтролю
- •Розділ 3 розчини
- •ОсМотичний тик розчинів. Зниження температури замерзання і підвищення температури кипіння розбавлених розчинів неелектролітів
- •Приклади розв'язування задач
- •Заняття №4 Тема: Колігативні властивості розчинів. Визначення молярної маси розчиненої речовини методом кріоскопії.
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення молярної маси розчиненої речовини методом Раста Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Заняття №5 Тема: Електрична провідність розчинів електролітів. Кондуктометричне титрування. Визначення ізотонічного коефіцієнту розчину електроліту.
- •Теоретична частина
- •Приклади розв'язування задач
- •Електропровідність розчинів електролітів
- •Приклади розв'язування задач
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Перелік питань, які виносяться на змістовий модуль 1
- •Лабораторна робота Визначення ізотонічного коефіцієнту розчину електроліту Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Розділ 4 електрохімія
- •Заняття №6 Тема: Електродні потенціали та електрорушійна сила гальванічних елементів. Окисно-відновні електроди. Потенціометричне визначення рН розчину.
- •Теоретичні відомості
- •Гальванічні елементи, їх класифікація
- •Приклади розв’язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Потенціометричне визначення рН водних розчинів Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Результати вимірювань ерс хлорсрібно-скляного кола
- •Питання для самоконтролю
- •Поясніть, чому потенціал хлорсрібного електрода при даній концентрації кСl є сталим?
- •Заняття №7
- •Теоретичні відомості
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Розділ 5 хімічна кінетика і каталіз
- •Методи визначення порядку реакції
- •Приклади розв’язування задач
- •Заняття № 8
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення константи швидкості реакції йодування ацетону
- •Експериментальна частина
- •Методика виконання роботи
- •Вивчення швидкості реакції йодування ацетону
- •Використовуючи рівняння (8.2) та значення Сац,0, сн,0, Сx і τ розраховують константу швидкості k.
- •Питання для самоконтролю
- •Заняття № 9
- •Теоретична частина вплив температури на швидкість реакції
- •Рівняння Арреніуса
- •Каталіз
- •Характерні особливості каталізаторів
- •Гомогенний каталіз
- •Кислотно-основний каталіз
- •Ферментний каталіз
- •Гетерогенний каталіз
- •Приклади розв’язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Перелік питань, які виносяться на змістовий модуль 2
- •Самостійна робота на занятті
- •Експериментальна частина
- •Методичні вказівки
- •Питання, які виносяться на модуль 1 «фізична хімія»
- •Банк тестів з фізичної хімії
- •1. Хімічна термодинаміка
- •2. Фазові рівноваги
- •3. Загальна характеристика розчиНів
- •4. Електрохімія
- •5. Хімічна кінетика
- •Засоби контролю знань студентів
- •Значення найважливіших фундаментальних сталих
- •Кріоскопічні та ебуліоскопічні константи деяких розчинників
- •Константи дисоціації деяких слабких електролітів при 25 °с
- •Стандартні ентальпії утворення ∆н0298, ентропії ∆s0298 та енергії Гіббса ∆g0298 деяких речовин при 298 к
- •Стандартні електродні потенціали деяких металів у водних розчинах
- •Перелік літератури Основна література
- •Додаткова література
Методичні вказівки
У даній роботі вивчають хімічну рівновагу на прикладі реакції:
2FeCl3
+ 2KI
![]() 2FeCl2
+ I2
+ 2KCl
2FeCl2
+ I2
+ 2KCl
або
в йонному вигляді: 2Fe3+
+ 2I–
![]() 2Fe2+
+ I2.
2Fe2+
+ I2.
Константу йонної рівноваги в даному випадку можна представити наступним виразом:
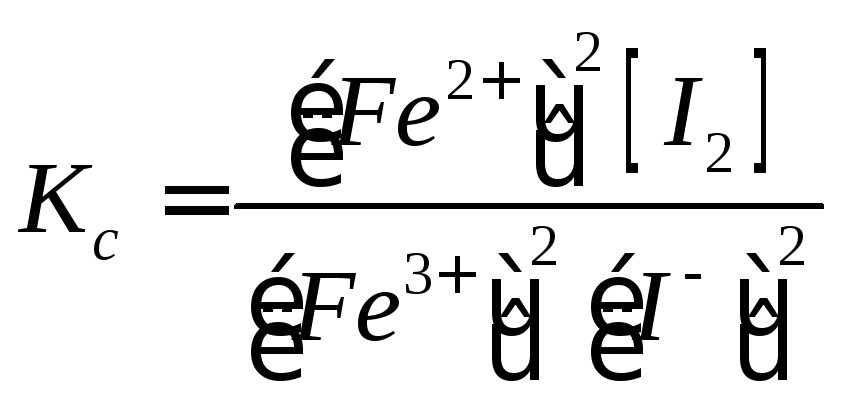 . (2.1)
. (2.1)
Послідовність виконання роботи. Беруть шість сухих колб з притертими корками ємністю 200 см3. Пронумерувавши колби, наливають кількості розчинів точної концентрації показані в табл. 2.1.
Таблиця 2.1
Вміст колб № 1-6
|
|
1 |
2 |
3 |
4 |
5 |
6 |
|
0,03 М FeCl3, см3 |
50 |
– |
50 |
– |
50 |
– |
|
0,03 М KI, см3 |
– |
50 |
– |
50 |
– |
50 |
Дослід проводять при різних температурах: кімнатній (17–20 0С), 40 та 60 0С (водяний термостат). Попередньо 30 хв колби витримують при заданих температурах: 1–2 при кімнатній, 3 – 4 при 40 0С, 5 – 6 при 60 0С. Паралельно готують конічні колби ємністю 100 см3 для аналізу відібраних проб (для титрування). Для цього в кожну колбу наливають 35–50 см3 дистильованої води і ставлять для охолодження у ванну з льодом.
Після термостатування колб 1-6 впродовж 30 хв зливають вміст колб 1 і 2, 3 і 4, 5 і 6. Колби із реакційною сумішшю щільно закривають корками та витримують за тих же температур.
Неменше ніж через 2 год після зливання з кожної колби, не виймаючи її із термостату, відбирають піпеткою 20 см3 розчину і зливають в охолоджену колбу для титрування. Йод, що виділився, відтитровують 0,02 Н розчином натрій тіосульфату до блідо-рожевого забарвлення. Потім додають декілька краплин розчину крохмалю та титрують до зникнення забарвлення. Світло-синє забарвлення, яке з’являється через деякий час після титрування не враховують. Однаковий об’єм розчину титранту, витрачений на титрування йоду в двох послідовних пробах із однієї колби, вказує на досягнення рівноваги.
Рівноважну концентрацію йоду розраховують за формулою:
![]() ,
(2.2)
,
(2.2)
де N1 – нормальність розчину натрій тіосульфату; V1 – об’єм розчину натрій тіосульфату, затрачений на титрування; V2 – об’єм відібраної проби (20 мл).
Згідно з рівнянням реакції, рівноважна концентрація йонів Феруму (ІІ) ([Fe2+]) рівна подвоєній рівноважній концентрації йоду:
![]() (2.3)
(2.3)
Концентрація [Fe3+] рівна:
![]()
або
![]() ,
(2.4)
,
(2.4)
де С0`(FeCl3) – концентрація FeCl3 до початку реакції (після зливання розчинів FeCl3 та KI).
Величину С0`(FeCl3) обчислюють із концентрації вихідного розчину (С0(FeCl3) = 0,03 М), враховуючи розбавлення при змішуванні розчинів FeCl3 та KI:
![]() ,
(2.5)
,
(2.5)
де а і b – об’єми розчинів FeCl3 та KI, відповідно взятих для проведення реакції (а = b = 50 мл).
Концентрацію [I –] обчислюють за рівнянням:
![]() .
(2.6)
.
(2.6)
Як і в попередньому випадку:
![]() ,
(2.7)
,
(2.7)
де С0`(KI) – концентрація KI до початку реакції (після зливання розчинів FeCl3 та KI); С0(KI) – вихідна концентрація KI (0,03 М).
Розрахунок константи рівноваги (Кс) при заданій температурі проводять за формулою (2.1).
Результати досліджень та розрахунків записують у таблицю 2.2.
Таблиця 2.2
Результати
дослідження хімічної рівноваги 2Fe3+
+ 2I–
![]() 2Fe2+
+ I2
при різних температурах
2Fe2+
+ I2
при різних температурах
|
T, K |
[Fe3+], моль/дм3 |
[Fe2+], моль/дм3 |
[I–], моль/дм3 |
[I2], моль/ дм3 |
Kc, дм3/моль |
1/T, K-1 |
ln Kc |
|
293 |
|
|
|
|
|
|
|
|
313 |
|
|
|
|
|
|
|
|
333 |
|
|
|
|
|
|
|
|
|
Н = кДж/моль | ||||||
Будують
графік залежності константи рівноваги
від температури в координатах ln Kc
– 1/T.
З графіка визначають величину зміни
ентальпії реакції:
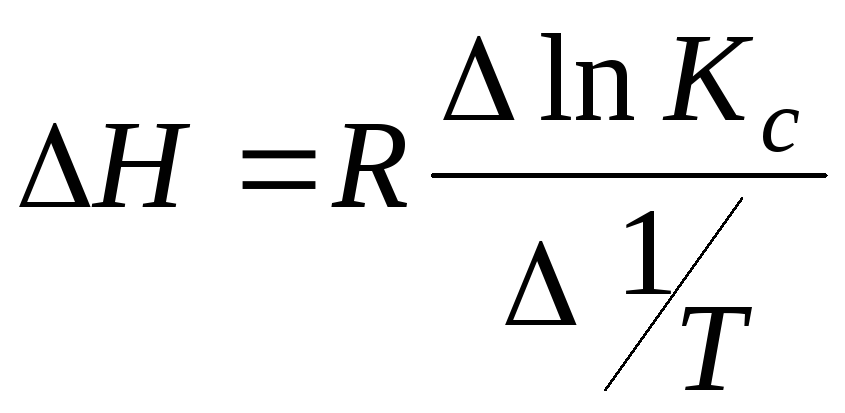 .
.
Оформлення протоколу.Експериментальні результати та результати розрахунків подають у вигляді таблиці. Приводять графічну залежність lnKc– 1/Tі розрахунок величиниН. Виходячи із знаку та величиниНроблять висновок про вплив температури рівноваги досліджуваної реакції.
