
- •Дмитрів а. М., Стецьків а. О., Сав’як о. Л. Фізична хімія Навчальний посібник
- •Івано-Франківськ – 2013
- •Передмова
- •Загальні правила роботи у лабораторії фізичної і колоїдної хімії
- •Правила техніки безпеки при виконанні робіт у лабораторії фізичної та колоїдної хімії
- •Основні правила надання першої допомоги при нещасних випадках
- •Розділ 1 Хімічна термодинаміка
- •Перший закон термодинаміки
- •1. Ізотермічний процес:
- •2. Ізохорний процес:
- •3. Ізобарний процес:
- •Термохімія
- •Залежність ентальпії реакції від температури. Рівняння кірхгофа
- •Приклади розв'язування задач
- •Заняття №1
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення теплового ефекту нейтралізації Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Заняття №2
- •Теоретична частина другий закон термодинаміки. Ентропія
- •Статистичний характер другого закону термодинаміки
- •Обчислення ентропії. Зміна ентропії у різних процесах
- •Третій закон термодинаміки. Абсолютне значення ентропії
- •Характеристичні функції
- •Термодинаміка хімічної рівноваги хімічний потенціал
- •Закон дії мас та константи рівноваги
- •Рівняння ізотерми хімічної реакції
- •Залежність константи рівноваги від температури. Рівняння ізохори та ізобари хімічної реакції
- •Приклади розв'язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Дослідження рівноваги оборотної хімічної реакції Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Вміст колб № 1-6
- •Питання для самоконтролю
- •Розділ 2 фазові рівноваги
- •Приклади розв'язування задач
- •Заняття №3 Тема: Термічний аналіз. Фазові перетворення в одно- і дво компонентних системах. Розподіл речовини між двома рідинами. Екстракція. Побудова діаграми стану бінарної системи.
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Побудова діаграми стану бінарної системи нафталін-фенол
- •Експериментальна частина
- •Методичні вказівки
- •Склад зразків
- •Питання для самоконтролю
- •Розділ 3 розчини
- •ОсМотичний тик розчинів. Зниження температури замерзання і підвищення температури кипіння розбавлених розчинів неелектролітів
- •Приклади розв'язування задач
- •Заняття №4 Тема: Колігативні властивості розчинів. Визначення молярної маси розчиненої речовини методом кріоскопії.
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення молярної маси розчиненої речовини методом Раста Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Заняття №5 Тема: Електрична провідність розчинів електролітів. Кондуктометричне титрування. Визначення ізотонічного коефіцієнту розчину електроліту.
- •Теоретична частина
- •Приклади розв'язування задач
- •Електропровідність розчинів електролітів
- •Приклади розв'язування задач
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Перелік питань, які виносяться на змістовий модуль 1
- •Лабораторна робота Визначення ізотонічного коефіцієнту розчину електроліту Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Розділ 4 електрохімія
- •Заняття №6 Тема: Електродні потенціали та електрорушійна сила гальванічних елементів. Окисно-відновні електроди. Потенціометричне визначення рН розчину.
- •Теоретичні відомості
- •Гальванічні елементи, їх класифікація
- •Приклади розв’язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Потенціометричне визначення рН водних розчинів Інформаційна частина
- •Експериментальна частина
- •Методичні вказівки
- •Результати вимірювань ерс хлорсрібно-скляного кола
- •Питання для самоконтролю
- •Поясніть, чому потенціал хлорсрібного електрода при даній концентрації кСl є сталим?
- •Заняття №7
- •Теоретичні відомості
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Експериментальна частина
- •Методичні вказівки
- •Питання для самоконтролю
- •Розділ 5 хімічна кінетика і каталіз
- •Методи визначення порядку реакції
- •Приклади розв’язування задач
- •Заняття № 8
- •Завдання для самостійної позааудиторної роботи
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Самостійна робота на занятті
- •Лабораторна робота Визначення константи швидкості реакції йодування ацетону
- •Експериментальна частина
- •Методика виконання роботи
- •Вивчення швидкості реакції йодування ацетону
- •Використовуючи рівняння (8.2) та значення Сац,0, сн,0, Сx і τ розраховують константу швидкості k.
- •Питання для самоконтролю
- •Заняття № 9
- •Теоретична частина вплив температури на швидкість реакції
- •Рівняння Арреніуса
- •Каталіз
- •Характерні особливості каталізаторів
- •Гомогенний каталіз
- •Кислотно-основний каталіз
- •Ферментний каталіз
- •Гетерогенний каталіз
- •Приклади розв’язування задач
- •Завдання для самостійної позааудиторної роботи і. Засвоїти основний матеріал навчальної програми
- •Іі. Дати письмові відповіді на контрольні запитання
- •Ііі. Розв’язати задачі
- •Перелік питань, які виносяться на змістовий модуль 2
- •Самостійна робота на занятті
- •Експериментальна частина
- •Методичні вказівки
- •Питання, які виносяться на модуль 1 «фізична хімія»
- •Банк тестів з фізичної хімії
- •1. Хімічна термодинаміка
- •2. Фазові рівноваги
- •3. Загальна характеристика розчиНів
- •4. Електрохімія
- •5. Хімічна кінетика
- •Засоби контролю знань студентів
- •Значення найважливіших фундаментальних сталих
- •Кріоскопічні та ебуліоскопічні константи деяких розчинників
- •Константи дисоціації деяких слабких електролітів при 25 °с
- •Стандартні ентальпії утворення ∆н0298, ентропії ∆s0298 та енергії Гіббса ∆g0298 деяких речовин при 298 к
- •Стандартні електродні потенціали деяких металів у водних розчинах
- •Перелік літератури Основна література
- •Додаткова література
Приклади розв'язування задач
Задача 1. Для лікування раку шкіри застосовується колхамінова мазь, яка складається з води, емульгатора, спирту, колхаміну, тимолу й синтоміцину. Скільки ступенів вільності має ця система?
Розв'язування. Число незалежних компонентів у цій системі К = 6 і співпадає з кількістю речовин, бо вони між собою хімічно не реагують. Кількість фаз Ф = 1, оскільки ця мазь є однорідною системою. Тоді за правилом фаз Ґіббса число ступенів вільності конденсованої системи становить: С=К – Ф+1=6 – 1+1 = 6, такими параметрами буде температура і ще 5 незалежних концентрацій будь-якої із 6 речовин. А концентрацію шостої речовини знаходять за різницею між 100 % і сумою п'яти інших.
Задача 2. Використовуючи діаграму стану Sb – Pb (рис. 2.1.), визначити кількість стибію, яка викристалізувалася, при охолоджуванні до 430°С 3 кг рідкого сплаву із вмістом 40 % свинцю.
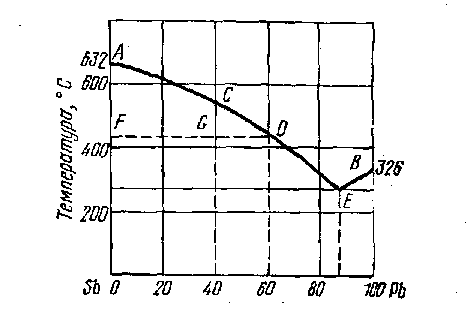
Рис. 2.1. Діаграма стану Sb – Pb
Розв'язування. Якщо сплав, що містить 40 % свинцю, охолодити до 430 °С, то стан його на діаграмі зображатиметься точкою G. У міру кристалізації сурми процентний вміст свинцю в рідкому сплаві зростає до 60 %. Позначимо масу сурми що викристалізувалася х, а масу рідкого сплаву – у. Згідно правила важеля (або правила відрізків) кількість фази (х), яка викристалізувалася, так відноситься до кількості взятого рідкого розплаву (у), як відрізок, прилеглий до кривої кристалізації GD, до відрізка FD, що характеризує склад рідкої фази при охолодженні до заданої температури, тобто
![]() .
.
З
даного рівняння визначаємо
![]() .
.
Із рис.2.1 визначаємо, що FD = 60, а GD = 60 – 20 = 40.
Тоді
![]() .
.
Відповідь: При охолоджуванні 3 кг рідкого сплаву із вмістом 40 % свинцю виділиться у вигляді кристалів 1 кг стибію.
Задача 3. Евтектичний сплав стибію і свинцю містить 13 % стибію (див. рис. 2.1). Який з металів і в якій кількості знаходитиметься в сплаві у вигляді кристалів, вкраплених в евтектику, якщо 10 кг рідкого сплаву, що містить 10 % стибію, охолодити до повного його затвердіння.
Розв'язування. Склад сплаву: Sb – 10%; Pb – 90%. Знаходимо кількість (кг) кожного із металів в 10 кг рідкого сплаву: свинцю 10∙0,9 = 9 кг, стибію 10∙0,1 = 1 кг. Оскільки процентний вміст стибію в сплаві менший ніж вміст його в евтектиці, то увесь стибій витрачається на утворення евтектики.
Визначимо масу евтектичного сплаву (х). Згідно умови в 100 кг евтектичного сплаву міститься 13 кг стибію. Складемо пропорцію і з одержаного рівняння визначаємо х:
![]() ,
,
![]() 7,7 кг.
7,7 кг.
Решта частина сплаву є кристалами свинцю, вкрапленими в евтектику. Маса їх дорівнює 10 – 7,7 = 2,3 кг.
Відповідь:7,7 кг і 2,3 кг.
Задача 4. Яку максимальну кількість йоду можна добути з 10 дм3 мінеральної води, в 1 дм3 сірковуглецю (екстрагентом служить 0,1 дм3 сірковуглецю), якщо при 25 0С коефіцієнт розподілу йоду між сірковуглецем та водою дорівнює 588. Молекулярна маса йоду в обох розчинниках однакова (в 1 дм3 Н2О міститься 3∙10-3 моль І2).
Розв'язування. Розраховуємо масу І2, яка може бути одержана при однократній екстракції. Знайдемо спочатку вміст йоду у вихідному розчині:
m0 = 254∙3∙10-3 ∙ 10 = 7,62 г.
Тоді:
![]()
Маса добутого йоду: 7,62 – 1,11 = 6,51 г.
