
- •Предмет, завдання і методологія біотехнології рослин
- •Історія розвитку методу культури клітин, тканин та органів рослин
- •Організація і обладнання біотехнологічної лабораторії
- •Посуд, інструменти і матеріали
- •Миття посуду
- •Методи стерилізації посуду
- •Методи стерилізації інструментів
- •Контрольні запитання і завдання
- •Живлення культури тканин
- •Мінеральне живлення
- •Вуглеводневе живлення
- •Вітаміни
- •Стимулятори росту
- •Фітогормони
- •Рослинні екстракти
- •РН – середовища
- •Приготування живильних середовищ
- •Стерилізація живильних середовищ
- •Стерилізація рослинного матеріалу
- •Контрольні запитання і завдання
- •Культура ізольованих органів і зародків
- •Контрольні запитання і завдання
- •Культура ізольованих клітин і тканин
- •Культура калюсних тканин
- •Особливості калюсних клітин
- •Генетика калюсних клітин
- •Культура клітинних суспензій
- •Культивування ізольованих клітин
- •Методи оцінки результатів
- •Мікроклональне розмноження рослин
- •Методи мікроклонального розмноження рослин
- •Етапи мікроклонального розмноження рослин
- •Контрольні запитання і завдання
- •Кріоконсервація клітин рослин
- •Контрольні запитання і завдання
- •Клітинна селекція
- •Спонтанні та індуковані мутанти
- •Контрольні запитання і завдання
- •Культура рослинних клітин і речовини вторинного синтезу
- •Фактори, які впливають на вихід продуктів
- •Компоненти середовища
- •Фізичні фактори
- •Селекція і відбір
- •Утворення вторинних речовин в культурах рослинних тканин
- •Глікозиди
- •Контрольні запитання і завдання
- •Культура ізольованих протопластів і соматична гібридизація
- •Виділення і очистка ізольованих протопластів картоплі
- •Виділення протопластів із мезофілу листка
- •Виділення протопластів із культури клітин
- •Культивування ізольованих протопластів
- •Умови культивування протопластів
- •Злиття ізольованих протопластів
- •Селекція соматичних гібридів
- •Генетична трансформація
- •Вектори для генетичної трансформації рослин
- •Плазміди агробактерій як вектори для трансформації
- •Вектори на основі днк-вмісних вірусів рослин
- •Методи перенесення чужинних генів у рослини
- •Трансгени і екологія
- •Контрольні запитання і завдання
- •Практичний курс Приготування і стерилізація живильних середовищ
- •Таблиця 8
- •Робота 1. Приготування маточних розчинів для середовища Мурасиге і Скуга (мс)
- •Робота 2. Приготування середовища Мурасиге і Скуга (мс). Стерилізація середовища автоклавуванням
- •Робота 3. Стерилізація рідких середовищ пропусканням через бактеріальний фільтр (холодна стерилізація)
- •Стерилізація рослинного матеріалу Робота 4. Стерилізація насіння і вирощування асептичних рослин
- •Робота 5. Стерилізація бульб, коренеплодів і кореневищ
- •Робота 6. Стерилізація листків
- •Робота 7. Стерилізація меристем
- •Калюсна культура Робота 8. Отримання первинного калюсу із різних експлантатів асептичних рослин
- •Робота 9. Дослідження явища фізіологічної полярності
- •Робота 10. Отримання перевивної калюсної культури
- •Робота 11. Дослідження впливу співвідношення ауксин:цитокінін у живильному середовищі на ріст калюсної тканини та її тип
- •КлітиннА суспензіЯ Робота 12. Отримання клітинної суспензії з калюсної тканини
- •Мікроклональне розмноження рослин Робота 13. Мікроклональне розмноження рослин живцями
- •Робота 14. Стебловий органогенез із листкових дисків тютюну
- •Таблиця 15 Середовища для мікроклонального розмноження тютюну та моркви (1 л середовища)
- •Робота 15. Ризогенез із листкових дисків тютюну
- •Робота 16. Прямий ембріогенез
- •Хід роботи
- •Робота 17. Непрямий ембріогенез
- •Культура ізольованих протопластів вищих рослин Робота 18. Виділення і культивування ізольованих протопластів вищих рослин
- •Словник термінів
- •Список літератури
Стимулятори росту
Для росту і диференціації будь-яких рослинних тканин і клітин при культивуванні їх на штучних живильних середовищах необхідна наявність у живильному середовищі стимуляторів росту. Без додавання до живильного середовища стимулюючих речовин в культурі здатні рости тільки пухлинні тканини (галові пухлини – їх утворення викликають галові кліщі; пухлини вірусного походження) і камбіальні тканини обмеженої кількості видів рослин (певних сортів моркви, а також верби і ожини). Однак при тривалому культивуванні тканини і ці останні потребують додавання до живильного середовища стимуляторів росту.
Окрему, групу гормоннезалежних тканин становлять, так звані, „звиклі” тканини. Такі тканини утворюють клітини, що виникають у популяції нормальних клітин під час культивування. Вважають, що їхня поява пов’язана зі зміною активності генів.
До речовин, які стимулюють ріст ізольованих тканин належать фітогормони: ауксини, цитокініни та гібереліни.
Багато дослідників для отримання первинної проліферації тканини в культурі і для підтримки інтенсивного недиференційованого росту тканини в пасажах додають до живильного середовища речовини невизначеного хімічного складу. Найчастіше використовують ендосперм кокосового горіха (кокосове молоко), кінського каштана, грецького горіха, кукурудзи, пшениці. Також широко використовують дріжджовий та солодовий екстракт (із пророслих зернівок ячменю), екстракти із різних частин рослин (листків, молодих частин стебла, плодів – томату, апельсину і кавуна). Ці екстракти виявляють рістактивуючі властивості.
Фітогормони
Для росту і диференціації будь-яких рослинних клітин необхідні ауксини і цитокініни. Оскільки різні клітини і тканини в культурі відрізняються за здатністю до автономного синтезу і метаболізму окремих груп фітогормонів, то у зв’язку з цим їхній ріст у різній мірі залежить від забезпечення екзогенними регуляторами росту.
За відмінністю в потребі в екзогенних ауксинах і цитокінінах виділяють кілька груп тканин:
1. тканини, які ростуть на середовищах з ауксинами;
2. тканини, для росту яких у складі середовища потрібні тільки цитокініни;
3. тканини, для росту яких необхідні ауксини і цитокініни.
До першої групи тканин належать експлантати бульби топінамбура, коренів цикорію і скорцени. Ріст тканини топінамбура прямо пропорційний від’ємному логарифму концентрації ауксину в середовищі, у зв’язку з цим ця тканина використовується для дослідження ауксинової активності природних рослинних екстрактів або нових синтезованих сполук.
Тканин, які ростуть при наявності в середовищі цитокініну, не багато. До них належать культура кінчика кореня турнепса і сім’ядолей сої. Тканину сої використовують для дослідження цитокінінової активності.
Найчисельнішою є третя група тканин, для росту яких в умовах in vitro в середовищі необхідні і ауксини, і цитокініни.
Із ауксинів для отримання і підтримання культури тканин найбільше використовуються β–індолілоцтова кислота (ІОК), α–нафтилоцтова кислота (НОК) і 2,4–дихлорфеноксіоцтова кислота (2,4-Д) у концентраціях 1–30 мг/л, 0,1–2 мг/л, 1 мг/л відповідно.
Для індукції калюсоутворення звичайно використовують 2,4-Д, яка у 300 разів активніша ніж ІОК і у 10 разів активніша ніж НОК.
Для індукції калюсоутворення звичайно використовують високі концентрації ауксинів, а при послідуючих пересадках тканина може рости при вмісті ауксинів у 10 разів меншому.
Для отримання калюсних культур дводольних рослин в середовища додається ІОК в концентраціях 1–10 мг/л. При послідуючих пересадках концентрацію зменшують до 0,1–0,05 мг/л.
Для отримання калюсу однодольних рослин використовуються досить високі дози 2,4–Д – 2–10 мг/л. Винятком є тканина ендосперму кукурудзи, яка здатна до автономного синтезу ауксину і росте на середовищі без регуляторів росту.
Цитокініни, а саме кінетин, були відкриті Скугом при вивченні росту калюсу тютюну. Встановлено, що він не тільки активує клітинні поділи, але є обов’язковим компонентом індукування органогенезу. Кінетин значно підвищує ріст багатьох калюсних культур, наприклад моркви, сої, топінамбура. Кінетин вводиться в середовище у концентраціях 0,001–10 мг/л .
Крім кінетину для культивування ізольованих рослинних тканин використовують і інші цитокініни, зокрема, бензиламінопурин (БАП) і зеатин, які мають більш високу активність підтримки росту та індукції органогенезу. Є дані, що високі концентрації кінетину (0,1 – 1 мг/л) можуть забезпечити ріст ауксиннезалежних калюсних тканин.
Цитокініни разом з ауксинами беруть участь в процесах органогенезу у рослин. Для закладення у калюсі коренів або пагонів необхідні певні концентрації і співвідношення цитокініну і ауксину (Рис. 1).
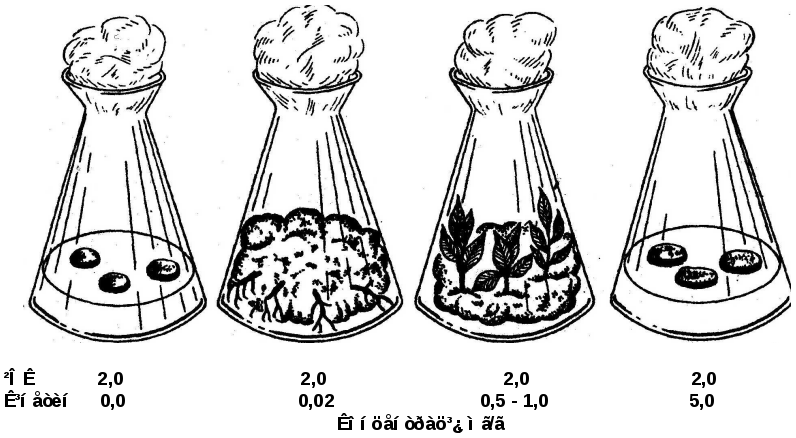
Рис.1. Схема спільної дії ІОК та кінетину на органогенез калюсу тютюну.
Для диференціації коренів у калюсі тютюну необхідно 2 мг/л ІОК і 0,02 мг/л кінетину (100:1). Підвищення концентрації кінетину до 0,5 – 1 мг/л індукує формування стеблових бруньок. Таким чином, зміщення співвідношення концентрацій ауксин-цитокінін в бік цитокініну сприяє утворенню стеблових бруньок, а в бік ауксину – закладанню коренів. Однак, як правило, і для індукції коренеутворення необхідна наявність цитокініну в низьких концентраціях.
Таким чином, ауксини додають для індукції клітинного поділу і диференціації; вони активують утворення коренів, регулюють регенерацію пагона. Цитокініни активують і прискорюють процес дедиференціації, клітинного поділу, калюсоутворення, активують диференціацію стеблових бруньок.
Гібереліни, як правило, не є необхідними для росту клітин у культурі, але Стюард і Стріт (1971) вказують, що при низький густині клітин явора у суспензії гібереліни необхідні. Крім цього гібереліни активують ріст і витягування стебла, тобто сприяють отриманню рослин з потужною надземною частиною.
