
- •Предмет, завдання і методологія біотехнології рослин
- •Історія розвитку методу культури клітин, тканин та органів рослин
- •Організація і обладнання біотехнологічної лабораторії
- •Посуд, інструменти і матеріали
- •Миття посуду
- •Методи стерилізації посуду
- •Методи стерилізації інструментів
- •Контрольні запитання і завдання
- •Живлення культури тканин
- •Мінеральне живлення
- •Вуглеводневе живлення
- •Вітаміни
- •Стимулятори росту
- •Фітогормони
- •Рослинні екстракти
- •РН – середовища
- •Приготування живильних середовищ
- •Стерилізація живильних середовищ
- •Стерилізація рослинного матеріалу
- •Контрольні запитання і завдання
- •Культура ізольованих органів і зародків
- •Контрольні запитання і завдання
- •Культура ізольованих клітин і тканин
- •Культура калюсних тканин
- •Особливості калюсних клітин
- •Генетика калюсних клітин
- •Культура клітинних суспензій
- •Культивування ізольованих клітин
- •Методи оцінки результатів
- •Мікроклональне розмноження рослин
- •Методи мікроклонального розмноження рослин
- •Етапи мікроклонального розмноження рослин
- •Контрольні запитання і завдання
- •Кріоконсервація клітин рослин
- •Контрольні запитання і завдання
- •Клітинна селекція
- •Спонтанні та індуковані мутанти
- •Контрольні запитання і завдання
- •Культура рослинних клітин і речовини вторинного синтезу
- •Фактори, які впливають на вихід продуктів
- •Компоненти середовища
- •Фізичні фактори
- •Селекція і відбір
- •Утворення вторинних речовин в культурах рослинних тканин
- •Глікозиди
- •Контрольні запитання і завдання
- •Культура ізольованих протопластів і соматична гібридизація
- •Виділення і очистка ізольованих протопластів картоплі
- •Виділення протопластів із мезофілу листка
- •Виділення протопластів із культури клітин
- •Культивування ізольованих протопластів
- •Умови культивування протопластів
- •Злиття ізольованих протопластів
- •Селекція соматичних гібридів
- •Генетична трансформація
- •Вектори для генетичної трансформації рослин
- •Плазміди агробактерій як вектори для трансформації
- •Вектори на основі днк-вмісних вірусів рослин
- •Методи перенесення чужинних генів у рослини
- •Трансгени і екологія
- •Контрольні запитання і завдання
- •Практичний курс Приготування і стерилізація живильних середовищ
- •Таблиця 8
- •Робота 1. Приготування маточних розчинів для середовища Мурасиге і Скуга (мс)
- •Робота 2. Приготування середовища Мурасиге і Скуга (мс). Стерилізація середовища автоклавуванням
- •Робота 3. Стерилізація рідких середовищ пропусканням через бактеріальний фільтр (холодна стерилізація)
- •Стерилізація рослинного матеріалу Робота 4. Стерилізація насіння і вирощування асептичних рослин
- •Робота 5. Стерилізація бульб, коренеплодів і кореневищ
- •Робота 6. Стерилізація листків
- •Робота 7. Стерилізація меристем
- •Калюсна культура Робота 8. Отримання первинного калюсу із різних експлантатів асептичних рослин
- •Робота 9. Дослідження явища фізіологічної полярності
- •Робота 10. Отримання перевивної калюсної культури
- •Робота 11. Дослідження впливу співвідношення ауксин:цитокінін у живильному середовищі на ріст калюсної тканини та її тип
- •КлітиннА суспензіЯ Робота 12. Отримання клітинної суспензії з калюсної тканини
- •Мікроклональне розмноження рослин Робота 13. Мікроклональне розмноження рослин живцями
- •Робота 14. Стебловий органогенез із листкових дисків тютюну
- •Таблиця 15 Середовища для мікроклонального розмноження тютюну та моркви (1 л середовища)
- •Робота 15. Ризогенез із листкових дисків тютюну
- •Робота 16. Прямий ембріогенез
- •Хід роботи
- •Робота 17. Непрямий ембріогенез
- •Культура ізольованих протопластів вищих рослин Робота 18. Виділення і культивування ізольованих протопластів вищих рослин
- •Словник термінів
- •Список літератури
Селекція соматичних гібридів
Селекцію соматичних гібридів здійснюють кількома методами.
При механічній ізоляції використовують морфологічно різні типи батьківських протопластів, після злиття продукти з’єднаних протопластів виявляють візуально під мікроскопом, ізолюють мікропіпеткою і культивують окремо. Наприклад при злитті протопластів тютюну і моркви як селективні маркери використовували зелені хлоропласти тютюну і червоно-оранжеві хромопласти моркви.
Другим методом, який дозволяє проводити відбір соматичних гібридів, є фізіологічна комплементація – спільна взаємодоповнююча дія різних генів. Протопласти двох видів тютюну N. glauca і N. langsdorfii утворювали клітинні стінки, але не могли ділитися і утворювати калюс на середовищі Нагата і Такебе. В той же час протопласти гібриду ділилися і утворювали калюс. Ще однією особливістю гібридного калюсу була здатність рости на середовищі без гормонів, що дало можливість створити цей метод селекції.
Існують також інші методи відбору соматичних гібридів. Наприклад: селекція за стійкістю до антибіотиків, гербіцидів, аналогів амінокислот і т.д.
Використання ізольованих протопластів не обмежується можливістю отримання соматичних гібридів. Ізольовані протопласти широко використовують у клітинній селекції та генетичній трансформації.
Контрольні запитання і завдання
1. Що таке ізольований протопласт?
2. Які існують методи виділення ізольованих протопластів?
3. Які фактори впливають на життєздатність ізольованих протопластів?
4. Чому у середовища для виділення та культивування ізольованих протопластів обов’язково додавати осмотичний стабілізатор?
5. Які речовини використовують при виділенні ізольованих протопластів як осмотичні стабілізатори?
6. Які ферменти використовують для виділення ізольованих протопластів?
7. Що обумовлює вибір складу ферментної суміші?
8. Із якого рослинного матеріалу можна виділяти ізольовані протопласти?
9. За яким методом проводять виділення ізольованих протопластів? Охарактеризуйте його.
10. Як щільність висіву ізольованих протопластів впливає на їхню життєздатність?
11. Що таке соматична гібридизація?
12. Які існують способи злиття ізольованих протопластів?
13. Які існують способи відбору та ідентифікації соматичних гібридів?
14. Які соматичні гібриди були одержані методом злиття ізольованих протопластів?
Генетична трансформація
Крім соматичної гібридизації і клітинної селекції є ще один метод створення in vitro покращених форм господарсько цінних рослин – це генетична трансформація.
Термін трансформація походить від латинського transformatio – перетворення і означає зміни в геномі та спадкових властивостей організму.
Генетична трансформація досягається шляхом проникнення крізь канали клітинної мембрани екзогенної ДНК і взаємодії останньої з клітинним геномом.
На відміну від соматичної гібридизації і клітинної селекції генетичну трансформацію розглядають як спосіб отримання більш обмежених і специфічних генетичних змін. У багатьох випадках окрема важлива у сільськогосподарському відношенні ознака, що контролюється одним або невеликою кількістю генів, може бути змінена шляхом трансформації, при цьому більша частина геному залишається без змін. Технологія рекомбінантних ДНК дозволяє виділити у чистому вигляді і в достатній кількості будь-який ген і при наявності вектора або іншим способом вбудувати цей ген до складу хромосомної ДНК і добитися його експресії. Використання цієї технології робить пошук цілеспрямованим і значно розширює можливості маніпулювання генетичним апаратом при скороченні часу отримання нових форм рослин.
В усьому світі проводяться дослідження по визначенню, виділенню, клонуванню і введенню в рослини генів, які відповідають за стійкість до холоду, посухи, засолення, тобто до стресових впливів оточуючого середовища, за стійкість до шкідників, гербіцидів і пестицидів, хвороб тощо. Той факт, що геном рослин вивчений гірше, ніж геном ссавців значно ускладнює такі дослідження. На сьогодні розроблено багато підходів до проблеми трансформації, однак з практичної точки зору відносно простий і відтворюваний метод базується на використанні Agrobacterium tumеfaciens.
A.tumеfaciens – це ґрунтова бактерія із родини Rhizobiaceae, яка здатна, поселяючись на раневих поверхнях рослин викликати утворення пухлин. Власне пухлинотворним агентом є плазміда, частина якої – Т-ДНК (від англ. transferred DNA), переноситься в хромосоми клітин рослини (Рис. 7). Плазміда – невелика кільцева молекула ДНК, здатна до стабільного, не зв’язаного з хромосомами існування і автономної реплікації (біосинтез дочірніх ДНК). Плазміди можуть вбудовуватися у хромосоми. Плазміди локалізовані в цитоплазмі бактеріальних клітин і клітинах деяких дріжджів. Після трансформації рослинні клітини починають швидко і неорганізовано рости і синтезувати особливі речовини – опіни (похідні амінокислот і цукрів), які бактерії використовують як джерело азоту і вуглецю. Тобто утворення пухлин супроводжується перебудовою метаболізму клітин, і вони починають синтезувати сполуки, необхідні лише для бактерій.
Раніше припускали, що A. tumеfaciens вражає саме пошкодженні рослини внаслідок руйнування клітинної стінки і усунення фізичного бар’єру, який ускладнює проникнення бактерій у клітину. Однак сьогодні вважається, що індуктором генетичної трансформації у агробактерій є фенольні сполуки, ацетосирингон і гідроксіацетосирингон, які виділяють рослини при пораненнях.Плазміди, які викликають пухлини називаються Ті-плазмідами (від англійського tumor inducing – індукуючі пухлину). Це кільцеві молекули ДНК

Рис.7. Етапи індукції корончатого галу після інфікування рослини Agrobacterium tumеfaciens.
довжиною близько 200 кб (3-5 % від розміру хромосоми агробактерії), які стабільно зберігаються в агробактеріях при температурі нижче 300С. В бактеріальних клітинах вони реплікуються автономно. Ті-плазміди розрізняють за типом опіну, який синтезується. Найчастіше зустрічаються плазміди, які кодують нопалін або октопін. Вважається, що клітина може містити лише один тип плазміди: або октопінову, або нопалінову.
Генетична карта Ті-плазміди повністю не розшифрована. З’ясовано тільки 4 ділянки: дві онкогенні (Т-область і vir-область) і дві ділянки (OR1, CON), які визначають морфологію пухлин, забезпечують реплікацію плазмід та їхню кон’югацію (Рис. 8). Генетичні дослідження показали, що гени, які відповідають за індукцію пухлини, синтез опінів і пригнічення диференціації, розташовані близько один від одного і входять до складу Т-області плазміди, яка вбудовується у хромосому клітини при інфекції. Т-сегмент має довжину близько 20 кб (10 % Ті-плазміди) і вбудовується в різні, очевидно неспецифічні, області хромосоми. На Т-області картовано сім генів, які відповідають за синтез опіну і за пригнічення диференціації клітин. Слід відмітити, що всі гени, які відповідають за перенесення та інтеграцію Т-ДНК, знаходяться не в Т-ДНК, а в області вірулентності (vir-область).
У
тих випадках, коли важко регенерувати
цілі рослини із окремих клітин, для
трансформації використовують Agrobacterium
rhizogenes,
яка
викликає посилене утворення коренів
при зараженні рослин. Рослини багатьох
видів можуть регенерувати із культури
коренів, які індукує ця бактерія.
Плазміди, які викликають коренеутворення,
називають Ri-плазмідами
(від англійського root
inducing
–
індукуючий корені). Корені швидко ростуть
у культурі подібно до тканини пухлин і
відсутність бактерій не впливає на
їхній ріст. З’ясувалося, що клітини
корінців також містять опіни, а їх геноми
містять по декілька копій Т-ДНК.
Ri-плазміди
відрізняються від Ті-плазмід тим, що
вони є природними
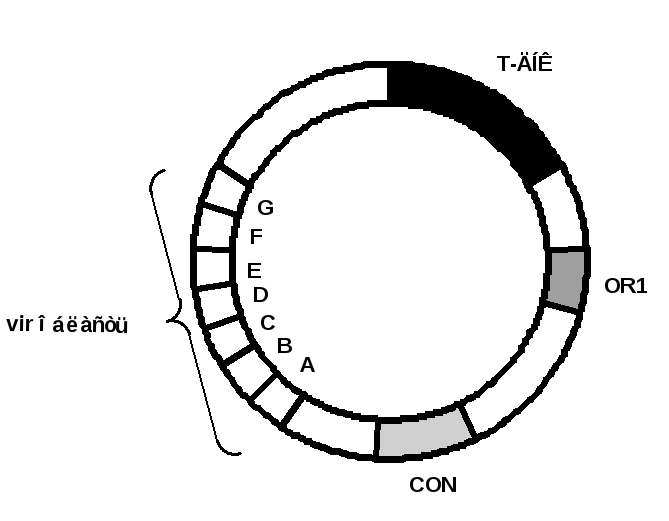
Рис.8. Узагальнена генетична карта Ti-плазміди Agrobacterium tumеfaciens:
vir-область – забезпечує вірулентність;
Т-ДНК – містить ген, який контролює синтез тільки одного із опінів;
OR1 –ділянка реплікації;
CON – ділянка кон’югації.
векторами, після трансформації якими рослинні клітини здатні регенерувати у здорові фертильні рослини. У даний час ці плазміди розглядають як перспективніші вектори для генетичної трансформації рослинних клітин.
