
- •Болезни в трех томах
- •Общая часть
- •8 Список сокращений
- •Основные сведения об инфекционных болезнях
- •Классификация инфекционных болезней
- •2 Ж. Возианова
- •Принципы лечения инфекционных болезней
- •Характер взаимодействия с микро-и макроорганизмом
- •Возможные побочные реакции
- •II. Аминогли-козиды
- •III. Тетрацик-лины
- •Специфическая профилактика инфекционных болезней
- •Заболевания преимущественно с воздушно-капельным механизмом передачи
- •1Ейраминидаза
- •Действие на факторы клеточного и гуморального иммунитета
- •Формирование антитоксического иммунитетаСтимуляция местных факторов защиты, в том числе завершенного фагоцитоза
- •Функциональные нарушения
- •Механизмов защиты
- •Внедрение микоплазм в слизистую оболочку дыхательных путей
- •Заболевания преимущественно с фекально-оральным механизмом передачи
- •Размножение сальмонелл в тонкой кишке
- •Вегетативная нс
- •Заболевания, вызываемые иерсиниями
- •Желудке (высвобождение эндотоксина при этом незначительное)
- •Непосредственное повреждающее действие шигелл на слизистую оболочку толстой кишки
- •Серогруппа 01 (холерные)
- •Всасывание фрагментов вибрионов в кровь Образование различных факторов агрессии
- •Выработка вибриоцидных антител
- •Структура и функции печени
- •Методы диагностики, использующиеся при обследовании больных вг, и их оценка
- •21 Ж. Возианова
- •Особенности лечения больных вирусным гепатитом с затяжным течением
- •Заболевания, вызываемые вирусами
- •Энтеровирусами Паралитические формы (полиомиелитоподобные заболевания)
- •Асептический серозный менингит
- •Энтеровирусный энцефалит
- •Синдром Гийена—Барре (полирадикулоневрит)
- •Острые респираторные заболевания («летний грипп»)
- •Лихорадка с экзантемой
- •Везикулярный стоматит с экзантемой (ящуроподобный синдром)
- •Герпетическая ангина (герпангина)
- •Эпидемический конъюнктивит
- •Энтеровирусная диарея (летние гастроэнтериты)
- •Энтеровирусный гепатит
- •Эпидемическая миалгия (плевродиния, борнхольмская болезнь)
- •Энтеровирусная инфекция у новорожденных
- •Бессимптомная инфекция
- •Лечение нематодозов
- •Лечение цестодозов
- •Протозойные заболевания
- •1Нфекц1йн1 I паразитарн1 хвороби
Протозойные заболевания
Простейшие
(общая характеристика)
Простейшие (protozoa) — тип микроскопических организмов, состоящих из одной клетки. В настоящее время известно уже более 7000 видов простейших, патогенных для человека, животных и растений.
Основные их особенности:
тело покрыто пеликулой, в клетке имеется дифференцированное ядро, содержащее генетический материал;
набор органоидов идентичен таковому клеток многоклеточных организмов;
это бесполые организмы, размножаются они посредством бинарного или множественного деления (исключение — кокцидии и периодически балантидии);
— они способны к активному движению, благодаря наличию органелл движения (жгутики, реснички) или псевдоподий;
они не продуцируют токсины;
так как патогенные простейшие имеют биохимическое сходство с клетками животных и человека, многие лекарственные вещества, которые применяют для лечения вызываемой простейшими патологии, оказывают токсическое действие и на организм человека (животного);
простейшие формируют слабый иммунный ответ, вследствие этого многие протозойные заболевания приобретают затяжное или хроническое течение;
низкая иммуногенность паразитарных антигенов объясняет сложность создания вакцин против простейших.
Классификация простейших еще окончательно не упорядочена. Наиболее часто пользуются классификацией, в основе которой лежит способ передвижения простейших. В соответствии с этим все патогенные простейшие человека делят на 4 класса:
саркодовые, или корненожки (Sarcodina, s.Rhizopoda), сюда относят различные виды амеб;
жгутиконосцы, или биченосцы (Mastigophora, s. Flagellata) — лямблии, трипаносомы, лейшмании;
реснитчатые, или инфузории (Ciliata, s.Infusoria) — балантидии;
ПРОТОЗОЙНЫЕ ЗАБОЛЕВАНИЯ
— споровики (Sporozoa) — малярийные плазмодии, токсоплазма, кокцидии.
В последнее время эта классификация изменена, выделяют 5 самостоятельных типов простейших, отличающихся по внутренней организации: саркожгутиконосцы (Sarcomastigophora), споровики (Sporozoa), книдоспоридии (Cnidosporidia), микроспоридии (Microsporidia), реснитчатые, или инфузории (Ciliophora). Но и это классификация далека от совершенства и, вероятно, еще будет меняться.
В специальной литературе приводятся данные, адаптированные к одной из этих классификаций, поэтому врач должен иметь представление о каждой из них.
амебиаз
Амебиаз — антропонозное протозойное заболевание, вызываемое дизентерийной амебой, характеризующееся широким диапазоном клинических проявлений — от бессимптомного носительста до тяжелых кишечных и внекишечных поражений (лат. — amoebiasis, англ. — amebiasis).
Краткие исторические сведения. Возбудитель амебиаза в 1875 г. был обнаружен и описан профессором Санкт-Петербургской Военно-медицинской академии Ф.А.Лешем. Дальнейшие исследования позволили доказать роль выделенного возбудителя в патологии человека. Так, в 1883 г. R.Koch обнаружил амебы в просвете и стенке кишечника людей, умерших в Египте от «тяжелой дизентерии», а в 1886 г. Kartulis нашел их не только в кишечнике, но и в печени погибших людей. В 1903 г. немецкий ученый F.Schaudin описал еще несколько видов амеб, выделенных им из кишечного содержимого людей, он же установил морфологические различия между ними. Детально патогенез заболевания был изучен в 1913 г. Walker и Sellards, убедительно доказавшими роль именно дизентерийной амебы в патогенезе возникновения особой формы дизентерии у человека.
Актуальность. По заключению ВОЗ (1988), амебиаз является одной из важнейших медицинских и социальных проблем в западных и юго-восточных районах Африки, Юго-Восточной Азии, Китае, Латинской Америке. Здесь амебиаз — одна из наиболее частых причин развития тяжелой диареи, нередко заканчивающейся летальными исходами, а число лиц, инвазированных дизентерийной амебой, составляет 20—70%.
В зонах умеренного климата амебиаз регистрируют в виде спорадических случаев, однако отсутствие настороженности врачей и знания этой патологии делают статистические данные о заболеваемости аме-биазом в этих регионах не вполне достоверными, тем более, что носительство дизентерийной амебы при тщательном обследовании выявляется у 5—15% обследованных и здесь. В нашей стране спорадические случаи амебной дизентерии встречаются преимущественно на юге. В странах СНГ наиболее неблагополучными являются государства Средней Азии и Закавказья, где носительство выявлено у 15—35% жителей.
Особое значение проблема амебиаза приобретает в настоящее время в связи с расширением контактов с разными странами, увеличением числа туристических и деловых поездок в регионы с жарким клима-
том. При этом создаются реальные условия для заражения в связи с высоким уровнем заболеваемости коренного населения в этих регио--нах. Вероятна также активация собственной инвазии, протекавшей, возможно, до того в форме бессимптомного носительства, этому могут способствовать перегревание, изменение условий питания и др. Не случайно в развитии такой полиэтиологичной патологии, как «диарея путешественников», амеб называют одной из ведущих причин.
Этиология. Возбудитель амебиаза — дизентерийная амеба (Entamoeba hystolytica), относится к подцарству простейших (protozoa), типу Sarcomastigophora, классу Sarcodina, отряду Amoebida.
В организме человека ее обнаруживают в виде вегетативных форм и цист. Однако в зависимости от условий, создающихся в кишечнике, вегетативная форма может существовать в виде двух форм — малой вегетативной (forma minuta) и большой вегетативной (forma magna).
Малая вегетативная форма (просветная форма) обитает в верхнем отделе толстой кишки человека, где находит наиболее благоприятные для себя условия жизни. Этот мелкий одноклеточный организм размерами 12—20 мкм в диаметре имеет неправильную форму с короткими ложноножками, обеспечивающими его подвижность. Питается содержимым кишечника путем эндоцитоза, размножается простым делением. Просветная форма в окружающей среде неустойчива, гибнет через 10—20 мин, выделяясь из кишечника с фекалиями при ускоренной перистальтике кишечника. Если перистальтика замедлена, то, попадая в нижние отделы толстой кишки (то есть в более неблагоприятные для нее условия), она последовательно превращается в предцистную форму (округлая, менее подвижная, без включений), а затем и в цисту.
Большая вегетативная форма (эритрофаг, гематофаг, тканевая) образуется из просветной при соответствующих условиях. Это уже более крупное простейшее (до 40 мкм в диаметре), обладающее активной подвижностью с помощью корненожек. Цитоплазма ее разделена на экто- и эндоплазму, содержит сферическое ядро до 3—7 мкм в диаметре. Питается, «захватывая» и переваривая эритроциты, которые можно обнаружить в ее эндоплазме. У таких амеб, перешедших к паразитическому способу существования, выявлена способность образовывать различные протеолитические ферменты, в том числе гиалуронида-зу — фермент, усиливающий повреждение кишечной стенки. Размножаются эритрофаги делением, но превращаться при неблагоприятных условиях снова в просветные формы или образовывать цисты они не способны. Очень неустойчивы в окружающей среде, где погибают уже через несколько минут.
Цисты дизентерийной амебы образуются из просветных форм, проходя последовательно стадии незрелых цист (одно-, затем двухъядер-ные), а затем превращаясь в зрелые — четырехъядерные. Размеры таких зрелых (инвазивных) цист 10—12 мкм в диаметре, они имеют двухконтурную оболочку, содержат в цитоплазме хроматоидные тела в виде палочек. Цисты довольно устойчивы в окружающей среде: в фекалиях могут сохраняться более 1 нед при температуре +28 °С... + 30 °С, еще дольше сохраняют жизнеспособность во влажной почве и в воде (сроки выживания определяются температурой окружающей среды), хорошо переносят высыхание. При кипячении погибают быстро — уже через несколько минут. Обычные дозы хлора, применяемые для обеззараживания питьевой воды, на них не действуют.
Культивировать дизентерийные амебы можно на искусственных питательных средах, наиболее часто используют среду Павловой, где они растут вместе с сопутствующей бактериальной флорой. Аксенические (безбактериальные) среды применяют главным образом для выделения культур, используемых затем для приготовления диагностикумов. Оптимум роста + 37 °С и рН 7,0.
До настоящего времени дискутируется вопрос о видовом единстве Е.histolytica. Мнение о наличии патогенных и непатогенных дизентерийных амеб поддерживают далеко не все исследователи. Большинство их считают, что Е.histolytica непатогенного вида не имеет: отдельные штаммы в отдельных регионах будут отличаться вирулентностью, но ее можно усилить или ослабить различными путями.
Эпидемиология. Источником инвазии являются лица с бессимптомным амебиазом (син. «просветный амебиаз»), которые выделяют в окружающую среду зрелые цисты дизентерийной амебы. Бессимптомный амебиаз является главной формой отношений «хозяин — паразит» между возбудителем и организмом человека, он может длиться многие годы, сохраняя свое эпидемиологическое значение. Такие лица представляют реальную опасность для окружающих, в особенности, если они работают на объектах питания или водоснабжения, так как могут выделять в течение суток огромное (1,5* 10 ) количество цист.
Больные кишечным амебиазом выделяют большие вегетативные формы, которые неустойчивы в окружающей среде, в связи с чем их эпидемиологическая роль весьма ограничена.
Механизм передачи при амебиазе — фекально-оральный.
Факторами передачи являются загрязненные цистами пищевые продукты, особенно овощи, не проходящие термической обработки перед употреблением. Важным фактором передачи является вода из открытых водоемов, загрязненных фекалиями, содержащими цисты амеб. Могут способствовать распространению цист и загрязнению ими пищевых продуктов тараканы, мухи , в кишечнике которых цисты длительно сохраняют свою жизнеспособность. Можно заразиться при непосредственном контакте с носителем (грязные руки), а также через загрязненные предметы обихода, игрушки. В различных климатогео-графических зонах какой-либо из этих факторов может быть ведущим, что оказывает влияние на сезонные подъемы заболеваемости.
Восприимчивость человека к заболеванию очень невысока. Большинство зараженных становятся бессимптомными амебоносителями. Вероятность заболеть кишечным амебиазом в значительной мере определяется функциональным состоянием пищеварительного тракта, трофикой слизистой оболочки, состоянием микробной флоры, общей реактивностью организма и другими факторами. Восприимчивость повышается при плохом питании, тяжелых заболеваниях кишечника.
Амебиаз сопровождается развитием иммунных реакций (тканевых и гуморальных), однако они не защищают человека от повторного заболевания и не всегда приводят к самоосвобождению от возбудителя.
Вместе с тем, известно, что, несмотря на высокую степень зараженности амебами населения тропических регионов, манифестные формы у них возникают реже, чем у лиц, прибывших из неэндемичных мест.
Классификация. В соответствии с рекомендациями ВОЗ (1988), выделяют следующие клинические формы амебиаза:
— бессимптомное амебоносительство (просветный амебиаз, бессимптомный амебиаз);
— амебную дизентерию (кишечный амебиаз);
внекишечный амебиаз (амебный абсцесс печени, легких, мозга). По выраженности клинических проявлений выделяют:
манифестную форму;
субклиническую форму.
По длительности течения амебиаз бывает:
острый (до 3 мес),
подострый (до 6 мес),
хронический (более 6 мес). По характеру течения выделяют:
амебиаз непрерывно прогрессирующий,
рецидивирующий. По тяжести различают:
легкое,
средней тяжести,
тяжелое течение амебиаза.
Выделяют как особую молниеносную форму амебиаза — очень тяжелое и сверхострое течение.
Примерная формулировка диагноза. 1. Бессимптомное амебоносительство (просветный амебиаз).
2. Амебная дизентерия рецидивирующая, течение средней тяжести.
3. Амебная дизентерия непрерывно прогрессирующая, тяжелое те- чение.
4. Абсцесс печени амебный, тяжелое течение.
Патогенез. Заражение происходит при заглатывании с пищей или водой вегетативных форм и цист амеб. Под действием кислого желудочного содержимого вегетативные формы гибнут, а цисты сохраняются и с содержимым желудка продвигаются далее. Во время прохождения тонкой кишки в цисте еще раз происходит деление, таким образом при эксцистировании ее в верхнем отделе толстой кишки выходят 8 просветных амеб. Эти амебы могут длительно (годами) жить и размножаться в просвете кишечника, не вызывая никаких патологических симптомов. Выявляться такой способ сосуществования амебы и человека может случайно при обнаружении в кале цист или (реже) малых вегетативных форм, что расценивается как «здоровое носительство».
Отношение к такому «здоровому носительству» пока не однозначно. До настоящего времени еще существует и полностью не опровергнута «теория облигатного паразитизма», в соответствии с которой даже при носительстве наблюдается повреждение поверхностного эпителия кишки, которое быстро регенерирует, не давая клинических проявлений.
Однако значительно большее признание получила теория «факультативного паразитизма», суть которой заключается в том, что лишь при определенных условиях амебы, обитающие в просвете кишечника, переходят к паразитическому существованию. Такими условиями, изменяющими жизненный цикл амеб, может быть перегревание организма (в результате наступает ишемия пищеварительного тракта, сопровождающаяся снижением его резистентности, активацией кишечной флоры), изменение диеты, особенно использование диеты углеводной (при этом меняются рН, состав кишечной микрофлоры), применение в большом количестве специй (раздражение слизистой оболочки) и т.д. Особенно важная роль отводится составу кишечной микрофлоры, что объясняют тем, что она способствует поддержанию рН среды, необходимой для жизни амеб, обмену их веществ, к тому же ядерная ДНК амеб частично синтезируется из ДНК фагоцитированных бактерий.
Таким образом, формируется довольно тесная взаимосвязь между амебами и кишечной микрофлорой, при этом постепенно развивается дисбактериоз, на фоне которого легче и чаще возникают острые кишечные заболевания. Наблюдающееся при этом повреждение слизистой оболочки способствует переходу амеб к паразитическому существованию, облегчает их внедрение в толщу кишки, активирует процесс выделения протеолитических ферментов. Особенно благоприятные условия для перехода амеб к паразитическому существованию создаются при шигеллезе, гельминтозах (микст-патологию регистрируют в некоторых регионах почти у 50 % больных амебиазом).
Действие Е.histolytica на кишечную стенку обусловлено цитолизом (об этом говорит само название — histolytica). Под действием цитолитических ферментов амеб наступает расплавление сначала поверхностных слоев слизистой оболочки, затем подслизистой оболочки и даже мышечного слоя. Этот процесс идет как при контакте с амебами, так и бесконтактным путем, предшествующим внедрению амеб. Распространение процесса вглубь сопровождается повреждением кровеносных сосудов. Эритроциты крови, излившейся в образовавшуюся язву, «заглатываются» амебами, которые таким образом переходят к новому способу питания, превращаясь в эритрофаги. Амебы обладают также способностью воздействовать на находящиеся рядом с ними лейкоциты, разрушая их, что является одной из причин отсутствия местной воспалительной реакции.
При проникновении амеб в ткани образуются мелкие узелки (микроабсцессы), наполненные детритом, которые, вскрываясь, превращаются в язвы. Особенностью амебных язв является отсутствие выраженной воспалительной реакции окружающих тканей, что обусловливает характерный вид язв — они расположены на неизмененном фоне, имеют форму глубоких щелей с подрытыми краями или бутылочек, горлышком обращенных в просвет кишки. Наиболее часто при амебиа-зе процесс локализуется в слепой и восходящей кишках (правосторонний колит). Дистальные отделы толстой кишки, в том числе и прямая кишка, поражаются реже и позже, что нужно учитывать при оценке результатов ректороманоскопии.
Размер язв колеблется от еле заметных до 2—2,5 см в диаметре. Глубина их может достигать серозной оболочки. Язвенный процесс в кишечнике сопровождается нарушением его функции в виде расстройства стула с наличием в нем патологических примесей (слизи и крови).
В начальный период в просвете кишечника содержится слизь с малым количеством клеточных элементов, главным образом эритроцитов. Слизь прозрачна, имеет вид «малинового желе».
При дальнейшем развитии болезни в толстой кишке выявляются язвы на различных стадиях развития, а кишечное содержимое приобретает гнойный характер за счет появления в нем и лейкоцитов.
Язвенный процесс в кишечнике носит прогрессирующий характер, в повреждении кишечной стенки при амебиазе важное значение приобретают сопутствующая микробная флора, а также продукты распада собственных тканей, ведущие к развитию аллергических реакций.
При вовлечении в процесс крупных сосудов возникают кишечные кровотечения. При наличии глубоких язв, достигающих серозной оболочки, развиваются симптомы периколита. Язвенный процесс в кишечнике может приводить к прободению стенки кишки и развитию перитонита. Рубцевание множественных язв может вызвать сужение просвета кишечника. Длительный язвенный процесс в стенке кишечника иногда сопровождается пролиферативными реакциями и приводит к возникновению опухолевидных образований — амебом.
При длительном рецидивирующем процессе развивается анемия, в основе которой лежат потеря крови; нарушение функции кишечника приводит к белково-энергетической недостаточности, полигиповитаминозу, истощению организма.
При разрушении формирующимися микроабсцессами крупных венозных сосудов амебы проникают в них и могут быть занесены с током крови во внутренние органы, что ведет к образованию внекишеч-ных амебных абсцессов. Наиболее часто поражается печень, в особенности ее правая доля. Возможно также развитие абсцессов легких, мозга, селезенки, половых органов. Абсцессы печени могут достигать 5—10 см в диаметре, они бывают единичными или множественными. Содержимое амебных абсцессов представляет собой полужидкую массу красного или шоколадного цвета, состоящую из распавшихся тканей, лимфоцитов, эритроцитов и элементов соединительной ткани. Возможно нагноение таких абсцессов при присоединении вторичной инфекции, что резко отягощает прогноз. В амебных абсцессах дизентерийные амебы обнаруживаются на границе между здоровой и расплавленной тканью.
При амебных абсцессах печени может возникать расплавление окружающих тканей и прорыв содержимого в соседние органы. Амебный абсцесс легких может быть следствием такого прорыва или обусловлен гематогенным заносом возбудителя в легкие. При заносе амеб в мозг возможно развитие абсцессов мозга.
Возможна также реакция печени на инвазию в виде неспецифического перипортального воспаления, сопровождающегося диффузным увеличением печени без заметного нарушения ее функции. Для обозначения этого состояния иногда пользуются термином «амебный гепатит», что неверно, поскольку амеб в биоптатах не обнаруживают.
Язвенное поражение кишки сопровождается местными и общими иммунными реакциями. Противоамебные антитела выявляются в стенке кишечника и в крови, однако они не приводят к освобождению от возбудителя. Наиболее вероятно, что местные и общие иммунные реакции определяют особенности течения заболевания — чередование ремиссий и обострений.
Клиника. Амебная дизентерия (кишечный амебиаз). Длительность инкубационного периода у лиц, проживающих в эндемичном по амебиазу регионе, в большинстве случаев установить не удается, учитывая постоянно существующую вероятность заражения и способность Е.histolytica к длительному обитанию в просвете толстой кишки без перехода к паразитическому существованию. Люди, прибывшие из эндемичного района после кратковременного пребывания там, могут дать более четкие сведения о вероятных сроках инвазирования. При этом инкубационный период может колебаться в пределах от нескольких дней до 2—3 мес и даже дольше (тем более, что у таких лиц тоже возможно длительное пребывание амеб в кишечнике в виде просвет-ных форм).
Начало заболевания чаще постепенное. В некоторых случаях первыми признаками болезни может быть появление слизи и крови в оформленном стуле, не сопровождающееся общетоксическими и (или) диспепсическими проявлениями. У таких больных диагноз может быть верифицирован лишь на основании обнаружения гематофагов в кале.
В большинстве случаев заболевание начинается с диарейного синдрома: появляется жидкий стул с неприятным гнилостным запахом 1—3—5 раз в сутки и более. Почти одновременно или несколько позже появляются жалобы на вздутие живота, боль (постоянную или в виде приступов), локализующуюся преимущественно в правой подвздошной области. При дальнейшем прогрессировании заболевания в кале обнаруживают примесь стекловидной слизи, окрашенной кровью (типа "малинового желе"). Характер стула может меняться (появляется примесь гноя, если присоединяется вторичная бактериальная инфекция). В начальный период общетоксические явления (слабость, повышенная утомляемость) могут быть выражены незначительно или даже отсутствовать.
У ослабленных людей заболевание может начинаться остро, с повышения температуры до 37,5—38 °С, схваткообразной боли в животе, жидкого стула до 2—4 раз в сутки, в котором уже с первых дней обнаруживают примесь крови и слизи.
В особо тяжелых случаях, особенно у людей с выраженным иммунодефицитом, может возникать молниеносная форма, при которой симптоматика (бурное начало, высокая температура до 39—40 °С и выше, очень частый стул со слизью и кровью, сильная разлитая постоянная или схваткообразная боль в животе, резкая общая слабость) нарастает очень быстро, и заболевание может закончиться смертью уже через несколько дней.
Манифестная форма амебной дизентерии может иметь как непрерывно прогрессирующее, так и рецидивирующее течение.
При непрерывно прогрессирующем течении клинические проявления неуклонно нарастают (иногда очень быстро, иногда — постепенно), периоды ремиссий при этом отсутствуют. К нарастающему гемо-колитическому синдрому присоединяются общетоксический синдром (слабость, повышение температуры, снижение работоспособности), снижается масса тела, развивается гипохромная анемия. Часто выявляют увеличение печени неспецифического характера, но возможно возникновение амебных поражений различных органов, в том числе и печени. При таком течении надежда на самопроизвольное излечение невелика.
При рецидивирующем течении острые проявления болезни различной степени выраженности продолжаются 4—5 нед, после чего процесс постепенно затихает и наступает ремиссия длительностью от нескольких недель до нескольких месяцев. Дальнейшее течение болезни на протяжении многих лет характеризуется чередованием периодов обострений и ремиссий. Такое течение может при неблагоприятных
условиях (кишечная бактериальная инфекция, прием глюкокортико-стероидов, беременность) перейти в непрерывно прогрессирующее.
Ведущим клиническим проявлением непрерывно прогрессирующего амебиаза является гемоколит с постепенным распространением язвенного процесса на всю толстую кишку. Длительное течение сопровождается развитием анемии, интоксикационного синдрома, снижением питания, дисбактериозом, гипополивитаминозом, нарушением функции пищеварительных желез. Возможно формирование амебных абсцессов различной локализации.
Тяжесть течения определяется выраженностью гемоколитического синдрома и быстротой его прогрессирования, развитием интоксикационного синдрома, наличием и характером осложнений.
Внекишечный амебиаз. Амебный абсцесс печени чаще одиночный, формируется преимущественно в правой доле печени при проникновении амеб по v.portae из толстой кишки. Амебный абсцесс может появляться на фоне кишечного амебиаза или возникать у людей, которые отрицают у себя в различные периоды жизни проявления кишечного амебиаза, что, естественно, затрудняет его распознавание.
В зависимости от локализации, быстроты увеличения, размеров абсцесса находится клиническая симптоматика. Заболевание может проявляться постепенно (чаще) или остро.
Первые признаки при постепенном развитии болезни обычно носят неопределенный характер и не позволяют думать о генезе и даже локализации патологического процесса: появляются слабость, иногда — боль в надчревной области или правом подреберье, снижение аппетита, субфебрилитет. При внимательном обследовании иногда удается обнаружить несколько увеличенную печень. По мере прогрессирования заболевания клиника нарастает: боль может стать весьма интенсивной, усиливается при движении, перемене положения тела. При пальпации печень болезненна. При увеличении абсцесса в направлении диафрагмы появляются дополнительные симптомы, которые могут симулировать заболевания дыхательной системы: боль усиливается при дыхании, иррадиирует в правое плечо, при пальпации появляется боль в межреберных промежутках справа. Иногда определяют ограничение подвижности правого легкого за счет увеличения печени, а иногда и возникающего ателектаза.
При пункции абсцесса обычно удается получить густую, коричневого цвета («шоколадную») массу, образовавшуюся в результате некроза печеночной ткани. Бактериальная флора в таком содержимом обычно отсутствует, но амебы могут быть обнаружены в стенке абсцесса (при гистологическом исследовании удаленного абсцесса).
В амебные абсцессы может проникать бактериальная флора, в этом случае возникает гнойный процесс с типичной клиникой бактериального абсцесса печени: гектическая лихорадка, озноб, профузный пот, гиперлейкоцитоз, резко увеличенная СОЭ. Содержимое абсцесса в этом случае становится гнойным (желто-зеленого цвета, с неприятным запахом).
Желтуха, выраженные нарушения функции печени для амебного абсцесса, не осложненного вторичной бактериальной инфекцией, не характерны.
В отдельных случаях амебные абсцессы могут начинаться остро с высокой температуры, боли в животе, выраженных общетоксических реакций. Но так как это бывает преимущественно у резко ослабленных лиц, можно полагать, что первые признаки болезни у большинства из них маскируются другими симптомами, обусловленными общим ослаблением организма.
Амебные абсцессы легких могут возникать в результате гематогенной диссеминации амеб, прорыва в легкие абсцесса печени или заноса эмбола из печени. При этом возникает кашель, бывает одышка, затрудненное дыхание. В зависимости от локализации и величины абсцесса клиника может напоминать пневмонию или абсцесс легких бактериальной природы. При вскрытии абсцесса в бронх отхаркивается обильная темно-коричневая мокрота. Нередко присоединение вторичной инфекции осложняет течение амебного абсцесса легкого.
Амебный абсцесс мозга — редкая патология. Проникают амебы в мозг гематогенным путем. В зависимости от локализации и величины абсцесса находится неврологическая симптоматика.
Еще реже возникают абсцессы других органов (селезенки, почек, кожи).
Осложнения. При амебиазе могут возникать многочисленные осложнения, которые условно можно разделить на две группы. Первая группа — осложнения амебной дизентерии:
кишечные кровотечения, которые возникают в результате повреждения крупного сосуда при формировании язв;
периколит, развивающийся при наличии глубоких язв, достигающих серозной оболочки, на его фоне в свою очередь могут формироваться спаечная болезнь, кишечная непроходимость;
амебома, которая, вызывая сужение просвета кишки, тоже может быть причиной кишечной непроходимости;
перитонит (разлитой или отграниченный) вследствие перфорации стенки кишки на месте глубоких язв;
формирование хронического язвенного колита после перенесенного кишечного амебиаза;
образование длительно незаживающих язв и (или) кондилом в области наружных половых органов и (или) промежности;
формирование кишечно-мочеполовых свищей;
дисбактериоз;
анемия.
Вторая группа — осложнения внекишечного амебиаза (амебных абсцессов);
прорыв абсцесса печени в плевральную полость с появлением массивного выпота и последующим развитием ателектаза легкого;
прорыв абсцесса печени в брюшную полость с развитием перитонита;
при локализации абсцесса в левой доле печени возможен прорыв его в полость перикарда с развитием тампонады сердца;
вторичное инфицирование амебных абсцессов с формированием гнойного процесса.
При амебиазе различной локализации может развиваться кахексия, усугубляется иммунодефицит.
Исходы. Зависят от длительности заболевания, особенностей клинического течения, наличия и характера внекишечных проявлений, фоновых заболеваний. При своевременно начатом лечении возможно полное выздоровление. Значительно ухудшает прогноз присоединение бактериальной инфекции. При нелеченом амебиазе летальность составляет 5—10%, а при возникновении хирургических осложнений она может доходить до 50%.
Методы диагностики. Общеклинические методы. Изменения в общем анализе крови определяются формой болезни (кишечный или вне-кишечный амебиаз), наличием и характером осложнений, тяжестью течения.
При амебной дизентерии с непрерывно прогрессирующим течением возможно появление лейкоцитоза с палочкоядерным сдвигом, увеличенной СОЭ, возможна анемия (иногда значительная).
При амебных абсцессах значительнее выражены лейкоцитоз, нейтрофилез, резко увеличена СОЭ.
В моче особых изменений нет, за исключением случаев тяжелого течения амебных абсцессов, когда появляются признаки токсической нефропатии.
При копроскопии обнаруживают свежие эритроциты, эозинофилы, кристаллы Шарко—Лейдена и амебы.
Биохимические методы. Функция печени при всех вариантах течения амебиаза нарушена мало, поэтому такие показатели, как уровень билирубина, активность ферментов цитолиза, обычно остаются в пределах нормы. При тяжелом течении наблюдается уменьшение общего количества белка в сыворотке крови, возможно небольшое повышение активности АлАТ, АсАТ.
Специфическая диагностика. В распознавании амебиаза важнейшая роль принадлежит паразитологическим методам — выявление простейших, их идентификация. Производят исследования различными способами, каждый из них имеет свои достоинства и недостатки.
Протозооскопия нативных мазков из исследуемого материала — наиболее простой и доступный метод. При этом на предметных стеклах из исследуемого материала (фекалии, содержимое язв, взятое при ректороманоскопии) готовят 2 мазка. К одному из них добавляют каплю изотонического раствора натрия хлорида (в этом мазке можно выявить особенности структуры и движения обнаруженных амеб), к другому — каплю раствора Люголя (можно определить особенности строения цист). Мазки накрывают покровным стеклом и исследуют под микроскопом.
При применении этого метода очень важно, чтобы материал был свежим: он должен быть исследован не позднее чем через 15—25 мин после забора, поскольку вегетативные формы очень быстро теряют подвижность, округляются и даже подвергаются разрушению, что резко затрудняет их идентификацию. При невозможности произвести исследование через 15—25 мин материал можно поместить в специальный консервант (Барроуза, Турдыева и др.), где вегетативные формы длительное время сохраняются, хотя и в обездвиженном состоянии.
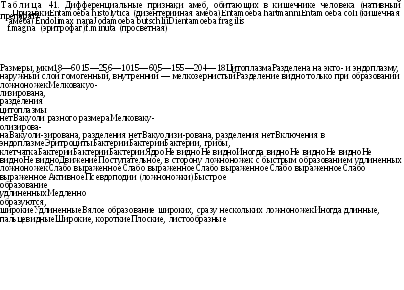
Паразитологическое исследование с идентификацией вегетативных форм и цист требует определенных навыков, поскольку в кишечнике человека могут обитать различные непатогенные амебы (5 видов). Дифференциально-диагностические признаки их (вегетативных форм и цист) представлены в табл. 41 и 42.
Протозооскопия мазков, окрашенных железным гематоксилином по Ганденгайну (постоянные препараты), хотя и является достаточно трудоемким методом, но позволяет сохранить особенности структуры ядра, оболочки и цитоплазмы амеб.
Культивирование амеб — дополнительный метод, чаще его используют при проведении научных исследований, для получения диагно-стикумов, применяемых для иммунодиагностики амебиаза. Для культивирования предложены среды, на которых выращивают простейших с бактериями (среды Павловой, Бека и др.) и без бактериальные (аксе-ничные). Этот метод не позволяет проводить дифференциальную диагностику между просветным и инвазивным амебиазом.
При наличии экспериментальной базы можно использовать биологической метод диагностики, основанный на ректальном заражении исследуемым материалом котят, кроликов, морских свинок и последующим выявлением возбудителя в кишечном содержимом этих животных.
Серологические методы особую ценность приобретают при наличии амебных абсцессов, особенно в тех случаях, когда кишечные проявления отсутствуют и паразитологические методы оказываются неинформативными. Высокочувствительна РИФ, которая ставится с диагности-кумом из культуры дизентерийной амебы, выращенной на аксеничных средах. Диагностический титр — не ниже 1:80, но обязательна постановка реакции в динамике. При амебных абсцессах РИФ положитель-
 на
почти в 100% случаев. Периоды обострений
и ремиссий сказываются на результатах
(высоте титров антител), что может
затруднять их интерпретацию. Наиболее
чувствительными считаются РЭМА и РНГА,
которые становятся положительными со
2—3-й недели болезни. Неин-вазивный
амебиаз не сопровождается появлением
специфических антител.
на
почти в 100% случаев. Периоды обострений
и ремиссий сказываются на результатах
(высоте титров антител), что может
затруднять их интерпретацию. Наиболее
чувствительными считаются РЭМА и РНГА,
которые становятся положительными со
2—3-й недели болезни. Неин-вазивный
амебиаз не сопровождается появлением
специфических антител.
Дополнительные методы диагностики. Ректороманоскопия — один из наиболее информативных методов распознавания амебной дизентерии. Характерным является наличие глубоких язв с подрытыми краями, располагающихся на неизмененной слизистой оболочке. При хроническом течении можно обнаружить язвы на разных стадиях развития — свежие, рубцующиеся. Однако следует помнить, что такая типичная картина в дистальном отделе кишечника (прямая и сигмовидная кишка) может отсутствовать даже при наличии явных клинических проявлений амебиаза, поскольку процесс может располагаться вне пределов досягаемости ректоскопа. Кроме того, в отдельных случаях при тяжелом течении и частых рецидивах процесс может носить диффузный характер, когда слизистая оболочка сплошь покрывается язвами, между которыми бывает трудно выявить непораженный участок, то же бывает при кишечной микст-патологии.
В распознавании амебных абсцессов любой локализации важную роль играют УЗИ, КТ, рентгенография (особенно при абсцессе печени, когда можно выявить выбухание в плевральную полость со стороны печени, при амебных поражениях легких), инфракрасная термография.
При амебном абсцессе печени иногда прибегают к его пункции, получение характерной густой вида шоколадного сиропа жидкости позволяет верифицировать диагноз, несмотря на отсутствие возбудителей. Но решиться на такую процедуру непросто, поскольку врач, производящий ее, должен быть уверен, что это не эхинококкоз, альвеококкоз, гнойный процесс. Гистологическому исследованию подвергают материал, взятый на границе абсцесса и здоровой ткани при операции, там можно обнаружить гистолитическую амебу.
Критерии диагноза. Думать о наличии у больного амебной дизентерии можно при наличии следующих признаков:
сооответствующий эпидемиологический анамнез (пребывание в регионах, эндемичных по амебиазу, и прежде всего в тропиках и субтропиках);
гемоколит с тенденцией к рецидивирующему течению;
несоответствие степени токсикоза выраженности гемоколитичес-кого синдрома, особенно в начальный период болезни (токсикоз выражен слабее, за исключением молниеносной формы);
локализация боли в правой подвздошной области;
отсутствие спазма сигмовидной кишки и тенезмов;
примесь слизи и крови в кале в виде «малинового желе»;
при ректороманоскопии выявляют глубокие язвы на неизмененной слизистой оболочке.
Диагноз, тем не менее, считается достоверным только при обнаружении гематофагов в фекалиях или содержимом язв, взятом при ректороманоскопии.
О возможности развития амебного абсцесса печени свидетельствуют:
пребывание в эндемичном по амебиазу регионе;
указание на наличие эпизода заболевания с типичной для амебной дизентерии клиникой (особую ценность этот признак приобретает, если амебная дизентерия была подтверждена выявлением эритро-фагов);
боль в правом подреберье различной интенсивности;
увеличение правой (преимущественно) доли печени;
преимущественное распространение абсцесса по мере его роста в сторону диафрагмы, деформация купола диафрагмы (вдавление) при наличии крупного абсцесса;
относительно удовлетворительное состояние больного, если не наступает осложнение (прорыв абсцесса, его инфицирование бактериальной флорой);
характерный вид пунктата («шоколадный сироп»).
Диагноз подтверждают главным образом серологическими методами.
Дифференциальный диагноз. Дифференциальная диагностика при амебиазе затруднена тем, что клиническая симптоматика определяется локализацией патологического процесса, длительностью и тяжестью течения заболевания, наличием и характером осложнений. Все это делает клинические проявления пестрыми, полиморфными, не отличающимися высокой степенью специфичности. Именно поэтому в неэндемичных регионах амебиаз прижизненно диагностируют редко, особенно относительно благоприятно протекающие формы. Частое сочетание с кишечными инфекциями и паразитозами еще больше затрудняет выявление больных амебиазом.
Начальные проявления кишечного амебиаза у большинства больных, особенно в неэндемичных регионах, не слишком их беспокоят, тем более, что интоксикация д\ительное время может отсутствовать, а боль сначала бывает весьма умеренной (исключение — молниеносные формы).
Появляющаяся в дальнейшем более упорная боль, иногда даже с те-незмами (при тотальном поражении кишечника), наличие слизи и крови в кале заставляют думать прежде всего о шигеллезе. Отличают шигеллез:
преимущественно острое начало;
наличие интоксикационного синдрома, коррелирующего с тяжестью течения и выраженностью диарейного синдрома с первых дней;
локализация боли, чаще схваткообразной, в левой подвздошной области; с первых же дней болезни нередко появляются тенезмы;
выявляемый с первых дней спазм сигмовидной кишки;
слизь в кале содержит эритроциты и лейкоциты (нейтрофилы) в большом количестве, за счет чего она становится мутной, непрозрачной;
при ректороманоскопии выявляют резкий спазм сигмовидной кишки, множественные геморрагии, эрозии, поверхностные язвы на диффузно гиперемированной отечной слизистой оболочке;
— преимущественно острое течение, даже без лечения симптомы заболевания постепенно стихают, хронизации не наступает.
Однако возможность сочетания амебной дизентерии и шигеллеза с появлением дополнительных симптомов, присущих шигеллезу, требует от врача особого внимания при сборе анамнеза, когда уточняется очередность появления отдельных симптомов, их выраженность и т.д.
Протозоологические исследования необходимо сочетать с бактериологическими всегда, когда имеются клинические признаки дистального колита.
С рецидивирующим течением и гемоколитом может протекать ба-лантидиаз — протозойное заболевание, вызываемое инфузорией Ва-lantidium coli. При проведении дифференциальной диагностики с этим протозоозом следует учитывать такие особенности балантидиаза:
человек заражается преимущественно от свиней, что определяет эпидемиологические особенности болезни;
для клинически выраженных форм характерна интоксикация, коррелирующая с тяжестью течения и выраженностью синдрома гемоколита;
— стул жидкий, обильный с примесью слизи, крови, гноя;
— при ректороманоскопии обнаруживают диффузное поражение кишки, отек слизистой оболочки с фибринозными налетами;
— в кишечном содержимом выявляют балантидии.
С синдромом гемоколита протекает кишечный шистосомоз, вызываемый тропическим гельминтом Schistosoma mansoni. Зоны распространения этого гельминтоза и амебиаза сходны. Отличия кишечного шистосомоза:
кишечной стадии предшествует период аллергических и общетоксических реакций длительностью до 1,5—2 мес;
возникающий в стадии развившейся инвазии гемоколит сопровождается интоксикацией, чередованием запоров и поносов, похуданием;
при ректороманоскопии выявляют диффузную гиперемию и отек слизистой оболочки кишки, язвы, полипы, свищи;
лейкоцитоз с эозинофилией;
в фекалиях обнаруживают яйца шистосом.
Боль в животе, периодические послабления стула, кровь в кале, главным образом выявляемая при его микроскопии, требуют иногда проведения дифференциального диагноза и с другими гельминтозами (трихоцефалез, гименолепидоз, стронгилоидоз и др.). Решают вопрос паразитологические исследования (гельминтологические и протозоологические). Всегда следует помнить о частом сочетании амебиаза с гельминтозами.
При рецидивирующей амебной дизентерии возникают симптомы, аналогичные неспецифическому язвенному колиту (чередование периодов обострений и ремиссий, похудание, наличие интоксикационного синдрома, гемоколит). Основные отличия неспецифического язвенного колита:
— отсутствие эпидемиологического анамнеза, свойственного аме-биазу;
— рано развивающийся интоксикационный синдром;
уже с самого начала стул приобретает характерный вид мясных помоев;
при ректороманоскопии находят диффузное эрозивно-геморра-гическое поражение слизистой оболочки кишки, отчетливую контактную ее кровоточивость;
при ирригоскопии выявляют потерю гаустрации и зазубренность контуров слизистой оболочки кишки, симптом «медовых сот».
Но неспецифический язвенный колит может сочетаться с амебной дизентерией или быть ее последствием.
Гемоколитом могут сопровождаться опухоли кишечника, при которых клиническая картина (боль, выраженность гемоколита, интоксикации) будет зависеть от размера опухоли, ее локализации, стадии роста. В этих случаях вопрос о диагнозе решается на основании комплексного исследования — ректороманоскопия, ирригоскопия, паразитологи-ческие методы. Не характерно для опухолей наличие в кале слизи, имеющей вид "малинового желе".
Определенные трудности возникают при проведении дифференциальной диагностики между амебным абсцессом печени и такими заболеваниями, как эхинококкоз печени, гепатокарцинома, бактериальный абсцесс печени.
Как и амебный абсцесс печени, эхинококковая киста располагается преимущественно в правой доле, хотя чаще, чем при амебном поражении, бывает и другая локализация; развивается эхинококк тоже постепенно, его рост тоже может сопровождаться болью в правой половине грудной клетки. Тем не менее, существуют некоторые различия, на которые следует обращать внимание при сборе анамнеза и обследовании больного. Так, эхинококковую кисту помогают распознать:
— профессиональный анамнез (чаще болеют люди, деятельность которых связана с животноводством);
—в период ранних проявлений (миграция гельминта) возможно возникновение общетоксических и аллергических реакций (слабость, недомогание, повышение температуры, кожный зуд и даже зудящие ур-тикарные высыпания). Так как от момента этих проявлений до формирования эхинококкового пузыря могут проходить месяцы и даже годы, больной успевает забыть о таком эпизоде, поэтому при сборе анамнеза врач должен проявить особое внимание;
— при локализации пузыря в области ворот печени возможна желтуха;
— нередко выявляется значительная эозинофилия в крови;
округлая эхинококковая тень может быть окружена кольцом обызвествления (эти особенности помогает установить УЗИ);
положительная внутрикожная проба (реакция Каццони), но при ее оценке нужно помнить о возможности ложноположительных результатов;
— отрицательные РИФ и РНГА с амебными диагностикумами. При малейшем подозрении на эхинококкоз от пункции пузыря необходимо отказаться из-за возможности диссеминации паразита.
Гепатокарциному от амебного абсцесса отличают:
быстрый рост;
нередко неправильная форма; наличие метастазов;
— отрицательные серологические реакции с амебным диагностику-мом.
Существенную помощь оказывают КТ, УЗИ, позволяющие уточнить особенности структуры и плотности опухолевидного образования. Для бактериальных абсцессов в отличие от амебных характерны:
— рано возникающие признаки общей интоксикации (слабость, высокая лихорадка, нередко гектического типа, пот);
гиперлейкоцитоз, резко увеличенная СОЭ;
быстро прогрессирующие явления интоксикации, кахексия;
в пунктатах — густое желто-зеленое зловонное содержимое;
— серологические реакции с амебным диагостикумом отрицательные.
Однако возможно проникновение бактериальной инфекции в уже сформировавшийся амебный абсцесс с дальнейшим развитием гнойного процесса в нем. В этом случае на фоне клиники такого абсцесса могут быть положительными серологические реакции с амебными диагностикумами, а при гистологическом исследовании иногда обнаруживают амебы.
При амебных абсцессах легкого приходится проводить дифференциальный диагноз с теми же заболеваниями, что и при абсцессах печени. Нередко абсцессы легкого и печени сочетаются. Определенные сложности могут возникнуть при локализации абсцесса в верхней доле легкого, в этом случае проводится дифференциальный диагноз с туберкулезом (кавернозным). Существенную помощь может оказать выявле: ние микобактерий туберкулеза в мокроте, положительная проба с туберкулином, отрицательные серологические реакции с амебным диаг-ностикумом.
Лечение. Лечение больных всеми формами амебиаза следует проводить в стационаре, учитывая возможность возникновения побочных реакций, необходимость проведения контроля за эффективностью лечения (паразитоскопия фекалий, ректороманоскопия).
Во время лечения, особенно при наличии кишечных проявлений, назначают щадящую легкоусвояемую диету с ограничением грубой клетчатки и углеводов, богатую витаминами, животными белками. Пищу принимают небольшими порциями 5—6 раз в день.
Этиотропная терапия. Все препараты, применяемые для этиотроп-ного лечения амебиаза, можно разделить на три группы.
Первая группа — амебоциды (противоамебные препараты) прямого действия (контактные амебоциды). Они действуют преимущественно на просветные формы амеб (вегетативные формы и цисты), поэтому их применяют главным образом для санации носителей.
Наиболее часто применяемым препаратом этой группы является ят-рен (хиниофон), содержащий 25—26% йода. Назначают его по 0,5 г 3 раза в сутки. Курс лечения — 10 дней. При необходимости курс может быть повторен через 10—12 дней.
Эффективен также дийодохин (назначают по 0,25 г 3—4 раза в сутки в течение 10 дней).
Изучается эффективность и возможность применения таких зарубежных препаратов, как йодохинол и дилоксанида фуроат.
Вторая группа — амебоциды тканевые, способные проникать в кишечную стенку, печень. Они не действуют на просветные формы.
Эметина гидрохлорид широко применяют при остром амебиазе, при котором он наиболее эффективен (значительно меньше — при затяжном и хроническом, когда усиливается местный воспалительный процесс). Назначают его внутримышечно в виде 1% раствора по 1,5 мл 2 раза в сутки (максимальная суточная доза не более 60 мг), курс лечения — 7—10 дней. Препарат достаточно токсичен, описаны случаи смерти от токсического миокардита, развивающегося во время лечения, поэтому перед его назначением нужно внимательно еще раз перечитать инструкцию (собственно, это относится ко всем противоамеб-ным препаратам). При лечении эметином быстро формируются эмети-ноустойчивые формы амеб, что приводит к неэффективности повторных курсов и при лечении больных хроническим амебиазом.
Эффективность лечения повышается, если эметин назначают в комбинации с ятреном или ятрен назначают в промежутках между циклами эметинотерапии (таких циклов при хорошей переносимости и под наблюдением врача может быть 2 с интервалом 7—10 дней).
Более эффективен дегидроэметин, производное эметина. Дозы и схемы лечения такие же, как и эметина гидрохлорида.
Хлорохин (делагил, резохин) обладает способностью накапливаться в печени, чем и обусловлена наибольшая эффективность его при амебных абсцессах печени. Но это же свойство может вызвать токсическое поражение печени, что следует учитывать при назначении препарата. Имеет много противопоказаний. Существуют различные схемы назначения хлорохина, наиболее часто суточная доза составляет 0,3—0,45 г (по 0,15 г 2—3 раза в сутки) в течение 2—3 нед. Иногда хлорохин сочетают с эметином или препараты назначают поочередно.
Третья группа — амебоциды универсального действия. Главным препаратом этой группы является метронидазол (флагил, трихопол), действующий на все формы амеб при любой их локализации.
При амебной дизентерии препарат назначают по 0,5—0,75 г 3 раза в сутки в течение 5—10 дней. При амебных абсцессах доза может быть несколько уменьшена с учетом способности препарата концентрироваться в печени. Существовавшее ранее мнение о низкой токсичности и безопасности препарата пересматривается: получены сведения о его канцерогенном и тератогенном действии.
Достаточно эффективен и другой универсальный амебоцид — ти-нидазол (фасижин). При кишечном амебиазе его назначают в суточной дозе 1,2 г (курс лечения 5—10 дней), при амебном абсцессе печени можно увеличивать суточную дозу до 1,5—2 г, однако курс лечения при этом сокращают до 3—5 дней.
При лечении амебиаза любой локализации амебоциды нередко сочетают с антибактериальными препаратами с учетом часто возникающего отягощающего влияния на течение амебиаза микробной флоры. Чаще других применяют антибиотики тетрациклинового ряда, сульфаниламиды, энтеросептол. Имеются сведения о том, что тетрациклин и сам способен действовать на вегетативные формы и цисты амеб, вызывая в них дегенеративные изменения, в результате чего действие аме-боцидов усиливается.
Очередность назначения всех вышеперечисленных препаратов, их возможные комбинации определяются периодом болезни, локализацией патологического процесса, наличием и характером фоновых заболеваний, а также степенью риска возникновения осложнений, связанных с лечением. Нередко при лечении внепеченочного амебиаза консервативная терапия бывает эффективной. Но иногда приходится прибегать и к оперативному лечению.
Патогенетическая терапия. Объем и характер ее зависят от состояния больного к моменту начала лечения. Обычно необходимость в назначении дополнительных средств (кроме этиотропных) возникает при длительном рецидивирующем течении амебиаза, сопровождающемся похуданием, полигиповитаминозом, дефицитом белков, ферментативной недостаточностью, дисбактериозом и др.
В этих случаях показано переливание альбумина, назначение различных витаминов, препаратов железа. Для улучшения переваривания пищи назначают ферментные препараты (панкреатин, панзинорм, фе-стал), для нормализации кишечной флоры — бифидумбактерин, коли-бактерин и др.
Если амебиаз сочетается с гельминтозом, до начала противоамебно-го лечения проводят дегельминтизацию. Если приходится лечить резко ослабленного больного, сначала показана общеукрепляющая терапия. Так как глюкокортикостероиды значительно отягощают течение аме
биаза, от них отказываются во всех ситуациях, более того, если больной получает курс лечения глюкокортикостероидами в связи с каким-либо заболеванием, его прерывают при малейшей возможности.
При наличии проктита, сигмоидита можно назначить клизмы с ромашкой, таннином, галаскорбином.
Спазмолитики, болеутоляющие средства следует применять с осторожностью, чтобы не пропустить такие серьезные осложнения, как перфорация, перитонит.
Лечение при амебиазе может быть длительным, до 1,5—2 мес, что требует терпения как от больного, так и от врача.
Правила выписки из стационара. Основанием для выписки рекон-валесцента является клиническое выздоровление и отрицательные результаты паразитоскопии. В ближайшие 1,5—2 мес паразитологиче-ские исследования неоднократно повторяют, так как возможны рецидивы.
Профилактика. Характер общих профилактических мероприятий при амебиазе соответствует таковым при всех кишечных инфекциях. Важная роль принадлежит выявлению бессимптомных амебоносите-лей среди представителей декретированных групп населения. При их выявлении проводят санацию амебоцидами прямого действия. Основные меры профилактики связаны с недопущением загрязнения воды и пищевых продуктов цистами дизентерийной амебы.
Специфическая профилактика не разработана.
лямблиоз
Лямблиоз — протозойное заболевание с фекально-оральным механизмом передачи, вызываемое лямблиями, для которого характерны как бессимптомное течение, так и манифестные формы, в клинике которых преобладают аллергические, токсические и диспепсические проявления (лат. — fambfiosis, англ. — giardiasis).
Краткие исторические сведения. Возбудитель лямблиоза впервые обнаружил в кишечном содержимом детей, страдавших диареей, профессор Харьковского университета Д.Ф.Лямбль в 1859 г. Он же описал строение, форму, размеры, особенности движения паразита, которому дал название Cereomonas intestinalis. В 1888 г. французский ученый Blanchard предложил назвать обнаруженные Д.Ф.Лямблем простейшие в его честь — Lamblia intestinalis. В зарубежной литературе встречается также термин Giardia intestinalis.
Актуальность. Комитет экспертов ВОЗ (1988 г.) считает лямблиоз эндемичным заболеванием для многих стран мира, в которых периодически наблюдаются «спорадические эпидемии болезни». Подсчитано, что в Африке, Азии и Латинской Америке число инвазированных достигает 200 млн человек. Хотя у большинства лиц инвазия протекает бессимптомно, тем не менее клинические проявления лямблиоза ежегодно выявляются у 500 ООО инвазированных. В развивающихся странах лямблиоз является одной из основных причин острой или упорной диареи. В США и Великобритании лямблиоз — одна из наиболее часто регистрируемых кишечных инвазий человека.
В Украине количество инвазированных лямблиями взрослых составляет примерно 10 %; среди детей, особенно младшего возраста, оно достигает 30—40 %, а в некоторых закрытых детских коллективах — 70 %.
Этиология. Возбудитель — Lamblia intestinalis — относится к Protozoa, классу жгутиконосцев. Жизненный цикл лямблии состоит из двух стадий (форм) — вегетативной и цистной.
Вегетативная стадия лямблий (трофозоит) имеет грушевидную форму (в профиль — серповидную), длину 10—18 мкм, ширину 8—15 мкм. Тело ее состоит из гомогенной цитоплазмы, покрытой оболочкой. В передней части тела имеется два овальных ядра. По продольной оси лямблий расположен аксостиль — упругая трубка, которая делит тело на две симметричные части. На вентральной поверхности тела имеется присасывательный диск, при помощи которого паразит крепится к щеточной кайме слизистой оболочки кишки.
Лямблии имеют 4 пары жгутиков, обеспечивающих их активную под-
вижность (передняя, средняя, вентральная и хвостовая пары). Предполагается также, что центральные жгутики являются насосом, откачивающим пищевые вещества из зоны микроворсинок. Лямблии не имеют ротового и анального отверстий, питание их осуществляется всей поверхностью тела (эндоосмотически). Этим же путем идет выделение продуктов метаболизма. Особенности питания лямблий обусловливают их избирательную локализацию в организме человека — верхние отделы тонкой кишки (двенадцатиперстная кишка, начальный отдел тощей кишки), где идет расщепление пищевых продуктов до усвояемых организмом форм и таким образом создаются наиболее благоприятные условия для питания и размножения лямблий. Особенно активно лямблии усваивают расщепленные белковые продукты, витамины.
Размножаются лямблии путем простого продольного деления. Длительность жизни вегетативных форм — 30—40 дней.
Вегетативные формы лямблий неустойчивы во внешней среде, где они быстро разрушаются. Кипячение, дезинфицирующие вещества, соляная кислота мгновенно уничтожают их.
Находящиеся в просвете тонкой кишки лямблии с кишечным содержимым продвигаются в дистальные отделы кишечника, попадая таким образом в неблагоприятные для них условия существования. При этом отдельные особи округляются, теряют подвижность и превращаются в цисты.
Цисты лямблий имеют овальную форму, длину 12—14 мкм. Раствором Люголя они окрашиваются в коричневый или желтый цвет. Передний конец цисты более узкий по сравнению с задним. У переднего конца цисты раположены слабоконтурированные ядра — два в незрелых цистах и четыре в зрелых. Внутри цитоплазмы определяются тонкие нити аксонем и жгутики, а также парабазальные тела. Внутренняя структура цист более отчетливо видна в препаратах, окрашенных железным гематоксилином.
Цисты лямблий устойчивы во внешней среде. В воде могут сохранять жизнеспособность до 5 нед, в почве — до 3 мес. Они устойчивы к действию желчи, соляной кислоты желудочного сока, большинству дезинфицирующих растворов; 5% раствор хлорной извести не оказывает заметного губительного действия на цисты лямблий.
Культивирование лямблий очень трудоемкий процесс. Оно осуществляется посевом дуоденального содержимого с трофозоитами на среду А.Е.Карапетяна или ее модификации.
Особенности антигенной структуры лямблий еще изучаются. Основной иммуноген связан с поверхностными структурами лямблий и имеет гликопротеиновую природу. В цистах обнаружен специфический антиген GSA-65, на основе которого созданы некоторые тест-системы для диагностики лямблиоза.
Эпидемиология. Источником инвазии при лямблиозе является человек (больной или носитель), выделяющий с испражнениями цисты лямблий (за сутки несколько миллиардов экземпляров). Заражение вегетативными формами невозможно, учитывая их быструю гибель во внешней среде.
Основным источником инфекции являются дети, показатель инва-зированности у них в 2—3 раза превышает таковой у взрослых. В последнее время установлено, что лямблии могут паразитировать в кишечнике обезьян и свиней.
Механизм передачи при лямблиозе, как и при всех кишечных инфекциях, фекально-оральный. Основными факторами передачи являются вода и пищевые продукты, обсемененные цистами и не прошедшие термической обработки перед употреблением. Способствуют распространению цист лямблий мухи, тараканы, заражение может происходить контактно-бытовым путем (грязные руки, предметы домашнего обихода).
Несмотря на высокую степень зараженности лямблиями населения земного шара (до 10 % взрослые и 20 % и более дети), клинические проявления инвазии встречаются значительно реже, что связывают с относительной резистентностью человека к этой инвазии. Вероятность заболеть лямблиозом при попадании цист в организм зависит от ряда факторов: заражающей дозы, возраста инвазированных, наличия других кишечных инфекций и хронических дисфункций, приводящих к нарушению полостного и пристеночного пищеварения, состояния питания и иммунной системы инвазированных и др.
Заболеваемость лямблиозом чаще всего носит спорадический характер. Имеются данные об эпидемических вспышках лямблиоза, обусловленных попаданием сточных вод в питьевую воду (водные вспышки). Наиболее восприимчивы к инвазии дети первых лет жизни. Количество инвазированных в детских коллективах может достигать 50—80 %, но у большинства из них инвазия протекает бессимптомно. С возрастом число инвазированных еще более снижается и к 16—17 годам достигает уровня обычного для взрослых (10—15 %). Снижение числа инвазированных с возрастом объясняют не только уменьшением вероятности заражения в результате приобретения элементарных гигиенических навыков, но и формированием специфического иммунитета. Наиболее убедительным доводом в пользу этого является тот факт, что в регионах, где инвазированность лямблиями особенно высока, клинические проявления у местных жителей встречаются значительно реже, чем у приезжих, впервые «встретившихся» с лямблиями. Не случайно лямблии признаются одним из основных возбудителей «диареи путешественников». Имеются сведения о более высокой чувствительности к лямблиозу детей и взрослых с группой крови А(П).
Наиболее интенсивное распространение лямблий происходит в странах с жарким климатом. В нашей стране показатели инвазированности населения более высокие в южных регионах по сравнению с северными. Во всех регионах существенное влияние на уровень инвази-рованности оказывают неблагоприятные санитарно-гигиенические условия, социальные факторы, особенности питания.
В экспериментальных условиях лабораторных животных заразить лямблиями человека удавалось, но доказано, что какой-либо значительной роли в эпидемическом процессе они не играют. Лямблии животных для человека не патогенны.
Классификация. Как и при многих других инфекционных заболеваниях, обилие классификаций лямблиоза отражает недостаточное знание патогенеза заболевания, а также индивидуальную позицию авторов в отношении степени патогенности лямблий, способности их проникать за пределы кишечника, оказывать специфическое действие на различные органы и системы.
Как известно, лямблии обитают в двенадцатиперстной кишке и верхних отделах тощей кишки. Ни в желудке, ни в желчевыводящих путях, ни в печени, ни в дистальных отделах кишечника они выживать и размножаться не могут. Не доказана способность лямблий распространяться гематогенным путем в другие органы (сердце, печень, мозг). Лямблии не вырабатывают токсических субстанций типа экзо- или эндотоксина, которые могли бы оказывать специфическое действие на определенные органы-мишени. Все это ставит под сомнение целесообразность выделения некоторыми авторами таких форм, как лямблиозный миокардит, лямблиозный холецистит и т.д.
Вряд ли можно согласиться и с термином «лямблионосительство», поскольку особенность жизни и питания лямблий в кишечнике человека (см. далее патогенез) не может не вызвать ответной реакции организма инвазированного человека. Поэтому мы считаем наиболее удачной простую клиническую классификацию лямблиоза А.М.Семенова (1959), который выделяет:
1. Лямблиоз без клинических проявлений (латентный лямблиоз).
2. Лямблиоз с клиническими проявлениями (манифестный лямбли- оз). В этом случае особенности клинических проявлений можно дета- лизировать (дискинезия желчевыводящих путей, энтероколит).
Обычно при постановке диагноза избегают уточнять остроту процесса, его давность, особенно при впервые выявленном лямблиозе, поскольку установить сроки заражения обычно не удается, да и нужно доказать еще, является лямблиоз в каждом конкретном случае изолированным заболеванием или протекает по типу микст-патологии. Это же относится и к оценке тяжести течения лямблиоза, поскольку тяжесть состояния больного нередко бывает обусловлена сопутствующими заболеваниями (иммунодефицит, вторичная инфекция, хронические болезни дигестивной системы и др.).
Примерная формулировка диагноза. 1. Латентный лямблиоз.
Манифестный лямблиоз (энтероколит).
Манифестный лямблиоз (энтероколит, аллергический дерматит). Патогенез. В патогенезе лямблиоза до настоящего времени еще не
все изучено, много спорных вопросов. Отсутствует единое мнение о степени патогенности лямблий (в том числе зависимость ее от штаммов), о том, как трактовать так называемое лямблионосительство. Сам характер жизнедеятельности лямблий предопределяет какую-то степень взаимодействия с организмом человека в любом случае, при этом не всегда качественные изменения, происходящие при клинически бессимптомном паразитировании лямблий, переходят в количественные (манифестный лямблиоз).
Заражение человека происходит при заглатывании цист лямблий. Если в желудок попадают трофозоиты, они погибают под действием соляной кислоты желудочного сока. Цисты же кислотоустойчивы, желудочный барьер в большинстве случаев они проходят беспрепятственно. Носительство или даже заболевание может возникнуть при попадании в кишечник 20—100 цист.
Эксцистирование происходит в двенадцатиперстной и тощей кишках, здесь же идет их размножение, накопление, так как здесь — основная среда их обитания. Лямблии не имеют собственных ферментов и приспособлены к существованию в условиях пристеночного пищеварения тощей кишки. Вегетативные формы крепятся к поверхности щеточной каймы при помощи присасывательного диска таким образом, что между телом лямблии и стенкой кишки образуется замкнутая полость, в которой находятся конечные продукты гидролиза пищевых веществ, готовые к всасыванию. При помощи центральных жгутиков идет отсасывание пищевых веществ на дорзальную поверхность тела, где они усваиваются путем пиноцитоза.
Размножение лямблий в кишечнике и накопление их до такого количества, которое может привести к нарушению функции тонкой кишки и других органов, происходит при наличии условий, которые имеются не у всех зараженных. Они определяются в значительной мере функциональным состоянием пристеночного и полостного пищеварения, состоянием местного иммунитета, характером питания, составом кишечной микрофлоры и др. Дефицит секреторного IgA, нередко генетически детерминированный, является важным фактором, способствующим развитию манифестного лямблиоза.
При больших заражающих дозах дисфункция тонкой кишки может развиваться сразу после эксцистирования лямблий. В других случах проходит довольно длительное время (до нескольких месяцев) от момента заражения до клинических проявлений болезни. Иногда клинические проявления могут и не развиться, несмотря на длительное выделение цист таким здоровым лямблионосителем.
Обитание лямблий в тонкой кишке сопровождается комплексом взаимодействий между макро- и микроорганизмом:
в результате прикрепления лямблий к слизистой оболочке наступает местная травматизация тканей, тем более выраженная, чем массивнее заражение (в эксперименте показано, что на 1 см2 слизистой оболочки может располагаться до 1 млн лямблий). При исследовании биоптата обнаруживают морфологические изменения — уплощение ворсинок, расширение крипт, гиперплазию лимфоидной ткани, клеточную инфильтрацию слизистого и подслизистого слоев кишки макрофагами и лимфоцитами. Иногда в этих слоях даже удается обнаружить трофозоитов;
при лямблиозе нарушаются процессы всасывания питательных веществ и витаминов в тонкой кишке в результате многих факторов: уменьшение всасывающей поверхности в результате заселения ее лямблиями, снижение активности пищеварительных ферментов в дуоденальном содержимом, более быстрое прохождение пищевых масс по кишечнику в результате усиления его перистальтики, возникающего вследствие раздражения интерорецепторов, и т.д. Особенно заметным бывает нарушение всасывания жиров и глюкозы;
нарушение питания, которое может наступить в результате потребления лямблиями различных питательных веществ и витаминов, поступающих в организм человека с пищей;
на фоне лямблиоза нередко изменяется микробный пейзаж кишечника, формируется дисбактериоз, что способствует более активному размножению лямблий; снижение местной реактивности в кишечнике как результат жизнедеятельности лямблий может способствовать активации патогенной микрофлоры, а также утяжеляет течение многих кишечных инфекций и инвазий;
продукты жизнедеятельности лямблий, всасываясь в кровяное русло, оказывают общетоксическое действие; при этом местом приложения действия этих продуктов могут быть ЦНС, сердце (главным образом сосуды сердца), желудок (с последующим нарушением его секреции); в результате токсического действия продуктов жизнедеятельности лямблий на систему кроветворения, а также дефицита витаминов может развиваться анемия;
в результате раздражения интерорецепторов тонкой кишки не только усиливается моторика кишечника, но и может рефлекторно возникать дискинезия желчевыводящих путей. При этом на фоне снижения кислотности желудочного сока, застоя в желчном пузыре создаются благоприятные условия для проникновения инфекции в желчные пути с развитием в дальнейшем холецистита, холангита. Не подтверждается мнение о возможности развития лямблиозного холецистита, холангита, поскольку концентрированная желчь оказывает выраженное бактерицидное действие; к тому же для лямблий, очень требовательных к пищевому рациону, весьма неподходящей является среда обитания, практически лишенная питательных веществ, а именно такая создается в желчевыводящих путях. Не доказана и возможность прямого повреждающего действия лямблий на печень;
при дискинезии желчевыводящих путей может повышаться давление в вирсунговом протоке, что на фоне повышения протеолитичес-кой активности приводит к повреждению поджелудочной железы, развитию панкреатита;
продукты жизнедеятельности лямблий и распада погибших особей обладают свойствами аллергенов, вызывая сенсибилизацию организма, следствием чего могут быть реакции типа крапивницы, астматического синдрома, артралгии и др.;
раздражение и повреждение слизистой оболочки кишки сопровождается выделением эндогенных факторов воспаления (гистамин, се-ротонин и др.).
Таким образом, характер клинических симптомов, их выраженность будут определяться комплексом вышеописанных факторов. До тех пор пока срабатывают компенсаторно-адаптационные механизмы человеческого организма, клинические проявления могут отсутствовать, хотя при серологических исследованиях в ряде случаев удается обнаружить специфические антитела против лямблий.
На фоне лямблиоза формируется гуморальный и клеточный иммунитет. В сыворотке крови больных обнаруживают антитела класса IgM, реконвалесцентов — IgG. Повышение уровня Ig выявлено и в биоптатах слизистой оболочки тонкой кишки. Антитела повышают резистентность кишечника к лямблиям, в связи с чем уменьшается выраженность клинических проявлений, особенно у лиц, проживающих в эндемичных по лямблиозу регионах, где они постоянно подвергаются возможности ре- и суперинфицирования.
Клиника. Лямблиоз с клиническими проявлениями составляет около 10 % от общего количества инвазированных. Длительность инкубационного периода очень неопределенна, иногда у человека в течение многих месяцев и даже лет могут обнаруживаться простейшие, а клинические проявления отсутствуют.
Начало заболевания обычно постепенное. Трудно назвать еще какое-либо заболевание, при котором наблюдался бы такой полиморфизм клинических проявлений, носящих неспецифический характер, как при лямблиозе. Нет, казалось бы, ни одной системы и органа, которые в той или иной степени не реагировали бы на инвазию. При этом в каждом отдельном случае клиника заболевания определяется комплексом индивидуальных патологических реакций, которые возникают в пораженном организме. У некоторых больных первыми проявлениями заболевания могут быть поражения пищеварительного тракта:
— гастрит, дуоденит, которые характеризуются появлением тяжести, а затем и боли в надчревной области различной интенсивности, они могут быть связаны с приемом пищи или не зависеть от нее. Нередко больные жалуются на отрыжку, изжогу. При прогрессировании процесса может периодически возникать рвота после еды. Все эти явления нередко полностью проходят после лечения;
энтерит — один из наиболее постоянных симптомов. При этом возникает боль в верхних отделах живота различной интенсивности, периодически — послабление стула до 3—5 раз в сутки. Стул чаще водянистый, без запаха, без патологических примесей. В отдельных случаях возможен очень частый, изнуряющий стул, но такие явления скорее можно считать исключением;
колит развивается при длительном паразитировании лямблий, нарушении состава кишечной микрофлоры, дисбактериозе. Больные жалуются на вздутие живота, урчание в кишечнике. У некоторых появляются схваткообразная боль внизу живота и даже слизь и кровь в кале.
На фоне этих симптомов поражения пищеварительного тракта, обусловленных нарушением процессов усвоения пищевых продуктов и авитаминозом, возможна значительная потеря массы тела вплоть до тяжелой кахексии.
При лямблиозе могут выявляться признаки дискинезии желчевыводящих путей, холангита, холецистита, панкреатита. Во всех этих случаях симптомы носят также неспецифический характер: появляется боль в надчревной области, в зоне проекции желчного пузыря, поджелудочной железы; боль может иррадиировать в поясницу или носить опоясывающий характер (при панкреатите), она может сочетаться с послаблением стула. В нарушении функции этих органов важная роль принадлежит не лямблиям, а вторичной микрофлоре.
У некоторых больных выявляют небольшое увеличение печени и даже легкую иктеричность, но функция печени при этом не нарушается.
Токсические и аллергические реакции, обусловленные главным образом действием продуктов жизнедеятельности лямблий, всосавшихся в кровь, могут иметь такие проявления:
повышение температуры тела (чаще бывает субфебрильной, реже — выше 38 °С);
аллергическая сыпь, артралгии; иногда формируются аллергические неспецифические реакции на различные пищевые продукты, медикаменты;
поражение нервной системы (слабость, повышенная утомляемость, нарушение ритма сна, головокружение). Иногда эти проявления расцениваются как вегетативно-сосудистая дистония, неврастения, астения. Описывают даже судорожные припадки, психозы;
может возникать миокардит (при этом выявляют приглушение сердечных тонов, тахикардию, больные отмечают неприятные ощущения в области сердца). Иногда бывает лабильность пульса, значительные перепады артериального давления;
имеются сведения о возможности поражения эндокринных желез — снижение функции щитовидной железы (гипотиреоз), надпочечников (уменьшение количества глюкокортикостероидов);
система кроветворения обычно страдает мало, но возможны различные токсические реакции, вплоть до выраженной анемии и даже панцитопении. При этом усиливается тахикардия, даже при небольшой нагрузке появляется одышка.
Как видно из изложенного, симптоматика лямблиоза черезвычайно пестра, комплекс клинических проявлений у каждого больного «свой», в значительной мере он будет определяться преморбидным состоянием организма, наличием и характером сопутствующих заболеваний, роль которых особенно велика. До сих пор ведутся споры о том, что первично и что вторично при лямблиозе: способствуют имеющиеся хронические заболевания (прежде всего дигестивной системы) активации лямблий или лямблиоз приводит к формированию вторичных нарушений в различных органах.
Лямблиоз (латентный и манифестный) может сочетаться с другими кишечными инфекциями (шигеллезом, брюшным тифом, сальмонелле-зом и др.), способствуя их затяжному и более тяжелому течению, изменяя клиническую картину болезни.
Для нелеченого манифестного лямблиоза характерно длительное течение с чередованием периодов обострений и ремиссий, постепенным расширением диапазона клинических проявлений.
Осложнения. Исходы. При лямблиозе нередко бывает трудно решить, что является осложнением, а что проявлением фоновых заболеваний. Наиболее убедительно связать с лямблиозом удается такие развившиеся состояния:
синдром мальабсорбции, сопровождающийся дефицитом белков, витаминов, безбелковыми отеками;
присоединение вторичной микрофлоры с формированием холецистита, холангита;
приобретенная полисенсибилизация к различным пищевым продуктам и медикаментам;
дисбактериоз;
стойкий астенический синдром.
Освобождение от лямблий может наступить не только в результате лечения, но и самопроизвольно. Нет сведений о пожизненном парази-тоносительстве.
После очищения организма от лямблий могут длительно сохраняться различные функциональные нарушения органов и систем, наиболее отреагировавших на инвазию.
Методы диагностики. Общеклинические методы. Гемограмма при
лямблиозе в большинстве случаев не отличается от нормы. Эозинофи-лию выявляют не всегда даже при наличии клиники. Лейкоцитоз свидетельствует обычно о наличии сопутствующей бактериальной инфекции. Анемия, и тем более панцитопения, могут наблюдаться при тяжелом длительном течении.
При копрологическом исследовании обнаруживают непереваренную клетчатку, измененные и неизмененные мышечные волокна, крахмал, нейтральные жиры, простейшие.
Биохимические методы. При лямблиозе может выявляться как ги-по-, так и гиперсекреция желудочного сока. На фоне мальабсорбции развивается дефицит белков и витаминов. Даже при тяжелом течении функциональные пробы печени остаются нормальными.
В дуоденальном содержимом может быть повышение уровня диастазы и липазы, снижение — трипсина. Обычно эти нарушения выявляют одновременно с вышеописанными изменениями в кале.
Даже при тяжелом течении функциональные пробы печени остаются нормальными.
Специфическая диагностика. Материалом для паразитологичес-кого исследования являются фекалии и дуоденальное содержимое.
В оформленном стуле обнаруживают цисты лямблий, в жидком — вегетативные формы. Паразитоскопию проводят не позднее чем через 20—30 мин после получения материала от больного. В случаях, если исследование сразу провести нельзя, используют консерванты (см. «Амебиаз»). С помощью фазово-контрастного или люминесцентного микроскопа (менее надежен обычный микроскоп) исследуют нативные мазки и препараты, окрашенные раствором Люголя.
При исследовании дуоденального содержимого нередко в порциях В и С лямблий бывает значительно больше, чем в порции А. Это обусловлено не тем, что лямблии у данного больного паразитируют в желчном пузыре и печени, а всего лишь усилением перистальтики кишечника после дачи желчегонных средств, в результате чего пристеночно расположенные в двенадцатиперстной кишке лямблии отрываются от слизистой и попадают в поток идущей через кишку желчи.
Выделение культуры лямблий на питательных средах — очень трудоемкий процесс, в клиниках им не пользуются.
Серологические методы. Для выявления сывороточных антител к антигенам лямблий чаще используют РНИФ и РФА.
РНИФ позволяет выявлять антитела различных классов (IgM, IgG) к антигенам трофозоитов и цистным антигенам. Наиболее чувствительна реакция при обследовании больных с клиническими проявлениями, особенно при наличии синдрома мальабсорбции (до 90 % положительных результатов). Диагностический титр 1:32. Антитела класса IgM быстро исчезают из крови (уже через несколько недель после освобождения организма от лямблий), IgG могут сохраняться еще 12—15 мес. Таким образом, раздельное определение антител различных классов может помочь в распознавании имеющейся паразитарной инвазии и бывшей (ретроспективная диагностика).
ИФА по чувствительности выше РНИФ, но уступает ей по специфичности, перекрестные реакции могут возникать и при наличии других простейших.
Этими же методами можно выявлять антитела в слюне больных и реконвалесцентов.
Существуют методы, основанные на определении антигенов лямблий в фекалиях. Наиболее широкое распространение получили ВИЭФ и РФА. Оба эти метода дают сопоставимые результаты, обладают высокой чувствительностью (до 95—98 %) и специфичностью (до 100 %). Значительным преимуществом этих методов является их способность выявлять антигены лямблий на самых ранних стадиях заболевания.
В США производится коммерческая тест-система Prospect/Giardia для диагностики лямблиоза. Эта тест-система позволяет выявить в фекалиях больных лямблиозом специфический антиген лямблий GSA-65. Чувствительность и специфичность ее высока — 96 и 100 % соответственно.
Аллергологические пробы с диагностикумом из желчи, содержащей лямблии, менее информативны и точны, чем прямая паразитоскопия и серологические методы.
Определение IgA в дуоденальном содержимом и слюне методом простой РИД по Манчини может быть использовано для разграничения латентного и манифестного лямблиоза.
Критерии диагноза. Полиморфизм клинических проявлений затрудняет распознавание лямблиоза. Тем не менее, об этом широкораспространенном заболевании врач должен помнить всегда, особенно при наличии:
стойкой рецидивирующей диареи, особенно у детей и лиц молодого возраста;
характерного стула — водянистого, чаще не более 2—3—4 раз в сутки;
приобретенной полиаллергии;
нарушения питания, несмотря на сохраняющийся аппетит;
прогрессирующей астенизации;
— изменений в кале, свидетельствующих о нарушении пищеварения.
Особое значение приобретает сочетание перечисленных признаков, полисимптомность клинических проявлений.
Но лишь обнаружение лямблий и их антигенов позволяет верифицировать диагноз.
Дифференциальный диагноз. Латентный лямблиоз диагностируют случайно при проведении плановых обследований или целенаправленном обследовании лиц с самой различной патологией, а также контактных с больным лямблиозом. Как известно, абсолютно здоровые люди встречаются редко, поэтому при обнаружении лямблий в фекалиях или дуоденальном содержимом нужно еще убедиться в том, что имеющиеся у больного клинические симптомы гастрита, дуоденита, холецистита, астении и другие связаны с паразитированием лямблий, а не с другими, не зависящими от лямблий, факторами. Наиболее убедительным доказательством взаимосвязи лямблий, обнаруженных в кишечнике человека, и имеющихся клинических проявлений, является исчезновение или заметное ослабление патологических симптомов после лечения и очищения организма от лямблий, но иногда для этого нужно достаточно длительное время.
Огромный полиморфизм клинических проявлений при лямблиозе, частое сочетание его с различными заболеваниями делает клиническую дифференциальную диагностику при отсутствии четких эпидемиологических данных (например, контакт с больным или носителем) практически нереальной. Тем большее значение имеет настороженность врача, помнящего о необходимости проведения повторных пара-зитологических исследований у лиц с полиорганной симптоматикой, а также хотя бы одного признака, перечисленного в разделе «Критерии диагноза».
Лечение. Лечение при лямблиозе должно включать соответствующую диету, протистоцидные препараты, а также патогенетические средства, направленные на нормализацию полостного и пристеночного пищеварения, сопутствующей микрофлоры, стимуляцию иммунитета и др. Проводить его следует в стационаре, учитывая возможность побочного действия препаратов и частоту возникновения неспецифических аллергических реакций.
Диету (№2, №4, №5) назначают в зависимости от особенностей нарушения функции желудка, кишечника, билиарной системы. Обязательным является ограничение острых блюд и углеводов.
Этиотропную терапию при лямблиозе проводят протистоцидными препаратами, главными из которых являются следующие:
— метронидазол (трихопол, флагил) по 0,25 г 2—3 раза в сутки в течение 5 дней;
тинидазол (фасижин) по 2 г 1 раз в сутки в течение 3 дней;
делагил (хингамин) по 0,25 г 3 раза в сутки в течение 5—б дней;
— аминохинол по 0,15 г 2—3 раза в сутки в течение 5—7 дней. Обычно, если лечение проводят впервые, назначают один из вышеперечисленных препаратов.
При отсутствии эффекта (лямблии не исчезают после курса лечения) проводят еще 2—3 курса лечения, но уже другим препаратом с интервалом между курсами 3—5 дней.
Нередко пользуются комбинацией из двух названных препаратов,
стремясь усилить их действие (трихопол + аминохинол; тинидазол + делагил).
Патогенетическая терапия. Одновременно с этиотропными препаратами, действующими на лямблии, следует назначать нистатин (по 500 ООО ЕД 3—4 раза в сутки в течение 5—7 дней), учитывая часто наблюдающееся увеличение грибковой флоры.
При наличии воспалительных заболеваний желчевыводящих путей и выделении бактерий из дуоденального содержимого назначают фу-разолидон или антибиотики, предпочтительнее макролиды (эритромицин) или тетрациклины, дозы общепринятые. Желательно перед назначением антибактериальных препаратов определять состав кишечной микрофлоры, наличие или отсутствие дисбактериоза, что тоже может повлиять на выбор антибиотика.
Поскольку лямблиоз сопровождается сенсибилизацией организма, а массовая гибель лямблий на фоне лечения может привести к усилению аллергических реакций, протистоцидные средства сочетают с антигис-таминными (диазолин, супрастин и др.).
После окончания курса лечения назначают желчегонные травы, сорбит, ксилит, при необходимости — слепые зондирования, что позволит быстрее освободиться от погибших лямблий и продуктов их разрушения, уменьшить интоксикацию. При нарушении процессов пищеварения показаны ферментные препараты (фестал, панзинорм и др.). При нарушении баланса витаминов можно назначить витамины группы В, аскорбиновую кислоту. Они же будут способствовать повышению общей реактивности организма.
Не следует забывать о симптоматических средствах, выбор которых определяется особенностями течения болезни. При бессоннице показаны снотворные средства, при повышенной возбудимости — седатив-ные.
При наличии боли, спазмов можно назначить антиспастические и обезболивающие препараты (но-шпу, белластезин и др.).
Критерием излеченности является отсутствие лямблий в исследуемом материале при трех-четырехкратном исследовании фекалий и желчи.
Правила выписки из стационара. Выписывают реконвалесцентов из стационара после проведения курса лечения, при этом клинические проявления могут еще сохраняться. Отрицательные результаты копро-скопического исследования и отсутствие лямблий в дуоденальном содержимом не являются обязательным условием, поскольку судить об эффективности лечения можно иногда лишь спустя 2—3 нед после его окончания. При этом может возникнуть необходимость в проведении повторного курса лечения.
Для декретированных групп, в том числе и для детей дошкольного
возраста, обязательным условием допуска к работе и в коллектив является очищение организма от лямблий.
Диспансерному наблюдению лица, перенесшие лямблиоз, не подлежат.
Профилактика. Общие профилактические мероприятия при лямблиозе совпадают с таковыми при всех кишечных инфекциях. Они включают меры по выявлению этой инвазии у декретированных лиц, у больных с острыми кишечными дисфункциями, а также у детей детских дошкольных и закрытых учреждений.
Больные лямблиозом подлежат госпитализации.
С целью предупреждения занос лямблий на пищевые предприятия необходимо всем лицам, оформляющимся на работу, проводить пара-зитоскопическое исследование кишечного содержимого. Эти же исследования необходимо проводить при оформлении детей в детские коллективы.
Очень важными направлениями общей профилактики являются строгое соблюдение санитарно-гигиенических правил в быту, на пищевых предприятиях, в детских дошкольных учреждениях, санация выявленных больных и носителей, обследование членов их семей. Описаны случаи резкого снижения числа инвазированных в коллективах только за счет проведения гигиенических мероприятий.
Специфическая профилактика не разработана.
НАВЧАЛЬНЕ ВИДАННЯ Воз1анова Жанна 1ван1вна
