
- •Болезни в трех томах
- •Общая часть
- •8 Список сокращений
- •Основные сведения об инфекционных болезнях
- •Классификация инфекционных болезней
- •2 Ж. Возианова
- •Принципы лечения инфекционных болезней
- •Характер взаимодействия с микро-и макроорганизмом
- •Возможные побочные реакции
- •II. Аминогли-козиды
- •III. Тетрацик-лины
- •Специфическая профилактика инфекционных болезней
- •Заболевания преимущественно с воздушно-капельным механизмом передачи
- •1Ейраминидаза
- •Действие на факторы клеточного и гуморального иммунитета
- •Формирование антитоксического иммунитетаСтимуляция местных факторов защиты, в том числе завершенного фагоцитоза
- •Функциональные нарушения
- •Механизмов защиты
- •Внедрение микоплазм в слизистую оболочку дыхательных путей
- •Заболевания преимущественно с фекально-оральным механизмом передачи
- •Размножение сальмонелл в тонкой кишке
- •Вегетативная нс
- •Заболевания, вызываемые иерсиниями
- •Желудке (высвобождение эндотоксина при этом незначительное)
- •Непосредственное повреждающее действие шигелл на слизистую оболочку толстой кишки
- •Серогруппа 01 (холерные)
- •Всасывание фрагментов вибрионов в кровь Образование различных факторов агрессии
- •Выработка вибриоцидных антител
- •Структура и функции печени
- •Методы диагностики, использующиеся при обследовании больных вг, и их оценка
- •21 Ж. Возианова
- •Особенности лечения больных вирусным гепатитом с затяжным течением
- •Заболевания, вызываемые вирусами
- •Энтеровирусами Паралитические формы (полиомиелитоподобные заболевания)
- •Асептический серозный менингит
- •Энтеровирусный энцефалит
- •Синдром Гийена—Барре (полирадикулоневрит)
- •Острые респираторные заболевания («летний грипп»)
- •Лихорадка с экзантемой
- •Везикулярный стоматит с экзантемой (ящуроподобный синдром)
- •Герпетическая ангина (герпангина)
- •Эпидемический конъюнктивит
- •Энтеровирусная диарея (летние гастроэнтериты)
- •Энтеровирусный гепатит
- •Эпидемическая миалгия (плевродиния, борнхольмская болезнь)
- •Энтеровирусная инфекция у новорожденных
- •Бессимптомная инфекция
- •Лечение нематодозов
- •Лечение цестодозов
- •Протозойные заболевания
- •1Нфекц1йн1 I паразитарн1 хвороби
Липидный
слой
Матричный
белок-
РНК
Полимераза
•Гемагглютииии
Нуклеопротеин
1Ейраминидаза
Строение вируса гриппа (схема)
варианты вирусов. По данным ВОЗ (1980), вирус гриппа имеет 12 типов гемагглютинина и 9 типов нейраминидазы. Гемагтлютинины 1, 2, 3 типов и нейраминидазы 1, 2 типов содержат вирусы, поражающие человека. Остальные антигены присущи вирусам гриппа животных (свиней, собак, лошадей, многих видов птиц и др.).
Относительно небольшие изменения в структуре гемагглютинина, позволяющие вирусу оставаться в пределах того же подтипа, получили название антигенного дрейфа. Дрейф осуществляется непрерывно из года в год. Полная замена гемагглютинина и (или) нейраминидазы новым антигенным вариантом называется антигенным шифтом (сдвигом). Шифт регистрируют 1 раз в 10—12 лет. Изменчивость наиболее присуща вирусу гриппа А. Вирусы гриппов В и С более стабильны. Объясняется это тем, что вирус А содержит 2 типа нейраминидазы и 3 — гемагглютинина, вирус В — 1 и 1 соответственно, поэтому он имеет лишь антигенные варианты внутри одного серотипа, вирус С содержит только гемагглютинин и не содержит нейраминидазу, но у него имеется рецепторразрушающий энзим. Вирус С не подвержен изменчивости.
Внутри серотипов существуют различные антигенные варианты, которые принято обозначать краткой формулой, включающей род вируса, тип его гемагглютинина и нейраминидазы, географическое происхождение, серийный номер и год выделения. Например, A(H3N2) Сычу-ань2/87 или A(H3N2) Шанхай 11/87.
Возможны генетические рекомбинации между отдельными штаммами вируса гриппа А, полученными от разных лиц, и даже от животных и птиц, в результате чего создается новый, более вирулентный штамм.
Вирусы гриппа малоустойчивы во внешней среде, в течение нескольких часов при комнатной температуре они разрушаются. Под действием дезинфицирующих растворов (спирта, формалина, сулемы, кислот, щелочей) они быстро погибают. Нагревание до 50—60 °С инак-тивирует вирусы в течение нескольких минут, в замороженном состоя-
3 Ж. Возианова
нии при температуре —70 "С они хранятся годами, не теряя инфекционных свойств, Оптимум размножения вируса происходит при + 37 "С в слабощелочной среде.
Как и другие вирусы, возбудитель гриппа совершенно не чувствителен к антибиотикам и сульфаниламидам, но чувствителен к производным амантадина (только тип А), оксолину, интерферону.
Вирус гриппа не растет на обычных питательных средах. Его можно выделить из материала, полученного от больного в первые дни болезни (смывы из носоглотки, мокрота), заражая культуры клеток или куриные эмбрионы.
Противогриппозный иммунитет долгое время считали непродолжительным, так как человек в течение жизни может болеть гриппом неоднократно. Данные, полученные в дальнейшем, продемонстрировали значительную продолжительность и прочность противогриппозного иммунитета, надежно защищающего человека от повторного заражения тем же штаммом вируса (Я.С.Шварцман и соавт., 1980). Однако высокая изменчивость возбудителя позволяет ему избегать воздействия факторов иммунитета. Прежде всего это касается вирусов гриппа типа А.
Традиционно считалось, что человеческий организм освобождается от возбудителя в ближайшие дни после выздоровления. Однако постепенно накапливались косвенные свидетельства, опровергающие эту точку зрения. И в 1985 г. были получены прямые доказательства формирования длительной персистенции вируса гриппа. У одного и того же человека удалось многократно выделять вирус гриппа в течение 9 мес. Как уже указывалось, возможность пожизненной персистенции вируса в организме человека продолжает изучаться.
Эпидемиология. Источником инфекции при гриппе является больной человек, а возможно, и вирусоноситель. Условия формирования вирусоносительства мало изучены. Известно, что фактором, способствующим персистенции вируса, является иммунодефицитное состояние хозяина. В последние годы не исключается также возможность развития хронической гриппозной инфекции. Роль этих форм в эпидемиологии пока что остается неясной.
Наиболее заразным является больной человек во время лихорадочного периода заболевания с выраженным катаральным синдромом. В опытах на добровольцах было показано, что выделение вируса практически прекращается через 5—10 дней после начала болезни, а максимальное содержание его определялось на 2-е сутки после инокуляции.
Известны случаи заражения людей вирусами гриппа животных, удавалось также и у животных выделять «человеческие» вирусы. Это позволило выдвинуть гипотезу о генетической рекомбинации между вирусами животных и человека и появлении пандемических штаммов. Эта гипотеза признается не всеми исследователями, так как вирусы животных в человеческой популяции не получают эпидемического распро-
странения (обычно это спорадические случаи или локальные вспышки). Больше изучена возможность распространения человеческих вирусов среди животных. Вирусы гриппа А и В выделяют у здоровых чаек, цапель, воробьев, косуль, белок, мышей и т.д. У китов обнаруживают вирус, который циркулировал в 1934—1940 гг., а затем исчез из человеческой популяции. До настоящего времени у животных не удалось выделить лишь вирус гриппа С человека.
Согласно другой точке зрения, вирусы человека изменяются независимо от вирусов животных. В отборе эпидемических штаммов ведущую роль играет коллективный иммунитет. Он же является основным фактором, заставляющим вирус изменяться. Штаммы, изолированные полвека назад и пассируемые на куриных эмбрионах и лабораторных животных, остаются антигенно стабильными до настоящего времени. Однако эта теория с каждым годом теряет своих сторонников.
Вирусы, против которых большая часть населения приобретает иммунитет, вытесняются из циркуляции, что подтверждает стойкость и специфичность противогриппозного иммунитета. Их место занимают вновь образованные штаммы либо те, которые отсутствовали в циркуляции длительное время. Так было в 1977 г., когда на эпидемическую арену неожиданно возвратился вирус A(H1N1), исчезнувший в 1956 г. Во время эпидемии наиболее восприимчивыми оказались люди моложе 20 лет, так как они не могли встречаться с указанным подтипом вируса ранее. Это событие примечательно еще и тем, что появление вируса AfH^Nj) не сопровождалось традиционным исчезновением вируса-предшественника подтипа A(H3N2).
До настоящего времени оба подтипа, представленные множеством штаммов, продолжают циркулировать совместно с вирусом типа В.
Для гриппа характерно то, что первая встреча с вирусом гриппа остается в иммунной памяти человека на всю жизнь. Каким бы новым подтипом он не заразился, много лет спустя первыми в крови появляются антитела не к этому новому вирусу, вызвавшему болезнь сегодня, а к тому, который вызвал первое заболевание много лет назад. Лишь последующее наблюдение и исследование в динамике (нарастание титров антител, эпидемическая ситуация) позволяют уточнить этиологические особенности вируса, вызвавшего данное заболевание. Зато это уникальное явление позволяет изучать закономерности изменчивости вирусов гриппа и их циркуляции в различных регионах в отдаленные времена путем определения противовирусных антител в ранние сроки болезни у больных различных возрастных групп в период очередных эпидемий. Это явление получило название, близкое библейскому, — «феномен антигенного первородного греха». Более того, иммунологическая память В-лимфоцитов фиксирует пожизненно все встречи с вирусами гриппа. Но достаточно малейших изменений в структуре нейраминидазы и (или) гемагглютинина, чтобы вспыхнула болезнь.
Против таких новых вирусов анамнестические антитела не срабатывают.
Именно этой способностью к изменчивости определяется частота эпидемий и пандемий.
Наиболее изменчивый вирус А вызывает почти ежегодный сезонный подъем заболеваемости (особенно подвержены заболеванию дети), а каждые 2—3 года — эпидемические вспышки, каждые 10—30 лет — пандемии (следствие антигенного шифта). Вирус гриппа В не вызывает пандемий. Сезонные подъемы заболеваемости наблюдаются через 3—4 года, эпидемический рост — через 5—7 лет. Вирус гриппа С вызывает только спорадические случаи.
Механизм передачи возбудителя при гриппе воздушно-капельный. Заражение происходит при вдыхании мельчайших капелек слизи с вирусом, попадающих в окружающую среду (воздух, предметы обихода, посуда) от больных.
Восприимчивость к гриппу очень высока у людей всех возрастных групп, она фактически всеобщая. Относительно редки случаи гриппа только среди детей первых месяцев жизни, получивших пассивный иммунитет от матери. С возраста б мес дети могут легко заражаться гриппом.
Заболеваемость гриппом носит ярко выраженный сезонный характер, преимущественно в зимние месяцы в Северном полушарии и в летние — в Южном. За время эпидемии заболевает 25—40% населения охваченного гриппом региона, особенно велика заболеваемость среди детей. Во время пандемий заболеваемость может быть еще выше.
Классификация. В диагнозе указывают тип вируса гриппа — А, В, С, вызвавшего заболевание, по возможности в виде соответствующей формулы — род вируса, тип его гемагглютинина и нейраминидазы, географическое происхождение, серийный номер и год выделения.
Например: A(H3N2) Виктория 35/72.
Если привести всю формулу нельзя, указывают хотя бы тип вируса, например, А2.
По тяжести клинического течения гриппа выделяют:
легкое течение,
средней тяжести,
тяжелое,
молниеносное (гипертоксическая форма).
Основные клинические критерии тяжести течения: выраженность токсикоза, сроки появления и характер осложнений.
Наличие или отсутствие осложнений позволяет судить о гриппе неосложненном или гриппе осложненном (указывают характер осложнения).
Примерная формулировка диагноза. 1. Грипп A(HjNj), тяжелое течение. Осложнение: острый левосторонний гайморит.
2. Грипп средней степени тяжести (при отсутствии лабораторного подтверждения такая формулировка допустима).
Нельзя ставить диагноз «токсический грипп», так как токсикоз — обязательный компонент гриппа. В тех случаях, когда токсикоз достигает критических величин, степени ИТШ, можно говорить о гипертоксической форме гриппа.
Патогенез. С определенной долей условности патогенез гриппа можно представить в виде последовательных фаз: проникновение и размножение вируса в эпителиальных клетках дыхательных путей, выход вируса, разрушение пораженных клеток, развитие катарального синдрома, вирусемии, токсемии, реконвалесценция, формирование иммунитета.
1. Проникновение и размножение вируса в эпителиальных клетках дыхательных путей. Находясь в капельках слизи, вирус втягивается воздушным потоком в дыхательные пути. Чем выше дисперсность аэ- розоля слизи, образованного при кашле и чиханье больных, тем глуб- же в дыхательные пути здорового человека проникает вирус. Экспери- ментально установлено, что нижние отделы дыхательных путей значи- тельно чувствительнее к вирусу гриппа, чем верхние. Главной мише- нью вируса являются клетки цилиндрического реснитчатого эпителия. Чтобы состоялось заражение, вирус должен преодолеть факторы не- специфической резистентности дыхательных путей. К ним относятся вязкие свойства слизи, постоянное движение ресничек цилиндричес- кого эпителия, неспецифические ингибиторы репликации вируса, со- держащиеся в слизи секрета дыхательных путей, макрофаги, захваты- вающие вирус и таким образом приостанавливающие его действие, се- креторные IgA. Кроме того, после проникновения первых вирусных частиц в клетки этими клетками вырабатывается и выбрасывается в межклеточную жидкость интерферон, основной задачей которого яв- ляется защита еще не зараженных клеток от проникновения в них ви- руса.
Если вирусу все же удается преодолеть все препятствия, он прикрепляется с помощью гемагглютинина к рецепторам клеток-мишеней (в данном случае к реснитчатому цилиндрическому эпителию) и проникает внутрь клетки, где происходит «раздевание» вируса («стриптиз вируса») и начинается внутриклеточный цикл репликации, который идет с огромной скоростью: уже через 4—б ч в клетке создается партия новых вирусов, которая «выталкивается» из клетки через поры мембраны. Через 24 ч число вирусов, предшественник которых проник в клетку, может достигать нескольких сотен миллионов. Именно такой быстротой репликации вируса и его накопления объясняется очень короткий инкубационный период — от нескольких часов до 2—3 дней.
2. Выход вируса, разрушение пораженных клеток. Непосредствен- ным предшественником оболочки вируса является мембрана клет- ки-хозяина, поэтому окончательное формирование вирусных частиц происходит на поверхности клетки. Важную роль в освобождении вируса играет нейраминидаза, предотвращающая агрегацию вирио-нов-потомков. Освободившиеся вирионы поражают соседние клетки, часть вирусов проникает в кровь. Оставленные вирусом пораженные клетки теряют продолговатую форму, округляются, ядро их сморщивается, фрагментируется. Происходит вакуолизация цитоплазмы с появлением в ней базофильных и оксифильных включений, теряются реснички. Последующая гибель этих клеток обусловлена не столько цито-патогенным действием вируса гриппа, сколько неспособностью клетки полностью восстанавливаться после активного потребления ее ресурсов в процессе синтеза в клетке всех компонентов вирусного нуклео-капсида. Тем фактом, что вирус гриппа выходит из клетки, не разрушая ее, а гибель клетки наступает позже, в пределах 3—24 ч, объясняется некоторое запаздывание катарального синдрома по отношению к токсикозу.
3. Развитие катарального синдрома, вирусемии, токсемии. Начало вирусемии и токсемии соответствует 1-му дню (часу) болезни (озноб, повышение температуры тела).
Одновременно происходят некроз и десквамация эпителия дыхательных путей. Нередко обширные участки слизистой оболочки обнажаются, становясь относительно беззащитными против бактерий. Зоны обширной десквамации эпителия приводят к обнажению подслизи-стого слоя. Различные раздражители — поток воздуха, проходящий через дыхательные пути, слущившийся эпителий — вызывают раздражение нервных окончаний и рефлекторный сухой кашель, который может стать мучительным, сопровождаясь жжением за грудиной. В это время в более глубоких слоях стенки дыхательных путей развиваются отек, полнокровие, клеточная инфильтрация. При наслоении бактериальной флоры может развиться гнойно-некротический трахеобронхит.
Характер поражения легких при гриппе дискутируется до настоящего времени. Часть авторов продолжают утверждать о возможности развития первичной вирусной пневмонии, особо характерной считая «геморрагическую гриппозную пневмонию». Большинство патоморфо-логов и клиницистов с этим не согласны. Изменения в легких расцениваются ими как следствие резких сосудистых нарушений, которые логично именовать токсическим геморрагическим отеком легких.
Нередко на изменения в легких, вызванные вирусом гриппа, наслаивается вторичная бактериальная микрофлора, что существенно отягощает течение болезни.
В крови вирус может находиться как в свободно циркулирующей форме, так и в виде комплексов «вирус — антитело». Кроме вирусных частиц, токсическими свойствами обладают также продукты распада эпителиальных клеток, попавшие в кровь. Выраженный токсикоз при
гриппе является существенной особенностью патогенеза, отличающей его от многих других респираторных вирусных инфекций. Вирус оказывает токсическое действие на сосудистую и нервную системы, причем выраженность поражений пропорциональна степени токсикоза. Значительно повышается проницаемость и ломкость сосудов, что в сочетании с расстройствами микроциркуляции может приводить к развитию геморрагического синдрома. В возникновении циркуляторных расстройств, помимо прямого действия на сосудистую стенку, большое значение имеет нейротропность вируса. Характерны фазовые поражения вегетативной нервной системы, затрагивающие обе ее части (симпатическую и парасимпатическую): гипертензия сменяется гипотензи-ей, тахикардия — брадикардией, повышается секреция слизи в дыхательных путях, появляется потливость.
Изменения во внутренних органах однотипны, обусловлены они генерализованной вазодилатацией.
При быстро развивающейся массивной вирусемии в первые часы болезни может возникнуть инфекционно-токсический шок с развитием сердечно-сосудистой недостаточности. В основе его лежат несколько факторов: сосудистый (непосредственное действие вируса на сосуды с повышением их проницаемости, вазодилатацией), геморрагический синдром с поражением надпочечников и дефицитом гормонов, нарушение функции миокарда. У таких больных смерть может наступить в ближайшие часы от начала заболевания.
В результате токсического поражения сосудистого аппарата центральной нервной системы наступает гиперсекреция спинномозговой жидкости, нарушается ликвородинамика, что ведет к повышению внутричерепного давления, может наступить отек мозга. Чаще все же поражаются мягкие мозговые оболочки, сосудистое сплетение, где можно выявить антигены вируса гриппа. В настоящее время не исключается возможность длительного персистирования вируса гриппа в ЦНС по типу медленной инфекции с развитием впоследствии такого патологического состояния, как паркинсонизм.
Частично вирус из организма выделяется почками, что, возможно, и обусловливает тот факт, что в эпителии дистальных канальцев, как и в эндотелии капилляров клубочков, выявляется значительное количество антигена вируса. Почками также выделяются иммунные комплексы, фрагменты клеток, что ведет к сенсибилизации тканей почки и впоследствии, спустя несколько недель и даже месяцев после перенесенного заболевания, может послужить причиной возникновения гломеруло-нефрита. Разрешающее действие в этом случае может оказать даже фактор, не имеющий антигенной природы (например, переохлаждение).
Инфекционно-аллергический процесс после перенесенной гриппозной инфекции может возникнуть также в эндокарде. Изменения в миокарде, определяемые по ЭКГ как миокардиодистрофия, обусловлены токсикозом и циркуляторными расстройствами.
Отек, очаговые кровоизлияния возникают в печени, но обычно грипп не сопровождается желтухой, цитолитическим синдромом, заметным увеличением печени, признаками печеночной недостаточности. Тем не менее, после перенесенного гриппа типа А, чаще у детей, может развиться синдром Рея — острая энцефалопатия и жировая дистрофия печени. Патогенез развития этого синдрома изучен недостаточно.
При гриппе отмечено угнетение клеточного иммунитета. Наиболее отчетливо выраженное снижение числа Т-лимфоцитов наблюдалось в тех случаях, когда заболевание было вызвано новым подтипом вируса А, отличавшимся по гемагглютинину и нейраминидазе от вирусов, с которыми заболевшие встречались ранее. Полное восстановление популяции Т-лимфоцитов отмечается не ранее чем через 4 нед от начала заболевания. При гриппе также резко снижена фагоцитарная активность нейтрофилов.
Иммунодепрессия, развивающаяся при гриппе, делает возможным присоединение бактериальных осложнений, активацию дремлющих в организме очагов инфекции.
4. Реконвалесценция, формирование иммунитета. Поскольку противовирусные антитела начинают определяться в сыворотке больных лишь к концу 1-й недели болезни, понятно, что они не могут участвовать в механизме выздоровления. Однако следует отметить, что заболевание протекает легче, если в сыворотке инфицированных содержатся антитела (после предшествующих заболеваний гриппом) против тех антигенных детерминант вируса, которые остались неизмененными в ходе антигенного дрейфа. Если же произошло инфицирование вирусом с незнакомым для организма набором антигенов, выздоровление возможно благодаря неспецифическим факторам защиты и «включению» клеточного иммунитета.
Из упомянутых ранее факторов неспецифической резистентности в противовирусной защите главная роль отводится интерферону, препятствующему размножению вируса в эпителии дыхательных путей. Важной защитной реакцией организма является повышение температуры тела. Оно стимулирует фагоцитоз, интерферонообразование, способствует подкислению биологических жидкостей организма, оказывает прямое угнетающее действие на репродукцию вируса.
В последние 10—20 лет получен ряд новых сведений о клеточном иммунитете и его роли в противовирусной защите. Одним из главных факторов клеточного противогриппозного иммунитета являются Т-лимфоциты. Формирование цитотоксических Т-лимфоцитов (киллеров) — важнейшее звено в механизме выздоровления. Т-киллеры ли-зируют клетки-мишени, пораженные вирусом, причем иммунные
Т-киллеры различают только типы вирусов гриппа, но не подтипы, что позволяет им оказывать перекрестное защитное действие. Они также секретируют лимфокины, активируют макрофаги. Т-хелперы взаимодействуют с макрофагами и р-лимфоцитами, стимулируя антителооб-разование.
Важную роль в инактивации вируса гриппа играют секреторные IgA-антитела. В дыхательных путях их образуется большое количество, но определяются они в низких титрах, т.к. постоянно устраняются глотанием. Предполагают, что скорость продукции секреторных антител выше, чем сывороточных. Эти антитела важны и с точки зрения эпидемиологии, так как они ограничивают рассеивание вируса инфицированным человеком.
Наряду с уничтожением возбудителя идет репаративный процесс в слизистой оболочке дыхательных путей, который начинается еще на фоне заболевания: уже через несколько дней от начала болезни обнаруживаются признаки регенерации эпителия. Эти новые клетки невосприимчивы к циркулирующему в организме вирусу. В течение 1 нед организм освобождается от инфекции, человек выздоравливает. А образовавшиеся антитела защищают его от повторного заражения тем же вирусом.
На рис. 7 схематично представлен патогенез гриппа.
Для того чтобы врач четче мог определять лечебную тактику и не назначать, как это нередко встречается, чисто симптоматическое лечение — «от головной боли», «для понижения температуры», «для нормализации давления», — мы приводим табл. 3, позволяющую судить о патогенезе ведущих клинических симптомов.
Клиника. Продолжительность инкубационного периода при гриппе колеблется от нескольких часов до 3 дней, чаще всего составляя 1—2 дня.
Обобщая многообразие клинических проявлений гриппа, можно выделить два основных синдрома — интоксикационный и катаральный. В последнем особое место занимает трахеобронхит.
Обычно болезнь начинается остро с явлений общей интоксикации. Почти все больные отмечают сильный озноб, сменяющийся вскоре чувством жара. Одновременно возникает резкая головная боль в области лба, надбровных дуг, висков, глаз. Боль усиливается при движении глазных яблок, сопровождается светобоязнью, головокружением, иногда бывают обмороки. Развиваются слабость, разбитость, адинамия, потливость, ломота в теле, артралгии, мышечные боли, особенно в мышцах спины, нарушение сна.
В первые же часы температура тела может достигать максимальных показателей (39—40 °С), но удерживается на этом уровне недолго. Через 2—3 дня она снижается — критически либо укороченным лизисом.
Оседание вируса на слизистой оболочке дыхательных путей
Проникновение вируса в клетки эпителия
J
Репликация вируса в клетке, "урожай вируса"
|
Разрушение клеток, зараженных вирусом | |
|
|
|
|
Вирусемия |
, токсемия |
Катаральный синдром
Стимуляция гуморального противовирусного иммунитета
Иммуно-депрес-сия, аллергия
Сосудистые поражения
Нейро-троп-ное действие
Лихорадка
Стимуляция выработки интерферона и других факторов защиты
Вторичная инфекция
Нарушения в органах
Санация
Рис. 7
Схема патогенеза гриппа
Осложнения
Таблица 3. Патогенез нарушений в различных органах и системах при гриппе
Симптомы
Причины возникших нарушений
Головная боль, головокружение, иногда явления менингизма
Лихорадка
Кашель, саднение и боль за грудиной, насморк
Носовое кровотечение, кровоточивость десен, иногда мелкие петехии на коже и слизистых оболочках, токсический геморрагический отек легких
Повышение и снижение АД, склонность к коллапсу, тахикардия и бра-дикардия, потливость, гиперемия лица и слизистых оболочек
Ноющая боль в мышцах, костях, суставах
Прямое токсическое действие вируса и метаболитов на нервные клетки Гиперпродукция ликвора, повышение внутричерепного давления в результате поражения сосудистого аппарата
Пирогенное действие вируса и метаболитов
Поражение вирусом слизистой оболочки, некроз и отторжение эпителиальных клеток
Повышение проницаемости и ломкости сосудов
Циркуляторные расстройства
Колебание тонуса симпатической и парасимпатической частей вегетативной нервной системы за счет токсического поражения диэнцефаль-ной области
Кровоизлияния в надпочечники Интоксикация
Общая продолжительность лихорадки при гриппе в большинстве случаев ограничена 5 днями. Иногда она длится всего 1—2 дня или затягивается до 6—7 дней. Выделить какой-либо характерный для гриппа тип температурной кривой не представляется возможным. Двухволно-вая кривая, когда-то считавшаяся типичной, в настоящее время регистрируется редко. Вторую волну лихорадки большинство авторов объясняют развитием бактериальных осложнений. Чаще температурная кривая регистрируется в виде continua; если же больной принимает жаропонижающие средства, она приобретает ремиттирующий характер. При критическом падении температуры возможны коллапсы.
В 1-е сутки болезни явления интоксикации доминируют над катаральным синдромом, который проявляется сухостью и першением в горле, заложенностью носа. Но уже к концу 1-х суток (иногда на 2-е сутки) начинается сухой кашель, интенсивность которого быстро нарастает. Этот симптом, отражающий выраженность трахеобронхита, заслуживает особого внимания. Появляются саднение и боль за грудиной, обусловленные воспалительным процессом в слизистой оболочке трахеи и бронхов, кашель становится мучительным, иногда приступообразным. Это приводит к повышению давления в системе верхней полой вены и в сочетании с повышенной ломкостью сосудов может способствовать проявлению геморрагического синдрома (носовые кровотечения, мелкие кровоизлияния на слизистой оболочке ротоглотки, изредка на коже). На 3-й — 5-е сутки кашель становится мягче, появляется скудная слизистая мокрота, уменьшается боль за грудиной.
С 1-го дня болезни носовое дыхание затруднено за счет отека слизистой оболочки носа, однако количество выделений невелико. Могут быть полнокровие и набухание нижних раковин носа, сухость, иногда кровоточивость слизистой оболочки. Позднее появляются скудные серозные или слизистые выделения. Обильная ринорея для гриппа не характерна.
В первые дни заболевания гриппом обращают на себя внимание выраженная гиперемия и одутловатость лица, блестящие глаза, инъеци-рованность склер и конъюнктив, что в совокупности напоминает лицо заплаканного ребенка. На слизистой оболочке неба, дужек, задней стенки глотки отмечают яркую разлитую гиперемию («пылающий» зев), более выраженную в области дужек. В последующие дни слизистая оболочка ротоглотки приобретает цианотичный оттенок (по причине циркуляторных расстройств), заметнее становится инъекция сосудов мягкого нёба. Язык влажный, равномерно обложен тонким белым налетом («фарфоровый»). Лимфатические узлы обычно не увеличены, но иногда может наблюдаться небольшое увеличение шейных лимфатических узлов.
Тоны сердца приглушены, однако молодые, исходно здоровые люди не отмечают каких-либо неприятных ощущений в области сердца. У людей старших возрастных групп бывает боль разной интенсивности, вплоть до приступов стенокардии. В 1-е сутки болезни отмечается тахикардия, в последующие дни пульс обычно отстает от температуры. В 1-й день заболевания возможно некоторое повышение артериального давления, позднее оно имеет тенденцию к снижению.
При аускультации легких в неосложненных случаях дыхание везикулярное с жестким оттенком, иногда прослушивают единичные сухие хрипы. На рентгенограммах видно усиление сосудистого рисунка, расширение корней легких.
Живот мягкий, безболезненный. При неосложненном гриппе увеличения печени и селезенки нет. Чаще стул задержан, но изредка бывает послабление стула. Эти нарушения функции пищеварительного тракта неспецифичны и связаны с изменениями тонуса вегетативной нервной системы под влиянием токсинов. Мнение некоторых врачей о существовании «кишечной» формы гриппа совершенно беспочвенно. Про-фузная диарея требует поиска других ее причин и не может быть объяснена гриппом.
Поражения ЦНС проявляются головной болью, головокружением, нарушениями сна, эмоциональной лабильностью. Тяжелые формы гриппа могут протекать с явлениями менингизма, рвотой центрального происхождения.
Клинические признаки поражения мочевыделительной системы при гриппе (неосложненном) не выявляются.
Снижение и даже нормализация температуры тела не означают выздоровления при гриппе. С момента ее снижения (если этот процесс произошел естественным путем без применения жаропонижающих средств) общее состояние улучшается, выраженность интоксикационного синдрома быстро уменьшается. Дольше обычно сохраняется катаральный синдром. Кашель к этому времени становится мягче, появляется слизистая мокрота, которая облегчает его, прекращается жжение за грудиной. Обычно кашель (покашливание), постепенно убывающей интенсивности, сохраняется еще 2—4 дня, но если он длится дольше и появляется гнойная мокрота, — это показатель возникшего бактериального осложнения. Значительно дольше (до 1 мес) сохраняется общая астенизация — слабость, снижение работоспособности, потливость, повышенная утомляемость. В это время нужно избегать дополнительных нагрузок, переохлаждений.
По тяжести выделяют легкое, среднетяжелое, тяжелое и молниеносное течение гриппа.
При легком течении гриппа температура тела не превышает 38 °С и нормализуется через 2—3 дня. Симптомы общей интоксикации и тра-хеобронхита выражены слабо.
Среднетяжелое течение гриппа характеризуется повышением температуры тела до 39 "С, выраженными явлениями интоксикации и поражения дыхательной системы. Лихорадка продолжается до 4—5 сут. Эту форму регистрируют наиболее часто. Поэтому выше и изложена клиника среднетяжелой неосложненной формы гриппа, поскольку она встречается особенно часто.
При тяжелом течении гриппа в клинической картине преобладают симптомы резко выраженной интоксикации. Возможны бред, галлюцинации, потеря сознания. Нередко появляются симптомы внутричерепной гипертензии, геморрагические явления. Температура тела выше 39 °С. В большинстве случаев просоединяются различные осложнения, в том числе геморрагический отек легких. Возможен коллапс.
Молниеносное течение (гипертоксическая форма) характеризуют крайняя тяжесть и быстрота развития поражений с развитием ИТШ. Температура тела при этом снижается. Летальный исход при такой форме гриппа может наступить от отека легких, сердечно-сосудистой недостаточности. Иногда даже не успевает развиться выраженный катаральный синдром.
Температура тела, ее высокие показатели не служат критерием тяжести в таких случаях, хотя именно на этот признак чаще всего ориентируются врачи поликлиники, решая вопрос о необходимости выдачи больничного листка. На первый план выступают проявления сосудистой недостаточности, острого менингоэнцефалита (при отеке-набухании головного мозга), острой дыхательной недостаточности (при геморрагическом отеке легких), острой сердечной слабости. Смерть может наступить через несколько часов с момента появления первых признаков болезни.
Имеются некоторые особенности клиники гриппа в разных возрастных группах. У детей раннего возраста на первый план могут выходить симптомы нейротоксикоза с многократной рвотой, явлениями ме-нингизма, судорогами на фоне субфебрильной или нормальной температуры тела. Иногда у них развиваются бронхиолит, ларингит, ложный круп. Кашель при крупе грубый, лающий; дыхание шумное, отмечается напряжение вспомогательных дыхательных мышц. В отличие от дифтерийного крупа явления стеноза гортани выражены слабо.
Для лиц пожилого возраста грипп опасен прежде всего тем, что на его фоне обостряются сердечно-сосудистые заболевания, активируются хронические воспалительные очаги. Протекает он чаще с невысокой температурой, но с выраженными явлениями интоксикации.
Следует отметить, что грипп может протекать и в виде атипичных клинических форм. Изучение естественной гриппозной инфекции и эксперименты с участием волонтеров позволили выявить афебрильные случаи заболеваний с минимально выраженным катаральным синдромом, а также субклинические формы, при которых инфекционный процесс не сопровождался какими-либо проявлениями. Развитие той или иной формы гриппа зависит от состояния неспецифической и специфической резистентности организма в момент заражения. Надежно диагностировать атипичные формы гриппа можно лишь с использованием вирусологических и серологических методов исследования. К врачам такие больные практически не обращаются.
Осложнения. Все возникающие при гриппе осложнения можно условно разделить на две группы:
первая группа — осложнения, обусловленные непосредственным действием вируса (гриппозной инфекцией);
вторая группа — осложнения, обусловленные вторичной микрофлорой (суперинфекцией или активацией хронического очага инфекции в организме).
Одним из наиболее тяжелых и ранних осложнений первой группы является токсический геморрагический отек легких, который может развиться в первые же дни болезни и явиться причиной летального исхода при тяжелой или молниеносной форме гриппа. На фоне выраженной интоксикации появляется одышка, нарастает цианоз, расстройство дыхания сопровождается возбуждением. В мокроте нередко появляется примесь крови, хотя ее отсутствие не исключает развития геморрагического отека легких. При аускультации выявляется большое количество разнокалиберных хрипов, удлиненный выдох в обоих легких. Одышка, тахикардия нарастают, АД снижается. В таких случаях сравнительно быстро при явлениях тяжелой дыхательной недостаточности наступает смерть.
Отек голосовых связок, рефлекторный спазм мышц гортани может привести к развитию ложного крупа. Это состояние возникает почти исключительно у детей и характеризуется внезапно (на высоте болезни) наступающим приступом удушья. Приступ возникает преимущественно в ночное время, сопровождается беспокойством, тахикардией. Если не оказать немедленную помощь (чаще всего введение спазмолитиков, отвлекающих средств), может наступить смерть. Иногда приступ так же внезапно заканчивается, как и возникает, но дожидаться этого не следует.
Сенсибилизация вирусом и продуктами распада клеток, инфицированных вирусом, слизистой оболочки трахеи и бронхов может послужить впоследствии основой для развития бронхиальной астмы, особенно при часто возникающих ОРВИ.
Предшествующая сенсибилизация почек вирусом, его антигенами, иммунными комплексами лежит в основе развития через 1—2 мес после перенесенного гриппа гломерулонефрита. Вероятность возникновения такого осложнения должен учитывать врач, рекомендуя избегать в ближайшие месяцы после перенесенного гриппа переохлаждения.
Возможные варианты поражения ЦНС при гриппе многообразны. Одним из наиболее распространенных является арахноидит. В основе его развития лежит нарушение ликвородинамики вследствие гиперпродукции спинномозговой жидкости и поражения сосудов с образованием впоследствии очагового слипчивого процесса, что нарушает всасывание спинномозговой жидкости в венозную сеть, увеличивая в свою очередь нарушение циркуляции ликвора. Клиническими проявлениями этого процесса являются регулярно повторяющиеся головная боль, головокружение, тошнота, слабость. Эти симптомы могут появляться уже через 2—3 нед после перенесенного гриппа.
При тяжелом течении гриппа в разгар болезни может возникнуть отек мозга с последующим вклинением его в большое затылочное отверстие. Клиническим проявлением этого состояния является упорнейшая разлитая головная боль с последующей потерей сознания, судорогами, смертью.
Тяжелое течение гриппа, особенно у лиц с отягощенным анамнезом (гипертоническая болезнь, атеросклероз), может сопровождаться кровоизлиянием в вещество головного мозга с последующим развитием параличей.
При гриппе, как и при многих других ОРВИ, может возникнуть синдром Гийена—Барре. Он характеризуется развитием периферических параличей мышц конечностей при сохранении поверхностной чувствительности. Процесс может приобретать восходящий характер с вовлечением мышц лица, глотки, гортани. В спинномозговой жидкости при этом определяют белково-клеточную диссоциацию. К счастью, этот синдром встречается очень редко. Предполагают инфекцион-но-аллергический генез этого синдрома.
Поражения нервной системы могут быть представлены при гриппе радикулитом, невралгией различной локализации, полиневритом. Особенно мучительную боль испытывают больные с невралгией тройничного нерва. Указанные осложнения развиваются чаще в период рекон-валесценции и могут удерживаться от нескольких дней до нескольких недель.
Своеобразным и редким осложнением гриппа является синдром Рея. Впервые его описал в 1963 г. австралийский патологоанатом Рей. Характеризуется синдром острой энцефалопатией и жировой дегенерацией внутренних органов. В большинстве случаев синдром Рея связан с гриппом А и встречается почти исключительно у детей в возрасте до 16 лет. Иногда он может возникать при других ОРВИ, ветряной оспе, вирусном гастроэнтерите. Это осложнение начинается после стихания клиники основного заболевания в период начальной реконвалес-ценции. Внезапная рвота является первым симптомом. Нарастающая затем энцефалопатия проявляется повышенной возбудимостью, крайней раздражительностью, агрессивностью. Бывают светлые промежутки адекватного поведения. Развиться синдром может очень быстро: иногда уже через несколько часов после появления рвоты ребенок входит в кому. Иногда наблюдают децеребрационную ригидность. У 30% больных в самом начале болезни выявляют небольшое увеличение печени, но желтуха при этом не развивается. Характерно повышение активности трансаминаз и увеличение концентрации аммиака в крови в сочетании с гипогликемией.
Есть данные о том, что развитию синдрома Рея способствует прием аспирина. Поэтому многие клиницисты, особенно зарубежные, предлагают воздержаться от назначения этого препарата детям.
Синдром Рея трудно дифференцировать с острыми энцефалопатия-ми другой этиологии. Диагноз считается бесспорным лишь после подтверждения его результатами биопсии печени. У больных выявляют нарушения аминокислотного и жирового обмена. Причины развития синдрома остаются неизвестными. Предполагают генетическую предрасположенность. Несомненным является лишь то, что для развития заболевания обязательным условием является предшествующая вирусная инфекция. Летальность очень высока и составляет 20—56%.
В разгар болезни на высоте токсикоза может развиться синдром внезапной смерти, обусловленный острым поражением капиллярной сети.
Сосудистые нарушения могут вызвать самые различные изменения в мышце сердца — от нетяжелых миокардитов, выявляемых только на ЭКГ, до инфаркта миокарда. Существенную роль в развитии таких осложнений играют тяжесть течения гриппа, возраст больного. В более поздние сроки заболевания может возникнуть эндокардит инфекцион-но-аллергического генеза.
Вторую группу осложнений составляют многочисленные заболевания, вызываемые бактериальной флорой. Чаще они появляются после 4—5-го дня болезни, но иногда и в более ранние сроки. Наиболее характерным из них является пневмония разнообразного характера: очаговая, сегментарная, сливная. Бактериальная флора в таких случаях представлена стафилококками, энтеробактериями, стрептококками, пневмококками, гемофильной палочкой.
Клинически пневмония проявляется кашлем, причем сухой гриппозный кашель часто сменяется кашлем с мокротой (слизисто-гнойной, гнойной). Нередко больные предъявляют жалобы на боль в груди, одышку. Над воспалительным очагом определяют укорочение перкуторного звука, на фоне ослабленного дыхания выслушивают крепити-рующие или мелкопузырчатые хрипы. Чаще поражается правое легкое.
Отмечено, что при пневмонии, возникающей в первые дни гриппозной инфекции, тяжелое течение наблюдается чаще, чем при пневмонии, развивающейся в более поздние сроки. Особенно тяжело протекает пневмония, вызванная стафилококком, имеющая склонность к абсцедированию у ослабленных больных.
Нередко при гриппе диагностируют различные ЛОР-заболевания, вызываемые бактериальной флорой. В период реконвалесценции могут развиться острые синусит, отит, фарингит либо обостриться хронические воспалительные процессы соответствующей локализации (гайморит, фронтит, тонзиллит).
Особенностью гриппозной инфекции является способность ее «проявлять» даже скрытые очаги инфекции независимо от их локализации (воспалительные заболевания мочеполовой, нервной систем и т.д.). Присоединение вторичной инфекции на любом этапе течения заболевания (разгар болезни, период реконвалесценции) существенно отягощает состояние больного, увеличивает частоту неблагоприятных исходов. По этому поводу французские клиницисты говорят, что «грипп выносит приговор, а бактериальная флора приводит его в исполнение».
Исходы. В подавляющем большинстве случаев грипп заканчивается полным выздоровлением. В последние десятилетия смертность от гриппа не превышает 1—3 случаев на 100 ООО населения. Однако дополнительная смертность во время эпидемий, косвенно связанная с гриппом, составляет в разных странах от 76,7 до 540 случаев на 100 ООО населения. В группу риска входят прежде всего люди пожилого и старческого возраста с сердечно-сосудистыми и хроническими воспалительными заболеваниями.
Исход заболевания в вирусоносительство изучен мало. Известно, что формированию персистенции вируса гриппа способствует имму-нодефицитное состояние организма. Предстоит выяснить, является ли иммунодефицит главным и необходимым условием для такого исхода.
Методы диагностики. Из общеклинических методов исследования определенное значение имеет общий анализ крови. В 1-е сутки болезни у 1/3 больных развивается лейкоцитоз (до 10—12* 109/л) с умеренным палочкоядерным сдвигом, обусловленным повышением количества циркулирующих нейтрофилов. На 2-е сутки содержание ней-трофилов быстро уменьшается, развивается лейкопения, сохраняющаяся до конца лихорадочного периода, а иногда и дольше.
Динамика содержания лимфоцитов иная. При заражении гриппом добровольцев было выявлено значительное уменьшение количества лимфоцитов в циркулирующей крови еще за несколько часов до начала болезни. Абсолютная лимфопения является характерной для гриппа и наблюдается в течение всего заболевания. В разгар гриппа имеет место относительный лимфоцитоз (за счет выраженной нейтропении). В первые дни периода выздоровления намечается тенденция к нормализации формулы крови. СОЭ в большинстве случаев остается в пределах нормы. Показатели гемоглобина, эритроцитов, гематокрита обычно не изменяются. Снижение уровня нейтрофилов в периферической крови объясняют их миграцией в очаг воспаления, а также повышенной продукцией кортизола в стрессовой ситуации, каковой является гриппозная инфекция для организма.
Изменения в моче не характерны. Но на высоте лихорадки могут отмечаться незначительная протеинурия, микрогематурия как следствие токсикоза и циркуляторных расстройств.
Специфическая диагностика. В ранние сроки диагноз гриппа можно быстро подтвердить методом РФА. Принцип метода состоит во взаимодействии с вирусом гриппа специфических антител, меченных изо-тиоцианатом флюоресцеина: последний обладает способностью светиться в ультрафиолетовых лучах. Из носовой полости больного берут мазки при помощи тампонов. Не позже чем через 3—4 ч из них на предметном стекле готовят препараты, фиксируемые ацетоном. Цель фиксации — обеспечить проницаемость клеточных мембран для крупных молекул антител. Затем производят иммунофлюоресцентную окраску препаратов, в ходе которой в клетках при наличии в них вируса образуются комплексы антиген — антитело. После тщательной отмывки препараты просматривают в люминесцентном микроскопе. Для постановки диагноза необходимо обнаружить в мазке не менее 5 клеток цилиндрического эпителия с флюоресцирующими включениями. Этот метод высокоспецифичен и информативен. Результат исследования может быть получен через 2—3 ч после взятия материала.
Серологическое исследование является ретроспективным методом исследования, то есть диагноз может быть установлен уже после выздоровления больного. В практическом здравоохранении чаще всего используют РТГА, иногда РСК, редко — реакцию нейтрализации и реакцию радиального гемолиза. Разработана также методика постановки реакции непрямой гемагглютинации. Для получения достоверного ответа необходимо исследование парных сывороток, первую из них берут в первые дни болезни, вторую — 7—10 дней спустя. Диагноз считают подтвержденным, если во второй сыворотке обнаруживают не менее чем четырехкратный прирост антител.
Вирусологическое исследование с выделением вируса на куриных эмбрионах является наиболее трудоемким и дорогостоящим методом диагностики и в практическом здравоохранении применяется редко.
Методы иммуноферментного анализа и молекулярной гибридизации также пока еще не получили широкого распространения.
Дополнительные методы. Учитывая характер и тяжесть вероятных осложнений, желательно при гриппе, особенно тяжелом его течении, делать ЭКГ и рентгенографию легких.
Критерии диагноза. При постановке диагноза гриппа следует основываться на таких данных:
эпидемический подъем заболеваемости в холодное время года;
острое, внезапное возникновение болезни;
— сочетание интоксикационного синдрома (высокая температура, головная боль с преимущественной локализацией в области лба, миал-гия) и катарального (сухой упорный кашель, сопровождающийся сад-нением за грудиной, затрудненное носовое дыхание);
внешний вид больного («лицо заплаканного ребенка»);
разлитая гиперемия с цианозом слизистой оболочки полости рта;
— наличие лейкопении с относительным лимфоцитозом при нормальной СОЭ.
Диагноз подтверждают РФА (на фоне клинических проявлений заболевания) и серологическими методами с использованием парных сывороток (ретроспективная диагностика).
Дифференциальный диагноз. Ежегодно в инфекционные стационары направляют большое количество больных с диагнозом «грипп». Почти у половины из них затем выявляют совершенно иные заболевания. Особенно больших масштабов гипердиагностика гриппа достигает во время эпидемии, когда одного лишь повышения температуры тела иногда бывает достаточно для постановки этого «популярного» диагноза. Ошибки в диагностике могут быть обусловлены не только низкой квалификацией врачей, но и объективной причиной — сходством отдельных симптомов гриппа с симптомами других заболеваний. Труднее всего проводить дифференциальную диагностику гриппа с другими ОРЗ в связи с наличием одного из ведущих общих для всех этих заболеваний синдрома — катарального.
Клиника парагриппа имеет много общих симптомов с гриппом. Однако существуют некоторые отличия:
парагрипп начинается постепенно и значительно уступает гриппу по выраженности интоксикации, температура редко превышает 38 °С;
вирусы парагриппа преимущественно поражают гортань с развитием симптомов ларингита, особенно у детей. Клинически это проявляется осиплостью голоса, лающим сухим кашлем;
слизистая оболочка ротоглотки неярко гиперемирована, а для гриппа характерна яркая, разлитая гиперемия в сочетании с мучительным надсадным кашлем и с болью за грудиной.
Риновирусная инфекция отличается от гриппа следующими симптомами:
обильными серозными выделениями из носа на фоне незначительной интоксикации;
слезотечением, частым чиханьем при отсутствии симптомов тра-хеобронхита;
— субфебрильной или даже нормальной температурой тела;
— слегка гиперемированной слизистой оболочкой ротоглотки. Аденовирусная инфекция вызывается вирусами, тропными не
только к эпителию дыхательных путей, но и к лимфоидной ткани. В клинической картине в отличие от гриппа обращают на себя внимание такие симптомы:
явления тонзиллита;
увеличение регионарных лимфатических узлов;
умеренный кашель, который может появиться на 3—4-й день;
иногда бывают увеличены печень и селезенка;
выражен экссудативный компонент, в то время как при гриппе только скудные выделения из носа;
дифференциальная диагностика облегчается при наличии характерного для аденовирусной инфекции конъюнктивита, зачастую асимметричного;
возможны боль в животе (особенно у детей) и диспепсические явления;
характерна большая (до 8—12 сут) продолжительность лихорадочного периода;
несмотря на наличие иногда высокой (до 39 °С) температуры тела, общее состояние нарушено меньше, чем при гриппе;
вместо лейкопении возможен умеренный лейкоцитоз.
При PC-инфекции ведущим является поражение нижних дыхательных путей, однако у взрослых клиническая картина может напоминать грипп, тем более, что по уровню интоксикации PC-инфекция занимает промежуточное положение между гриппом и парагриппом. Отличие состоит в следующем:
в меньшей выраженности катаральных изменений в слизистой оболочке носоглотки; дужки и мягкое небо слабо гиперемированы;
в клинике преобладают явления бронхита, иногда с бронхоспа-стическим компонентом; трахеит с чувством жжения за грудиной отсутствует;
— у детей нередко развиваются бронхиолит, пневмония.
Внезапное начало заболевания, озноб, миалгия, головная боль, упорный кашель, возникающие при микоплазменной пневмонии, требуют также дифференциальной диагностики с гриппом.
Микоплазменная пневмония отличается от гриппа такими симптомами:
— бледностью кожи, отсутствием явлений трахеита;
— нередко появлением полиморфной экзантемы с преимущественной локализацией вокруг суставов;
иногда увеличенной печенью;
умеренным лейкоцитозом в крови;
длительностью заболевания (до 4 нед).
Корь, как и грипп, характеризуется острым началом, интоксикацией, кашлем. Для кори характерны:
лающий кашель,
конъюнктивит,
светобоязнь.
Главное ее отличие — наличие высыпаний:
— на 2—3-й день болезни на слизистой оболочке щек появляются пятна Коплика, а с 3—4-го дня на коже лица — характерная сыпь, которая поэтапно распространяется по всему телу.
В ряде случаев клиническая дифференциальная диагностика гриппа с другими ОРВИ настолько затруднительна, что окончательную ясность может внести лишь использование иммунофлюоресцентного и серологического методов исследования.
Тем не менее в особо сложных случаях нельзя пренебрегать анамнезом, который должен быть собран с особой тщательностью, имеет значение все: очередность возникновения клинических симптомов, их выраженность, сочетание, динамика и т.д. Всегда следует помнить, что катаральный и интоксикационный синдромы — обязательные признаки гриппа. Отсутствие любого из них должно заставить врача подумать о наличии другого заболевания, прежде чем установить диагноз «грипп». Иногда катаральный синдром при гриппе может запаздывать, но не более чем на 1 сут.
Нередко диагноз «грипп» ошибочно выставляют в начальный период любого заболевания, начинающегося с синдрома общей интоксикации. Причиной диагностических ошибок в данном случае является недооценка роли катарального синдрома (прежде всего, трахеобронхита). До сих пор среди части практических врачей бытует мнение о существовании так называемых акатаральных форм гриппа, что совершенно неверно. Убедительные доказательства существования гриппа с выраженным токсикозом, но без катаральных явлений отсутствуют.
Дифференцировать грипп с брюшным тифом при классическом постепенном начале последнего не представляет особых трудностей. Значительно труднее поставить диагноз в случаях острого начала брюшного тифа. При этом следует учитывать наличие ряда сходных с гриппом симптомов: головная боль, относительная брадикардия, гипотензия, лейкопения с относительным лимфоцитозом.
Однако при брюшном тифе:
не характерны гиперемия и одутловатость лица, слезящиеся глаза;
ринит отсутствует;
кожа бледная, сухая, со 2-й недели — розеолезная сыпь;
потливость, часто наблюдаемая при гриппе, — редкое явление при брюшном тифе, но может искусственно вызываться приемом аспирина;
головная боль интенсивная, но разлитая, при гриппе же она локализуется в области лба, надбровных дуг, глазных яблок;
язык обильно обложен сероватым налетом, утолщен, края и кончик его остаются чистыми;
увеличены печень и селезенка, живот вздут, стул задержан;
ценным диагностическим признаком брюшного тифа является симптом Падалки;
у подавляющего большинства больных катаральный синдром отсутствует.
Следует отметить, что дифференциальную диагностику гриппа с брюшным тифом имеет смысл проводить лишь в первые 4—5 дней болезни. При сохранении синдрома интоксикации и лихорадки более продолжительное время вопрос о гриппе, естественно, снимается.
Бывает трудной дифференциальная диагностика гриппа с лепто-спирозом, что обусловлено наличием в первые дни болезни ряда сходных симптомов: острое начало с ознобом и быстрым подъемом температуры, одутловатость и гиперемия лица, инъецированность склер, сильная головная боль, миалгия. При постановке диагноза следует учитывать следующее:
миалгия при гриппе диффузная, тогда как при лептоспирозе боль преимущественно локализуется в' икроножных мышцах;
при лептоспирозе меньше других систем страдают органы дыхания: лишь у отдельных больных возможно развитие бронхита, значительно уступающего по интенсивности гриппозному поражению дыхательных путей;
геморрагический синдром с большим постоянством и выраженностью встречается при лептоспирозе;
закономерным для лептоспироза является поражение почек с развитием в тяжелых случаях острой почечной недостаточности, сопровождающейся олигурией, анурией и грубыми изменениями в моче (белок, микро- и даже макрогематурия), тогда как изменения в почках при гриппе незначительны и носят скоропроходящий характер;
дифференциальный диагноз значительно облегчается при наличии у больного желтухи или характерной для тяжелого течения геморрагической сыпи;
отличить грипп от лептоспироза в первые дни их возникновения помогает анализ крови: вместо характерной для гриппа лейкопении с относительным лимфоцитозом для лептоспироза типичны лейкоцитоз с выраженным сдвигом формулы влево, лимфопения, значительное увеличение СОЭ (до 50—60 мм/ч);
помогает диагностике анализ эпидемиологических данных: летний сезон, купание в водоемах со стоячей водой, пребывание в местах обитания грызунов свидетельствуют в пользу лептоспироза. Диагноз «грипп» в летнее время всегда сомнителен.
В преджелтушный период вирусного гепатита А ошибочный диагноз гриппа — нередкое явление. Этому способствуют острое начало гепатита с ознобом и повышением температуры тела до высоких показателей, головная боль, ломота, разбитость, лейкопения с относительным лимфоцитозом. Однако от гриппа вирусный гепатит отличается следующими признаками:
при вирусном гепатите А имеет место разлитая головная боль, а не только в лобной области;
важным дифференциально-диагностическим признаком гепатита является отсутствие или скудность катаральных явлений, тогда как при гриппе они появляются не позднее 2-х суток от начала болезни и бывают одним из ведущих симптомов;
при вирусном гепатите А с первых дней болезни можно обнаружить увеличение печени и селезенки;
через 2—3 дня температура тела может снижаться при обоих заболеваниях, но если больные гриппом испытывают при этом облегчение, то у больных вирусным гепатитом А начинается желтушный период, т.е. заболевание переходит в новую фазу, которая гриппу несвойственна;
высокая активность сывороточных трансфераз (в первую очередь АлАТ) в первые же дни болезни еще до появления желтухи является решающим диагностическим признаком вирусного гепатита А.
Грипп приходится иногда дифференцировать с различными формами менингококковой инфекции. Для менингококкового назофаринги-та типичны заложенность носа, першение в горле, головная боль, иногда появляется сухой кашель. Вместе с тем:
температура сравнительно редко достигает высоких показателей;
катаральный симптом проявляется в форме назофарингита, а не трахеобронхита;
обращает на себя внимание бледность лица в отличие от гиперемии, наблюдаемой при гриппе;
вместо «пылающего» гриппозного зева характерен контраст между отечной, гиперемированной задней стенкой глотки и неизмененными или слегка гиперемированными миндалинами, мягким небом, небными дужками;
выделения из носа чаще слизисто-гнойные, иногда сукровичные, их можно увидеть стекающими в виде дорожек по задней стенке глотки. Гриппу же присуща сухость слизистой оболочки носоглотки;
в крови — лейкоцитоз.
Явления менингизма, наблюдаемые иногда при тяжелой форме гриппа на высоте интоксикации, требуют дифференциальной диагностики с менингококковым менингитом (а также с менингитами иной этиологии). Гриппозный менингеальный синдром развивается на фоне катарального синдрома, в котором ведущее место занимает трахео-бронхит. Менингококковому менингиту часто предшествуют явления назофарингита, но иногда он возникает даже на фоне кажущегося полного благополучия. Решающее значение для дифференциальной диагностики имеет спинномозговая пункция. При обусловленном гриппом менингизме обнаруживается повышенное давление спинномозговой жидкости, клеточный и белковый состав ее не изменен. При менинго-кокковом менингите спинномозговая жидкость мутная или опалесци-рующая, выявляются плеоцитоз с преобладанием нейтрофилов, повышено содержание белка.
Менингококцемию отличить от гриппа помогает наличие таких симптомов:
характерная геморрагическая сыпь, появляющаяся часто уже в первые часы от начала болезни. Элементы сыпи различной величины и формы, плотные на ощупь, выступают над уровнем кожи, локализуются преимущественно на конечностях. Следует помнить, что обильная сыпь (за исключением единичных петехий) не характерна для гриппа;
герпес часто появляется при менингококковой инфекции, нередко с первых дней болезни, тогда как при гриппе он наблюдается редко, возникает не ранее 4—5-го дня заболевания и обычно свидетельствует о присоединении вторичной бактериальной инфекции на фоне имму-нодепрессии.
В первые дни заболевания сыпной тиф (а также болезнь Брилля) и грипп имеют много общего: острое начало, головная боль, гиперемия и одутловатость лица, гиперемия слизистой оболочки полости рта, разбитость, ломота в теле. Но различная тропность возбудителей (к эпителию дыхательных путей вируса гриппа и к эндотелию сосудов риккет-сий Провачека) обусловливает различия в клинических проявлениях. Для сыпного тифа характерны следующие признаки:
— скудные катаральные симптомы, нередко они вообще отсутствуют;
явления васкулита можно обнаружить уже на 2—3-й день болезни в виде точечных кровоизлияний на мягком небе (энантема Розен-берга) и на переходной складке конъюнктивы (симптом Киари — Ав-цына);
поражение продолговатого мозга при сыпном тифе проявляется фибриллярными подергиваниями языка, толчкообразным тремором при попытках высунуть его за линию зубов (симптом Говорова—Годелье);
обращают на себя внимание возбуждение больного, словоохотливость, несмотря на сильную, разлитую, в отличие от гриппа, головную боль, беспокойный сон с кошмарными сновидениями; больные гриппом, напротив, вялы, апатичны;
закономерно появляющаяся на 4—5-е сутки розеолезно-петехи-альная экзантема позволяет завершить клиническую дифференциальную диагностику в пользу сыпного тифа;
в противоположность лейкопении при гриппе сыпной тиф сопровождается умеренным нейтрофильным лейкоцитозом.
Важно учитывать эпидемиологический анамнез (наличие педикулеза), степень контагиозности больного, длительность течения болезни.
Внезапное начало, озноб, ломота во всем теле, головная боль иногда требуют проведения дифференциальной диагностики между гриппом и малярией. Для малярии характерны такие симптомы:
соответствующий эпидемиологический анамнез (приезд из неблагополучной в отношении малярии местности);
циклическое течение болезни (озноб, жар, пот), регулярное повторение приступов;
отсутствие катарального синдрома;
увеличение печени и селезенки;
— наличие в крови малярийных паразитов, прогрессирующая анемия.
При некоторых формах малярии четкая регулярность приступов в начальный период заболевания может отсутствовать, но остальные признаки (гепатолиенальный синдром, малярийные паразиты в крови) сохраняют свое дифференциально-диагностическое значение.
В период подъема заболеваемости гриппом нередко приходится проводить дифференциальный диагноз с бактериальной пневмонией. Ошибочному диагнозу способствуют соответствующая эпидемическая ситуация, наличие интоксикационного и катарального синдромов, иногда — острое начало болезни.
Пневмонию от Гриппа отличают такие признаки:
более длительная лихорадка;
характер катарального синдрома (кашель глубокий, со слизи-сто-гнойной мокротой, иногда боль в груди при дыхании, отсутствие жжения за грудиной);
отсутствие типичного для гриппа «лица заплаканного ребенка»;
влажные хрипы в легких на фоне ослабленного дыхания над зоной воспаления, укорочение перкуторного звука;
лейкоцитоз с нейтрофилезом, увеличенная СОЭ.
Следует лишь помнить, что пневмония может осложнять течение гриппа с первых дней болезни, так что возможна патология-микст.
В данном разделе приведены лишь клинические дифференциально-диагностические признаки и различия в общем анализе крови. Обычно уточнить диагноз позволяют специфические методы исследования — выявление возбудителя, серологические реакции. О сроках, наиболее приемлемых для использования этих методов, их оценке подробно сказано в разделах, касающихся каждого из вышеперечисленных заболеваний.
Пожалуй, трудно назвать инфекционное заболевание, которое могло бы соревноваться с гриппом по частоте ошибочных диагнозов. «Грипп» — очень «популярный» диагноз: в подавляющем большинстве :лучаев лихорадящему больному при первичном обращении, особенно в первые дни, ставят именно этот диагноз. Обусловлено это не всегда незнанием врача, а иногда и тем, что в первые сутки заболевания у больных преобладают неспецифические симптомы интоксикации (лихорадка, головная боль, слабость, боль в мышцах, отсутствие аппетита и т.д.). Ориентируясь только на них, без учета эпидемиологической ситуации, сезона, наличия или отсутствия других важных признаков, а затем и динамики болезни легко можно допустить ошибку. Поэтому почти при всех заболеваниях в разделах, посвященных дифференциальной диагностике, еще и еще раз придется встречаться с гриппом.
Лечение. Лечение больных гриппом при среднетяжелом и легком течении проводят на дому. Госпитализации подлежат лишь больные с тяжелым течением. Наличие у больного хотя бы одного из таких признаков, как гипертермия (40—41 °С и выше), менингеальный синдром, рвота, судороги, одышка, цианоз, аритмия, гипотензия, требует безусловной госпитализации. Госпитализацию также проводят по эпидемиологическим показаниям (проживание в общежитиях, гостиницах).
Больному назначают постельный режим в течение всего лихорадочного периода (необходимо помнить о возможности коллапса) и богатую витаминами, легкоусвояемую, разнообразную пищу с достаточным количеством жидкости. Помещение, в котором находится больной, необходимо регулярно проветривать, избегая при этом переохлаждения воздуха, т.к. как это может усилить кашель и даже привести к бронхоспазму.
Этиотропная терапия. В 1-е сутки от начала заболевания (лучше в первые часы) показано назначение ремантадина, оказывающего действие на вирус гриппа А. Его принимают внутрь после еды, запивая водой: в 1-е сутки — по 0,1 г 3 раза, во 2-е и 3-й — по 0,1 г 2 раза. При назначении препарата со 2-х суток болезни лечебный эффект выражен слабее. Назначенный в более поздние сроки ремантадин не оказывает заметного действия на течение болезни. Препарат хорошо переносится, поэтому его предпочитают мидантану (амантадину), оказывающему сходное противовирусное действие, но дающему заметный побочный эффект (головная боль, бессонница, диспепсические явления). Препарат противопоказан при заболевании печени и почек, беременности, тиреотоксикозе. Активен при гриппе рибавирин, вводимый в аэрозоле.
Для лечения больных с тяжелым течением гриппа или ослабленных прежде широко применяли противогриппозный иммуноглобулин, приготовленный из крови доноров, иммунизированных гриппозной вакциной. Его вводят внутримышечно по 3—6 мл 2 раза в сутки с интервалом 8—12 ч до получения лечебного эффекта, который тем выше, чем раньше препарат применен. Слабый эффект иммуноглобулина может наблюдаться в тех случаях, когда грипп вызван вирусом, значительно отличающимся по антигенной структуре от вакцинного штамма. В такой ситуации приходится рассчитывать лишь на неспецифическое об-щестимулирующее действие иммуноглобулина. В последние годы целесообразность использования иммуноглобулина для лечения больных подвергается сомнению.
Для лечения больных гриппом применяют препараты интерферона (человеческий лейкоцитарный или рекомбинантный а-интерферон). Наиболее эффективен он при назначении в первые дни и даже часы болезни. Назначают его либо в виде ингаляций (содержимое трех ампул интерферона смешивают с подогретыми до 37 °С 10 мл воды и вдыхают из ингалятора) 2 раза в сутки, либо закапывают в нос (интерферон смешивают с дистиллированной водой в соотношении 1:2) 5—6 раз в сутки. Однако вероятность возникновения аллергических реакций на препарат и содержащиеся в нем балластные вещества заставляют с осторожностью относиться к его назначению, более того, применять его рекомендуют лишь в условиях стационара.
Патогенетическая и симптоматическая терапия. Совершенно неоправданным следует считать стремление во что бы то ни стало снизить температуру. Лихорадка является одной из важных неспецифических защитных реакций организма. Клинический опыт показывает, что систематический прием жаропонижающих средств с первых дней болезни способствует пролонгированию катарального и интоксикационного синдромов, повышает частоту осложнений. При слишком высокой, плохо переносимой температуре возможно ограниченное использование небольших (0,25—0,5 г однократно) доз анальгина. Можно назначить в этой ситуации, особенно пожилым людям, мефенамовую кислоту (производная антраниловой кислоты). Она обладает довольно мягким аналгезирующим и жаропонижающим свойствами, близкими к действию других нестероидных противовоспалительных веществ. Ее назначают до 3 г в сутки в первые дни болезни. Но большое количество противопоказаний (язвенная болезнь, заболевания пищеварительного тракта, органов кроветворной системы, почек) требует осторожного и четко обоснованного назначения препарата. К тому же в отдельных случаях возможно резкое снижение температуры, что может привести к коллапсу. Значительно лучше использовать физические методы снижения температуры, например, протирание кожи теплым 0,25 % — 0,5 % раствором уксуса, обильное введение жидкости в организм (2—2,5 л в сутки) в сочетании с потогонными средствами (отвар цветков липы, чай с лимоном, малиновым вареньем, калиной). От аспирина сейчас практически отказались (усиливает кровоточивость), а детям до 16 лет он вообще противопоказан (угроза развития синдрома Рея).
С первых дней болезни традиционно применяют горчичники, улучшающие кровообращение в органах дыхания за счет рефлекторных реакций. Можно назначать аскорутин (рутин 0,05 г, аскорбиновая кислота 0,05 г, глюкоза 0,2 г) по 1 таблетке 3 раза в сутки в течение 5—6 дней. Он уменьшает проницаемость и ломкость капилляров и таким образом снижает вероятность возникновения геморрагического синдрома.
Антигистаминные препараты уменьшают проницаемость капилляров, предупреждают развитие вызываемого гистамином отека тканей, обладают противовоспалительными и десенсибилизирующими свойствами. Один из таких препаратов, как диазолин или тавегил, назначают в острый период гриппа в течение 4—5 дней.
С первых дней болезни применяют метилурацил по 0,5 г 4 раза в сутки сроком на 4—5 дней. Препарат стимулирует клеточные и гуморальные факторы защиты, ускоряет клеточную регенерацию, обладает противовоспалительным свойством, стимулирует лейкопоэз.
Поскольку при гриппе с первых дней развивается синдром трахео-бронхита, больным необходимо назначать отхаркивающие средства. Облегчают отделение слизи трава термопсиса, мукалтин (применяют по 0,05 г 3 раза в день), пертуссин (применяют по 1 столовой ложке 3 раза в день). Один из перечисленных препаратов назначают в острый период гриппа.
Не рекомендуется в первые дни болезни назначать препараты, угнетающие кашлевой рефлекс (кодеин и др.), так как они способствуют задержке в дыхательных путях вируса, клеток, инфицированных вирусом, и в результате этого инфекция спускается в нижние дыхательные пути. К этим препаратам можно прибегнуть на 2—3 дня после 3-го дня болезни, когда местный процесс (репликация вируса в клетках эпителия) практически завершился, вирус находится главным образом в крови, а кашель еще остается мучительным, причиняющим боль и беспокойство. Облегчают кашель паровые ингаляции, но их с осторожностью следует применять при наличии у больного ИБС, гипертензии и др.
При затрудненном носовом дыхании интраназально используют 2% раствор эфедрина (сосудосуживающее действие), нафтизин (противо-отечное действие, уменьшает приток крови к венозным синусам). Оба препарата противопоказаны при гипертонической болезни, выраженном атеросклерозе.
Назначение антибиотиков при гриппе неэффективно. Показаниями к их применению являются:
— наличие хронического очага инфекции;
— признаки присоединения вторичной инфекции — суперинфекция (независимо от сроков болезни);
— резкое ослабление организма с выраженным иммунодефицитом;
— длительность лихорадки больше 5 дней при сохраняющейся выраженной интоксикации.
С профилактической целью назначение антибиотиков не только не показано, но даже вредно, поскольку они могут усиливать сенсибилизацию, иммунодепрессию. Если же антибиотик необходим, то выбор его — это компетенция только врача. Назначение антибиотика определяется характером осложнения, аллергологическим анамнезом больного, степенью токсичности препарата и т.д.
Больные гриппом в течение всего времени болезни нуждаются в наблюдении, учитывая возможность возникновения коллапсов и других осложнений. Коррекцию нарушения деятельности сердца осуществляют индивидуально с учетом характера нарушения, преморбидного состояния органа.
При возникновении таких осложнений, как отек мозга, ИТШ и другие, проводят соответствующие мероприятия.
Порядок выписки из стационара. Выписка реконвалесцентов осуществляется по клиническим показаниям. Больной гриппом должен находиться в стационаре или оставаться дома до полного клинического выздоровления.
Реконвалесценты после гриппа нуждаются в диспансерном наблюдении в поликлинике по месту жительства. В первую очередь диспансеризации подлежат реконвалесценты с тяжелыми заболеваниями сердечно-сосудистой, дыхательной, нервной, эндокринной систем. Минимальный срок диспансеризации — 1 мес после перенесенного заболевания.
Больным, лечившимся в домашних условиях, не следует поспешно, сразу после снижения температуры приступать к работе, т.к. к этому времени болезнь еще не завершается, сохраняется астенизация, защитные силы организма снижены, может присоединиться бактериальная инфекция и болезнь затянется надолго. Желательно, чтобы общий срок больничного листка был не менее 7—10 дней.
Профилактика. Неспецифическая сезонная профилактика включает ряд средств и методов повышения резистентности организма к возбудителям гриппа и других ОРВИ.
Рекомендуют закаливающие процедуры (полоскание горла прохладной водой, хождение босиком, сон в холодное время года при открытой форточке).
Используют поливитаминные препараты «Декамевит», «Гексавит», «Ундевит» по 1 драже 2—3 раза в день; экстракт элеутерококка, который обладает общеукрепляющим и тонизирующим свойствами, повышает неспецифическую резистентность организма. Применяют его по 20—40 капель на прием 2—3 раза в день в течение 25—30 дней. Рекомендуют также продигиозан. Он стимулирует Т-систему иммунитета, продукцию интерферона, факторы неспецифической резистентности. Применяют 0,005 % раствор интраназально с помощью распылителя-дозатора.
Специфическая профилактика заключается в проведении вакцинации — массового и эффективного метода борьбы с гриппом. Применяемые в настоящее время вакцины делятся на инактивированные и живые. Инактивированные вакцины могут быть цельновирионными и расщепленными (состоящими из продуктов расщепления вирусных частиц с помощью детергентов). Инактивированные гриппозные вакцины вводят парентерально, поэтому они индуцируют в основном гуморальный иммунитет. С 1989 г. использование безыгольных инъекторов запрещено в связи с риском передачи ВИЧ-инфекции.
Живые аллантоисные вакцины вводят в носовые ходы распылителем-дозатором. Они выгодно отличаются от инактивированных тем, что, кроме гуморального, стимулируют и местный иммунитет дыхательных путей (секреторные антитела, клеточный иммунитет).
Живые вакцины рекомендуют использовать в первую очередь в небольших коллективах и для иммунизации детей, инактивированные — в больших коллективах на крупных предприятиях. Необходимости в поголовной вакцинации нет. Прежде всего следует вводить вакцину лицам с повышенным риском осложнений (людям пожилого возраста, имеющим хронические воспалительные, обменные, гематологические заболевания, тяжелую неврологическую патологию и др.). Но следует помнить, что вакцина эффективна только против определенного типа
вируса. А предсказать, каким свойством будет обладать вирус, который вызовет очередную эпидемию, удается далеко не всегда. Поэтому и необходимую вакцину предусмотреть трудно. Вакцинацию следует проводить не позднее чем за 2 мес до предполагаемого начала эпидемии.
Экстренную профилактику проводят в период эпидемии гриппа. Довольно эффективной считается химиопрофилактика гриппа с помощью ремантадина, который применяют по 0,05 г 1 раз в сутки в течение 7 дней. Прием препарата следует начинать при появлении первого больного в семье (детям — с 13 лет) или среди сотрудников.
Оксолин обладает противовирусной активностью и применяется для профилактики гриппа в виде 0,25% оксолиновой мази. В период эпидемии рекомендуют двукратное ежедневное смазывание мазью слизистой оболочки носа.
Интерферон применяют преимущественно для экстренной защиты от гриппа и других ОРЗ детей дошкольного возраста. Человеческий лейкоцитарный интерферон выпускают в сухом виде в ампулах. Содержимое ампулы растворяют в 2 мл кипяченой воды комнатной температуры и закапывают в каждый носовой ход по 5 капель 2 раза в сутки с интервалом не менее б ч. Профилактический курс продолжают до тех пор, пока сохраняется опасность заражения.
При уходе за больным гриппом средством индивидуальной профилактики является марлевая маска.
Парагрипп
Парагрипп — острое вирусное заболевание с капельным механизмом передачи, протекающее с преимущественным поражением верхних дыхательных путей и умеренным токсикозом (лат. — parainfluenza, англ. — parainfluenza)*
Краткие исторические сведения. В 1956 г. R.Chanock выделил от ребенка, больного ложным крупом, вирус, названный им croupasso-ciated — СА (связанный с крупом), и описал его свойства. В последующие годы были описаны другие возбудители, вызывавшие заболевания, подобные гриппу. Б 1959 г. эти вирусы были выделены в самостоятельную группу и названы парагриппозными (ПГВ).
Актуальность. ПГВ распространены повсеместно. По данным ВОЗ, они вызывают около 10% всех ОРЗ в мире. По мнению отечественных исследователей, этот показатель еще выше (16—20%). Наиболее часто и тяжело этими вирусами поражаются дети первых лет жизни, у которых парагрипп иногда становится причиной летальных исходов. Ежегодно из каждых 100 заболевших болеют 20—40 детей в возрасте моложе 2 лет, 10—15 детей школьного возраста.
Причиной тяжелы* заболеваний у маленьких детей чаще являются ПГВ 1—3 типов.
Выявлена связь парагриппозной инфекции с бронхитом, пневмонией. Доказано, что вирус обладает сенсибилизирующими свойствами, что способствует формированию бронхоспастической обструкции и поливалентной аллергии, развитию тяжелых форм пара-гриппозной инфекции, в том числе и с поражением ЦНС. Высказывается мнение о причастности ПГВ к хроническим неврологическим заболеваниям. Медленное формирование нестойкого иммунитета, наличие различных типов вируса является причиной того, что человек неоднократно в течение года может болеть парагриппом. Возможность персистенции вируса в сочетании со способностью его проникать в клетки ЦНС требует уточнения связи ПГВ с медленными инфекциями.
Этиология. ПГВ входят в первый род парамиксовирусов семейства paramyxoviridae. Они разделяются на 4 антигенных типа (старое название — «гемадсорбирующие агенты») на основе особенностей компле-ментсвязывающих и гемагглютинирутощих антигенов.
ПГВ-1 включает штамм НА-2 вируса парагриппа человека и вирус Сендай, вызывающий парагрипп у мышей. Штаммы этого типа часто вызывают гемолиз куриных эритроцитов.
ПГВ-2 включает крупассоциированный штамм (СА), выделенный в 1956 г. R.Chanock, и вирусы парагриппа обезьян SV-5, DA и др.
К ПГВ-3 относят штаммы парагриппа человека и крупного рогатого скота.
ПГВ-4 включают штаммы двух подтипов — А и В. ПГВ обладают антигенной стабильностью. Несмотря на то что вирусы, подобные ПГВ-1, 2, 3, были изолированы и от животных, перекрестного инфицирования пока не зарегистрировано.
Размеры вирусных частиц — от 120 до 300 нм. Геном ПГВ состоит из однонитчатой РНК с молекулярной массой 5« 106 D. Геном парамиксо-вирусов не фрагментирован, как у вируса гриппа, что обеспечивает им антигенную стабильность. На поверхности вириона находятся два гли-копротеида — HN и F. Они же являются поверхностными антигенами ПГВ. Особенностью парамиксовирусов является наличие гемагглюти-нирующей и нейраминидазной активности на одной и той же молекуле HN. С гликопротеидом F связывают цитотоксическую и гемолитическую активность вируса. Гликопротеиды HN и F занимают по массе около 25% всей вирусной частицы. Внутри вирусной частицы находятся большой нуклеокапсидный белок, матриксный белок, полимераза, представленная фосфопротеином, и др.
ПГВ хорошо репродуцируются в культуре клеток почек человека, обезьян и некоторых других млекопитающих. Цитопатогенное действие проявляется в образовании синцития и цитоплазменных включений. Некоторые штаммы растут в куриных эмбрионах при заражении в амниотическую полость. В культуре клеток вирусы можно обнаружить, используя феномен гемадсорбции.
Моделировать парагриппозную инфекцию можно на восприимчивых животных — обезьянах, хомяках, белых крысах, белых мышах, морских свинках.
Зараженные ПГВ клетки нередко сохраняют способность к митозу. Вирус переходит при этом в дочерние клетки. В клеточных культурах получена персистентная инфекция ПГВ. В настоящее время доказана возможность формирования персистенции ПГВ-3 в организме человека. Этому явлению способствуют иммунодефицитные состояния, различные хронические заболевания.
ПГВ обладают тропностью к цилиндрическому мерцательному эпителию дыхательных путей подобно вирусам гриппа. Однако возбудители парагриппа иногда могут поражать клетки других органов и систем (например, клетки головного мозга).
Вирусы парагриппа нечувствительны к ремантадину. Получены обнадеживающие результаты испытания нового противовирусного препарата дейтифорина.
ПГВ нестойки во внешней среде, погибают при комнатной температуре в течение 2—4 ч.
4 Ж. Возианова
Иммунный ответ при парагриппе типоспецифичен и направлен против гликопротеидов вирусной оболочки. Вырабатываются при этом секреторные и сывороточные антитела, формируется клеточно-опосре-дованный иммунитет (цитотоксические Т-клетки). Несмотря на наличие иммунитета, возможны повторные заражения с развитием заболеваний, протекающих легче, чем при первичном инфицировании.
Эпидемиология. Источником инфекции является больной человек, возможно, вирусоноситель. Вероятно, большая часть заражений происходит от детей дошкольного возраста, так как заболеваемость парагриппом у них значительно выше, чем у взрослых. Продолжительность выделения вируса в окружающую среду — 3—10 дней (в острый период заболевания).
Механизм передачи инфекции при парагриппе — воздушно-капельный. Как и при гриппе, заражение осуществляется при вдыхании аэрозоля, образованного при кашле, чиханье, разговоре с больным парагриппом.
Восприимчивость к парагриппу практически всеобщая и зависит главным образом от возраста, причем разные типы ПГВ не одинаково поражают различные возрастные группы.
Заболевания, вызываемые ПГВ-1 и ПГВ-2, начинают регистрироваться у детей с 4—5-месячного возраста, когда угасает полученный от матери иммунитет. Заболеваемость сохраняется на высоком уровне до 6—7 лет, после чего значительно снижается. ПГВ-3 поражает новорожденных, несмотря на наличие материнских антител, при этом иногда бывают летальные исходы, связанные с поражением нижних дыхательных путей. К годовалому возрасту половина детей уже переносят парагриппозную инфекцию, вызванную ПГВ-3, в той или иной форме, а к 5 годам антитела к этому типу вируса регистрируются у 90% детей. Роль ПГВ-4 в патологии человека невелика. Этот тип ПГВ был впервые выделен у подростков, заболевания, вызванные им, регистрируются в виде спорадических случаев.
Заболеваемость парагриппом носит преимущественно спорадический характер с периодическими вспышками и эпидемиями. Для парагриппа, вызываемого ПГВ-1, характерна двухлетняя периодичность эпидемий, обусловленных ПГВ-2 — несколько лет. Эпидемические вспышки, вызываемые ПГВ-1 и ПГВ-2, обычно чередуются. На высоте подъема заболеваемости, вызванной одним из этих типов вируса парагриппа, другой тип не встречается (т.е. эти типы не вызывают сочетан-ного поражения).
ПГВ-3 обычно вызывает спорадические случаи. Он может встречаться одновременно с ПГВ-1 и ПГВ-2.
Характерна осенне-зимняя сезонность для ПГВ-1, ПГВ-2 и весенне-летняя для ПГВ-3.
Заболеваемость парагриппом значительно повышается в эпидемиче-
ские по гриппу периоды, что объясняется иммунодепрессивной способностью вируса гриппа.
Классификация. Существует лишь клиническая классификация, в основу которой положены преимущественная локализация процесса и тяжесть его течения.
В табл. 4 предлагается классификация клинических форм парагриппа (Е.С.Кетиладзе, 1967).
Таблица 4. Классификация парагриппа
|
Клиническая форма |
Локализация |
Клинические |
Общие |
Тяжесть |
|
поражения |
проявления |
симптомы |
течения | |
|
Парагрипп: острый |
Верхние ды- |
Ринит, реже |
Токсикоз |
Легкое |
|
риноларингит или |
хательные |
фарингит, ла- |
слабый или |
|
|
риноларинготрахеит |
пути |
рингит |
отсутствует |
|
|
Парагрипп: острый |
Нижние ды- |
Ларингит, ино- |
Лихорадка |
Среднетя- |
|
риноларинготрахеит |
хательные |
гда в сочета- |
непостоян- |
желое |
|
или риноларинготра- |
пути |
нии с трахеи- |
ная |
|
|
хеобронхит (бронхи- |
|
том, могут |
|
|
|
олит) |
|
присоединяться бронхит, бронхиолит |
|
|
|
Парагрипп: острый |
Легкие |
Пневмония |
Выражен- |
Тяжелое |
|
риноларингит. Пнев- |
|
|
ный токси- |
|
|
мония. Или: острый |
|
|
коз |
|
|
риноларинготрахео- |
|
|
|
|
|
бронхит. Пневмония |
|
|
|
|
При любой клинической форме парагриппа может возникнуть такое осложнение, как ложный круп, что бывает причиной смерти. Поражение легких может быть обусловлено как вирусом парагриппа, так и вторичной бактериальной флорой (протекает по типу микст-инфекции).
Примерная формулировка диагноза. 1. Острый парагриппозный риноларингит, легкое течение.
Парагриппозная пневмония, тяжелое течение.
Парагрипп, ложный круп, тяжелое течение.
Патогенез. Патогенез парагриппа во многом сходен с патогенезом гриппа. Существенными отличиями его являются кратковременность и низкая интенсивность вирусемии, меньшая выраженность иммунодеп-рессии. В патогенезе парагриппа можно выделить следующие стадии.
1. Проникновение вируса в эпителиальные клетки дыхательных путей и репликация в них. Проникая в дыхательные пути, большая часть вирусных частиц оседает на слизистой оболочке носа и гортани. Но при условии преодоления факторов неспецифической резистентности (вязкая слизь, ингибиторы, движение ресничек мерцательного эпителия), а при повторных заражениях и местного иммунитета (секреторные антитела, клеточный иммунитет) вирус проникает в поверхностные эпителиальные клетки дыхательных путей и начинает в них размножаться. Установлено, что вирусные частицы накапливаются в цитоплазме пораженных клеток.
Выход вируса, разрушение пораженных клеток. Освободившись из эпителиальных клеток, вирионы проникают в соседние клетки, повторяя циклы репликации. При этом максимально поражается эпителий слизистой оболочки носа, гортани, меньше — трахеи. ПГВ-3 с большим постоянством поражает эпителий нижних дыхательных путей, особенно у детей 1-го года жизни. Выход вирусных частиц сопровождается некрозом пораженных клеток. Небольшое количество вирусов может проникать в кровь.
Развитие катарального синдрома, вирусемии, токсемии. В слизистой оболочке дыхательных путей развивается воспалительный процесс, наиболее выраженный в местах максимальной репродукции вируса (гортань, нижние дыхательные пути у детей). В меньшей степени, чем при гриппе, поражаются трахея и бронхи. Воспаление сопровождается резкой гиперплазией эпителия, ядра клеток становятся крупными, светлыми, хроматин располагается по периферии. В острую стадию, на 4—5-й день болезни, выявляют выраженную лимфоидную инфильтрацию эпителия пораженных отделов с мелкими очагами дегенерации. Нередко возникает перибронхиальный отек. Одним из наиболее характерных морфологических признаков парагриппа является своеобразное подушкообразное разрастание эпителия в мелких и средних бронхах. Подобные мелкоочаговые разрастания наблюдаются и в легочной ткани вокруг бронхиол. Обычно, особенно у детей первого года жизни, при этом отмечают довольно заметные изменения мелких кровеносных сосудов легких: стенки их отечны, с набухшим эпителием, периваскулярным отеком. В легких выявляют умеренной плотности очаги. Все эти изменения дают клинику ларингита, бронхита, пневмонии, могут возникнуть явления дыхательной недостаточности, особенно у детей (сужение просвета трахеи и бронхов за счет отека окружающих тканей, рефлекторный ларингоспазм, поражение нижних дыхательных отделов).
Несмотря на кратковременность и низкую интенсивность вирусемии, она оказывает влияние на различные органы и ткани. Изменения структуры клеток находят практически во всех органах. Более того, вирус ПГВ-3 обладает определенной тропностью к ЦНС, где его можно обнаружить преимущественно в эпителиальных клетках хориоидаль-ных сплетений, эпендимоцитов желудочков мозга. Результатом этого являются гемо- и ликвородинамические нарушения.
Кратковременность вирусемии обусловливает меньшую по сравнению с гриппом интоксикацию, менее выраженное мотальное поражение сосудов. Однако в некоторых случаях токсикоз может быть весьма значительным.
Угнетение иммунитета при парагриппе выражено в меньшей степени, чем при гриппе или PC-инфекции. Отмечают снижение ответа лимфоцитов на Т-клеточный митоген с первых дней заболевания. Иногда уменьшается содержание Т-лимфоцитов в периферической крови. В связи с этим возможно присоединение бактериальных осложнений.
При крупе имеется дефект супрессорной функции. Размножение лимфоцитов сопровождается выделением гистаминстимулирующего фактора, что приводит к накоплению избыточных количеств гистами-на и стенозу гортани.
4. Формирование иммунитета, реконвалесценция. Механизм выздоровления от парагриппа до конца не изучен. Сывороточные антитела, как и при гриппе, вряд ли имеют серьезное значение в борьбе с начавшейся инфекцией, особенно при первой встрече с вирусом. Их наличие расценивают как показатель относительной защищенности человека от заражения. Они могут играть роль в подавлении активности пер-систирующего вируса.
Секреторные антитела появляются в ближайшие дни от начала болезни, однако зависимости между их титрами и клиническим течением заболевания не выявлено. Показателем активности иммунитета является уровень специфических IgA в отделяемом из носа.
Наибольшую роль в локализации инфекции и в процессах выздоровления играет клеточный иммунитет. В эксперименте эффекторные клетки (Т-киллеры) появляются перед повышением титра вируснейтра-лизующих антител, что совпадает по времени с исчезновением вируса из легких инфицированных животных. Этим подтверждается их роль в механизме выздоровления.
Параллельно с формированием иммунного ответа идет процесс регенерации эпителия слизистой оболочки дыхательных путей.
По-видимому, в результате мобилизации всех факторов защиты в большинстве случаев происходит полное очищение организма от возбудителя. Вместе с тем, у некоторых больных возможно формирование вирусоносительства. Причины этого явления изучены недостаточно. Персистенция вирусов парагриппа выявлена у больных хроническим бронхитом и бронхиальной астмой, сопровождающимися иммунодефицитом IgA и IgM.
Повторные заболевания парагриппом протекают обычно легче. Особенности возникновения отдельных симптомов, наиболее часто встречающихся при парагриппе, представлены в табл. 5.
Клиника.
Инкубационный
период длится 3—6 дней. Чаще заболевание
начинается постепенно, хотя описаны
случаи острого начала. У большинства
больных температура тела не превышает
38 "С. Иногда лихорадка отсутствует.
Продолжительность лихорадочного
периода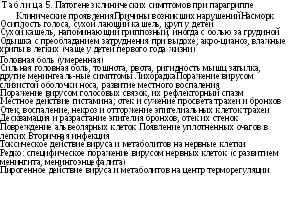
широко варьирует: от 1 до 8 дней у взрослых и до 14 дней у детей. Чем старше ребенок, тем легче у него протекает заболевание.
Первыми симптомами парагриппа обычно являются заложенность носа, сухой кашель, першение или незначительная боль в горле. В последующие дни количество выделений из носа увеличивается. Вначале они носят серозный, затем серозно-слизистый характер. Количество выделений больше, чем при гриппе, но меньше, чем при аденовирусной и риновирусной инфекциях. Появление гнойных выделений свидетельствует о присоединении бактериальных осложнений.
Типичным для парагриппа считается развитие ларингита и ларинго-трахеита с грубым лающим кашлем, иногда болью за грудиной, охриплостью или осиплостью голоса. Вместе с тем, некоторые клиницисты считают, что роль симптома ларингита в клинической диагностике парагриппа у взрослых преувеличена, частота ларингитов у них составляет менее 20%.
Из катаральных явлений у взрослых чаще всего отмечают ринофа-рингит на фоне незначительной или умеренно выраженной интоксикации. Последняя проявляется слабостью, недомоганием, нерезкой го-
ловной болью в области лба, висков или глазных яблок. Мышечная боль, потливость, адинамия, рвота бывают редко.
Цвет лица при парагриппе чаще нормальный, но иногда бывает бледность или гиперемия. При исследовании ротоглотки выявляют неяркую гиперемию дужек и мягкого неба, в меньшей степени — задней стенки глотки. Нередко шейные и подчелюстные лимфатические узлы слегка увеличены.
В легких везикулярное дыхание, иногда с жестковатым оттенком. Пульс обычно соответствует температуре, артериальное давление остается неизмененным.
Тяжесть течения парагриппа определяется локализацией поражения и находится в обратной зависимости от возраста больных. Но существенное влияние на тяжесть течения и клиническую симптоматику оказывают хронические воспалительные заболевания, если они имеются у больного.
При легком течении заболевание начинается постепенно, температура тела нормальная или субфебрильная. Интоксикация практически отсутствует. Ведущими симптомами являются кашель, нередко лающий, но не приносящий больному большого беспокойства, першение в горле, незначительное серозное отделяемое из носа. Такие больные чаще всего к врачам не обращаются, не лечатся, в связи с чем все симптомы могут затягиваться (на 2 нед и более).
При среднетяжелом течении в процесс вовлекаются нижележащие отделы дыхательных путей, добавляются явления трахеобронхита и даже бронхиолита. Температура тела может достигать 38 °С и более. Отчетливее выражены явления токсикоза. Эта форма по клинике очень напоминает грипп среднетяжелой формы, дифференциальная диагностика с которым бывает непростой. Но нет отека и гиперемии лица, в большинстве таких случаев кашель носит типичный лающий характер.
В последние годы все больше утверждается мнение о том, что отношение к парагриппу как к легко протекающему у взрослых заболеванию явно связано с незнанием или недооценкой этой инфекции.
Тяжелое течение парагриппа характеризуется выраженным токсикозом, признаками поражения как дыхательной системы, так и ЦНС. Болезнь в этих случаях нередко начинается остро с озноба, повышения температуры тела до 39—40 "С, хотя возможно и более постепенное начало с продромальных явлений в течение 2—3 дней в виде слабости, разбитости, расстройства сна, ломоты в теле.
На высоте температуры появляются головная боль распирающего характера, ломота во всем теле, озноб, могут возникать слуховые и зрительные галлюцинации, тошнота. Одновременно появляются характерный кашель, изменение голоса, затрудненное носовое дыхание. При осмотре больного обращают на себя внимание бледность кожных покровов, незначительные изменения в ротоглотке в виде умеренной гиперемии. Могут появляться менингеальные знаки. Иногда у таких больных развивается типичная картина менингита. Длительность лихорадочного периода — до 7—8 дней, но при присоединении бактериальных осложнений он затягивается. Критическое падение температуры может сопровождаться коллапсом.
При тяжелом течении нередко возникает парагриппозная пневмония, которая может сопровождаться явлениями дыхательной недостаточности. У детей первого года жизни парагриппозная инфекция, вызванная ПГВ-3, чаще всего протекает с тяжелыми бронхиолитом и пневмонией, что может привести к летальному исходу. ПГВ-1 и ПГВ-2 часто вызывают у детей клинику острого ларингита с явлениями стеноза гортани. Течение парагриппозного (ложного) крупа обычно благоприятное и редко требует интубации или оперативного вмешательства. Но следует помнить, что от 30 до 45% всех случаев ложного крупа у детей приходится на долю парагриппозной инфекции.
Заболевание, вызванное ПГВ-4, часто протекает легко или даже суб-клинически, особенно у взрослых.
Осложнения. К редким осложнениям, наблюдаемым в острый период заболевания, относятся парагриппозные менингит и менингоэнце-фалит. Как указывалось выше, возможно прямое поражение ПГВ нервных клеток. При этом отмечают головную боль, тошноту, рвоту, бессонницу. Положительны симптомы Кернига, Брудзинского, имеется ригидность затылочных мышц. Давление спинномозговой жидкости умеренно повышено, лимфоцитарный плеоцитоз может достигать 400—500 клеток в 1 мм3. Менингеальные симптомы иногда удерживаются до 2—2,5 нед.
Но менингит и менингоэнцефалит, как и парагриппозную пневмонию, можно рассматривать не как специфические, обусловленные непосредственным действием вируса, осложнения, а как варианты течения парагриппозной инфекции.
К числу ранних, довольно частых у детей и редких у взрослых осложнений относится ложный круп. Он обычно возникает в разгар болезни, внезапно, чаще в ночное время. Появляется ощущение нехватки воздуха. Больной беспокоен, мечется в постели, у него нарастают цианоз, тахикардия. В таких ситуациях нужно немедленно применить отвлекающие средства, бронхолитики, спазмолитики.
Большая часть осложнений при парагриппе обусловлена вторичной бактериальной инфекцией. Наиболее частым таким осложнением является пневмония, которая обычно развивается на 4—5-й день болезни, но иногда и в более ранние сроки. При этом усиливается кашель, отмечается ухудшение общего состояния, температура повышается до более высоких показателей, появляется головная боль, увеличивается количество мокроты, в которой бывает примесь крови. Иногда появляется боль в боку при дыхании. Чаще поражаются нижние доли легких,
воспалительный процесс обычно носит очаговый характер. Над участком пораженной легочной ткани выслушивают влажные хрипы, укорочен перкуторный звук. Изменяется картина крови — появляется лейкоцитоз с нейтрофильным сдвигом. Из мокроты можно выделить пневмококки, стафилококки, гемофильную палочку, энтеробактерии и др. Особенно тяжело протекает пневмония, развившаяся с первых дней болезни (чаще у детей). Обычно бактериальная пневмония возникает при наличии хронических воспалительных очагов в легких, бронхах, миндалинах. Суперинфекция при неотягощенном анамнезе при парагриппе — довольно редкое явление. На фоне сниженной реактивности могут возникать синусит, отит.
Исходы. Обычно течение парагриппа благоприятное. Подавляющее большинство больных выздоравливают, и организм освобождается от вируса. У детей (чаще 1-го года жизни) иногда регистрируют летальные исходы в результате поражения нижних дыхательных путей (бронхио-лит, пневмония) или от ложного крупа при неадекватной терапии.
Требуют уточнения роль ПГВ в формировании хронических воспалительных процессов (хронический бронхит, бронхиальная астма, хроническое неврологическое заболевание) и механизм развития перси-стенции.
Методы диагностики. Общеклинические методы исследования
практического значения в диагностике парагриппа не имеют. Обычно парагрипп не вызывает у взрослых заметных сдвигов в формуле крови. Иногда в первые 2 дня болезни отмечают небольшой лейкоцитоз со сдвигом формулы влево. В дальнейшем определяется тенденция к некоторой лейкопении. СОЭ остается в пределах нормы. Нарастание лейкоцитоза свидетельствует о развитии бактериальных осложнений.
Симптоматика, свидетельствующая о поражении нервной системы, может сопровождаться изменениями в спинномозговой жидкости: повышается ликворное давление, в прозрачной жидкости обнаруживают относительно невысокий цитоз (до 100 клеток и более в 1 мл) в сочетании с нормальным уровнем белка и сахара.
Специфические методы. В первые дни болезни диагноз может быть подтвержден с помощью РФА, что позволяет выявить возбудителя в бронхиальном секрете уже в первые часы болезни.
Ретроспективно диагноз парагриппа подтверждают серологическим методом. В РТГА и РН исследуют парные Сыворотки больных, взятые с интервалом 10—14 дней. Четырехкратное, нарастание титра антител подтверждает диагноз. Следует помнить, что возбудители из группы парамиксовирусов могут давать перекрестные реакции за счет наличия общих антигенов. Кроме того, интервала 10—-14 дней бывает недостаточно при парагриппе для подтверждения диагноза при исследовании парных сывороток, так как нарастание титров антител при парагриппе идет очень медленно, иногда необходимое увеличение их можно получить лишь к концу 3—4-й недели. Поэтому серологические реакции не всегда дают достоверную информацию.
Вирусологический метод — выделение вируса в культуре ткани (культура почек эмбриона человека или обезьян) — доступен лишь специальным лабораториям. При этом вирус обнаруживается благодаря вызываемому им цитопатическому или гемаглютинирующему действию.
Дополнительные методы. Информативными в отдельных случаях могут оказаться такие методы, как ЭКГ, рентгенография легких.
Критерии диагноза. Диагноз парагриппа в типичных случаях основывается на следующих данных:
эпидемиологическая ситуация, свидетельствующая о росте числа больных с ларинготрахеитом в детских коллективах;
осенне-зимний или весенний период;
постепенное начало заболевания, вялое течение, незначительные явления интоксикации;
явления ринофарингита, ларингита (серозное отделяемое из носа, першение в горле, лающий кашель);
«спокойная» гемограмма.
Диагноз подтверждают специфическими методами исследования (РФА, серологические методы).
Дифференциальный диагноз. Клиническую дифференциальную диагностику парагриппа с другими ОРВИ легче проводить у детей. Высокая частота поражения гортани с проявлением характерных симптомов упрощает задачу распознавания заболевания. Значительные трудности вызывает клиническое распознавание парагриппа у взрослых, так как развитие симптомов ларингита отмечается лишь у небольшой части больных. Этим можно объяснить то обстоятельство, что практические врачи редко диагностируют парагрипп. Большинство случаев парагриппа скрывается под общим диагнозом ОРВИ.
Более того, больные парагриппом сравнительно редко обращаются к врачу в первые дни заболевания, продолжая работать и инфицировать окружающих. Обычно причиной обращения за медицинской помощью являются возникшие в различные сроки осложнения или (что бывает реже) тяжелое течение болезни.
Тем не менее при внимательном осмотре больного, тщательно собранном анамнезе нередко все же удается провести дифференциальную диагностику с другими ОРВИ.
Дифференциальная диагностика с гриппом изложена в разделе «Грипп».
Клинически отличить парагрипп от PC-инфекции часто непросто. Постепенное начало, локализация патологического процесса (носоглотка, нижние дыхательные пути), возможность ларингита — все эти признаки характерны для обоих заболеваний, но PC-инфекцию отличают такие особенности:
более выраженная интоксикация;
выше лихорадка (температура тела нередко достигает 38—39 °С);
кашель часто носит приступообразный характер, сопровождаясь одышкой экспираторного типа;
у детей может развиться астматический синдром; иногда бывают склерит, конъюнктивит, гранулезный фарингит;
характерно частое поражение бронхиол и легких с возникновением участков ателектазов и эмфиземы, что выявляется как перкутор-но и аускультативно, так и рентгенологически.
Но формы PC-инфекции, развивающиеся по типу назофарингита или бронхита, отличить от парагриппа удается лишь с помощью специальных методов исследования.
Для риновирусной инфекции характерны:
— обильное серозное отделяемое из носа (ринорея);
— частое чиханье при незначительном интоксикационном синдроме;
— отсутствие, как правило, явлений фарингита. Аденовирусные заболевания многолики. Но в большинстве случаев появляются симптомы, которые не характерны для парагриппа:
— боль и (или) першение в горле сопровождают гранулезный фарингит; кашель при этом весьма умеренный;
закономерно увеличение миндалин, а также подчелюстных и шейных лимфатических узлов;
возможно возникновение катарального, фолликулярного или пленчатого конъюнктивита (преимущественно одностороннего);
— нередко увеличиваются печень и селезенка;
заболевания, как правило, начинаются остро, протекают более длительно;
интоксикация в большинстве случаев значительнее, чем при парагриппе, температура тела выше.
С микоплазменной инфекцией приходится проводить дифференциальную диагностику в тех случаях, когда она протекает по типу ОРЗ без пневмонии.
Но в отличие от парагриппа:
— заболевание сопровождается болью в горле, диффузной гиперемией слизистой оболочки ротоглотки, увеличением миндалин; возможно увеличение подчелюстных лимфатических узлов;
— часто возникают склерит и конъюнктивит.
Першение в горле, ринит в сочетании с весьма умеренной интоксикацией могут встречаться и при менингококковом назофарингите, но для него характерны:
— гнойное отделяемое из носа с 1-го дня заболевания;
отек задней стенки глотки с гипертрофированными фолликулами;
истечение содержимого полости носа в виде гнойных «дорожек» по задней стенке глотки;
отсутствие кашля, бывает покашливание (отхаркивание) при избыточном затекании отделяемого из носа;
выявление при микроскопии отделяемого из носа лейкоцитов в большом количестве, диплококков, расположенных в них внутриклето-чно.
При парагриппозном ларингите прежде всего необходимо исключить дифтерию, которая может сопровождаться осиплостью голоса, нарушением дыхания (при наличии крупа). Для дифтерии характерны:
— выраженная прогрессирующая интоксикация;
типичные отложения на миндалинах, голосовых связках и даже трахее; выраженный отек тканей ротоглотки;
истинный круп (возникающий при дифтерии круп отличается от ложного парагриппозного крупа постепенным развитием, нарастающими признаками удушья и симптомов общей интоксикации; типичными местными изменениями на голосовых связках, в трахее);
круп при дифтерии возникает в любое время суток, при поражении трахеи он развивается у взрослых так же часто, как и у детей;
— в крови — нейтрофильный лейкоцитоз.
Лечение. Лечение взрослых больных парагриппом проводят в основном в домашних условиях. Госпитализацию осуществляют лишь по эпидемиологическим показаниям. Дети с тяжелой формой парагриппа безусловно подлежат госпитализации.
В острый период заболевания соблюдают постельный режим. Лечебное питание не требуется. Предпочтение следует отдавать легкоусвояемой пище, богатой витаминами.
Этиотропное лечение парагриппа не разработано. Детям в случаях тяжелого течения заболевания (с крупом, бронхитом, пневмонией) рекомендуют введение любого донорского иммуноглобулина (внутримышечно 3 мл) в первые дни болезни в расчете на наличие у доноров анамнестических антител против ПГВ и на его неспецифическое стимулирующее действие. Но о современном критическом отношении к иммуноглобулинам говорилось уже неоднократно.
Принципы патогенетической и симптоматической терапии парагриппа аналогичны таковым при гриппе (см. соответствующий раздел). Лечебные мероприятия должны быть направлены на поддержание естественных защитных реакций организма. Не следует использовать жаропонижающие препараты (к тому же при парагриппе в них редко возникает необходимость).
При явлениях ларингита показаны паровые ингаляции. Развитие ложного крупа у детей требует применения паровых ингаляций, горячих
ножных ванн, горчичников, антигистаминных препаратов (тавегил, ди-азолин, супрастин в соответствующих возрасту дозах), лишь в тяжелых случаях показаны спазмолитики и глюкокортикостероиды. Необходимость в трахеостомии обычно не возникает.
При развитии осложнений назначают антибиотики. Принципы лечения пневмонии такие же, как и при гриппе.
Порядок выписки из стационара. Выписку реконвалесцентов из стационара осуществляют по клиническим показаниям, после нормализации температуры тела и угасания катарального синдрома. Диспансеризации подлежат лишь дети, перенесшие парагрипп, осложненный пневмонией.
Профилактика. Общая профилактика, описанная в разделе «Грипп», актуальна для всей группы ОРВИ.
Специфическая профилактика парагриппа изучена недостаточно. В нашей стране разработана и испытана живая вакцина, включающая ПГВ трех типов, но до стадии промышленного выпуска она пока не доведена. Представляет интерес разработка субъединичных вакцин, содержащих поверхностные антигены HN и F.
В порядке экстренной профилактики во время подъема заболеваемости применяют 0,25 % оксолиновую мазь, а также интерферон (дозу и кратность приема см. в разделе «Грипп»).
Риновирусная инфекция
Риновирусная инфекция — острое респираторное вирусное заболевание, протекающее с преимущественным поражением слизистой оболочки носоглотки, обильной риноре-ей и в типичных случаях — слабо выраженными симптомами интоксикации (лат. — morbus rhinoviralis, англ. — common cold).
Краткие исторические сведения. Первые доказательства заразности «простуды» (common cold) представил W.Kruse в 1914 г., заражая добровольцев фильтратами слизи, взятой из носа у больных. В 1930 г. A.Dochez с коллегами доказал, что заболевание может быть передано через фильтраты слизи, свободные от бактерий, и предположил вирусную его этиологию. Большой объем работы по изучению заразного насморка проделали C.Andrewes и D.Tyrell с сотрудниками, однако попытки изолировать вирус от больных и инфицированных добровольцев длительное время оставались безрезультатными. Лишь с середины 50-х годов начался качественно новый этап в изучении этого заболевания, когда W.Price (1956) и W.Pelon (1957) независимо друг от друга выделили новый вирус, впоследствии названный rhinovirus 1А. В последующие годы было выделено множество новых различных серотипов ри-новирусов, и заболевание, вызванное ими, получило название «риновирусная инфекция».
Актуальность. Риновирусная инфекция занимает важное место в патологии человека, так как риновирусы имеют широчайшее распространение на всех континентах. Подсчитано, что человек переносит в среднем 2—3 острых респираторных заболевания в год, из них 0,5—0,7 заболеваний вызывается риновирусами. Удельный вес риновирусной инфекции становится еще выше осенью и весной — до 40% от общего числа ОРВИ.
Несмотря на легкость и относительную непродолжительность заболевания, оно все же обусловливает значительные трудопотери из-за своей массовости. К тому же риновирусы, так же как и возбудители других ОРВИ, иногда провоцируют бактериальные осложнения, обостряют течение хронических воспалительных процессов.
Количество серотипов риновирусов так велико, что человек, заражаясь ежегодно новым вирусом, может болеть всю жизнь. До настоящего времени эффективных методов профилактики риновирусной инфекции не существует.
Этиология. Риновирусы относятся к семейству Picomaviridae, куда входят также энтеровирусы. По-видимому, они происходят от общего
вируса-предшественника. Вирусные частицы имеют размеры от 20 до 40 нм, содержат однонитчатую РНК. Капсиду присуща кубическая симметрия. В естественном состоянии вирусы содержат поверхностные типоспецифические антигены. В настоящее время известно более 110 серотипов риновирусов и субтип 1А. Для риновирусов оспаривается возможность антигенного шифта, но не исключается вероятность антигенного дрейфа, что может быть причиной повторного заражения тем же типом вируса вскоре после перенесенного заболевания.
Риновирусы устойчивы к эфиру и чувствительны к кислотам.
В окружающей среде риновирусы нестойки, до 3 ч они выживают на коже и на поверхности различных предметов, чувствительны к высыханию. Гемагглютинации и гемолиза не вызывают.
Вирусы не удается культивировать на куриных эмбрионах и мелких лабораторных животных. Получены экспериментальные модели рино-вирусной инфекции на гиббонах и шимпанзе, однако основная масса исследований проведена на добровольцах. Для выделения вирусов используют культуры эмбриональных клеток легких и почек человека или приматов (чаще макаки-резус). В зависимости от способности к росту на человеческих (human) или обезьяньих (monkey) клеточных культурах риновирусы делят на Н- и М-штаммы соответственно. Это деление довольно условно, т.к. показана возможность адаптации Н-штаммов к росту на почечных клетках обезьяны. Имеются штаммы (О-штаммы), которые размножаются только в культурах мерцательного эпителия носа и трахеи человека. Температурный оптимум роста + 33... + 35 "С, что соответствует температуре слизистой оболочки полости носа. При повышении температуры тела до 37 °С выход вируса из клетки резко снижается. До настоящего времени не получены химиопрепараты, которые бы действовали на возбудителя in vivo.
Перенесенная инфекция обусловливает появление строго типоспе-цифического нестойкого (продолжительностью около 2 лет) иммунитета. Учитывая большое количество серотипов, человек может неоднократно болеть риновирусной инфекцией в течение года, тем более, что перекрестный иммунитет к различным серотипам не формируется из-за отсутствия общих групповых антигенов.
Эпидемиология. Источником инфекции является инфицированный человек с симптомами болезни или без таковых (субклиническая форма инфекции). Наибольшую опасность для окружающих представляет больной на 2—3-й день болезни, что совпадает с максимальным содержанием вируса в носовом секрете. При исследовании носоглоточных смывов у добровольцев небольшие количества вируса обнаруживали в течение 2 нед, что, очевидно, соответствует продолжительности контагиозное™ больных.
Основной механизм передачи риновирусов — воздушно-капельный. Вместе с тем, вероятно, значительная часть заражений осуществляется путем переноса вируса загрязненными руками на слизистую оболочку носа или конъюнктиву (контактно-бытовой путь), что подтверждается экспериментальными данными. Заражение добровольцев легко удается путем закапывания в нос жидкости, содержащей даже ничтожные количества вируса.
Восприимчивость к риновирусной инфекции всеобщая. Несколько чаще болеют школьники по сравнению со взрослыми, что связано, по-видимому, с более тесным и постоянным контактом. Но, как правило, в случае, если болеет кто-либо из членов семьи, в течение короткого времени заболевают все остальные. Соотношение клинически выраженных и инаппарантных форм составляет 3:1.
Максимум заболеваемости приходится на сентябрь. Зимой она снижается, но в апреле-мае нередко наблюдают второй пик подъема. Вспышки нередко возникают при теплой погоде, поэтому такой провоцирующий фактор, как переохлаждение, при риновирусной инфекции имеет меньшее значение. В тропиках заболеваемость повышается в сезон дождей.
Несмотря на формирование типоспецифического иммунитета, человек в течение года может болеть до 5—6 раз (новый тип вируса, реин-фекция при слабом иммунном ответе на предшествующее заболевание). В коллективе одновременно может циркулировать несколько типов риновирусов, что способствует длительному течению болезни у членов этого коллектива за счет новых заражений другим типом.
Классификация. По тяжести выделяют легкое и среднетяжелое течение риновирусной инфекции. Главные критерии тяжести — выраженность ринита и наличие осложнений. Тяжелое течение встречается очень редко. Заболевание может протекать в манифестной или субклинической форме.
Примерная формулировка диагноза. 1. Риновирусная инфекция, легкое течение.
2. Риновирусная инфекция, течение средней тяжести. Правосторонний гайморит.
Патогенез. Патогенез риновирусной инфекции изучен недостаточно. Главным местом внедрения и репликации вируса является слизистая оболочка носа, ее призматический мерцательный эпителий. Одной из вероятных причин указанной тропности вируса является температура поверхностного слоя этого участка дыхательных путей, соответствующая оптимальным условиям для репликации возбудителя (33—35 °С). Подобным же образом можно объяснить и редкую (наблюдаемую чаще у детей) поражаемость риновирусами нижних дыхательных путей, где температура слизистой оболочки у взрослых на несколько градусов выше.
Роль факторов неспецифической резистентности в защите от риновирусов, по-видимому, невелика. Исходно здоровые добровольцы мо-
гут быть легко заражены ничтожно малыми дозами вируса при отсутствии у них иммунитета к используемому штамму. Устойчивость к заражению прямо пропорциональна титрам секреторных и сывороточных антител к циркулирующему штамму, прежде всего уровню IgA и IgG в носовом секрете.
При условии преодоления факторов местной защиты дыхательного аппарата вирус проникает в клетки слизистой оболочки. Репликация происходит в цитоплазме инфицированной клетки без ее разрушения. Более того, первые циклы репликации не сопровождаются какими-либо морфологическими и (или) функциональными изменениями в клетках слизистой оболочки. Определяется лишь выраженный отек под-эпителиальной соединительной ткани с редкой инфильтрацией ее ней-трофилами, лимфоцитами, плазматическими клетками и эозинофила-ми, и значительно повышена активность желез, продуцирующих слизь, которая содержит большое количество белка, Ig. Полагают, что при ри-новирусной инфекции вирус выступает в роли стимулятора выработки местно различных химических медиаторов, что и обусловливает клиническую картину болезни. Затем наступает выраженный отек слизистого и подслизистого слоев, расширение и кровенаполнение сосудов, усиливается секреция слизи.
Уже через 1 сут после заражения вирус появляется в носовом секрете, что совпадает по времени с началом ринореи. Отделяемое вначале носит серозный, затем серозно-слизистый характер. Появление гнойных выделений свидетельствует о присоединении бактериальной флоры, размножение которой становится возможным благодаря предшествовавшему действию риновирусов, ослабляющих факторы местной защиты.
Генерализация риновирусной инфекции не наступает, так как естественная температура внутренней среды организма (выше 37 °С) губительно действует на вирус. Секреторные и сывороточные антитела появляются слишком поздно (к концу 2-й недели болезни и позже), чтобы играть какую-либо роль в выздоровлении. Есть все основания полагать, что в механизмах выздоровления при риновирусной инфекции, как и при других ОРВИ, важную роль играют клеточный иммунитет и интерферон, хотя этот вопрос изучен недостаточно.
Устойчивость к последующему заражению тем же вирусом пропорциональна титрам сывороточных и секреторных антител, хотя в опыте удавалось заражать добровольцев с очень высокими титрами антител, используя большие дозы вируса.
Постинфекционный иммунитет типоспецифичен и непродолжителен. Вместе с тем, доказано существование неспецифической резистентности к инфицированию риновирусами после недавней инфекции, вызванной гетерологичным штаммом.
К концу 2-й недели от начала болезни обычно завершается регенерация слизистой оболочки.
Клиника. Инкубационный период составляет 1—6 дней (в среднем 2—3 дня). Чаще болезнь начинается остро, с небольшого познабливания, возможно повышение температуры до уровня субфебрильной. В первые же часы заболевания появляются чиханье, заложенность носа, сухость и першение в горле, иногда в сочетании с умеренной болью. Ранним и наиболее характерным симптомом является насморк. Объем жидких серозных выделений настолько велик, что степень выраженности ринита можно оценивать по количеству использованных за день носовых платков. Носовое дыхание затруднено, а часто и невозможно из-за выраженного отека слизистой оболочки. Появляются боль в области носа и придаточных пазух, недомогание, отсутствует обоняние, притупляются вкусовые ощущения, иногда появляется нерезкая головная боль в области лба. У некоторых пациентов возникает легкий катаральный конъюнктивит со слезотечением. Кожа вокруг носовых отверстий часто мацерирована, впоследствии отмечается ее шелушение.
При осмотре ротоглотки выявляется неяркая гиперемия мягкого неба и задней стенки глотки. Миндалины обычно интактны. Могут слегка увеличиваться и становиться чувствительными при пальпации подчелюстные и переднешейные лимфатические узлы. Изредка возникает ларингит, сопровождающийся покашливанием и небольшой осиплостью голоса. Поражение нижележащих дыхательных путей расценивается многими клиницистами как редкое явление, так как размножение риновирусов в трахее и бронхах маловероятно из-за относительно высокой местной температуры. Вместе с тем, есть данные, что кашель регистрируется почти у 40% больных риновирусной инфекцией. Полагают, что он чаще всего является следствием обострения хронического патологического процесса в легких и бронхах, присоединения вторичной инфекции, проявлением сенсибилизации (особенно у детей).
У большинства больных температура остается нормальной на протяжении всего периода болезни. У некоторых она может повышаться до субфебрильной, редко достигая 38 °С. Длится лихорадка не более 2—3 дней. У детей же, особенно младшего возраста, риновирусная инфекция может сопровождаться высокой температурой (до 38—39 °С). У них чаще бывают и осложнения, обусловленные бактериальной флорой. Болезнь у взрослых протекает обычно в легкой форме и длится в среднем 1 нед с максимальной выраженностью клинических проявлений (ринореей) на 2—3-й день. Вместе с тем почти у каждого четвертого больного симптомы ринита могут удерживаться до 2 нед. На более продолжительный срок болезнь может затягиваться лишь за счет присоединения бактериальной флоры. У 1/3 больных заболевание протекает в субклинической форме.
Осложнения. К ранним и наиболее типичным осложнениям риновирусной инфекции можно отнести синусит, отит и гайморит, возникающие иногда на 3—5-й день болезни. Развитию этих осложнений способствует выраженный отек слизистой оболочки носоглотки. При этом частично или полностью перекрываются отверстия, через которые придаточные пазухи сообщаются с полостью носа, суживаются также просветы отверстий евстахиевых труб. Ухудшение дренажа создает благоприятные условия для активации вторичной бактериальной флоры. Имеет значение и снижение местной резистентности, обусловленное действием вируса. К редким осложнениям, наблюдаемым в более поздние сроки, относятся пневмония, мастоидит, гнойный менингит. Имеются сведения о том, что риновирусная инфекция провоцирует астматические приступы у детей. Частые риновирусные заболевания отягощают течение хронического легочного процесса, вплоть до развития дыхательной недостаточности.
Исходы. Заболевание протекает, как правило, благоприятно и заканчивается полным выздоровлением. Исходы осложненных форм определяются характером и тяжестью этих осложнений, своевременностью и адекватностью проводимого лечения.
Методы диагностики. Общеклинические методы диагностической ценности не имеют, изменения в периферической крови незначительны и непостоянны. Появление нейтрофильного лейкоцитоза указывает на наличие бактериальных осложнений.
Специфическая диагностика. Диагноз риновирусной инфекции можно подтвердить выделением возбудителя из носоглоточной слизи на культуре эмбриональных клеток или почек человека. Метод информативен, однако применение его ограничено из-за технической сложности. Куриные эмбрионы непригодны для выделения риновирусов.
Более доступны методы серологические. В реакции нейтрализации (РН) или в РСК исследуют парные сыворотки. Учитывая позднее появление антител, первую сыворотку следует брать в первые дни болезни, а вторую — не ранее чем через 2 нед. Четырехкратное нарастание титра антител является ретроспективным доказательством перенесенной риновирусной инфекции. В серологических реакциях используют смесь антигенов разных серотипов риновирусов. В практическом здравоохранении серологические реакции, направленные на выявление се-ротипа циркулирующего вируса, нецелесообразны, т.к. проведение их весьма трудоемко из-за большого количества серотипов, к тому же они не всегда достоверны из-за возможных перекрестных реакций.
Критерии диагноза. Диагноз риновирусной инфекции основывается на:
эпидемиологических данных (весна или ранняя осень, наличие подобных заболеваний у окружающих);
наличии обильной носовой секреции серозного или серозно-сли-зистого характера (ринорея);
отсутствии выраженной интоксикации;
наличии легкого першения в горле.
Диагноз подтверждают четырехкратным нарастанием титров специфических антител при исследовании парных сывороток.
Дифференциальный диагноз. Распознавание риновирусной инфекции облегчается во время вспышек этого заболевания в семьях и учреждениях весной (апрель-май) или осенью (сентябрь). Спорадические же случаи всегда затруднительны для диагностики, особенно в зимнее время, когда отмечается сезонный подъем заболеваемости, обусловленной другими вирусными и бактериальными инфекциями дыхательных путей.
Так как наиболее постоянным признаком при риновирусной инфекции является выраженная ринорея при отсутствии симптомов интоксикации (несоответствие выраженности местных и общетоксических симптомов, значительное преобладание первых), то дифференциальную диагностику следует проводить с заболеваниями, имеющими сходную симптоматику, и прежде всего ринорею.
При аденовирусных инфекциях:
ринит является лишь одним из многих и вовсе не ведущих симптомов. К тому же ринорея при аденовирусной инфекции никогда не достигает такой интенсивности, как при риновирусной;
при аденовирусных заболеваниях выявляют фарингит, тонзиллит, увеличение регионарных лимфатических узлов, гепатолиенальный синдром (часто), возможна даже легкая иктеричность;
больные могут жаловаться на першение и боль в горле, дети к тому же — на боль в животе;
интоксикация — частый признак;
температура может быть высокой.
Конъюнктивит, столь часто наблюдаемый при аденовирусных заболеваниях, может выявляться и при риновирусной инфекции при заносе вируса руками в глаза. Но он при этом обычно носит катаральный характер, протекает легко и существенно отличается от упорного фолликулярного или пленчатого аденовирусного конъюнктивита.
Грипп от риновирусной инфекции отличается:
незначительным ринитом;
выраженной интоксикацией;
явлениями трахеобронхита с первых дней болезни. При парагриппе отмечают:
умеренные ринорею и интоксикацию;
боль и першение в горле;
часто осиплость голоса и лающий кашель. PC-инфекция от риновирусной отличается:
большей выраженностью явлений интоксикации;
температурой, достигающей нередко 38—39 °С;
незначительным ринитом;
преимущественным поражением бронхов и бронхиол с развитием бронхиолитов, сопровождающихся кашлем, столь нехарактерным для риновирусной инфекции.
Для менингококкового назофарингита характерны:
гнойное отделяемое из носа с первых дней болезни;
часто боль в горле, головная боль;
— гранулезный фарингит с гнойными «дорожками» на задней стенке глотки;
— умеренный лейкоцитоз;
— лейкоциты в большом количестве с внутриклеточно расположенными диплококками в носоглоточной слизи.
Дифтерия переднего отдела носа имеет такие особенности:
— отделяемое из носа необильное, может быть с примесью крови, сукровичное;
— отек носовых ходов умеренный;
при риноскопии можно обнаружить на слизистой оболочке носа пленки, кровоточащие участки;
процесс упорный, длительный, может продолжаться недели и даже месяцы;
часто поражение слизистой оболочки носа сочетается с дифтерийным процессом другой локализации, выраженной интоксикацией;
нейтрофильный лейкоцитоз. Гаймориту присущи следующие особенности:
процесс носит преимущественно односторонний характер;
отделяемое из носа непостоянное, гнойное, необильное;
слизистая оболочка носа с пораженной стороны умеренно гипе-ремирована и нерезко отечна;
подчелюстные лимфатические узлы нередко увеличены на стороне поражения.
Существенным методом диагностики, позволяющим верифицировать диагноз гайморита, является пункция верхнечелюстной (гайморовой) пазухи.
Клинику риновирусной инфекции может имитировать аллергический ринит. Помощь в дифференциальной диагностике в этом случае может оказать тщательно собранный анамнез (контакт с возможными аллергенами, подобные реакции в прошлом). В пользу аллергии свидетельствуют эозинофилия в периферической крови и выделениях из носа, а также положительный эффект при лечении антигистаминными препаратами.
Особую сложность для диагностики представляют случаи риновирусной инфекции, при которой выражены явления фарингита, ларингита, бронхита. Однако следует помнить, что такие случаи относительно редки, кроме того, они все равно сопровождаются выраженными явлениями ринита. Тем не менее окончательный диагноз может быть установлен лишь после выделения возбудителя или проведения серологических исследований в парных сыворотках.
Помогает провести дифференциальную диагностику между ринитами вирусной, бактериальной и аллергической природы исследование носового секрета: при вирусной инфекции в клеточном составе преобладают лимфоциты, при бактериальной — нейтрофилы, при аллергии — эозинофилы.
Лечение. Больные риновирусной инфекцией не нуждаются в госпитализации. Во избежание развития осложнений в острый период заболевания следует соблюдать домашний режим, не допускать охлаждения. Диета не требуется.
Специфического этиотропного лечения нет. В подавляющем большинстве случаев риновирусное заболевание вообще не требует медикаментозного лечения. При полном отсутствии носового дыхания могут быть применены сосудосуживающие препараты в виде капель в нос (2% раствор эфедрина, нафтизин), паровые ингаляции через носовой тубус. Слизистую оболочку носа можно смазать вазелином, чтобы защитить ее от мацерации. Но эти медикаментозные средства не сокращают продолжительности заболевания, давая лишь временное облегчение.
Совершенно неоправданным является закапывание в нос растворов антибиотиков или сульфаниламидов. Не оказывая никакого действия на возбудитель, они лишь способствуют аллергизации. Учитывая особенности температурного режима репликации вируса, прием анальгина, аспирина не рекомендуют. К тому же, аспирин вообще противопоказан детям из-за возможности развития синдрома Рея.
Антибактериальная терапия необходима только при развитии осложнений. Антигистаминные препараты целесообразно назначать лишь больным, у которых заболевание протекает на аллергическом фоне (особенно при наличии аллергического ринита).
Благотворное действие на течение болезни оказывают аскорбиновая и лимонная кислоты, поливитамины.
Профилактика. Общая профилактика, описанная в разделе «Грипп», актуальна и для риновирусной инфекции.
Специфическая профилактика не разработана. Работу по созданию вакцины вряд ли можно считать целесообразной, принимая во внимание количество серотипов возбудителя, кратковременность иммунитета и относительную легкость течения заболевания, вызываемого риновирусами.
В качестве экстренной профилактики (при появлении первых заболеваний в коллективе) может быть применена 0,25% оксолиновая мазь или интерферон (его можно закапывать или вдувать в нос, вводить в носовые ходы с помощью насыщенных интерфероном ватных тампонов). При использовании последнего метода получен наилучший результат. Но не следует забывать и о возможности появления ринита при лечении интерфероном вследствие развития аллергии.
——i—
I
I i-^i
I
|
—и I
I— ■ и
I
■ I,
I —I BHMUrtpj
Респираторно-синцитиальная инфекция (РС-инфекция)
РС-инфещия — острое антропонозное вирусное заболевание с капельным механизмом передачи, протекающее в виде пневмонии, бронхита и бронхиолита, регистрирующееся преимущественно у детей младшего возраста {лат, — morbus respiratorio-syncytialis, англ. — respiratory syncytial virus infection).
Краткие исторические сведения. Возбудитель PC-инфекции был выделен в 1956 г. Morris, Blount, Savage у шимпанзе при заболевании, характеризующемся синдромом поражения верхних дыхательных путей. Он получил название «агент насморка шимпанзе» (Chimpanzee coryza Agent). В 1957 г. антигенно идентичные вирусы были выделены и от маленьких детей при заболеваниях, протекающих с поражением нижних дыхательных путей (Chanock, Roizman, Myers). Дальнейшие исследования подтвердили ведущую роль этих вирусов в развитии пневмонии и бронхиолита тяжелой формы у детей 1-го года жизни. Изучение свойств вируса позволило выявить особый характер воздействия его на пораженные клетки — образование синцития (сетевидной структуры, которая состоит из клеток, связанных друг с другом цито-плазматическими отростками). Это позволило дать название выделенному вирусу «респираторно-синцитиальный (РСВ)». В 1968 г. антитела к РСВ были обнаружены в крови у крупного рогатого скота, а спустя 2 года он был выделен у быков. Последующие годы ознаменовались обнаружением подобного возбудителя у многих домашних, диких и сельскохозяйственных животных, что свидетельствовало о широком распространении РСВ.
Актуальность. РСВ выявляется у населения всех континентов. Исследования показали, что антитела к вирусу обнаруживаются у 40% обследованных. Особое место PC-инфекция занимает среди заболеваний детского возраста: по распространенности и тяжести ей принадлежит первое место среди ОРВИ у детей 1-го года жизни. Она является и одной из основных причин смертности детей этого возраста, а также детей с иммунодефицитом.
У взрослых удельный вес PC-инфекции меньше — не более 10—13% всех ОРВИ. Результаты исследований последних лет позволили изменить взгляд на PC-инфекцию как сравнительно безопасную для взрослого населения. Оказалось, что PC-инфекция может быть причиной развития тяжелой пневмонии, поражения ЦНС и различных патологи
ческих состояний и у взрослых. Тяжело инфекция протекает у стариков, сопровождаясь значительной летальностью.
Проблемой PC-инфекция стала для педиатрических учреждений и детских стационаров, являясь одной из основных факторов внутри-больничного инфицирования. Это же создает еще одну проблему — большую степень вероятности заражения сотрудников таких учреждений.
Кратковременность иммунитета, формирующегося после перенесенного заболевания, создает сложности в создании вакцин.
Этиология. РСВ относится к роду Pneumovirus семейства Рага-mixoviridae.
Возбудитель имеет лишь 1 серотип, в котором выделяют 2 классических штамма — Лонг и Рэндолл. Антигенные различия этих штаммов столь незначительны, что не выявляются при исследовании сывороток. Это дает право рассматривать РСВ как единый стабильный серотип.
РСВ имеет плеоморфную или нитчатую форму, размеры 200—300 нм. В отличие от других возбудителей семейства Paramixoviridae он не содержит нейраминидазы и гемагглютинина.
Геном вируса — одноцепочечная нефрагментированная РНК. В настоящее время идентифицируют 13 функционально различающихся РСВ-полипептидов, из которых 10 — вирусспецифические. Вирус содержит М-белок (матриксный или мембранный), имеющий участки, способные взаимодействовать с мембранами инфицированных клеток. Инфекционная активность РСВ обусловлена наличием гликополипеп-тида.
Оболочка вируса имеет 2 гликопротеина в виде выростов — F-белок и GP-белок (прикрепляющий, он способствует присоединению вируса к чувствительной клетке, в цитоплазме которой впоследствии происходит репликация вируса).
Большинство РСВ неполноценны, они лишены внутренних структур и неинфекционны.
РСВ хорошо растут на различных культурах клеток, но особый тропизм проявляют к легочной ткани молодых животных и эмбриона человека. Так, в органных культурах из легких трехдневных американских хорьков вирус размножается в 100 раз быстрее, чем в культуре ткани из легких взрослого животного. По-видимому, это явление лежит в основе особой чувствительности маленьких детей к действию РСВ.
Клетки, пораженные вирусом, деформируются, сливаются, образуя синцитий. Усиливают процесс слияния клеток тромбин и трипсин. Ри-бавирин подавляет репродукцию РСВ в культуре клеток.
Возможна персистенция вируса в культуре тканей, но формирование ее в организме человека не доказано.
Экспериментальной моделью для воспроизведения РС-инфекции являются хлопковые крысы, приматы, белые африканские хорьки.
РСВ нестоек во внешней среде: на одежде, в свежих выделениях, на инструментах, игрушках он погибает через 20 мин — 6 ч. На коже рук может сохраняться до 20—25 мин.
При температуре +37 °С стабильность вируса сохраняется до 1 ч, через 24 ч при этой температуре его инфекционность составляет лишь 10 %. При температуре +55 °С он погибает через 5 мин. Губительно действует быстрое высушивание. Вирус устойчив к медленному замораживанию. Относительно стабилен при рН 4,0 и выше. Чувствителен к хлорамину. Неорганические соли (Мд, Са), глюкоза, сахароза предохраняют вирус от инактивации.
Эпидемиология. Человек — единственный источник РС-инфекции. Выделяет вирус больной человек с 3-го по 8-й день после заражения, у маленьких детей этот период может затягиваться до 3 нед.
Механизм передачи в основном воздушно-капельный. С капельками носового секрета и отделяемого из трахеи при кашле вирус передается здоровому человеку. Особенность этого процесса — необходимость близкого контакта, поскольку наибольшая возможность инфицирования возникает при попадании в носовые ходы здорового человека крупных капель слизи, содержащих вирус, мелкодисперсные аэрозоли менее опасны. Входными воротами являются также слизистая оболочка глаз, меньшее значение имеет попадание вируса в полость рта, на слизистую оболочку глотки, трахеи. Вирус может быть занесен в глаза и нос руками, загрязненными носовым секретом больного. Описаны случаи заражения через кожу, а также с почечными трансплантатами.
Заболевание отличается высокой контагиозностью, во время внут-рибольничных вспышек инфицируются практически все больные и медицинский персонал. По своей значимости как внутрибольничная PC-инфекция занимает ведущее место. Особенно часто такие эпидемические вспышки возникают в отделениях новорожденных, соматических отделениях для детей младшего возраста, а также в гериатрических учреждениях, стационарах для больных с иммунодефицитом.
Особенно чувствительны к заражению РСВ дети в возрасте до одного года. При первичном контакте с вирусом заболевают все 100% инфицированных, при повторных — около 80%. Уже на 2-м году жизни практически все дети оказываются инфицированными. В возрастной группе до 3 лет имеется повышенный риск заболеть тяжелой формой РС-инфекции. Дети в возрасте после 4 лет и взрослые болеют, как правило, значительно легче, а поэтому достоверной регистрации заболеваемости в этих возрастных группах нет.
Отсутствие стойкого иммунитета после перенесенной РС-инфекции обусловливает ежегодные сезонные (в холодное время года) подъемы заболеваемости с регистрацией наибольшего числа случаев среди детей 1-го года жизни (первичное инфицирование). В остальных случаях эти подъемы связаны с реинфекцией, вероятность которой велика не только у детей, но и у взрослых.
Сезонность отражает показатель коллективного иммунитета со спадом его к концу осени. В годы эпидемических вспышек гриппа наблюдается снижение коллективного иммунитета к PC-инфекции и отмечается более высокая, чем обычно, заболеваемость, вызываемая РСВ. Ежегодные вспышки длятся обычно до 5 мес. Летом, как правило, тяжелые случаи PC-инфекции (бронхиолит) не возникают.
Заболевание чаще регистрируют в крупных городах с высокой плотностью населения.
Связи между инфицированностью и расовой принадлежностью не ' обнаружено. Мальчики заболевают в 1,5 раза чаще девочек.
Возможность участия в эпидемическом процессе домашних и диких животных не доказана.
Классификация. Общепринятой классификации PC-инфекции нет.
PC-инфекция у детей младшего возраста (до 3 лет) может протекать в форме пневмонии, бронхиолита, у детей старше 4 лет и взрослых может проявляться еще и клиникой назофарингита или бронхита. У маленьких детей эти варианты клинического течения изолированно от поражения нижних дыхательных путей не встречаются. Заболевание протекает в легкой, среднетяжелой, тяжелой и субклинической формах. Критерии тяжести — возраст больного, степень токсикоза и дыхательной недостаточности.
Примерная формулировка диагноза. 1. Респираторно-синцитиаль-ная пневмония, среднетяжелое течение (или: PC-инфекция — пневмония интерстициальная, среднетяжелое течение).
2. Острый бронхиолит (респираторно-синцитиальный) с тяжелым течением, осложнившийся крупом.
Патогенез. Патогенез PC-инфекции изучен недостаточно. Мало того, имеющиеся данные настолько противоречивы, что к настоящему времени нет единой, признаваемой всеми, теории патогенеза. Предлагаются различные схемы патогенеза, в основу которых положены иммунологическая незрелость младенцев (иммунологический дисбаланс), реакции гиперчувствительности замедленного типа и другие факторы. Вероятно, все эти механизмы играют определенную роль в развитии патологического процесса, но долевое участие каждого из них до конца не выяснено.
Внедрение вируса в организм происходит главным образом через слизистую оболочку носа, если преодолевается нейтрализующая активность носового секрета, связанная частично с наличием неспецифических ингибиторов, в частности антител класса IgA. РСВ является слабым интерфероногеном, который в свою очередь является индуктором активности нормальных киллеров. Таким образом, это звено защиты существенной роли не играет. В том случае, если это реинфекция, в носовом секрете содержатся защитные специфические антитела в титре не менее 1:4. Антитела, имеющиеся в крови, не защищают от инфицирования, они способны лишь облегчить течение болезни.
Вирус, преодолев защиту, «прилипает» к чувствительной клетке, а затем проникает в нее, благодаря слиянию с мембраной клетки. В цитоплазме идет репликация, накопление вируса, а затем — выход его из клетки, но более 90% вирусов остаются связанными с клеткой. Вирус не подавляет метаболизм инфицированной клетки, но может изменять ее внешний вид, деформировать ее. Признаком РС-инфекции является формирование синцития при деформации клетки.
Тропность вируса к клеткам легких, бронхиол и бронхов обусловливает основную локализацию патологического процесса с развитием бронхита, бронхиолита, пневмонии. Чем меньше возраст ребенка, тем чаще возникают и тяжелее протекают у него пневмония и бронхит.
При бронхите и перибронхите в результате действия защитных факторов (макрофаги, антитела, нормальные киллеры и др.) возникает гибель внеклеточно расположенных вирусов и клеток, содержащих вирус. Результатом являются некроз эпителия, отек и крутлоклеточная инфильтрация подслизистого слоя, гиперсекреция слизи. Все эти факторы приводят к сужению просвета воздухоносных путей, тем более выраженному, чем меньше их калибр. При обширном поражении бронхиальных структур может возникнуть дыхательная недостаточность. Возможна полная обтурация бронхов с развитием ателектазов, что чаще наблюдается при бронхиолите. Дополнительным фактором, способствующим уменьшению просвета бронхов и бронхиол, является их спазм. В основе этого, как полагают, лежат несколько факторов: повышение уровня секреторных и сывороточных IgE, индукция бронхо-спастических факторов в результате взаимодействия иммунных комплексов с нейтрофилами, повышенный выход гистамина как следствие стимулирования лимфоцитов вирусными антигенами.
Поражение легких при РС-инфекции характеризуется интерстици-альным воспалением, генерализованной инфильтрацией, отеком и некрозом эпителия бронхов, бронхиол, альвеол.
Избирательной тропностыо вируса к эпителию дыхательных путей объясняется клиническая симптоматика, характер осложнений. Имеются, правда, сведения о способности самого вируса вызывать еще и средний отит. В других органах и тканях РСВ обнаружить пока не удалось. Поэтому некоторые проявления РС-инфекции могут быть обусловлены сенсибилизацией, гипоксией, присоединением вторичной инфекции.
Цитотоксические реакции, направленные на уничтожение клеток, инфицированных вирусом, осуществляемые через макрофаги и нормальные киллеры, начинают действовать с первых дней, пик цитотоксической активности приходится на 5-й день после заражения. В ответ на инфекцию в организме вырабатываются антитела против вирусов, их фрагментов и инфицированных клеток. Антитела к F-белку вируса могут подавить слияние клеток и выход вируса из клетки, антитела к GP-белку способны нейтрализовать вирус. Цитотоксические антитела класса IgG проходят через плаценту.
Полагают также, что иммунные комплексы, содержащие компоненты вируса, способны усиливать специфический фагоцитоз, приводящий к инактивации вируса или агрегатов РСВ с антителами. Защитные реакции, направленные на уничтожение вируса и инфицированных клеток, сочетаются с развитием местной сенсибилизации к РСВ и усиливаются при повторных инфицированиях. Обратное развитие бронхиолита сопровождается исчезновением из периферической крови фактора, вызывающего торможение миграции лейкоцитов, который мог отражать уровень сенсибилизации к РСВ в острый период.
Иммунитет, формирующийся после перенесенной РС-инфекции, непродолжительный, при этом местный иммунитет к PC-инфекции в нижних дыхательных путях более продолжительный, чем в верхних. В крови циркулируют специфические антитела класса IgG. При повторных заражениях антитела определяются в более высоких титрах, они сохраняются длительнее, но от реинфекции все же не защищают в период очередного сезонного подъема заболеваемости.
Много спорного в вопросах патогенеза PC-инфекции у детей 1-го года жизни. Не подтверждается существовавшее ранее мнение о том, что дети, имеющие высокие титры материнских антител, защищены от инфекции; наоборот, они болеют тяжелее и длительнее. Сторонники такой точки зрения полагают, что пассивно приобретенные антитела, оставшиеся в организме ребенка, могут блокировать индукцию Т-кил-леров и затруднять освобождение от вируса.
Действительно, антитела, полученные от матери, не гарантируют защиту от инфекции, которая все-таки в первые 2—3 нед жизни ребенка протекает легче. Дети старше 3 мес болеют тяжелее, что связано с тем, что концентрация материнских антител к этому времени снижается. У детей 1-го года жизни защитные механизмы при PC-инфекции настолько ненадежны, что реинфекция может наступить уже через несколько недель после первичного инфицирования. Возможно и внутриутробное заражение РСВ от больной матери. У таких детей антитела не появляются и, как полагают, возможно персистирование вируса.
После нескольких встреч с вирусом происходит совершенствование секреторного и сывороточного иммунитета, число заболеваний при очередном контакте с больным уменьшается.
При возникновении PC-инфекции у стариков, как установлено, появление антител запаздывает, их титры не коррелируют с тяжестью течения заболевания, протекающего нередко в виде тяжелых пневмоний и обструктивного бронхита, течение которых еще больше осложняется наличием у большинства из них хронических заболеваний сердца или легких.
Клиника. Наиболее отчетливо клиника РС-инфекции проявляется у детей в возрасте до 3 лет, причем заболевание может возникнуть и в первые дни после рождения ребенка. Чем старше ребенок, тем легче протекает заболевание.
Инкубационный период составляет 2—5 дней. Первыми проявлениями болезни являются ринорея и фарингит. Грудные дети становятся беспокойными, отказываются от груди, дети старшего возраста жалуются на боль в горле, головную боль. При осмотре обращают на себя внимание обильное серозное отделяемое из носа, гиперемия и отечность задней стенки глотки, бывает конъюнктивит. Через 1—3 дня начинает повышаться температура, достигая иногда 38—39 °С, держится она обычно 3—4 дня. В дальнейшем на фоне развернутой клинической картины болезни возможны периодические кратковременные подъемы температуры. В это же время, а иногда и с первых дней болезни, появляется сухой кашель. С этого времени симптомы заболевания быстро нарастают, ведущим становится кашель, часто возникающий в виде приступов, он может сопровождаться рвотой.
На основании клиники провести дифференциальный диагноз между пневмонией и бронхиолитом (а именно эти клинические формы наиболее часты при РС-инфекции у детей первых трех лет жизни) практически невозможно, тем более, что эти варианты поражений могут сочетаться.
По мере прогрессирования заболевания возникают признаки обструкции бронхов — дыхание становится шумным, свистящим, в нем активно участвуют межреберные мышцы. Иногда грудная клетка выглядит раздутой. Частота дыханий увеличивается, достигая 60 и более, но даже это не в состоянии компенсировать прогрессирующую гипоксемию. Возможны короткие (до 15 с) периоды апноэ. В легких выслушиваются сухие свистящие и влажные хрипы на фоне ослабленного дыхания.
Кожный покров бледен, нередко цианотичен, но иногда при тяжелой гипоксемии цианоза может не быть (т.е. цианоз не всегда критерий тяжести процесса). Возникающая при этом гипоксия ЦНС может сопровождаться адинамией, спутанностью сознания, состоянием прострации.
У детей на фоне поражения бронхиол и легких могут появляться признаки среднего отита, что сопровождается усилением беспокойства, плачем из-за боли в ушах. Этиологическая связь процесса с РС-ин-фекцией доказана повышением титров специфических антител к РСВ в отделяемом из ушей. Длительность болезни — от 5 дней до 3 нед.
Чем старше ребенок, тем легче протекает заболевание. У детей старше 4 лет и у взрослых существенных различий в течении РС-инфекции нет. При реинфицированиях патологический процесс может протекать бессимптомно и выявляется по нарастанию уровня специфических антител в сыворотке крови.
Клинически выраженные формы у взрослых протекают чаще всего с симптомами поражения верхних дыхательных путей, проявлением чего являются чиханье, насморк, кашель, боль в горле. Заболевание часто сопровождается умеренным повышением температуры, но иногда лихорадка отсутствует. В острый период заболевания могут появляться конъюнктивит, склерит. Задняя стенка глотки и мягкое нёбо отечны, гиперемированы.
Особенностью PC-инфекции по сравнению с другими ОРВИ является более длительное течение — в среднем до 10 дней, но возможны варианты (от 1 до 30 дней), кашель сохраняется дольше других симптомов.
У части взрослых больных (чаще это пациенты с хроническими заболеваниями легких, сердца, бронхов, с иммунодефицитом) РС-инфек-ция тоже может протекать с поражением бронхов, бронхиол, легких. Клиника в этих случаях напоминает таковую у маленьких детей: высокая температура, приступообразный кашель, периодические приступы удушья, одышка, цианоз. Появляется тахикардия, определяются глухость сердечных тонов и снижение АД. Перкуторно в легких выявляют эмфизематозные участки, а при аускультации на фоне жесткого дыхания выслушиваются разнокалиберные влажные и сухие хрипы. Признаки поражения легких и бронхов и у взрослых, и у детей младшего возраста сочетаются с явлениями ринита, фарингита. Не характерны для PC-инфекции у взрослых тяжелые обструкции дыхательных путей, явления крупа, апноэ. Хотя случаи развития тяжелого бронхоспазма с летальным исходом описаны и у взрослых.
У стариков PC-инфекция часто проявляется в форме тяжело протекающей бронхопневмонии.
Осложнения. Осложнения при PC-инфекции могут возникать в различные периоды болезни.
В острый период у детей бывает круп с асфиксией за счет распространенной обтурации бронхов и бронхиол, у взрослых возможен тяжелый бронхоспазм со смертельным исходом.
РСВ способствует активации хронической инфекции (обострение хронического бронхита, пневмонии). Пневмония, гнойный отит могут быть и следствием суперинфицирования бактериальной флорой больных, однако при PC-инфекции вторичная бактериальная флора играет значительно меньшую роль, чем при других ОРВИ.
PC-инфекция может быть причиной синдрома внезапной смерти новорожденных (чаще детей в возрасте 2—4 мес), возникающего на фоне полного клинического благополучия.
Основной причиной развития астматического синдрома у детей моложе 5 лет считают перенесенную РС-инфекцию.
При частом инфицировании возможно развитие хронического обструктивного бронхита (чаще у курильщиков). Наблюдения последних лет позволяют судить о связи неврологических расстройств (энцефалит, энцефалопатия) у детей первых лет жизни с действием РСВ. PC-инфекция ассоциируется с заболеваниями ЦНС (менингит, атаксия, гемиплегия), при этом в спинномозговой жидкости обнаруживают антитела к РСВ. Предполагают возможность развития миокардита, полной блокады сердца. Существуют указания на возможную связь с РСВ болезни Педжета (обнаружен при этом вирус в срезах костей), синдрома Рея, лейкоза. Есть сообщения о возникновении совсем необычных проявлений РС-инфекции — лихорадки с сыпью и сепсисоподобным синдромом без поражения дыхательной системы.
Патогенез таких клинических проявлений неясен, что лишь подтверждает скудность наших сведений об РС-инфекции.
Исходы. Летальность при РС-инфекции составляет примерно 0,5%, преимущественно погибают дети первого года жизни и старики. Среди детей с иммунодефицитом она достигает 20—25%.
Следствием перенесенной РС-инфекции могут быть бронхиальная астма, обструктивный бронхит.
Методы диагностики. Общеклинические методы исследования. При исследовании крови выявляют чаще нормоцитоз, но возможен небольшой лейкоцитоз или даже лейкопения. В формуле крови существенных изменений нет. СОЭ нормальная или слегка увеличена.
При исследовании мочи изменений не обнаруживают.
Специфическая диагностика. Выделение вируса из материала, взятого из носа, гортани, возможно в течение первых 6—7 дней болезни. Заражают полученным материалом клетки фибробластов легких эмбриона человека, почки обезьяны. Цитопатический эффект наступает через 3—7 дней, чаще — на 4-й день. Метод доступен специальным лабораториям.
РФА широко применяют для ускоренной диагностики РС-инфекции. Более чувствителен непрямой вариант РФА. Имеются коммерческие препараты (Wellcome Lab., Canada), для иммунофлюоресцентной диагностики РС-инфекции, обладающие высокой специфичностью и чувствительностью. Материалом для исследования служит слизь из носовых ходов, аспираты слизи, взятые из голосовой щели.
В последние годы широко используют метод, основанный на определении отдельных компонентов вирусных частиц в РФА.
Серологические исследования относят к методам ретроспективной диагностики. Наиболее широко ставят РСК и РН. Обычно первое исследование производят не ранее 2—3-й недели болезни, повторное исследование — еще через 2—3 нед.
Установлено, что чувствительность РН выше, чем РСК. Старики, повторно инфицированные, могут не продуцировать антитела в количестве, достаточном для определения их в РСК и РН.
Биохимические методы позволяют обнаружить гипоксемию различной степени выраженности, иногда сочетающуюся с ацидозом.
Дополнительные методы диагностики: рентгенография (выявляются признаки интерстициальной пневмонии и перибронхиальные уплотнения у 50—80% больных), ЭКГ.
Критерии диагноза. Диагноз PC-инфекции ставят, принимая во внимание такие ее особенности:
— сезонность с учетом эпидемической обстановки, наличия подобных заболеваний или отдельных симптомов у окружающих. Особенно тщательно анализируют групповые внутрибольничные вспышки ОРВИ;
— возраст больного (чем младше ребенок, тем вероятнее, что симптомы ОРВИ обусловлены РСВ);
— сочетание ринореи с поражением нижних дыхательных путей у маленьких детей, верхних отделов дыхательных путей — у взрослых (т.е. при групповых вспышках различия в течении у детей первых трех лет жизни и взрослых);
— свистящее дыхание, свидетельствующее о нарушении проходимости дыхательных путей (у детей, людей пожилого возраста);
— одышку экспираторного типа при поражении бронхов и бронхиол;
— выявляющиеся при поражении нижних отделов дыхательных путей характерные изменения в легких (сухие и влажные хрипы, ослабленное или жесткое дыхание на отдельных участках; чередование эмфизематозных участков и зон притупления при перкуссии);
— отсутствие высокой лихорадки;
рентгенологические данные, характерные для интерстициальной пневмонии, бронхита;
возможность длительного течения (до 3 нед);
— отсутствие существенных изменений в формуле крови. Подтверждают диагноз методом РФА или с помощью серологических исследований (ретроспективно).
Дифференциальный диагноз. О наличии PC-инфекции у детей в возрасте до 3 лет в первую очередь следует думать при возникновении любого респираторного синдрома. Дифференциальная диагностика PC-инфекции и сходных с нею заболеваний у детей изложена в соответствующих руководствах по педиатрии.
У взрослых при наличии преимущественной клинической симптоматики поражения верхних дыхательных путей необходимо проводить дифференциальный диагноз с гриппом, парагриппом, риновирусной и аденовирусной инфекциями. Основанием для этого является наличие у больных с PC-инфекцией трахеобронхита, кашля, насморка, умеренных лихорадки и интоксикации, возможность появления склерита, конъюнктивита.
Грипп от PC-инфекции в этих случаях отличается:
острым началом;
выраженной интоксикацией с первых дней болезни;
преобладанием ощущения заложенности носа над ринореей;
характером кашля, который нередко бывает мучительным, с чувством жжения за грудиной.
Неосложненный грипп длится не более 5—6 дней.
Для парагриппа в отличие от PC-инфекции характерны:
явления ларингита;
осиплость голоса;
умеренная ринорея;
Риновирусная инфекция отличается тем, что:
как правило, не сопровождается кашлем, болью в горле;
явления конъюнктивита, склерита отсутствуют;
пневмония для нее не характерна.
При аденовирусной инфекции в отличие от РС-инфекции:
возникает увеличение подчелюстных, а иногда шейных и подмышечных лимфатических узлов, печени и селезенки;
конъюнктивит бывает пленчатый или фолликулярный, а не катаральный, часто односторонний;
ринорея умеренная;
боль в горле в сочетании с интоксикацией — ведущие симптомы в первые дни болезни.
При развитии бронхита, бронхиолита, пневмонии РС-инфекцию приходится дифференцировать с орнитозом, микоплазменной и бактериальной пневмонией, болезнью легионеров.
Основанием для проведения дифференциальной диагностики с этими заболеваниями служат интоксикация, кашель, изменения в легких.
Орнипгоз от PC-инфекции отличают:
эпидемиологический анамнез (указание на контакт с птицами);
острое начало, выраженный общеинтоксикационный синдром;
отсутствие признаков бронхоспазма;
увеличение печени и селезенки;
брадикардия;
резко увеличенная СОЭ;
отсутствие аналогичных заболеваний в окружении больного (т.е. нет контагиозности).
Микоплазменная пневмония наиболее сходна по клинике с РС-ин-фекцией, поскольку микоплазма также поражает трахею, бронхи, бронхиолы, легочную ткань и может сопровождаться фарингитом, отитом, бронхоспазмом, однако эта инфекция имеет свои отличия:
для нее не характерна ринорея;
типична полиорганность поражений (поражение ЦНС, сердечно-сосудистой системы, суставов).
При бактериальной пневмонии отличительные симптомы такие:
ринит либо отсутствует, либо слабо выражен;
кашель со слизисто-гнойной мокротой;
явления бронхоспазма, как правило, не возникают;
тяжелая одышка появляется при обширных процессах в легких, легко выявляемых при перкуссии и аускультации;
при рентгеноскопии обнаруживаются очаговые тени различных размеров и локализации;
в крови — нейтрофильный лейкоцитоз, увеличенная СОЭ;
подобные заболевания в окружении больного отсутствуют. Для легионеллеза в отличие от PC-пневмонии характерно:
острое начало;
отсутствие ринита;
наличие диареи;
частое вовлечение в патологический процесс почек;
— поскольку поражается преимущественно легочная ткань, а не бронхи и бронхиолы, бронхоспазм не характерен;
— рентгенологические исследования выявляют очаговую пневмонию;
— физикальные данные также характерны для очаговой, лобарной, но не интерстициальной пневмонии;
— в крови — нейтрофильный лейкоцитоз;
— пик заболевания — летнее время, период наиболее интенсивного пользования кондиционерами.
Окончательный диагноз устанавливают после проведения специфических методов исследования.
Лечение. Госпитализации подлежат все дети 1-го года жизни, а при возможности и в возрасте до 3 лет независимо от тяжести состояния.
Необходимость и целесообразность госпитализации взрослых больных определяются особенностями течения заболевания, возможностью изоляции больного в домашних условиях.
Специальной диеты не требуется. Режим в неосложненных случаях — полупостельный в первые дни (на фоне возможной лихорадки), в дальнейшем вопрос решается индивидуально.
Этиотропная терапия находится в стадии разработки. Перспективным оказался противовирусный препарат рибавирин (синтетический нуклеозид), который в виде аэрозоля вводят в дыхательные пути в течение 3 дней. На фоне лечения рибавирином заболевание протекает легче. Достоинством препарата является его нетоксичность. Перспективен ремантадин.
Так как все коммерческие иммуноглобулины содержат антитела к основным возбудителям ОРВИ, в том числе к РСВ, предприняты попытки применить их при лечении больных PC-инфекцией. При этом получены неоднозначные результаты: обнаружено как общее стимулирующее, так и подавляющее действие иммуноглобулина на выработку собственных антител (последнее наблюдается при высоком титре антител в препарате). Поэтому при решении вопроса о целесообразности введения иммуноглобулина ребенку следует иметь сведения о титрах антител к РСВ в имеющемся препарате. На тяжесть течения заболевания иммуноглобулин, тем не менее, существенного влияния не оказывает.
Интерферон не играет большой роли в защите от РС-инфекции и в механизмах выздоровления, поэтому целесообразность его назначения для лечения проблематична (тем более не стоит забывать о возможных побочных реакциях, см. «Грипп»).
Таким образом, основное место в лечении больных с РС-инфекцией занимает патогенетическая терапия. Гипоксемия, возникающая при РС-инфекции, особенно при тяжелом ее течении, свидетельствует о необходимости применения оксигенотерапии.
Наличие бронхоспазма при тяжелой форме является показанием к назначению бронхолитиков.
Глюкокортикостероиды показаны лишь при тяжелом течении, сопровождающемся астматическими приступами, тяжелым бронхоспаз-мом, аллергией.
Антибиотики назначают лишь при наличии бактериальных осложнений. Предпочтение отдают эритромицину (внутрь), ампициллину (парентерально) в обычных терапевтических дозах.
Порядок выписки из стационара. После исчезновения клинических проявлений реконвалесцентов выписывают. Диспансеризации рекон-валесценты не подлежат.
Профилактика. Общая профилактика сводится прежде всего к выявлению больных детей, их изоляции. Необходима тщательная обработка и проветривание помещений, в которых содержатся больные.
Возможность осуществления специфической профилактики сначала инактивированной, а затем живой аттенуированной вакциной изучают с 60-х годов. Однако, как выяснилось, вакцины не только не защищали, но даже способствовали более тяжелому течению заболевания при повторном заражении. Кроме того, вакцинацию при ее эффективности следовало бы проводить ежегодно, учитывая нестойкий кратковременный иммунитет и ежегодные сезонные подъемы заболеваемости.
Есть предложения вакцинировать беременных женщин незадолго до родов, что способствует повышению уровня специфических антител класса IgG в сыворотке крови новорожденного. Дополнительным фактором защиты являются антитела, содержащиеся в молозиве иммунизированной женщины. Целесообразность такого подхода к профилактике РС-инфекции у детей первых месяцев жизни изучается.
Применение иммуноглобулинов, интерферона как средств экстренной профилактики себя не оправдало.
Аденовирусная инфекция
Аденовирусная инфекция — антропонозные вирусные заболевания преимущественно с воздушно-капельным механизмом передачи, вызывающиеся многочисленными серотипами аденовирусов и характеризующиеся поли-органностью поражений (дыхательные пути, глаза, кишечник, лимфоидная ткань) и отсюда полиморфизмом клинических проявлений, протекающие часто с умеренно выраженными симптомами общей интоксикации (лат. — infectio adenovirals, англ. — adenovirus infection).
Краткие исторические сведения. Датой открытия аденовирусов считают 1953 г., когда W.Rowe и соавторы при длительном культивировании тканей миндалин и аденоидов, удаленных во время операций у детей, выделили цитопатогенный агент. Это был первый шаг к расшифровке этиологии гриппоподобных заболеваний, которые еще в 1937 г. АА.Смородинцев назвал «острые сезонные катары». Последующие исследования позволили выявить наличие вируса, который и обусловливал характерный цитопатический эффект (1954 г.). Новые штаммы вируса были выделены в ходе дальнейших исследований и от клинически здоровых детей, в связи с чем они были отнесены к латентным и названы АД-вирусами (вирусами аденоидной дегенерации).
В 1954 г. R.Huebner получил новые данные, указывающие на то, что аналогичные вирусы обнаруживаются также в секретах больных с острым фарингитом и конъюнктивитом, в связи с чем они были названы «аденоидо-фарингеально-конъюнктивальные вирусы».
В этом же 1954 г. другая группа исследователей (Хиллеман и Вернер) при изучении и уточнении этиологии ОРЗ и атипичных пневмоний у новобранцев армии США выделили ранее неизвестный вирус, назвав его RI-67. В дальнейшем была доказана его идентичность с аденои-до-фарингеально-конъюнктивальным вирусом.
В последующие годы такие вирусы были выделены от больных во время вспышек эпидемического кератоконъюнктивита, хотя как самостоятельное заболевание он был описан еще в 20-х годах.
Более того, ретроспективный анализ клинических описаний некоторых вспышек респираторных заболеваний, относящихся еще к прошлому веку, позволяет высказать предположение, что острые респираторные синдромы, вызываемые аденовирусами, были известны более чем за 100 лет до выделения и изучения аденовирусов.
Дальнейшее изучение аденовирусов, открытие новых их серотипов позволили установить, что они являются причиной возникновения не только респираторных заболеваний, но и диареи, мезаденита, геморрагического цистита и других патологических состояний.
В 1962 г. J.Trentin и соавторы, а также R.Huebner описали первый случай индукции злокачественной опухоли у животных патогенным вирусом человека — им оказался аденовирус-12, вызывавший опухоли у грызунов. Онкогенность аденовирусов послужила сильнейшим стимулом для их дальнейшего детального молекулярно-биологического изучения.
В настоящее время уже известно более 40 серотипов аденовирусов человека, их число с каждым годом растет.
Актуальность. Клиническое значение аденовирусных заболеваний определяется их широким распространением (почти все взрослые имеют антитела к вирусам типов 1—7), значительным удельным весом в структуре ОРВИ (особенно в детском возрасте) вирусных диарей, поражений конъюнктив, лимфоидной ткани, возможностью возникновений эпидемических вспышек заболевания.
Особую актуальность приобретают отдельные биологические аспекты аденовирусной инфекции, а именно:
— способность вызывать онкогенную трансформацию у животных;
способность к длительной латенции в некоторых типах клеток хозяина;
возможность интерференции с другими вирусами с образованием гибридных вирусов, обладающих особыми биологическими свойствами, в том числе и усилением онкогенности.
На модели аденовирусов изучают важные молекулярно-биологичес-кие феномены.
Этиология. Аденовирусы относятся к ДНК-сод ер жащим вирусам и составляют семейство Adenoviridae, включающее 2 рода: вирусы млекопитающих — Mastodenovirus (М) и вирусы птиц — Aviadenovirus (А).
Аденовирусы изолированы не только от человека, но и от большого числа животных и птиц, являющихся их естественными хозяевами (эти вирусы непатогенны для человека).
Аденовирусы имеют большое число серотипов: в роду М — их более 90, из них человеческих 41, в роду А — их 18.
Размеры вирусных частиц колеблются от 70 до 90 нм; они содержат двунитчатую ДНК. Капсид в форме икосаэдра лишен внешней липо-протеиновой оболочки, состоит из 252 капсомеров; по количеству соседствующих аналогичных структурных субъединиц одни капсомеры названы гексонами, другие пентонами. Имеются характерные отрост-чатые структуры, называемые фиберами (фибриллами), эти структуры различаются между собой не только морфологически, но и иммуноло-гически (различия в антигенном строении).
В вирионе насчитывается 7 различных антигенных структур. Основными из них считаются А, В, С.
Общим группоспецифическим антигеном для аденовирусов рода М является антиген гексона А. В его составе есть две реактивные группы. Одна из них ведет к образованию группоспецифических антител, которые могут быть определены в реакции связывания комплемента. Другая ответственна за образование типоспецифических антител, которые определяются в реакции нейтрализации.
Антиген пентона (В-антиген) — токсический антиген, он ингибирует действие интерферона, повышает тяжесть ассоциированных респираторных инфекций.
Антиген фибрилл (С-антиген) — типоспецифический, способствует адсорбции аденовирусов на эритроцитах обезьяны или крысы и обусловливает их агглютинацию.
Кроме этих поверхностных, имеются внутренние антигены белковой природы, окружающие ДНК, которые принимают участие в интеграции генома аденовируса.
Аденовирусы чувствительны к высоким температурам: они легко инактивируются прогреванием и уже при температуре +56 °С через 30 мин разрушаются. В условиях комнатной температуры ( + 22 °С) аденовирусы могут сохраняться до 14 дней. Они длительно сохраняются при низких температурах (при температуре —40 "С — до 70 дней). Вирусы устойчивы в кислой среде, резистентны к органическим растворителям, в частности к эфиру, но инактивируются хлором в умеренных концентрациях. При ультрафиолетовом облучении инфекцион-ность разрушается быстрее, чем гемагглютинирующая, токсическая и трансформирующая активность.
Клеточные поражения, вызываемые аденовирусами, характеризуются своеобразным цитопатическим эффектом, по которому проводят их распознавание. Адсорбция аденовирусов происходит на чувствительных клетках прежде всего цилиндрического эпителия дыхательных путей, на мукопротеиновых рецепторах клеток человека. Зараженные аденовирусами клетки округляются, теряют обычную структуру, формируют гроздьевидные скопления и в конце концов отмирают. В процессе дегенерации клеток под действием аденовирусов выделяют две фазы. Первая связана с токсическим эффектом, другая — с истинным размножением вирусов, которое происходит внутри ядер и в цитоплазме зараженной клетки.
Аденовирусы обладают гемагглютинирующими свойствами: все се-ротипы аденовирусов человека (кроме 18) способны агглютинировать эритроциты обезьян-резус или крыс. По этому признаку аденовирусы человека делят на 4 подгруппы (I—IV).
Онкогенные свойства аденовирусов человека (способность вызывать развитие злокачественных опухолей у хомяков) впервые были выявлены у 12-го серотипа. Сейчас онкогенные свойства подтверждены еще у 7 серотипов аденовирусов человека. По онкогенной способности аденовирусы делят на 5 подгрупп (А, В, С, D, Е). Различают высокоон-когенные и слабоонкогенные серотипы аденовирусов.
Клетки, трансформированные in vivo и in vitro, содержат два новых антигена: Т-антиген (опухолевый) и трансплантационный.
В опухолевых клетках людей, больных раком различных локализаций, Т-антигены аденовирусов пока не обнаружены.
В существующей ныне классификации аденовирусов человека выделяют подгруппы по онкогенности, гемагглютинации, серотипам и другим признакам.
Один и тот же аденовирус может вызывать разные формы заболеваний, вместе с тем разные серотипы аденовирусов могут вызывать заболевание со сходной клинической симптоматикой.
Выделение аденовирусов человека возможно только на тканевых чувствительных культурах (эпителиальные клетки человека). В отличие от вирусов гриппа и парагриппа они не размножаются на куриных эмбрионах и не патогенны для экспериментальных животных.
Аденовирусы способны специфически взаимодействовать с другими типами вирусов.
Так, адено-аденогибриды возникают при совместном культивировании аденовирусов человека и аденовирусов обезьян. При этом аденовирусы обезьян выступают в роли помощников в размножении аденовирусов человека.
Участие в патологических состояниях человека этих гибридных вирусов пока не доказано. Но они представляют уникальную модель для разработки вопросов вирусного патогенеза, онкогенеза и создания вакцин.
Аденоассоциированные вирусы (ААВ) — это мелкие ДНК-содержа-щие дефектные вирусы, которые входят в группу парвовирусов. Они могут размножаться только в присутствии аденовирусов; ААВ обнаруживаются в культурах аденовирусов, изолированных от человека и животных. У большинства детей уже к десятому году жизни могут быть обнаружены антитела к одному из серотипов ААВ. В культуре клеток инфекционность и онкогенность аденовирусов снижаются в присутствии ААВ. Механизм такого взаимодействия не расшифрован.
Эпидемиология. Источником инфекции является больной человек в острой стадии заболевания, реконвалесцент либо вирусоноситель. Выделяются возбудители с носоглоточным секретом, мокротой, отделяемым конъюнктивы, фекалиями, мочой (преимущественно у лиц с им-мунодепрессией).
Сроки выделения возбудителей достаточно длительны: из дыхательного аппарата и с конъюнктивы — до 25 и даже до 50 дней, с фекалиями — еще дольше.
Основной механизм заражения — воздушно-капельный. Вероятность реализации также и воздушно-пылевого пути передачи связана с достаточно высокой резистентностью аденовирусов к неблагоприятным факторам окружающей среды. Возможен фекально-оральный механизм передачи, учитывая длительное выделение аденовирусов с фекалиями, их устойчивость в окружающей среде и способность поражать клетки слизистой оболочки кишечника.
Имеются также доказательства возможности заражения через конъюнктиву глаз при купании в плавательных бассейнах, при заносе возбудителя в глаз инфицированными руками (то есть контактный путь).
Факторами передачи аденовирусов могут служить продукты питания, вода, бытовые вещи, предметы медицинского обихода — инструментарий, пипетки, мензурки и т.д.
Аденовирусные заболевания регистрируют в виде спорадических заболеваний и вспышек. Для вспышек характерно постепенное медленное их развитие, что связано с продолжительностью инкубационного периода и длительностью течения самого заболевания. Описаны внутрибольничные вспышки аденовирусных конъюнктивитов в глазных отделениях, среди медицинского персонала, работающего с детьми, больными аденовирусными заболеваниями.
Аденовирусные заболевания возникают во всех возрастных группах, но чаще всего болеют дети раннего и младшего возраста.
Аденовирусы могут вызывать заболевания в течение всего года. Те из них, которые протекают с синдромом поражения дыхательных путей как основным, преимущественно возникают в холодное время года, аналогично другим респираторным вирусным инфекциям. Фарин-гоконъюнктивальная лихорадка и эпидемический кератоконъюнкти-вит чаще регистрируют в летнее время, что связано с пребыванием людей в лагерях, купанием в бассейнах, открытых водоемах (в этих случаях «срабатывает» другой механизм передачи, а заболевания могут возникать в виде вспышек).
Диарею аденовирусной этиологии у детей также отмечают чаще в летнее время.
Классификация. Единая общепринятая клиническая классификация аденовирусных заболеваний до настоящего времени не разработана.
Аденовирусная инфекция может протекать в виде манифестных, субклинических и латентных форм.
Клинические проявления аденовирусных заболеваний отличаются большим разнообразием, что обусловлено способностью аденовирусов поражать слизистые оболочки дыхательных путей (глотки, гортани, трахеи, бронхов, легких), кишечника, мочевого пузыря, конъюнктивы, а также лимфоидную ткань и клетки нервной системы. Следует отметить, что в разных возрастных группах клинические проявления могут различаться.
Все имеющиеся клинические классификации построены по принципу выделения ведущего клинического синдрома (с большей или меньшей его детализацией, в частности, в синдроме острого респираторного заболевания).
Суммируя все описанные к настоящему времени клинические синдромы при аденовирусных заболеваниях, клиническую классификацию их можно представить в виде следующих форм:
1) аденовирусные ОРЗ (ринит, тонзиллит, ринофаринготонзиллит, трахеобронхит);
аденовирусная пневмония;
фарингоконъюнктивальная лихорадка;
эпидемический кератоконъюнктивит;
аденовирусный геморрагический цистит;
аденовирусная диарея (гастроэнтерит);
аденовирусные поражения нервной системы (энцефалит, менин-гоэнцефалит, полирадикулоневрит);
аденовирусные заболевания при иммунодефицитах, в том числе при СПИДе.
По степени тяжести каждая из клинических форм может иметь легкое, среднетяжелое и тяжелое течение. Подавляющее большинство аденовирусных заболеваний характеризуется возможностью самоизлечения и протекает без осложнений. Наиболее тяжелое течение возможно у детей раннего возраста.
По длительности течения практически все клинические формы относятся к острым инфекциям; но следует помнить, что аденовирусная инфекция может протекать латентно и хронически, с возможными периодическими обострениями (например, хронический тонзиллит).
Примерная формулировка диагноза. 1. Аденовирусное заболевание (ринофаринготонзиллит), течение средней тяжести.
2. Фарингоконъюнктивальная лихорадка, легкое течение.
Патогенез. Патогенез аденовирусной инфекции в деталях остается не полностью расшифрованным (как и при многих других вирусных инфекциях). В основе патогенеза лежит характер взаимодействия вируса с клетками организма.
Для аденовирусов в настоящее время известно 3 типа взаимодействия с клетками организма хозяина.
Первый тип — литическая инфекция с полным репликативным циклом в эпителиальных клетках человека, приводящая к накоплению огромного числа новых вирусных частиц, из которых до 5% являются инфекционными, и гибели клетки хозяина.
Второй тип — латентная или хроническая инфекция, протекающая обычно в лимфоидных клетках. Механизмы латенции до конца не расшифрованы.
Третий тип — онкогенная трансформация клеток хозяина. В этом случае ДНК аденовирусов встраивается в геном клетки хозяина. Роль аденовирусов в онкогенной трансформации подтверждает наличие большого количества специфического аденовирусного Т-антигена в клетках некоторых опухолей.
Для остропротекающих аденовирусных заболеваний человека наиболее характерен первый тип взаимодействия, т.е. литическая инфекция. В патогенезе аденовирусных заболеваний типичным считается поражение слизистых оболочек дыхательных путей, конъюнктив, кишечника, лимфоидной ткани.
Входными воротами, местом первичной локализации и первичного накопления аденовирусов служат эпителиоциты. В зависимости от механизма заражения это может быть эпителий носа, ротоглотки, слизистая оболочка конъюнктивы, эпителий кишечника.
Инкубационный период соответствует времени накопления вирусов в эпителиоцитах и регионарных лимфатических узлах. Воспалительный процесс в дыхательных путях характеризуется резко выраженной экссудацией. Он может протекать как стадийнонисходящий: верхние дыхательные пути -» мелкие бронхи —» легкие. При этом выявляют некроз эпителия трахеи и бронхов, поражение не только слизистого, но и подслизистого слоя, перибронхиальной ткани. Процесс может сопровождаться увеличением трахеобронхиальных и бронхиальных лимфатических узлов. В легких аденовирусы могут интенсивно размножаться, обусловливая возникновение очаговой и (или) интерстициальной пневмонии.
Попадание вируса в кишки может происходить при различных условиях. При наличии назофарингита у больного заглатывание носоглоточной слизи, содержащей аденовирусы, приводит к попаданию их в кишечник и инфицированию его эпителия. При только алиментарном пути заражения эпителий кишок поражается первично с развитием воспалительного процесса и появлением диареи, поражением регионарных лимфатических узлов с симптомами мезаденита, но без признаков вовлечения в процесс дыхательных путей.
Появление лихорадки, интоксикационного синдрома обычно соответствует стадии первичной вирусемии. Наличие вирусемии при аденовирусных заболеваниях доказано выделением аденовирусов из крови (чаще у детей младшего возраста), куда они проникают при разрушении пораженных клеток и по лимфатическим путям. Возникающее при этом повышение проницаемости сосудов способствует развитию резко выраженного экссудативного местного процесса. В дальнейшем происходит выпадение фибрина, что в сочетании с некрозом эпителиальных клеток верхних дыхательных путей и конъюнктивы приводит к образованию пленчатых налетов (на миндалинах, задней стенке глотки, конъюнктиве). Вирусемия обычно довольно длительная. Она может наблюдаться не только при клинически выраженных случаях заболевания, но и при латентной инфекции. На фоне вирусемии происходит занос аденовирусов в паренхиматозные органы (печень, селезенку, почки), лимфатические узлы, нервную систему. Там происходит их дальнейшее размножение и накопление, что сопровождается увеличением печени и селезенки, системной лимфаденопатией. Очевидно, повторные волны вирусемии обеспечивают длительность лихорадки, ее всплески. Имеются доказательства того, что аденовирусы могут находиться в лейкоцитах и мононуклеарных лимфоцитах.
Механизм выздоровления при аденовирусных заболеваниях обусловлен факторами гуморального и клеточного иммунитета.
Антитела к аденовирусам начинают обнаруживаться в крови с 8—10-го дня болезни, достигая максимума через 14—21 день. Определяемые в РН и РСК антитела появляются практически одновременно. Но если уровень комплементсвязывающих антител начинает существенно снижаться уже через 2—4 мес, то высокий уровень нейтрализующих антител почти не меняется в течение многих лет, обеспечивая стойкий длительный типоспецифический иммунитет.
Дети первых б мес жизни, имея типоспецифические материнские антитела, обычно аденовирусными заболеваниями не болеют.
Наиболее восприимчивы к аденовирусам дети в возрасте от б мес до 3 лет. В последующие годы у них увеличивается количество антител к различным типам аденовирусов.
У 80% взрослых обнаруживают антитела к аденовирусам, что свидетельствует о перенесенных заболеваниях и косвенно подтверждает высокую восприимчивость населения к аденовирусной инфекции. Предполагают, что реинфицирование теми же серотипами протекает бессимптомно, в связи с чем взрослые болеют редко.
Имеющиеся сведения об остро протекающих аденовирусных заболеваниях позволяют представить их патогенез в виде следующей схемы (рис. 8).
Примечание. Некоторые (латентные) аденовирусы могут персисти-ровать в организме как в результате бессимптомной инфекции без местной воспалительной реакции, так и после перенесенного аденовирусного заболевания с типичной клинической картиной.
Представленные в табл. 6 сведения дают возможность выбрать оптимальную лечебную тактику с учетом механизма возникновения наиболее типичных клинических симптомов.
Клиника. Инкубационный период при аденовирусных заболеваниях колеблется от 4 до 14 дней, чаще составляя 5—7 дней.
Аденовирусные заболевания отличают следующие особенности:
— полиморфизм клинических симптомов, обусловленный поражением различных органов и систем — дыхательных путей, глаз, кишок, лимфоидной ткани, вовлечением в процесс все новых органов и сис-
Внедрение аденовирусов
|
Кишечник |
Дыхательные пути |
Конъюнктива | |||
|
|
|
|
| ||
|
Регионарный лимфаденит |
|
Размножение и накопление аденовирусов в месте внедрения |
—► |
Стимуляция факторов местной защиты (макрофаги, интерферон,^) | |
Интоксикационный синдром
Генерализация(пер-вичная вирусемия)
Стихание местного процесса
Увеличение печени, селезенки, генерализованная лимфаденопатия
Паренхиматозная диффузия
Стимуляция факто- ров гуморального и клеточного иммунитета
Повторная генерализация
Выздоровление
Рис. 8
Схема патогенеза аденовирусных заболеваний
тем с соответствующим появлением новых симптомов, что и обеспечивает относительно длительное течение заболевания (до 2—3 нед);
преобладание выраженного экссудативного компонента при поражении дыхательной системы над умеренными проявлениями симптомов общей интоксикации;
длительное (от 5—7 до 14 дней и более) повышение температуры тела обычно в пределах 38—39 °С, чаще с лихорадкой неправильного типа (но она может быть различной — постоянной, ремиттирующей, волнообразной).
Манифестные формы аденовирусных заболеваний имеют различные варианты течения.
1. Острое респираторное заболевание — наиболее распространенная форма аденовирусных заболеваний как у детей, так и у взрослых.
Таблица 6. Патогенез основных клинических симптомов аденовирусных заболеваний
Клинические проявления
Механизм возникновения
Ринит Фарингит Тонзиллит Трахеобронхит Конъюнктивит Отек, набухание слизистых оболочек Возможное образование налетов, в т.ч. пленчатых Диарея
Боль в животе
Увеличение селезенки, печени, лимфатических узлов
Повышение температуры
Интоксикация
Поражение ЦНС Менингеальный или менингоэнцефалити-ческий синдром (без изменения состава спинномозговой жидкости) Менингит Менингоэнцефалит (с изменением состава спинномозговой жидкости)
Пневмония
Поражение аденовирусами эпителиальных клеток носовых ходов, глотки, трахеи, бронхов, конъюнктив; дегенерация клеток, воспалительный процесс с вовлечением подслизистого слоя
Поражение эндотелия сосудов: выраженная экссудация, выпадение фибрина на некротизированных клетках эпителия
Поражение аденовирусами эпителия слизистой оболочки кишечника, развитие местного воспалительного процесса с вовлечением подслизистого слоя
Занос и размножение вируса в мезентериальных лимфатических узлах, их увеличение, развитие меза-денита
Занос вируса в период вирусемии в паренхиматозные органы, дальнейшее накопление и размножение аденовирусов в этих органах
Пирогенное действие продуктов распада некротизированных клеток эпителия и циркулирующих клеток периферической крови.
Воздействие токсических антигенов аденовирусов Циркуляторные церебральные расстройства
Занос вируса в ЦНС, развитие специфической воспалительной реакции
Поражение аденовирусами альвеолярных клеток Присоединение вторичной флоры
Часто первым его симптомом является ринит. Кроме отека, набухания слизистых оболочек носовых ходов и затруднения дыхания, у больного отмечается характерная выраженная ринорея. Выделения вначале серозные, вскоре они становятся серозно-слизистыми, впоследствии могут приобретать слизисто-гнойный характер. Длительность ринита может затягиваться до 4 нед.
Одновременно или через 1—2 дня появляются симптомы фарингита и тонзиллита.
Фарингит встречается у 80—90% больных. Он сопровождается умеренной болью в горле при глотании, чувством жжения, «царапания», першения в области задней стенки глотки. Слизистая оболочка ротоглотки отечна, чаще бледная (но возможна умеренная гиперемия с цианозом). Мягкое нёбо обычно интактно. Наибольшая выраженность процесса отмечается на задней стенке глотки, где видны гиперплазиро-ванные фолликулы, что создает впечатление «булыжной мостовой». Это и дает основание говорить о гранулезном фарингите. В отдельных случаях в зоне воспаления могут появляться нежные слизистые налеты, еще реже налеты приобретают пленчатый характер. Но даже в этих случаях они легко снимаются без последующей кровоточивости подлежащих слизистых оболочек.
Фарингит часто (у 50—60% больных) сочетается с тонзиллитом. Миндалины при этом выглядят умеренно набухшими и гиперемиро-ванными. Иногда на них также могут появляться налеты, симулируя картину фолликулярной ангины. Иногда налеты на миндалинах приобретают пленчатый характер. Несмотря на то что имеется объяснение такому характеру налетов (экссудация, выпадение фибрина, некроз эпителиальных клеток), не исключается в этих случаях возможность микст-инфекции с присоединением вторичной микробной флоры (стрептококки, стафилококки), что следует учитывать при назначении лечения и объема диагностических исследований.
В отдельных случаях наблюдается одновременно поражение задней стенки глотки, слизистой оболочки носа, миндалин, что, таким образом, дает клинику комбинированного поражения — ринофаринготон-зиллита.
Дальнейшее нисходящее распространение процесса может приводить к развитию трахеита, бронхита разной степени выраженности. Каких-либо особо характерных признаков они не имеют, но следует помнить о закономерном наличии экссудативного компонента, поэтому кашель обычно продуктивный, со слизистой мокротой. Известны случаи течения аденовирусных респираторных заболеваний с синдромом ложного крупа (у маленьких детей). Возможно, отдельно следует упомянуть о коклюшеподобном синдроме при аденовирусных заболеваниях (некоторые авторы даже выделяют его в отдельную клиническую форму). Речь идет о случаях, когда у больного наблюдают клинические проявления, типичные для коклюша, но при этом не обнаруживают Bordetella pertussis, зато многократно были выделены определенные серотипы аденовирусов. Все же окончательная роль аденовирусов
в таком патологическом состоянии и их взаимоотношение с возбудителями коклюша требуют дополнительного изучения.
Вовлечение лимфоидной ткани в патологический процесс проявляется увеличением прежде всего регионарных лимфатических узлов (подчелюстных, переднеушных, шейных), но возможна и системная лимфаденопатия с увеличением подмышечных, паховых и мезентери-альных лимфатических узлов. Лимфатические узлы увеличиваются нерезко, консистенция их мягкоэластическая, обычно они безболезненны, не спаяны ни между собой, ни с окружающими тканями, не нагнаиваются.
Нередко у больных с респираторным синдромом, кроме лимфадено-патии, можно обнаружить увеличение печени, селезенка пальпируется реже.
Длительность и высота температуры, выраженность интоксикационного синдрома определяются распространенностью процесса и его тяжестью.
2. Пневмония как самостоятельная и первичная форма аденовирус- ной инфекции признается не всеми, но она, очевидно, все же имеет место у детей раннего возраста и больных с иммунодепрессией. Проте- кает она обычно как фульминантное заболевание, сочетаясь с брон- хиолитом. Прогноз обычно неблагоприятный.
Самостоятельность же аденовирусной пневмонии у взрослых, особенно возникающей не в первые дни болезни, как и при многих других вирусных инфекциях, считается спорной. С наибольшей вероятностью, в большинстве случаев имеют место вирусно-бактериальные ассоциации.
Для аденовирусной пневмонии характерна выраженная интоксикация. Заболевание может начинаться остро, с высокой температуры, мышечной боли, кашля со слизистой мокротой. Тяжесть процесса в легких обусловлена вовлечением подслизистого слоя, выраженным экссудативным компонентом, приводящим к нарушению проходимости бронхов. Поражаются преимущественно нижние дыхательные пути по типу очаговой пневмонии. При физикальном обследовании определяются притупление перкуторного тона, обилие влажных хрипов.
Нередко при рентгеноскопии выявляют увеличение паратрахеаль-ных лимфатических узлов. При генерализации процесса могут возникать генерализованная лимфаденопатия, увеличение печени.
Если пневмония возникает не первично, а по нисходящему типу, у больных можно обнаружить и признаки фарингита, тонзиллита, ринита, а нередко и конъюнктивита, обычно предшествующие легочным проявлениям.
Значительно отягощает течение аденовирусной пневмонии присоединение вторичной (бактериальной) инфекции.
3. Фарингоконъюнктивальная лихорадка — наиболее четкая и дос- тупная клинической диагностике форма аденовирусных заболеваний. Она характеризуется наличием конъюнктивита, фарингита, ринита, увеличением лимфатических узлов, повышением температуры до 38 "С. Обычно длительность температуры — 3—5 дней, но она может держаться 12—14 дней и более.
Эта клиническая форма обычно вызывается аденовирусом типа 3. Заболевание чаще начинается остро: появляются царапанье, а затем и боль в горле, заложенность носа, ломота во всем теле, боль в глазах, повышается температура тела. Эти симптомы могут появляться одновременно или развиваться последовательно в течение 1—2 дней (в таком случае первыми признаками являются поражения дыхательной системы).
Конъюнктивит при аденовирусных заболеваниях, пожалуй, один из самых характерных клинических симптомов, позволяющий отличить их от других острых респираторных инфекций.
Конъюнктивит бывает катаральный, фолликулярный и пленчатый. Наиболее типичны фолликулярный и пленчатый. Он может появляться в первые дни болезни или позже, даже на второй волне заболевания. Больные при этом часто предъявляют жалобы на резь и ощущение «песка» в глазах. Но таких жалоб может и не быть, а патологические изменения при внимательном обследовании больного все же находят. В типичных случаях глазная щель сужена, веки отечны, резко отечна, гипе-ремированная конъюнктива, появляется скудное отделяемое. Иногда отчетливо видны гиперплазированные фолликулы (отечная слизистая оболочка будто посыпана песком). На фоне резко выраженной экссудации может появиться пленчатый налет.
Обычно вначале поражается один глаз, но часто вскоре присоединяется поражение и второго глаза.
Конъюнктивит сохраняется часто и после снижения температуры, тогда как боль в горле к этому времени обычно проходит. Регионарный лимфаденит выявляется еще дольше (иногда в течение нескольких недель). Заболевание сопровождается общеинтоксикационным синдромом (мышечная и головная боль, слабость, отсутствие аппетита), иногда возникают явления менингизма. Возможна длительная астенизация (особенно у детей) после перенесенного заболевания.
4. Эпидемический кератоконъюнктивит вызывается наиболее часто аденовирусом типа 8. При этом инкубационный период может удлиняться до 24 дней, а конъюнктивит может сохраняться до 4 нед.
Начало заболевания обычно постепенное, часто поражаются оба глаза сразу. Почти всегда увеличены предушные лимфатические узлы. Кератит обычно развивается уже тогда, когда конъюнктивит идет на убыль, но длится он долго — иногда несколько месяцев — и может приводить к снижению зрения. Интоксикационный синдром, как правило, выражен слабо. Катаральные явления отсутствуют, и этиологию керато-
конъюнктивита уточняют, исследуя соскобы и смывы с конъюнктивы, где удается обнаружить аденовирус. Заболевание может протекать и как конъюнктивит без вовлечения в процесс роговицы. В этом случае жжение в глазах и слезотечение остаются основными жалобами.
Лица, находящиеся в близком контакте с больными, инфицированными аденовирусами типов 8, 19, 37, подвергаются значительному риску инфицирования (отсюда название «эпидемический кератоконъюнк-тивит»). Остальные типы аденовирусов могут вызывать лишь спорадические случаи конъюнктивита, протекающие чаще по типу фолликулярного.
5. Геморрагический цистит — редко встречающаяся форма адено- вирусной инфекции. Болеют преимущественно дети и молодые люди. Заболеваемость среди мальчиков в 2,5—3 раза выше, чем среди дево- чек, что ставит под сомнение инфекцию восходящую. Вместе с тем, аденовирус у таких больных выделить из крови еще не удавалось (ви- русемия отсутствует?). Таким образом, путь проникновения вируса в мочевые пути остается еще невыясненным.
Заболевание начинается обычно внезапно с выраженных дизуриче-ских явлений (боль при мочеиспускании, частые позывы, в том числе ложные). Одновременно появляется макрогематурия, которая сохраняется несколько (до 3—4) дней, а в дальнейшем еще в течение 7—10 дней может выявляться микрогематурия. К этому времени уменьшается и выраженность дизурических явлений. Общая длительность заболевания — до 2 нед. Многократные бактериологические исследования в этих случаях отрицательны («стерильная моча»), но при вирусологическом исследовании часто удается обнаружить аденовирусы типов 11 и 21.
Аденовирусы типа 11 могут вызывать и субклинические формы болезни, что подтверждается частым обнаружением у детей, не имевших соответствующих клинических проявлений, как аденовирусов, так и антител к аденовирусам.
6. Диарея (гастроэнтерит) как отдельная клиническая форма забо- левания возникает в подавляющем большинстве случаев у новорож- денных и детей младшего возраста. Для нее характерно острое, неред- ко бурное начало с тошнотой, рвотой, частым жидким стулом. Чем бы- стрее стул теряет каловый характер, тем тяжелее течение, так как воз- можно значительное обезвоживание.
Сначала возникают боль в животе, урчание и вздутие кишечника. Температура тела может повышаться до 39—39,5 "С. В большинстве случаев диарея у детей сочетается с признаками поражения дыхательных путей и конъюнктивитом. Наиболее частыми этиологическими агентами таких энтеритов являются аденовирусы типов 1 и 3.
Однако в последние годы доказано, что аденовирусы типов 40 и 41 также способны вызывать диарею. Они получили название «кишечные», или «некультивируемые», из-за особенностей своей репликации. Эти аденовирусы могут вызвать изолированный диарейный синдром без признаков поражения других органов и систем.
Диарея может возникать и у взрослых, но она обычно протекает намного легче, чем у детей: больные жалуются на слабость, приступообразную боль по всему животу, жидкий стул. У взрослых диарея не сопровождается обезвоживанием. Температура тела может подниматься до 38 "С, но обычно общеинтоксикационный синдром выражен умеренно. Длительность заболевания — 1—4 дня.
Особым вариантом кишечной формы аденовирусной инфекции является инвагинация кишок, которая возникает преимущественно у детей. Этиологическая связь с аденовирусной инфекцией подтверждалась обнаружением в клетках эпителия кишок и лимфатических узлах аденовирусов типов 1, 2, 3 и 5. Нередко инвагинации предшествует респираторный синдром (ринит, фарингит, тонзиллит), что далеко не всегда учитывают при верификации диагноза. Этот вариант можно рассматривать и как осложнение аденовирусной инфекции.
Во время операции в таких случаях практически всегда обнаруживают значительное увеличение регионарных лимфатических узлов (регионарный мезаденит), что и является, как полагают, основной причиной инвагинации.
При обследовании этих больных следует помнить, что, несмотря на большую частоту выделения аденовирусов при оперативных вмешательствах, нарастание титров сывороточных антител бывает редко, поэтому серологические методы диагностики не используются для верификации диагноза.
7. Поражение нервной системы при аденовирусных заболеваниях чаще проявляется в виде общемозговой симптоматики вследствие церебральных циркуляторных расстройств и квалифицируется как ме-нингизм. При этом симптомы, свидетельствующие о поражении ЦНС (упорная головная боль, ригидность мышц затылка, положительный симптом Кернига), возникают на фоне клинических проявлений одной из форм аденовирусных заболеваний (ОРЗ, пневмония, фарингоконъ-юнктивальная лихорадка и др.). При спинномозговой пункции, приносящей больному явное облегчение, спинномозговая жидкость вытекает под повышенным давлением, но ее состав в большинстве случаев не изменен.
Однако описаны варианты течения с преимущественным специфическим аденовирусным поражением нервной системы: серозный менингит и менингоэнцефалит, полирадикулоневрит. Диагноз подтверждается нарастанием титров антител в крови и обнаружением аденовирусных антигенов в спинномозговой жидкости при использовании РФА. Такие клинические формы могут возникать как самостоятельно,
так и в сочетании с другими проявлениями аденовирусных заболеваний или на их фоне.
8. Особый интерес представляет пока еще недостаточно изученный феномен — течение аденовирусных заболеваний у больных с иммунодефицитом, в частности СПИДом. У таких больных из крови и мочи чаще выделяют аденовирусы типов 34 и 35. Заболевание обычно протекает по типу пневмонии или цистита. Изучается степень и характер связи между ВИЧ и аденовирусами.
Аденовирусная инфекция —■ патология преимущественно детского возраста. Но у новорожденных первых месяцев жизни она может протекать легко или даже бессимптомно, если мать имеет достаточно напряженный иммунитет. Тяжело болеют дети 1 -го года жизни, это наиболее уязвимая группа. У них респираторные проявления могут сочетаться с ложным крупом, астматическим синдромом, дыхательной недостаточностью, а диарейный синдром сопровождаться обезвоживанием.
У детей старшего возраста преобладают легкие формы заболевания в виде ринита, фарингита.
Взрослые болеют реже и сравнительно легко. Связано это не столько с наличием специфических антител к определенному типу вируса, сколько с защитной ролью гетерологичных антител (то есть антител к другому типу аденовируса, отличному от того, который циркулирует в настоящее время). Полагают, что частые инфицирования человека различными серотипами аденовирусов приводят к увеличению напряженности гуморального иммунитета как к гомологичным, так и к гетероло-гичным видам. В связи с этим в большинстве случаев реинфекция не сопровождается развитием заболевания или протекает легко.
Некоторые формы заболевания у взрослых (тонзиллит, фарингит) бывают обусловлены активацией латентной инфекции, чаще на фоне других заболеваний, снижающих общую и местную реактивность организма.
Осложнения. Чаще всего они связаны с вторичной инфекцией и проявляются пневмонией, синуситом, отитом. Более того, существует мнение, что в большинстве случаев аденовирусное поражение дыхательных путей сопровождается присоединением или активацией дополнительной, чаще бактериальной, инфекции, что существенно сказывается на течении и исходах аденовирусных заболеваний, особенно у маленьких детей.
Еще остается нерешенным вопрос о возможной роли аденовирусов в развитии перикардита, краснухоподобного синдрома, врожденных уродств и других патологических состояний. Исследователи признают, что аденовирусная инфекция может быть причиной таких осложнений, как долевые ателектазы, бронхоэктатическая болезнь (главным образом у детей).
Увеличение печени может сопровождаться нарушением ее функции, развитием желтухи. Эти проявления обычно нерезко выражены, но могут привести иногда к определенным сложностям при дифференциальной диагностике с вирусным гепатитом.
Исходы аденовирусных заболеваний в большинстве случаев благоприятные. Летальные случаи (от интоксикации, легочной недостаточности, обезвоживания) редки и бывают главным образом у детей 1-го года жизни.
Методы диагностики. Общеклинические методы. При исследовании крови выявляется нормоцитоз или умеренный лейкоцитоз, в формуле крови — небольшой нейтрофилез, лимфопения. В период реконвалесценции может появляться небольшая эозинофилия. СОЭ нормальная или незначительно увеличена.
Существенные изменения в моче (макрогематурия в сочетании с единичными лейкоцитами) появляются лишь при геморрагическом цистите. В остальных случаях моча без патологических изменений, лишь при тяжелой интоксикации могут появляться единичные эритроциты и цилиндры.
При развитии аденовирусного менингоэнцефалита в спинномозговой жидкости выявляется умеренный цитоз (до 200 клеток в 1 мм3) со значительным преобладанием лимфоцитов (до 90 %).
Биохимические исследования. При появлении желтухи необходимо исследовать уровень билирубина, активность АлАТ, АсАТ.
Уровень билирубина может быть повышен незначительно (в 1,5—2 раза), преимущественно за счет прямого.
Активность АлАТ и АсАТ при увеличенной печени, и тем более желтухе, также может повышаться, но не более чем в 2—4 раза. Крайне редко отмечается более выраженный цитолиз. В этих случаях целесообразно более детальное обследование для исключения вирусного гепатита.
На фоне небольшой желтухи могут стать слабоположительными реакции на уробилин и желчные пигменты в моче.
Специфическая диагностика. Вирусологические методы диагностики предусматривают выделение аденовирусов в культуре чувствительных клеток из содержимого носоглоточного секрета, мокроты, фекалий, отделяемого с конъюнктивы. Метод трудоемкий, длительный, дорогостоящий, и в повседневной клинической работе его не применяют.
Обнаружение антигенов аденовирусов в пораженных клетках верхних дыхательных путей и конъюнктивы с использованием РФА по общепринятым методикам вполне приемлемо и доступно для клиницистов. Этот метод позволяет обнаруживать вирус в острый период заболевания, в период реконвалесценции, а также выявлять латентные вирусы.
Для обнаружения вируса в фекалиях при диарее используют также РФА.
Серологическая диагностика основана на определении нарастания титров антител в парных сыворотках (РСК, РН, РТГА, РНГА). Диагностическим считается четырехкратное нарастание титров антител.
С учетом наличия латентных форм аденовирусной инфекции выделение вируса из организма человека должно сочетаться с достоверными серологическими результатами.
Критерии диагноза. Аденовирусные заболевания распознают на основании совокупности клинических синдромов, наиболее постоянными из которых являются:
— преимущественное поражение верхних отделов дыхательных путей по типу гранулезного фарингита, тонзиллита, ринита с выраженным экссудативным компонентом и нерезкой местной гиперемией;
— лимфаденопатия, нередко генерализованная;
возможность сочетания респираторного синдрома с конъюнктивитом (фолликулярным, пленчатым), нередко односторонним;
возможное сочетание респираторного синдрома и диареи (обычно умеренной);
увеличение печени (реже и селезенки);
умеренно выраженный интоксикационный синдром;
— последовательное появление отдельных клинических симптомов, свидетельствующих о вовлечении в патологический процесс новых органов и систем;
— длительность заболевания 2—3 нед.
Полиморфизм клинических проявлений аденовирусных заболеваний определяет многообразие клинических форм, при которых отдельные вышеизложенные ведущие симптомы могут отсутствовать. Тем более важную роль в постановке диагноза играет наличие хотя бы 3—4 из перечисленных.
Дифференциальный диагноз. Дифференциальный диагноз при аденовирусных заболеваниях нередко бывает сложен, что обусловлено полиморфизмом клинических проявлений разных форм и вовлечением в патологический процесс многих органов и систем.
В целях систематизации дифференциальной диагностики представляется оправданным использование синдромального подхода.
Поражение дыхательных путей, повышение температуры, симптомы общей интоксикации встречаются практически при всех респираторных инфекциях.
Для гриппа и аденовирусных заболеваний общими симптомами являются: повышение температуры тела, симптомы токсикоза, признаки поражения верхних дыхательных путей. Отличительными симптомами гриппа являются:
— острое, внезапное начало;
— наличие выраженного общего токсикоза;
поражение дыхательной системы по типу трахеита с выраженной болью за грудиной при кашле (при аденовирусных заболеваниях трахеит возможен, но это — весьма умеренно выраженный и непостоянный симптом);
отсутствие заметного экссудативного компонента, что проявляется заложенностью носа, а не ринореей, сухим кашлем;
отек и яркая гиперемия слизистых оболочек полости рта без признаков тонзиллита, гранулезного фарингита;
— отсутствие явлений гранулезного, пленчатого конъюнктивита (конъюнктивы отечные, гладкие, блестящие, гиперемированные, склеры обоих глаз инъецированы равномерно);
— отсутствие генерализованной лимфаденопатии, увеличения печени и селезенки, диарейного синдрома;
длительность неосложненного гриппа не более 5—б дней. Парагрипп имеет следующие отличия:
незначительный токсикоз;
респираторный синдром проявляется в виде ларингита (с осиплостью голоса, лающим кашлем);
отсутствие ринореи, тонзиллофарингита; генерализованной лимфаденопатии; гепатолиенального синдрома; экссудативного компонента; конъюнктивита, кератита.
Риновирусные заболевания могут протекать не только с явлениями ринита, но в ряде случаев сопровождаются, как и аденовирусные, фарингитом и даже трахеитом. Их отличия:
выраженная ринорея с обильным серозным отделяемым (ведущий симптом!);
отсутствие интоксикации (в большинстве случаев) и грануляций на задней стенке глотки, тонзиллита, а также лимфаденопатии, гепатолиенального синдрома, поражений глаз.
Коронавирусные заболевания, как и аденовирусные, сопровождаются ринитом с серозно-слизисто-гнойным отделяемым, умеренной лихорадкой и интоксикацией. Могут быть фарингит и трахеит, в связи с чем клинический дифференциальный диагноз бывает весьма сложен. Тем не менее такие признаки, как конъюнктивит, лимфаденопа-тия, гепатолиенальный синдром, при коронавирусной инфекции отсутствуют.
При PC-инфекции, как и при аденовирусной, могут поражаться нижние дыхательные пути — бронхи, бронхиолы, легочная ткань. Однако в отличие от аденовирусных бронхита, трахеита, при PC-инфекции наблюдают:
— преимущественно поражения нижних дыхательных путей (у детей), трахеи и бронхов (у взрослых);
— процесс не сопровождается выраженным экссудативным компонентом;
интактны миндалины, задняя стенка глотки;
не увеличены печень, селезенка;
отсутствует гранулезный конъюнктивит.
Микоплазменные заболевания верхних дыхательных путей весьма сходны с аденовирусными. Для обоих характерны умеренный токсикоз с длительной (до 2 нед и более) лихорадкой, возможны явления трахеобронхита. Но при микоплазмозе:
— отсутствуют явления тонзиллофарингита, конъюнктивита (тем более одностороннего);
— слабо виражен ринит;
— нет системного поражения лимфоидной ткани. Энтеровирусные заболевания с симптомокомплексом поражений
верхних дыхательных путей, фарингитом могут протекать и с лимфа-денопатией, диарейным синдромом, что затрудняет их дифференциальную диагностику с аденовирусными заболеваниями.
В пользу заболеваний энтеровирусной этиологии наиболее надежно свидетельствуют:
отсутствие кератоконъюнктивита;
слабо выраженный экссудативный компонент.
— генерализованная лимфаденопатия редко встречается при энте-ровирусных заболеваниях в отличие от аденовирусных.
Инфекционный мононуклеоз может иметь много общего с аденовирусными заболеваниями: длительная лихорадка с умеренным токсикозом, системная лимфаденопатия, тонзиллит с различными по характеру налетами, увеличение размеров печени и селезенки, поражение конъюнктивы. Отличить инфекционный мононуклеоз от аденовирусного заболевания помогают:
меньшая выраженность экссудативного компонента (не ринорея, а лишь заложенность носа);
наличие только инъекции сосудов конъюнктивы (нет гранулезного и тем более пленчатого конъюнктивита);
четче выражена лимфаденопатия, часто возникает генерализованная лимфаденопатия;
большая выраженность гепатолиенального синдрома;
общий анализ крови: относительный лимфоцитоз, моноцитоз и увеличение числа атипичных мононуклеаров (вироцитов).
Тонзиллит или тонзиллофарингит со слизисто-гнойными налетами, ринит, умеренная температурная реакция и умеренные симптомы общего токсикоза являются общими для аденовирусного заболевания и менингококкового назофарингита. В дифференциальной диагностике могут помочь симптомы, характерные лишь для менингококкового назофарингита:
— наличие гнойной «дорожки» на задней стенке глотки;
увеличение преимущественно подчелюстных лимфатических узлов (генерализованная лимфаденопатия отсутствует);
отделяемое из носа с первых дней болезни носит слизисто-гной-ный характер;
— конъюнктивит не характерен;
— возможны кровоизлияния в склеру, если начинается менинго-кокцемия;
печень, селезенка не увеличены;
токсикоз весьма умеренный.
Тонзиллит, фарингит в сочетании с увеличением регионарных (подчелюстных) лимфатических узлов, интоксикацией может наблюдаться как при аденовирусных заболеваниях, так и при катаральной дифтерии миндалин. Поставить истинный диагноз еще сложнее, если при дифтерии в процесс вовлекается слизистая оболочка носа (то есть возникает ринофаринготонзиллит).
Основными отличиями дифтерийного поражения слизистой оболочки ротоглотки, носа и миндалин являются:
— степень токсикоза часто не соответствует характеру и выраженности местных изменений (т.е. он более выражен);
в ротоглотке отек преобладает над гиперемией;
голос может приобретать гнусавый оттенок;
отделяемое из носа — слизисто-гнойное, иногда даже с прожилками крови (при дифтерии носа);
увеличены и болезненны шейные лимфатические узлы; генерализованной лимфаденопатии нет;
возможен отек подчелюстного пространства и шеи с одной или обеих сторон;
печень и селезенка не увеличены;
конъюнктивит не характерен.
В том случае, если при дифтерии на миндалинах появляются характерные грязно-серые налеты, дифференциальная диагностика значительно облегчается. Хотя не следует забывать о том, что значительный экссудативный компонент при аденовирусных заболеваниях может привести к образованию на миндалинах и задней стенке глотки нежного беловатого налета. Такой налет бывает и при дифтерии, преимущественно в первые дни болезни. Но при проведении дифференциальной диагностики тем большее значение приобретают все остальные вышеперечисленные признаки. К тому же пленчатые налеты на миндалинах при аденовирусных заболеваниях — довольно редкий признак, снимаются они легко, обнаженная поверхность не кровоточит.
Повышение температуры тела, интоксикация, увеличение печени и селезенки, иктеричность склер, а иногда и кожи могут привести к
ошибкам в дифференциальной диагностике между ВГА и аденовирусным заболеванием. ВГА отличают:
кратковременная лихорадка, предшествующая желтухе (не более 3—4 дней);
отсутствие катарального синдрома, конъюнктивита, лимфадено-патии;
отчетливо определяющийся с первых дней болезни гепатолие-нальный синдром;
значительное ( в десятки раз) повышение активности клеточных ферментов (АлАТ, АсАТ), тогда как при аденовирусных заболеваниях цитолитический синдром обычно выражен слабо;
в крови обнаруживают основные маркеры острого вирусного гепатита А — анти-HAV IgM и HAV.
Поражения глаз в виде конъюнктивита и кератоконъюнктивита могут наблюдаться не только при аденовирусных заболеваниях, но и при энтеровирусных, дифтерии глаза, глазобубонной форме туляремии.
Пленчатая форма конъюнктивита аденовирусной этиологии может напоминать дифтерию глаза. Но дифтерийное поражение глаза отличают:
— редкость возникновения изолированного дифтерийного поражения глаза (обычно оно встречается с дифтерией другой локализации), т.е. при комбинированных формах;
— постепенное начало;
— характер изменений (пленки, после удаления которых обнажается кровоточащая поверхность);
— отсутствие системной лимфаденопатии, гепатомегалии. Возможность быстрого получения результатов бактериоскопическо-
го исследования отделяемого конъюнктивы при дифтерии позволяет во многих случаях уже в первые часы пребывания больного в стационаре провести более четкую дифференциальную диагностику между аденовирусной и дифтерийной этиологией процесса (обращают внимание на наличие в мазках палочек, морфологически сходных с дифтерийными).
Эпидемический геморрагический конъюнктивит, вызываемый энтеровирусом-70, имеет много общих черт с аденовирусным эпидемическим кератоконъюнктивитом. Отличительными чертами при энтеро-вирусном поражении можно считать большую частоту кровоизлияний в конъюнктиву и меньшую частоту пленчатых налетов. Для окончательного решения вопроса нужны лабораторные исследования.
Конъюнктивит может возникать при таких вирусных заболеваниях, как корь, ветряная оспа, грипп и другие, но во всех этих случаях он является одним из проявлений общеинфекционного процесса (причем далеко не главным). Характерно при этом поражение обоих глаз, выра
scanned
женность проявлений конъюнктивита уменьшается с угасанием основных клинических симптомов этих заболеваний.
Фолликулярный конъюнктивит может вызываться вирусом простого герпеса. Но при этом:
— в процесс почти закономерно вовлекается роговица;
— везикулезные высыпания часто обнаруживают на губах, по краю век;
— отсутствуют генерализованная лимфаденопатия и гепатомегалия. Для глазобубонной формы туляремии основными отличительными признаками следует считать:
— наличие некротических изменений в конъюнктиве с частым образованием язвочек;
наличие регионарного резко болезненного бубона;
отсутствие системной лимфаденопатии;
отсутствие катаральных явлений.
Конъюнктивит могут вызывать и другие бактерии — стафилококки, пневмококки, гонококки и др. При этом, как и при аденовирусных заболеваниях, может наблюдаться односторонний процесс, отек конъюнктивы, века. Однако основными отличиями бактериальных воспалительных процессов являются:
гнойное отделяемое (иногда столь обильное, что веки как бы склеиваются);
отсутствие катаральных явлений (или незначительная их выраженность);
незначительный интоксикационный синдром;
отсутствие лимфаденопатии, гепатоспленомегалии.
Диарея аденовирусной этиологии не имеет дифференциально-диагностических отличий от вирусной диареи другой этиологии, прежде всего ротавирусной. Существенную помощь, тем не менее, при установлении клинического диагноза оказывают наличие, сроки появления, характер и выраженность поражений дыхательной системы, глаз, столь часто наблюдающиеся при аденовирусных заболеваниях. Но расшифровка диагноза иногда возможна лишь при использовании комплекса лабораторных исследований.
Мезаденит аденовирусной этиологии протекает в сочетании с другими симптомами аденовирусных заболеваний и не встречается как моносимптомное заболевание.
Лечение. Этиотропные препараты для лечения больных аденовирусными заболеваниями пока не разработаны.
В большинстве случаев аденовирусные заболевания у взрослых протекают в легкой форме и в специальном лечении не нуждаются.
Лечение большинства больных проводят в домашних условиях. Госпитализации подлежат больные с тяжелым течением аденовирусных
заболеваний (пневмония, поражение нервной системы), осложнениями (пневмония) и по эпидемиологическим показаниям.
В диету следует включать свежие овощи, фрукты. При невозможности обеспечить полноценное витаминное питание за счет естественных продуктов и при тяжелом течении инфекции можно использовать аскорбиновую кислоту, рутин.
Основные рекомендации по лечению больных соответствуют таковым при других ОРВИ: не нагружать больного жаропонижающими и аналгезирующими препаратами, не назначать антибактериальные препараты с профилактической целью.
Даже при тяжелой форме аденовирусной инфекции вряд ли оправдано внутримышечное введение нормального иммуноглобулина человека.
В случае развития пневмонии или других бактериальных осложнений показано назначение антибиотиков. Выбор антибиотика и дозы зависит от тяжести и характера осложнений. Целесообразность назначения антибиотиков тетрациклинового ряда всегда следует тщательно взвешивать, учитывая возможное поражение печени при аденовирусных заболеваниях.
Объем и характер дезинтоксикационной терапии (внутривенная или пероральная детоксикация, ее состав) определяются клиническими особенностями течения болезни, степенью токсикоза и метаболических нарушений.
Для облегчения носового дыхания и уменьшения экссудации можно рекомендовать местно нафтизин, санорин, галазолин.
При явлениях трахеита, фарингита показаны ингаляции растворов новоиманина, ромашки, эвкалипта, а также различные отхаркивающие средства, полоскание горла теплыми щелочными растворами (аденовирусы устойчивы в кислой среде).
Лечение при конъюнктивите и кератоконъюнктивите должно осуществляться обязательно совместно с окулистом. Можно использовать 0,2% раствор дезоксирибонуклеазы, его закапывают в конъюнктиваль-ный мешок несколько раз в день. Лечение может быть длительным, в течение нескольких недель.
При наличии менингеального синдрома назначают мочегонные средства (маннитол, лазикс, фуросемид), эуфиллин. Но иногда может возникнуть необходимость и в спинномозговой пункции, тем более, что она позволяет провести дифференциальную диагностику менин-гизма и менингита.
Порядок выписки из стационара. Выписывают реконвалесцентов по клиническим показаниям (стойкая нормализация температуры, удовлетворительное состояние, обратное развитие имевшихся симптомов, отсутствие осложнений). Срок выписки на работу определяет индивидуально участковый врач.
Диспансерное наблюдение за переболевшими не предусмотрено.
Профилактика. Общая профилактика аденовирусных заболеваний состоит прежде всего из комплекса неспецифических мер: выявление и изоляция больных, текущая дезинфекция.
Специфическая профилактика была разработана в США для новобранцев в армейских коллективах. Вначале использовали формализованную вакцину из убитых аденовирусов типов 3, 4 и 7, выращенных в культурах почек обезьян. Но после открытия феномена образования гибридных вирусов эту вакцину использовать перестали и в дальнейшем перешли на применение живой пероральной вакцины.
Вакцинацию детей не проводят, так как иммунизация их аттенуиро-ванной вакциной из аденовирусов типов 4 и 7 оказалась неэффективной.
Ослабленным детям ясельного возраста, контактировавшим с больным, может проводиться экстренная профилактика нормальным иммуноглобулином человека (вводят однократно). Но так как эта мера не гарантирует от развития заболевания, а риск суперинфицирования всегда сохраняется, врач всегда должен сам определить степень целесообразности и безопасности этой процедуры.
Ветряная оспа и опоясывающий лишай
Ветряная оспа — инфекционное антропонозное заболевание с капельным механизмом передачи, возникающее при первичном инфицировании Varicella zoster virus (VZV) и характеризующееся в типичных случаях появлением везикулезных высыпаний на фоне умеренной интоксикации (лат. — varicella, англ. — varicella, chickenpox).
Опоясывающий лишай — рецидивы VZV-инфекции, возникающие в результате активации VZV, сохраняющихся преимущественно в нервных ганглиях после первичного инфицирования (herpes zoster — лат., англ.).
К такой активации может привести снижение реактивности организма под влиянием самых разнообразных экзо- и эндогенных факторов.
Краткие исторические сведения. Ветряная оспа известна с глубокой древности. Длительное время она отождествлялась с натуральной оспой и считалась легким вариантом ее течения. В 1772 г. Vogel выделил это заболевание в самостоятельную нозологическую единицу под названием «varicella».
Лишь в 1909 г. J.Bokay обратил внимание на этиологическую общность ветряной оспы и опоясывающего лишая, а два года спустя (1911 г.) у больных ветряной оспой были обнаружены и описаны бразильским ученым Араго особые образования, в дальнейшем получившие название «тельца Араго». Однако выделен сам вирус был лишь в 1951 г., с этого времени начинается настоящее изучение патогенеза заболеваний, вызываемых VZV. В дальнейшем идентичность вирусов, вызывающих оба заболевания, была подтверждена с помощью лабораторных исследований (электронная микроскопия, выделение вируса на культуре тканей, серологические реакции), а вирус получил название «varicella zoster virus — VZV».
В то время как ветряная оспа известна давно, опоясывающий лишай как вирусное заболевание изучают лишь с начала XX ст., а поэтому данные о его распространении, патогенезе еще накапливаются.
Актуальность. Ветряная оспа имеет повсеместное распространение и по числу регистрируемых заболеваний занимает третье место после гриппа и других ОРЗ. В большинстве стран заболеваемость выше в городских населенных пунктах (700—900 на 100 000 населения) и значи
smartpe
тельно меньше — в сельских. Болеют в основном дети: на возраст до 14 лет приходится 80—90% всей заболеваемости. Высокая контагиозность и почти 100 % восприимчивость к этой инфекции оправдывают ее название «детская инфекция». Относительно нетяжелое течение, низкая летальность были долгое время причиной спокойного отношения к этой инфекции. Однако сейчас значительно расширились наши сведения о клинических проявлениях заболеваний, вызываемых VZV, при которых, как оказалось, поражаются не только кожа и нервная система, но и пищеварительный тракт, легкие, мочеполовая система. Вирус оказывает также влияние на развитие плода и течение беременности.
Установлена возможность активации вируса на фоне неопластических процессов, болезней крови, ВИЧ-инфекции и других заболеваний, которые сопровождаются иммунодефицитом.
Этиология. VZV относится к семейству герпесвирусов (Herpesviri-dae), включающему множество вирусов, вызывающих заболевания у птиц, животных, земноводных, человека. Возбудители этого семейства разделены на 3 подсемейства:
— Alphaherpesviruses (включает вирусы простого герпеса — ВПГ 1 и 2 типов и VZV);
— Betaherpesviruses (представитель — цитомегаловирус — CMV);
— Gammaherpesviruses (представитель — вирус Эпштейна—Барр — EBV).
Семейство герпесвирусов изучают, дополняют новыми представителями, связь которых с патологией человека еще предстоит уточнить (например, лимфотропные вирусы герпеса).
Герпесвирусы имеют сходную структуру, геном их состоит из дву-нитчатой ДНК, вирион представлен капсидом и окружен оболочкой, содержащей липиды. Несмотря на большое сходство, эти возбудители имеют ряд различий в структуре генома, капсида, оболочки, тропности к отдельным тканям, чувствительности к ним различных лабораторных животных, характеру процесса, вызываемого в зараженном организме.
Все герпесвирусы чувствительны к химическому и физическому воздействию, в том числе к высокой температуре, длительно сохраняются при замораживании (до 70 °С), но при повторном оттаивании и замораживании быстро теряют свою инфекциозность, что необходимо учитывать при ампулировании и хранении исследуемого материала.
Репродукция вирусов в организмах чувствительных животных начинается в ядрах клеток, в цитоплазме обнаруживают зрелые частицы.
Большинство вирусов этой группы обладают способностью длительно, а нередко и пожизненно, персистировать в зараженном организме, что дает основание относить их к возбудителям медленных инфекций.
Заболевания, вызываемые представителями этого семейства вирусов, отличаются высокой контагиозностью, в связи с чем инфициро-ванность населения наступает в большинстве случаев уже в детском
возрасте. Вирусы обладают отчетливым тератогенным, а многие из них — еще и онкогенным свойствами: возникновение лимфомы Бер-китта, саркомы Капоши, рака молочной железы и половых органов, карциномы носоглотки связывают с действием этих вирусов. Им свойственна полиорганность поражений. Наряду с локализованными, могут возникать генерализованные формы с поражением ЦНС, легких, печени, других органов и систем, дающие высокую летальность, особенно у новорожденных.
Сами обладая иммунодепрессивным свойством, вирусы семейства Herpesviridae активируются на фоне других заболеваний, угнетающих защитные силы организма (лейкоз, новообразования, СПИД), поэтому их считают маркерами иммунодефицита.
VZV имеет диаметр 160—200 нм. Его нуклеокапсид включает 162 капсомера. Оболочка выявляется не у всех вирусов. Но инфекционные свойства присущи лишь тем вирионам, которые имеют оболочку.
VZV обладает выраженной антропонозностью, им редко удается заразить человекообразных обезьян или морских свинок, что затрудняет экспериментальное изучение инфекции. В лабораториях вирус выращивают на культурах клеток человека (костно-мышечная ткань, клетки амниона, почек). В организме человека VZV проявляет тропность к эпителиальным клеткам, к клеткам слизистых оболочек, нервной ткани, что и определяет ведущую клиническую симптоматику. На фоне выраженного иммунодефицита спектр чувствительности к вирусу увеличивается, и может в результате возникать поражение различных органов и систем.
VZV чувствителен к действию ДНК-ингибиторов (ацикловир, вида-рабин и др.). Нечувствителен к действию антибиотиков и сульфаниламидов.
Эпидемиология. Источником инфекции при заболеваниях, вызываемых VZV, являются больные не только ветряной оспой, но и опоясывающим лишаем. Вирус содержится в элементах сыпи на коже и слизистых оболочках.
Хотя ветряную оспу традиционно относят к респираторным инфекциям, в смывах из носоглотки вирус обнаруживается лишь тогда, когда появляются высыпания на слизистых оболочках полости рта, и то в значительно меньшем количестве, чем в содержимом пустул и везикул на коже. Корочки вирус не содержат. Эта особенность и определяет период заразности больного — с момента появления высыпаний на слизистых оболочках и коже до периода образования корочек.
Механизм заражения — преимущественно капельный (при наличии высыпаний на слизистых оболочках), контактный и реже — вертикальный. Передать инфекцию плоду может мать, больная либо ветряной оспой (что бывает крайне редко, так как к периоду детородного возраста практически все женщины успевают пройти этап первичного ин-
фицирования), либо опоясывающим лишаем. VZV может проникать через плаценту и инфицировать плод в течение всего периода беременности. Если заражение происходит в I триместре, существует реальная опасность развития уродств плода, если в более поздние сроки, то у такого ребенка после рождения инфекция чаще проявляется не в форме ветряной оспы, а в форме опоясывающего лишая.
Таким образом, первичное инфицирование, независимо от того, произошло оно от больного ветряной оспой или опоясывающим лишаем, проявляется в виде ветряной оспы. Для опоясывающего лишая характерен эндогенный механизм реактивации персистентной инфекции. Описаны случаи развития опоясывающего лишая после вакцинации против ветряной оспы.
Восприимчивость населения к ветряной оспе очень высока (90— 95%). Дети в возрасте до одного года устойчивы к заражению в связи с наличием пассивного (материнского) иммунитета. По мере его угасания восприимчивость возрастает. Самая высокая заболеваемость приходится на детей в возрасте 4—5 лет, после чего у них вирус переходит в состояние длительной персистенции. По мере угасания приобретенного иммунитета преимущественно регистрируется опоясывающий лишай, 45% которого приходится на больных старше 65 лет.
Таким образом, ветряной оспой болеют преимущественно дети и лица молодого возраста, а опоясывающим лишаем — пожилые люди. Но отдельные случаи ветряной оспы и опоясывающего лишая бывают у лиц всех возрастных групп. Ветряную оспу регистрируют как в виде спорадических случаев, так и в виде массовых заболеваний (вспышек) в детских коллективах. Опоясывающий лишай обычно носит спорадический характер и связан с состоянием иммунитета инфицированного, на который могут оказывать влияние различные факторы. Но и он может быть причиной эпидемических вспышек ветряной оспы в детских коллективах, если там появляется больной опоясывающим лишаем.
Периодичность подъема заболеваемости ветряной оспой с возникновением эпидемий составляет несколько лет (малые циклы) и с интервалами 20 лет и более (большие циклы).
Подъем заболеваемости в осенний период совпадает с возвращением после каникул детей в детские учреждения (детские сады, школы). Росту заболеваемости ветряной оспой весной способствуют перепады температуры, снижение иммунитета и рост ОРЗ.
Классификация. Единой классификации инфекции, вызванной VZV, нет. По распространенности процесса и по тяжести течения критерии для ветряной оспы (первичное инфицирование) и опоясывающего лишая (рецидив) одинаковы.
По распространенности процесса инфекцию, вызванную VZV, можно разделить на такие формы:
byj|
smartpe
локализованные (изолированное поражение кожи и слизистых оболочек любой локализации);
генерализованные (сочетанные поражения кожи, слизистых оболочек и внутренних органов).
При инфицировании VZV возможно течение болезни:
легкое,
средней тяжести,
тяжелое.
Тяжесть течения определяется характером местных изменений (буллы, геморрагии), распространенностью и генерализацией процесса, степенью интоксикации. К тяжело протекающим формам относят геморрагическую, буллезную, гангренозно-некротическую.
Примерная формулировка диагноза. При постановке диагноза ветряной оспы учитывают тяжесть течения, распространенность процесса, осложнения. Например:
1. Ветряная оспа, легкое течение.
2. Ветряная оспа, генерализованная форма, тяжелое течение. Осло- жнение: правосторонняя очаговая пневмония.
При формулировке подробного диагноза при опоясывающем лишае нужно учитывать локализацию и тяжесть процесса, его распространенность, частоту рецидивов, осложнения, сопутствующие заболевания.
Поскольку больных с опоясывающим лишаем лечат преимущественно в неврологических отделениях, точная формулировка диагноза с указанием локализации повреждения нервных ганглиев и соответственно иннервируемых ими сегментов кожи находится в компетенции невропатологов. Мы будем говорить об особенностях течения herpes zoster с учетом распространенности процесса (локализованная, диссе-минированная, генерализованная).
Патогенез изучен недостаточно, что связано с отсутствием экспериментальной модели для воспроизведения VZV-инфекции. При заражении человека VZV проникает в клетки слизистых оболочек в месте внедрения, где идет репродукция и накопление вируса (период инкубации). Преодолев местные защитные барьеры, вирус проникает в кровеносное русло, следствием чего является вирусемия.
Это совпадает с началом клинических проявлений. Обладая выраженной дермотропностью, VZV проникает в эпителиальные клетки кожи, где размножается, вызывая характерные изменения в пораженных клетках и окружающих тканях. Вследствие расширения сосудов на коже вначале появляются мелкие пятна, затем развивается серозный отек кожи и образуются папулы. В дальнейшем при отслоении эпидермиса появляются везикулы (пузырьки, наполненные серозным содержимым), при их нагноении образуются пустулы, а в дальнейшем при их подсыхании — корочки. Повреждаются обычно лишь поверхност
ные слои кожи, поэтому рубцы не образуются, за исключением тяжелых случаев заболевания или наслоения вторичной инфекции. В пораженных клетках эпителия обнаруживаются внутриядерные эозино-фильные включения, а в шиловидном слое кожи — гигантские многоядерные клетки.
В процессе генерализации вирусы могут проникать во внутренние органы. При этом на слизистых оболочках дыхательных путей, пищеварительного тракта и других органов появляются множественные везикулы, которые быстро эрозирутотся. В тканях пораженных органов обнаруживают кровоизлияния, округлые очажки некрозов, а вокруг — многоядерные клетки и эозинофильные включения без выраженной воспалительной реакции. Могут развиваться тяжелые повреждения печени с участками некроза, геморрагиями.
Вирус обладает тропностью и к нервной ткани. В спинальных нервных ганглиях, корешках чувствительных нервов, рогах спинного мозга развиваются некротические и дегенеративные процессы. При электронной микроскопии в клетках ганглиев и в соседних клетках обнаруживаются внутриядерные включения и вирус, что характерно для пер-систенции вируса.
VZV может поражать и вещество головного мозга, при этом возникают изменения, характерные для энцефалита: участки некроза, пери-васкулярный отек, петехиальные кровоизлияния.
Во время пребывания вируса в организме происходит стимуляция клеточного и гуморального иммунитета, появляются вируснейтрализу-ющие и комплементсвязывающие антитела; все это способствует освобождению от вируса, циркулирующего в крови, и от поврежденных вирусом клеток. Недоступными действию защитных факторов оказываются вирусы, проникшие в клетки нервных ганглиев, где инфекция длительное время сохраняется в «дремлющем», латентном, состоянии.
Механизм латенции при инфекции, обусловленной VZV, практически не изучен.
Способствовать активации VZV могут различные факторы, снижающие защитные силы организма. Это может быть связано с новыми инфекционными заболеваниями, перегреванием или переохлаждением, ультрафиолетовым облучением, радиацией, стрессами, гормональными нарушениями, тяжелыми заболеваниями (лейкозы, злокачественные новообразования), приемом некоторых лекарств (глюкокортикостеро-иды, цитостатики, иммунодепрессанты и др.).
Активация инфекции сопровождается дегенеративными изменениями клеток нервных ганглиев, шванновских клеток, нервных волокон, инфильтрацией тканей лимфоцитами и полинуклеарами, стазами в кровеносных сосудах.
По нервным стволам VZV проникает в кожу или слизистые оболочки, где возникают герпетические высыпания по ходу этих стволов. В
ядрах пораженных клеток обнаруживают включения вирусных частиц. В шиповидном слое кожи появляются многоядерные гигантские клетки, часть клеток некротизируется, выражен также отек эпидермаль-ных клеток. Процесс носит поверхностный характер, как и при первичном инфицировании, поэтому рубцы тоже возникают редко.
Вирусы из разрушенных клеток в период обострения поступают и в кровеносное русло, стимулируя как специфический иммунитет, так и развитие аллергических процессов. В некоторых случаях вирусемия завершается диссеминацией и поражением внутренних органов (печень, легкие, селезенка, пищеварительный тракт, ЦНС). При микроскопическом исследовании в этих органах обнаруживают округлые очажки некрозов, кровоизлияния, многоядерные клетки.
В развитии осложнений (энцефалит, лептоменингит, миокардит) важную роль играют аутоиммунные реакции.
В процессе клинического выздоровления принимают участие факторы гуморального и клеточного иммунитета. При этом более важную роль играет клеточный иммунитет (макрофаги, Т- и В-клетки). Гуморальному иммунитету принадлежит второстепенная роль. Антитела усиливают киллерную функцию Т-лимфоцитов по уничтожению инфицированных клеток, но не препятствуют активации процесса (рецидиву болезни), что, как правило, связано с угнетением клеточного иммунитета. Опоясывающий лишай, как и многие другие вирусные инфекции (простой герпес, инфекционный мононуклеоз), является признанным маркером иммунодепрессии.
Патогенез инфекции, вызываемой VZV, можно представить в виде схемы (рис. 9).
Клиника. Ветряная оспа. Инкубационный период при ветряной оспе длится 5—21 день, в среднем — 1—2 нед.
Клинические проявления заболевания можно объединить в два основных синдрома, обусловленных дермотропностью вируса и его ток-сигенностью:
поражение кожи и слизистых оболочек,
интоксикация.
Заболевание, как правило, начинается остро с повышения температуры, высота которой определяется тяжестью течения процесса. Редко этому предшествуют продромальные явления в виде недомогания, ухудшения аппетита. Вслед за повышением температуры в 1-й, реже на 2-й день болезни появляются высыпания на коже.
Лихорадка длится обычно 2—7 дней, при обильных высыпаниях и тяжелом течении болезни — до 10 дней и более. Она может быть постоянной или ремиттирующей, субфебрильной и высокой (39—40 °С и выше). Как показывают наблюдения, существует корреляция между длительностью и выраженностью лихорадочной реакции и интенсивностью высыпаний. 6*
