
- •Болезни в трех томах
- •Общая часть
- •8 Список сокращений
- •Основные сведения об инфекционных болезнях
- •Классификация инфекционных болезней
- •2 Ж. Возианова
- •Принципы лечения инфекционных болезней
- •Характер взаимодействия с микро-и макроорганизмом
- •Возможные побочные реакции
- •II. Аминогли-козиды
- •III. Тетрацик-лины
- •Специфическая профилактика инфекционных болезней
- •Заболевания преимущественно с воздушно-капельным механизмом передачи
- •1Ейраминидаза
- •Действие на факторы клеточного и гуморального иммунитета
- •Формирование антитоксического иммунитетаСтимуляция местных факторов защиты, в том числе завершенного фагоцитоза
- •Функциональные нарушения
- •Механизмов защиты
- •Внедрение микоплазм в слизистую оболочку дыхательных путей
- •Заболевания преимущественно с фекально-оральным механизмом передачи
- •Размножение сальмонелл в тонкой кишке
- •Вегетативная нс
- •Заболевания, вызываемые иерсиниями
- •Желудке (высвобождение эндотоксина при этом незначительное)
- •Непосредственное повреждающее действие шигелл на слизистую оболочку толстой кишки
- •Серогруппа 01 (холерные)
- •Всасывание фрагментов вибрионов в кровь Образование различных факторов агрессии
- •Выработка вибриоцидных антител
- •Структура и функции печени
- •Методы диагностики, использующиеся при обследовании больных вг, и их оценка
- •21 Ж. Возианова
- •Особенности лечения больных вирусным гепатитом с затяжным течением
- •Заболевания, вызываемые вирусами
- •Энтеровирусами Паралитические формы (полиомиелитоподобные заболевания)
- •Асептический серозный менингит
- •Энтеровирусный энцефалит
- •Синдром Гийена—Барре (полирадикулоневрит)
- •Острые респираторные заболевания («летний грипп»)
- •Лихорадка с экзантемой
- •Везикулярный стоматит с экзантемой (ящуроподобный синдром)
- •Герпетическая ангина (герпангина)
- •Эпидемический конъюнктивит
- •Энтеровирусная диарея (летние гастроэнтериты)
- •Энтеровирусный гепатит
- •Эпидемическая миалгия (плевродиния, борнхольмская болезнь)
- •Энтеровирусная инфекция у новорожденных
- •Бессимптомная инфекция
- •Лечение нематодозов
- •Лечение цестодозов
- •Протозойные заболевания
- •1Нфекц1йн1 I паразитарн1 хвороби
Заболевания преимущественно с фекально-оральным механизмом передачи
Представителей этой группы инфекционных болезней объединяет прежде всего механизм заражения — возбудитель попадает в организм главным образом через рот с инфицированными водой и пищей. Естественный для микроорганизмов «жизненный путь» начинается в пищеварительном тракте, но во многих случаях вовсе не ограничивается этим «жизненным пространством». Многие возбудители этой группы болезней выходят в различные фазы патогенеза за пределы кишечника, проникая в другие органы и ткани. При этом органная симптоматика, обусловленная внекишечным расположением возбудителя и (или) действием его токсинов на различные органы, может значительно преобладать над проявлениями поражения пищеварительного тракта и даже служить непосредственной причиной смерти больного (трихинеллез, ботулизм и др.).
Описание этой группы болезней мы начинаем с брюшного тифа и паратифов А и В, возбудители которых относятся к роду Salmonella. Брюшной тиф является той классической моделью для изучения закономерностей инфекционного процесса при кишечных инфекциях, с которой обычно начинается их изучение. Мы отдаем дань традиции, излагая сведения о брюшном тифе перед разделом «Сальмонелле-зы» — группой заболеваний, вызванных другими представителями этого рода.
Не все заболевания, изложенные в этом разделе, относятся к группе болезней с фекально-оральным механизмом передачи (ВГВ, ВГС, BID и др.), но размещение их именно здесь (с определенными пояснениями, приведенными в соответствующих разделах) обусловлено логической связью между отдельными нозологическими формами и удобством усвоения материала.
-,л СПЕЦИАЛЬНАЯ ЧАСТЬ 340
Брюшной тиф
Брюшной тиф — острое антропонозное заболевание с фе-кально-оральным механизмом передачи, вызываемое Salmonella typhi и характеризующееся поражением лимфатического аппарата тонкой кишки и бактериемией с развитием таких основных клинических симптомов, как лихорадка, интоксикация, нарушение функции кишечника, гепатосп-леномегалия, характерная сыпь (лат. — typhus, abdomina/is; англ. — typhoid fever).
Краткие исторические сведения. Со времен Гиппократа (460— 377 гг. до н.э.) вплоть до XIX ст. тифом (от греческого слова typhos — «дым», «туман») называли все те «горячечные» болезни, которые сопровождались высокой лихорадкой, затемнением сознания и бредом. Поэтому очень долгое время слово «тиф» употребляли в чисто симптоматическом смысле: под этим названием проходили такие заболевания, как чума, сепсис, сыпной тиф и др. И только в начале XIX ст. накопившиеся клинические и морфологические данные позволили выявить особенности течения различных «лихорадок».
Еще в 1804 г. И.П.Пятницкий описал клинику брюшного тифа под названием «особая болезнь», а в 1810 г. в Германии Hildebrand указал на характерные для брюшного тифа симптомы, отличавшие его от других сходных заболеваний. Типичные для брюшного тифа поражения кишечника описали также в 1813 г. Prost, Petit и Serres. Достоверные описания клиники брюшного тифа были сделаны французскими врачами Bretanno (1826) и C.Louis (1829). C.Louis и предложил название болезни «fievre typhoide» (франц.).
К 1866 г. брюшной тиф был выделен из группы других лихорадочных заболеваний на основании клинических особенностей, а классическое описание его клиники и осложнений было сделано в 1868 г. С.П.Боткиным. Однако лишь после того как была обнаружена брюшнотифозная палочка — возбудитель заболевания (Брович, 1874; Н.И.Соколов, 1876; C.Eberth, 1880), брюшной тиф как отдельное заболевание был признан уже почти всеми, а возбудитель получил название «палочка Эберта» в честь одного из первооткрывателей ее.
В чистой культуре возбудителя удалось получить G.Gaffky в 1884 г., а выделить его из крови больного — А.И.Вильчуру в 1887 г. Широко применяющаяся и по настоящее время реакция агглютинации (реакция Видаля) была предложена в 1896 г. Gruber и Vidal (она так и называлась реакция Грубера—Видаля).
Актуальность. В прошлом столетии брюшной тиф был широко распространен во всех странах мира. Обусловлено это было отсутствием знаний об эпидемиологии этого заболевания, большой скученностью населения, особенно в больших городах, низкой санитарной культурой, отсутствием благоустройства городов, нищетой.
В одном из руководств по инфекционным болезням, относящихся к 1906 г., профессор Ананьев писал: «Брюшной тиф встречается почти повсюду. Только некоторые местности, у нас Царское село, считаются до известной степени свободными от брюшного тифа. Впрочем, и в Царском селе недавно еще наблюдалась маленькая эпидемия...».
По данным Л.В.Громашевского, показатель заболеваемости брюшным тифом в Царской России составлял 16,9—32,8 на 10 ООО населения, значительно повышаясь в годы голода, неурожая, войн. Так, в период гражданской войны и интервенции он увеличился до 48,9 на 10 ООО населения, при этом очень высокой была летальность — из 100 зарегистрированных больных умирал каждый четвертый.
В 70—80-е годы заболеваемость брюшным тифом в нашей стране снизилась в 30—50 раз по сравнению с 1913 г. Если учесть, что регистрация болезней в дореволюционные годы была далеко не совершенной, то фактический показатель снижения заболеваемости окажется значительно большим.
В настоящее время наиболее высокая заболеваемость брюшным тифом наблюдается в развивающихся странах Африки, Южной Америки, Азии, наименьшая — в странах Западной Европы. Резко снизилась и летальность: в экономически развитых странах она колеблется от 0,03 до 2,3 %.
Однако эта инфекция все еще встречается повсеместно, поражая людей всех возрастов, возникая в виде эпидемических вспышек или спорадических случаев, вызывая значительные экономические потери.
90-е годы нашего столетия ознаменовались ростом инфекционной заболеваемости, в том числе и брюшным тифом, в различных регионах. Это объясняется несколькими причинами:
обстановка на земном шаре неспокойна: войны, стихийные бедствия, интенсивная миграция населения создают идеальные условия для возникновения и распространения эпидемий;
отсутствует настороженность к этой инфекции, отсюда — поздняя госпитализация больных (3/4 их госпитализируют на 2-й неделе заболевания и позже), таким образом создаются условия для распространения брюшного тифа;
постепенно формируется устойчивость брюшнотифозных палочек к левомицетину — основному этиотропному средству, применяемому для лечения больных, а беспорядочное применение антибиотиков, в том числе добавление их в пищу сельскохозяйственным животным, создает дополнительные условия для формирования резистентности микроорганизмов.
Не решена проблема хронического брюшнотифозного бактерионосительства; носитель может оставаться пожизненным источником инфекции.
Несмотря на то что только человек болеет брюшным тифом, вряд ли можно ставить вопрос о ликвидации этой инфекции на земном шаре. Можно лишь путем строжайшего выполнения всех санитарных норм и правил добиться максимального снижения заболеваемости в каждом отдельном регионе.
Этиология. Возбудитель Salmonella typhi относится к обширному роду Salmonella семейства кишечных (Enterobacteriaceae), серологической группе D по диагностической антигенной схеме Кауффманна — Уайта. S.typhi патогенна только для человека.
Бактерия брюшного тифа — короткая грамотрицательная палочка с закругленными концами, длиной 2—5 мкм, толщиной 0,5—0,8 мкм. Морфологически не отличима от других сальмонелл. Подвижна, имеет 8—12 жгутиков, число и форма жгутиков зависят от продолжительности культивирования и состава питательных сред. Спор и капсул не образует. Является факультативным аэробом. По ферментативной активности отличается от других сальмонелл (ферментирует глюкозу, мальтозу, сорбит, маннит с образованием кислоты и газа или только кислоты, арабинозу и ксилозу с образованием сероводорода и индола).
Как и другие сальмонеллы, она хорошо растет на обычных питательных средах, но особенно — на содержащих желчь. Оптимум роста + 37 °С, рН 7,2—7,4. На плотных питательных средах образуют мелкие прозрачные круглые колонии величиной 1—3 мм, на бульоне дают равномерное помутнение и небольшой осадок.
Колонии брюшнотифозных бактерий могут находиться в S-форме (гладкой) и R-форме (шероховатой). Переход из одной формы в другую — процесс сложный, до конца не изученный. R-формы микробов почти не обладают серологической специфичностью. Из S-форм выделяют полисахаридную фракцию, вызывающую антителообразование.
В окружающей среде брюшнотифозные палочки относительно устойчивы, хорошо переносят низкие температуры и даже замораживание в течение нескольких месяцев. Под действием высокой температуры быстро гибнут (при температуре +50 °С через 1ч, +60 °С — через 20—30 мин, при кипячении — мгновенно).
Выживаемость S.typhi в воде зависит от условий: в проточной воде они сохраняются несколько дней, в водопроводной —до 3 мес, в иле колодцев и болот — до 6 мес.
Очень хорошо S.typhi сохраняются в пищевых продуктах, особенно в молоке, твороге, сметане, мясном фарше, в овощных салатах, где могут даже размножаться.
Прямые солнечные лучи действуют губительно на S.typhi. Под действием 3 % раствора хлорамина, 5 % раствора карболовой кислоты, сулемы (1:1000), 95 % этилового спирта они гибнут через несколько минут.
Брюшнотифозная палочка имеет сложную антигенную структуру. Основными антигенами брюшнотифозных бактерий, как и других сальмонелл, являются О-, Н-, Vi-антигены.
Специфической основой термостабильного О-антигена является ли-пополисахарид (ЛПС), по которому все сальмонеллы подразделяются на серогруппы в соответствии с классификацией Кауффманна — Уайта. S. typhy относится к группе D.
Специфическая основа термолабильного Н-антигена заложена в белковой фракции и характеризуется определенным набором аминокислот. Н-антиген не обладает токсическими свойствами. S. typhy содержат I фазу Н-антигена.
Самым поверхностным является Vi-антиген (антиген вирулентности), состоящий из трех различных фракций.
В зависимости от чувствительности к специфическим типовым Vi-бактериофагам брюшнотифозные бактерии подразделяются более чем на 100 фаготипов.
Бактерии брюшного тифа и паратифов под действием различных неблагоприятных факторов склонны к различным формам изменчивости: диссоциации, мутации, адаптации, L-трансформации, образованию фильтрующихся форм.
Считают, что процесс диссоциации имеет защитно-приспособительный характер, ослабление вирулентности бактерий связано с блокированием некоторых этапов синтеза О-антигена.
Под влиянием бактериофага и антибиотиков образуются L-формы, устойчивые к антибиотикам и способные вызывать рецидивы болезни, а также реверсировать в исходные формы. Они обладают и менее выраженным иммунизирующим свойством.
Сальмонеллы брюшного тифа способны оказывать цитопатогенное действие на культуры тканей. Установлено также, что брюшнотифозные палочки могут проникать в лимфоидные клетки зараженного неиммунного человека и размножаться там, в то время как в цитоплазму иммунных лимфоцитов, полученных из периферической крови привитых людей и хронических носителей, бактерии не проникают, а располагаются вокруг таких лимфоцитов. Многие свойства брюшнотифозных палочек — вирулентность, агглютинабельность, лизабель-ность — не являются величиной постоянной, неизменной, они могут изменяться под влиянием облучения, антибиотиков, бактериофагов и других неблагоприятных для бактерий факторов. Даже у одного больного в процессе заболевания свойства возбудителя меняются.
Выделенный на высоте болезни микроб более вирулентен, чем обнаруженный в период угасания болезни, так как пребывание его в иммунном организме ведет к уменьшению содержания в клетке Vi-антигена. Штаммы от острых носителей обычно обладают большей вирулентностью, чем штаммы, выделенные от хронических носителей. В период высокой эпидемической заболеваемости непрерывный пассаж возбудителя из одного чувствительного организма в другой ведет к росту вирулентности микробов. Наоборот, повышение коллективного иммунитета населения способствует снижению их вирулентных свойств.
Основные факторы патогенности брюшнотифозной палочки — Vi-антиген и эндотоксин (липидно-сахаридный комплекс), который выделяется при разрушении бактерии (ее гибели). Помимо выраженных пирогенных свойств, этот токсин, как и токсин других сальмонелл, оказывает токсическое действие на ЦНС, солнечное сплетение, вегетативную нервную систему, сосуды, мышцу сердца, что обусловливает характерную клиническую картину. Общее токсическое действие эндотоксина S.typhi выражено сильнее, чем у других сальмонелл.
Возбудители брюшного тифа подобно другим сальмонеллам обладают большим набором ферментов, повышающих их агрессивность: гиа-луронидазой, фибринолизином, лецитиназой, гемолизином и др.
Эндотоксин, ферменты, способность к внутриклеточному паразити-рованию, наличие R-фактора и Vi-антигена, способность образовывать L-формы, не дающие иммунного ответа, — все это факторы агрессии, благоприятствующие внедрению возбудителя в организм, сохранению и развитию в нем патологического процесса. Брюшнотифозная палочка настолько приспособилась к человеческому организму, что даже желчь, губительно действующая на большинство микроорганизмов, стала обязательным компонентом сред, используемых для выращивания культур S.typhi.
Эпидемиология. Брюшной тиф относится к антропонозам. Источником инфекции является больной или носитель S.typhi. Больной выделяет возбудителей в окружающую среду с испражнениями, мочой, слюной. В 1 г фекалий больного в разгар болезни (на 2—3-й неделе) содержатся сотни миллионов микробов, а в 1 мл мочи — до 180 млн. Если учесть, что в среднем человек выделяет в сутки около 2 л мочи, то получается астрономическое количество выделенных в окружающую среду брюшнотифозных палочек. При попадании в организм 105 микробных тел заболевают 25 % инфицированных, 107 — 50 %, 109 — 100 %.
Так как большинство больных брюшным тифом с тяжелым течением выявляют и госпитализируют, они реже становятся источником инфекции. Интенсивно рассеиваются возбудители в окружающей среде больными с легким течением и атипичными формами болезни. Эпидемиологическая опасность больного с любой клинической формой брюшного тифа значительно уменьшается в период реконвалесценции.
Особую опасность в распространении инфекции представляют бактерионосители, особенно те, которые по роду своей деятельности связаны с пищевыми продуктами, источниками водоснабжения.
Механизм передачи инфекции — фекально-оральный. Передача возбудителя происходит контактно-бытовым, водным, пищевым путями, определенную роль играют мухи. Факторами передачи возбудителя служат инфицированная вода, пищевые продукты. Водные вспышки брюшного тифа могут быть кратковременными или длительными. Возможно возникновение случаев брюшного тифа среди людей, купающихся в загрязненных водоемах при случайном заглатывании ими инфицированной воды. Водные вспышки брюшного тифа чаще носят взрывной характер. Кривая заболеваемости в случае одномоментного массового заражения имеет крутой подъем и быстрый спад после принятия соответствующих мер, например, на водопроводе, а «эпидемический хвост» обусловлен контактными случаями заражения. Водные вспышки брюшного тифа протекают относительно легче пищевых, с продолжительным инкубационным периодом, меньшей летальностью ввиду попадания в организм относительно небольшой дозы возбудителя. Тяжелые формы болезни при водных вспышках регистрируют редко.
Пищевые вспышки брюшного тифа характеризуются быстрым нарастанием количества заболевших и возникают преимущественно при употреблении инфицированных молока, молочных продуктов, изделий с кремом, так как в них возбудители не только сохраняются, но и могут размножаться, особенно в жаркое время года. Заразиться брюшным тифом можно при употреблении в пищу инфицированного мороженого, сливочного масла. Овощи, фрукты, хлеб реже являются факторами передачи инфекции, так как на них возбудители обычно не размножаются. Инфицирование пищевых продуктов, в том числе готовых блюд, происходит при нарушении санитарных норм и правил переработки сырья, хранения, транспортировки и реализации готовой пищевой продукции.
Молочные вспышки брюшного тифа, связанные с употреблением централизованно реализуемого молока, напоминают водные вспышки, но в отличие от последних доза возбудителя обычно большая, инкубационный период более короткий, заболевание протекает тяжелее и с более высокой летальностью. При употреблении рыночного нецентрализованно реализуемого инфицированного молока возникают обычно спорадические, реже — групповые заболевания брюшным тифом. При пищевых вспышках источником инфекции чаще является носитель S.typhi, этим объясняется необходимость строжайшего контроля за работниками предприятий общественного питания.
При контактно-бытовом пути возбудитель передается через загрязненные руки (прямой путь передачи), посуду, белье, дверные ручки (косвенный путь). При этом заболеваемость невысока, но при сохранении источника заражения новые случаи заболевания могут регистрироваться длительно. Контактно-бытовой путь передачи возбудителя способствует возникновению спорадических заболеваний, а источник инфекции удается выявить лишь в 10—15% случаев. Описаны случаи внутриутробного инфицирования плода с последующим развертыванием клиники брюшного тифа у новорожденного.
В распространении заболевания в летне-осенний период значительную роль могут играть мухи, которые переносят возбудителей брюшного тифа на пищевые продукты. Жизнеспособных S.typhi обнаруживали в кишечнике мух.
Брюшной тиф характеризуется летне-осенней сезонностью, на долю которой приходится 40—60% всех случаев заболеваний. Считают, что сезонный подъем заболеваемости брюшным тифом обусловлен не только упрощенным механизмом передачи инфекции, но и снижением реактивности организма под влиянием избыточной инсоляции, нарушением водного обмена, употреблением в пищу в значительном количестве углеводов и воды, снижением барьерной функции желудка и бактерицидных свойств сыворотки крови. Определенное значение в распространении инфекции имеет также усиление миграции населения в летнее время (туризм, отдых у моря и др.), купание в загрязненных водоемах, употребление некипяченого молока, немытых ягод, фруктов, овощей.
Восприимчивость к брюшному тифу всеобщая. Невосприимчивость определенной части населения обусловлена наличием специфического иммунитета в результате перенесенного в легкой форме заболевания (бытовая иммунизация) или проведения специфической профилактики. Наиболее резистентны к брюшному тифу лица с 0(1) группой крови, у них же реже формируется носительство. Более подвержены этому заболеванию люди с AB(IV) группой крови. Высокое число бактерионосителей среди лиц с А(П) группой крови генетически детерминировано.
Классификация. Брюшной тиф может протекать в субклинической и манифестной формах. Течение манифестных форм по степени тяжести можно разделить на легкое, среднетяжелое и тяжелое.
В основе такой градации лежит выраженность клинических проявлений, степень токсикоза. Наличие и характер осложнений не всегда коррелируют с выраженностью клинических проявлений болезни.
Манифестные формы брюшного тифа могут быть типичными или атипичными (протекают в стертой или абортивной форме).
Заболевание может протекать как циклическое (наиболее частый вариант течения), а также с обострениями и рецидивами.
Брюшнотифозная инфекция может принимать характер брюшнотифозного бактерионосительства, которое бывает:
острым (возбудитель выделяется еще около 3 мес после клинического выздоровления);
хроническим (возбудитель выделяется длительно, иногда пожизненно).
транзиторным (возбудитель высевается однократно, никаких специфических изменений в иммунном статусе, свидетельствующих о наличии инфекционного процесса, при обследовании не выявляют).
Примерная формулировка диагноза. В диагнозе следует указать тяжесть течения, наличие и характер осложнений. Рекомендуется указать также, каким методом исследования подтвержден диагноз.
Брюшной тиф (гемокультура « + »), тяжелое течение. Кишечное кровотечение. Вторичная гипохромная анемия.
Хроническое брюшнотифозное бактерионосительство (урино-культура « + »).
Патогенез. Доза возбудителя, способная вызвать заболевание, составляет 105—109 микробов, но она может быть значительно меньше, так как зависит от вирулентности возбудителя и состояния макроорганизма.
Патогенез брюшного тифа традиционно излагается в виде последовательных, четко определенных клинических стадий (фаз):
стадия внедрения;
стадия лимфозащитных реакций;
генерализация процесса (бактериемия);
стадия интоксикации;
стадия паренхиматозной диффузии;
выделение из организма возбудителей;
формирование иммунных реакций;
выздоровление.
Такая схема патогенеза была разработана еще в 30-е годы XX ст. Ш.Ашаром и В.Лаверне, но последующие исследования позволили сделать вывод об определенной условности ее. Так, возбудитель в крови обнаруживается уже в первые, начальные, фазы болезни, проникновение в печень и селезенку происходит раньше, чем в другие органы, и т.д.
Патогенез брюшного тифа с учетом современных представлений можно представить следующим образом.
Проникнув через рот в желудок, брюшнотифозные палочки частично гибнут (желудочный сок — первый защитный барьер), остальные достигают нижнего отдела тонкой кишки. Нормальная кишечная флора — антагонист брюшнотифозных палочек (очередной защитный барьер), поэтому при дисбактериозе процесс их размножения идет более активно. В процесс защиты включаются и секреторные антитела (IgA), однако и им не всегда удается подавить размножение и накопление брюшнотифозных палочек.
В дальнейшем возбудитель внедряется в пейеровы бляшки и соли-тарные фолликулы, где развивается реакция пролиферативного характера с последующим образованием гранулем, представляющих собой скопление крупных «тифозных» клеток со светлой протоплазмой. Эти клетки обладают способностью фагоцитировать брюшнотифозные палочки. По лимфатическим сосудам возбудители достигают мезентери-альных и забрюшинных лимфатических узлов, где также образуются гранулемы. Если лимфатические узлы не выполняют полностью барьерной функции, то от них по лимфатическим сосудам брюшнотифозные палочки попадают в кровоток. Это — первичная бактериемия, очень кратковременная, наступающая уже через 24—72 ч после заражения. Она не сопровождается клиническими проявлениями. Но во время этой бактериемии брюшнотифозные палочки заносятся в печень и селезенку. В печени и желчном пузыре S.typhi находят наиболее благоприятные условия для своего сохранения и размножения.
Клетки, захватившие S.typhi, на ранних этапах не в состоянии справиться с ними, так как возбудитель угнетает окислительные процессы в нейтрофилах и моноцитах. Поэтому брюшнотифозные палочки размножаются и накапливаются в клетках РЭС. Это сопровождается образованием брюшнотифозных гранулем в мезентериальных лимфатических узлах, печени, селезенке, дистрофическими и некротическими изменениями в них.
Все вышеперечисленные процессы происходят еще в инкубационный период, длительность которого зависит от дозы возбудителя и в значительной мере — от реактивности организма человека, способности включать защитные механизмы на разных этапах взаимодействия с возбудителем.
Накопление S.typhi в клетках лимфатических узлов, печени и селезенки завершается их выходом в кровь — наступает вторичная генерализация инфекции, которая и сопровождается первыми клиническими проявлениями заболевания. Но для того чтобы возникли эти проявления, должна быть достигнута определенная (пороговая) концентрация возбудителей в крови. Слабой интенсивности (подпороговая) бактериемия обнаруживается уже в конце инкубационного периода.
Вторичная бактериемия сопровождается «доставкой» S.typhi во все органы и ткани (происходит паренхиматозная диффузия). Брюшнотифозные гранулемы, аналогичные описанным выше, формируются не только в лимфатических узлах, печени, селезенке, но и в костном мозге, почках, слюнных железах, яичках. Именно в этих органах происходит дальнейшее размножение и накопление возбудителей.
Вторичная бактериемия носит персистирующий характер — она поддерживается за счет новых поступлений возбудителей из очагов размножения. Бактериемия сопровождается также очередной доставкой S.typhi из крови в паренхиматозные органы, образованием новых очагов. Таким образом, идет непрерывный процесс: бактериемия паренхиматозная диффузия.
Особенно активное размножение бактерий происходит в желчном пузыре, куда они попадают из крови и печени и где желчь создает наиболее благоприятные условия для их роста.
На ранних стадиях бактериемии гибель циркулирующих в крови бактерий обеспечивают неспецифические факторы — бактерицидные свойства крови. При гибели брюшнотифозных бактерий освобождается эндотоксин (липополисахарид), действие которого лежит в основе большинства клинических проявлений брюшного тифа. Эндотоксин обладает широким спектром повреждающего действия: он оказывает токсическое влияние на ЦНС, вызывая развитие statys typhosus, непосредственное токсическое действие на мышцу сердца, костный мозг (угнетение кроветворения), солнечное сплетение, чревные нервы (перераспределение крови, коллапс), угнетает выработку пищеварительных ферментов, снижает активность иммунных реакций. Эндотоксин является мощным пирогеном, его действием главным образом и объясняется лихорадка при брюшном тифе. Эндотоксин способствует возникновению ДВС-синдрома, хотя и слабо выраженного при брюшном тифе (уменьшается количество тромбоцитов, в результате токсического действия на лейкоциты освобождаются прокоагулазы и протеазы). Под действием эндотоксина нарушается синтез белков, витаминов.
Брюшнотифозные палочки в период диссеминации обнаруживаются практически во всех органах и тканях, но в сердечной мышце, легких, ЦНС брюшнотифозные гранулемы не образуются, и основные изменения, возникающие в них, обусловлены действием эндотоксина, циркуляторными и метаболическими нарушениями. Попавшие в эти органы возбудители могут быть и причиной образования местных специфических реакций: абсцессов в почках, брюшнотифозной пневмонии, брюшнотифозной ангины (ангины Дюге) и др.
Более сложен механизм повреждений органов, в которых формируются брюшнотифозные гранулемы. В зоне, где имеется скопление макрофагов, выделяются большое количество активных цитокинов (в том числе опухолевый некротический фактор), а также другие активные вещества, вызывающие местное повреждение тканей и образование участков некрозов. Эти же факторы, проникшие в кровь, усиливают токсическое действие на костный мозг (угнетение его функции), увеличивают сосудистую нестабильность, интенсивность лихорадочной реакции. Кроме того, в зонах местного повреждения тканей (в лимфатическом аппарате тонкой кишки, мезентериальных лимфатических узлах, печени, селезенке) формируется постепенно местная сенсибилизация тканей. Повторные поступления возбудителей (реинвазия на фоне бактериемии и паренхиматозной диффузии) вызывают здесь и гиперергическую реакцию, в которой принимают участие цитотоксические Т-лимфоциты. Следствием ее является гибель инфицированных клеток, образование некрозов. Наиболее бурно этот процесс происходит в лимфатическом аппарате кишки, туда S.typhi поступают в большом количестве из желчного пузыря, где активно размножаются и накапливаются. При этом пик выделения возбудителя из желчного пузыря и соответственно из кишечника приходится на 2—3-ю неделю болезни, то есть на сроки, когда в лимфатическом аппарате тонкой кишки уже сформировалась достаточно выраженная ГЗТ. Поэтому процесс «прохождения» S.typhi через кишечник сопровождается рядом последовательно возникающих морфологических изменений:
1-я неделя болезни — «мозговидное набухание» лимфатического аппарата кишечника как гистиомоноцитарная реакция на внедрение S.typhi;
2-я неделя — на фоне сформировавшейся ГЗТ повторное массовое поступление возбудителя с желчью приводит к образованию местных некрозов в области фолликулов; некрозы могут распространяться вглубь, достигая иногда мышечного слоя и даже брюшины;
3-я неделя — отторжение некротических масс и образование язв; если при этом повреждается стенка кровеносного сосуда, возможно кровотечение, если имело место глубокое проникновение в мышечный слой, может возникнуть перфорация кишечника;
4-я неделя — полное очищение язв, возможны на этом фоне кровотечение, перфорация;
5-я неделя — заживление язв. Зажившие язвы не оставляют после себя рубцов, стриктур.
Попадание возбудителей в кровяное русло приводит в действие иммунные механизмы защиты. В крови появляются и постепенно накапливаются антитела против возбудителя и отдельных его антигенов. Уже со 2-й недели болезни можно обнаружить агглютинирующие бактерии антитела, антитела против О-, Н-, Vi-антигенов. Они способствуют более быстрому «очищению» крови от S.typhi, но не играют решающей роли в процессе выздоровления, так как не могут подействовать на внутриклеточно расположенные микроорганизмы.
Механизмы, обеспечивающие уничтожение возбудителей в тканях, изучены еще недостаточно, но полагают, что основная роль принадлежит формированию ГЗТ, повышению активности макрофагов, а также действию ИК. Следствием этого является гибель инфицированных клеток.
Но ИК могут оказывать и повреждающее действие на организм. Так, ИК были обнаружены в почках брюшнотифозных больных, у которых развивался гломерулонефрит, нефротический синдром. Не исключают ведущую роль ИК в формировании у больных брюшным тифом таких осложнений, как синдром Гийена—Барре, поперечный миелит и др.
Помимо реакций, направленных на уничтожение S.typhi, очищение организма происходит путем выведения возбудителей с калом и мочой. Собственно, в разгар болезни брюшнотифозную палочку можно обнаружить во всех биологических жидкостях (слюна, грудное молоко, моча и т.д.), но практическое значение имеет выведение возбудителей с мочой и калом. В этих субстратах S.typhi можно обнаружить уже с первых дней болезни и даже в конце инкубационного периода, наибольшее количество возбудителей выделяется со 2-й недели болезни.
Брюшной тиф (нелеченый) может длиться до 5—7 нед.
Перенесенное заболевание оставляет довольно стойкий иммунитет. Случаи повторного заболевания редки, к тому же они протекают легче и поэтому, возможно, не всегда распознаются.
Носительство формируется у 2—5 % людей, перенесших брюшной тиф, чаще при нерациональном лечении. Но интимные механизмы этого процесса остаются еще мало изученными. Вероятно, играет роль множество факторов: фомирующаяся резистентность к антибиотикам, наличие L-форм, несовершенство факторов местного и гуморального иммунитета и т.д.
Особенности патогенеза брюшного тифа следующие:
не всегда тяжесть течения коррелирует с частотой таких осложнений, как кровотечение, перфорация;
частота формирования носительства не зависит от тяжести течения;
высокие титры антител против S.typhi, О-, Н-, Vi-антигенов не являются показателями защищенности организма от брюшного тифа, так как основная роль принадлежит ГЗТ.
Упрощенная схема патогенеза брюшного тифа представлена на рис.15.
Течение заболевания сопровождается развитием ряда клинических симптомов (специфических и неспецифических), имеющих диагностическое и прогностическое значение. Правильная оценка их с учетом периода болезни помогает избрать более рациональную тактику ведения больного. Патогенез ведущих симптомов изложен в табл. 14.
Клиника. Инкубационный период при брюшном тифе колеблется от 3 до 25 дней, наиболее часто он составляет 9—14 дней, но описаны случаи, когда он длится до 50 дней. Продолжительность инкубационного периода определяется многими факторами, но прежде всего количеством попавших в организм возбудителей, их вирулентностью, состоянием макроорганизма.
В большинстве случаев заболевание начинается постепенно: появляются слабость, повышенная утомляемость, чувство разбитости, ухудшается аппетит, нарушается сон. Одновременно с этими симптомами или (реже) через 1—2 дня начинает постепенно повышаться температура тела, достигая своего максимума примерно к 5—7-му дню болезни. Нарастание температуры сопровождается усилением симптомов
Внедрение S. typhy
I
t
Формирование
Лимфатический аппарат
тонкой кишки 1 г
~1
Усиление
|
|
ГЗТ |
|
Образование |
|
-*- |
|
язв |
Мезентериальные и забрюшинные лим- фатические узлы (лимфогенно) *
Печень и селезенка (гематогенно)
Кровотечения, перфорации
Размножение и накопление S. typhy
I
Гибель S. typhy, освобождение эндотоксина
Поражение органов и систем
Развернутая картина болезни
Поступление S. typhy с желчью в тонкую кишку
I
Выделение S. typhy в окружающую среду с калом
Бактериемия
ZE1
Паренхиматозная диффузия (в том числе очередное поступление S. typhy в печень и селезенку). Размножение и накопление в клетках РЭС
Поступление S. typhy в почечные канальцы
I
Поступление S. typhy в желчные ходы
Выделение S. typhy в окружающую среду с мочой
Стимуляция специфического гуморального иммунитета
Стимуляция ГЗТ в тканях
Т
|
Уничто- |
|
Уничто- |
|
жение |
|
жение |
|
S. typhy |
|
S. typhy |
|
в тканях |
|
в крови |
I
Очищение организма от инфекции
Выздоровление
■ процессы, реализуемые в инкубационный период;
процессы, соответствующие разгару болезни и периоду реконвалесценции
Рис. 15
Схема патогенеза брюшного тифа

|
СПЕЦИАЛЬНАЯ ЧАСТЬ | |
|
Продолжение табл.14 | |
|
Симптом |
Патогенез |
|
Кишечное кровотечение |
Гиперергические реакции в тонкой кишке (3—4-я неделя) Уменьшение числа тромбоцитов, факторов свертывания крови (развитие ДВС-синдрома) |
|
Носовые кровотечения, кровотечения из десен |
ДВС-синдром Тромбоците пения |
|
Панцитопения |
Гранулемы, очаги некроза в костном мозге Угнетающее действие эндотоксина на костный мозг |
|
Парадоксальная ишурия, диарея |
Ваготропное действие токсина |
общей интоксикации: головная боль становится постоянной, появляется бессонница, сильная слабость заставляет больного оставаться постоянно в постели, исчезает аппетит, стул задержан. Больной теряет интерес к окружающему, неохотно отвечает на вопросы; отчетливо видны заторможенность, загруженность больного при попытке установить с ним словесный контакт. При тяжелом течении появляются спутанность сознания («затуманенность»), нечеткая ориентация в окружающем, бред, может возникнуть психоз. В этом случае больной беспокоен, полностью дезориентирован в окружающем, иногда у него появляются галлюцинации и агрессивность.
Характерен внешний вид больного: он малоподвижен в постели, лицо бледное, амимичное, взгляд «томный», отрешенный, словно для больного ничто окружающее не существует. Кожа туловища бледная, сухая на ощупь.
Язык утолщен, с отпечатками зубов, со 2-й недели он покрывается черным налетом (фулигинозный язык). Со 2-й недели появляется также характерная розеолезная сыпь. Живот умеренно вздут, при пальпации безболезненный. При перкуссии определяют укорочение звука в илео-цекальной области — симптом Падалки. Пульс обычно ритмичный, с первых дней заболевания отмечается относительная брадикардия. Дик-ротию пульса (дополнительный более слабый пульсовой удар после основного) можно определить нечасто. Тоны сердца приглушены, иногда на верхушке можно выслушать систолический шум. АД снижено.
В клиническом течении брюшного тифа можно выделить последовательные стадии:
1-я стадия — stadium incrementi (нарастание клинических симптомов). Она соответствует примерно 1-й неделе болезни. В это время на фоне постепенного повышения температуры — «разогревания» организма — вырисовываются и ведущие жалобы больного — головная боль и бессонница, составляя таким образом триаду наиболее постоян
ных симптомов. Уже в этот период отчетливо проявлены бледность кожи, вздутие живота, брадикардия, снижение АД, симптом Падалки, уже можно обнаружить при пальпации увеличение печени, реже — селезенки. Стул задержан.
II стадия — stadium fastigii (разгар болезни) по времени соответству- ет 2—4-й неделе болезни. На 2-й неделе болезни температура достигает своего максимума и обычно держится на высоких постоянных показате- лях в течение всей стадии. Вторая неделя характеризуется появлением дополнительных симптомов — уже отчетливо пальпируют печень и се- лезенку, появляется сыпь, становится фулигинозным язык, интоксика- ционный синдром может проявляться уже в виде status typhosus.
На 3—4-й неделе возможны осложнения в виде перфорации, кровотечения. На фоне этих осложнений обычно возникает тахикардия — иногда первый их клинический предвестник.
Кожа к этому времени становится сухой, стопы и ладони приобретают желтоватый цвет (симптом Филипповича).
При тяжелом течении в этой стадии возможны коллапс, бред, психоз, а также метастатические пневмония, менингит, отит, нефрит (т.е. специфические брюшнотифозные поражения различных органов с четкой органной симптоматикой). Запор иногда сменяется профузным поносом.
III стадия — stadium decrementi (постепенное обратное развитие бо- лезни) по срокам соответствует примерно 5-й неделе болезни. Первым клиническим признаком начинающегося выздоровления является по- степенное снижение температуры тела. Это совпадает с уменьшением интоксикации — ослабевает, а затем и полностью исчезает головная боль, улучшается сон, появляется аппетит, больной начинает проявлять интерес к окружающему.
Далеко не всегда все вышеописанные стадии отчетливо прослеживаются. Раннее применение антибиотиков в большинстве случаев значительно сокращает длительность течения брюшного тифа, иногда буквально «обрывает» его. Но отсутствие настороженности, а иногда и просто знаний о брюшном тифе способствует все же тому, что и в настоящее время начало (то есть 1-я неделя) болезни часто просматривается участковыми врачами, хотя клинические проявления болезни бывают достаточно типичными.
Больной брюшным тифом может обратиться к врачу в самые различные сроки болезни. А поэтому, чтобы поставить диагноз при таком циклическом заболевании, каким является брюшной тиф, необходимо знать динамику симптомов во времени, их не только диагностическое, но и прогностическое значение.
Лихорадка — постоянный симптом брюшного тифа. Наиболее типичной для брюшного тифа является температурная кривая Вундерлиха: для нее характерны постепенное (в течение 4—6 дней) нарастание температуры тела, затем в течение 1—3 нед температура постоянно дер-
жится высокой с перепадами между утренней и вечерней менее 1 °С, а затем происходит постепенное (в течение недели) ее снижение до нормы (рис. 16). Такая температурная кривая характерна для среднетяже-лого течения болезни. Под влиянием своевременно (не позднее 6—7-го дня) начатой антибактериальной терапии сроки лихорадки могут значительно укорачиваться.
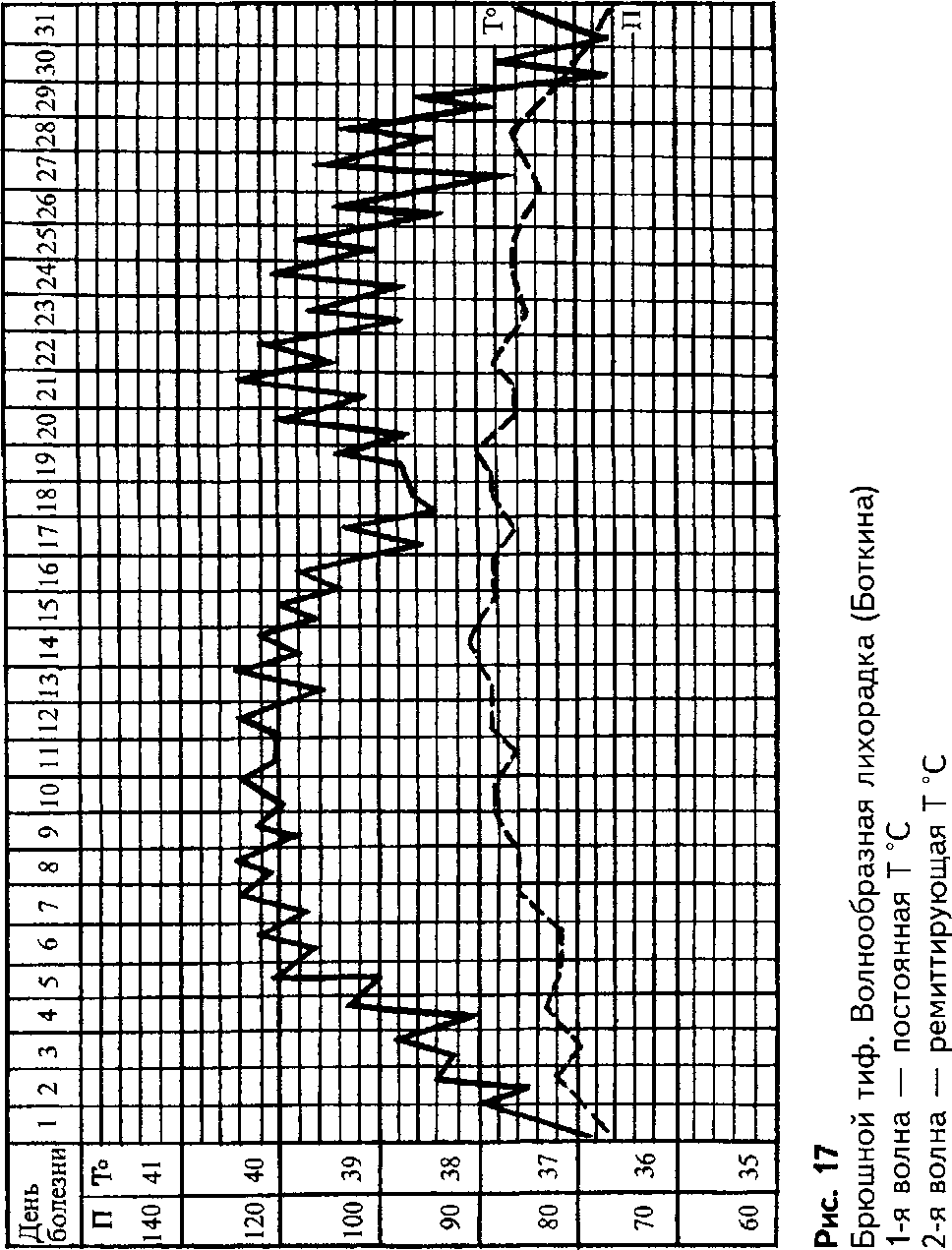
Нередко встречается Боткинская (волнообразная) температурная кривая, которая отражает неравномерность поступления возбудителя из очага. При этом в пределах первой волны температура тела может принимать характер continua, затем снижаться на 1,5—2 °С на 1—3 дня, не достигая нормы, а затем снова повышается, формируя очередную волну. При этом на фоне второй волны лихорадки она может оставаться постоянной или приобретает ремиттирующий характер (рис. 17).
В настоящее время на фоне широко применяющихся антибиотиков Боткинская температурная кривая практически не встречается. Но если она все же вырисовывается у какого-либо больного, следует еще раз тщательно проанализировать всю лечебную тактику: своевременность приема антибиотика, правильный его выбор, достаточность дозы и т.д. Неэффективность антибактериальной терапии позволит «вырисоваться» Боткинской температурной кривой за счет более длительной лихорадки.
Иногда при массивной заражающей дозе возбудителя период нарастания лихорадки может сократиться до 2—3 дней. В том случае, если реактивность организма хорошая либо имеется определенный уровень исходного иммунитета (например, при рецидиве), в начальный период температура может принимать амфиболический (amfibola) характер. Такая же температура нередко наблюдается и в stadium decrements при обратном развитии клинических симптомов (см. рис. 16).
В начальный период заболевания температурная кривая характеризуется постепенным уменьшением ее перепадов (утренней и вечерней) с неуклонным ростом, в период выздоровления — увеличением перепадов и снижением до нормы. Таким образом, падение температуры при брюшном тифе (особенно нелеченом) идет чаще не ступенеобразно, а по амфиболическому типу.
При хорошей реактивности организма в stadium fastigii лихорадка может приобретать ремиттирующий характер. Обычно это бывает при достаточной реактивности, тогда и быстрее наступает выздоровление.
И вообще следует помнить, что чем меньше перепады между утренней и вечерней температурой, тем тяжелее течение.
Пульс обычно отстает от температуры (относительная брадикардия). Но в том случае, когда начинается кровотечение, возникает компенсаторная тахикардия, что на температурном листе отражается в виде «чертова креста» (см. перекрест температуры и пульса на рис. 18). Обычно это бывает на 3-й неделе болезни.
В
период реконвалесценции возможно
появление тахикардии и
аритмии за счет развития позднего миокардита. Эти явления бывают редко, но помнить о них следует.
Длительный субфебрилитет в период реконвалесценции — часто предвестник обострения заболевания.
Сыпь при брюшном тифе появляется не ранее 7—8-го дня болезни, что доказывает участие в ее возникновении иммунных механизмов. Обычно сыпь скудная, и чтобы обнаружить розеолезные элементы, необходим очень внимательный осмотр, особенно трудно ее заметить на загорелой коже. Сыпь локализуется главным образом на коже живота
|
День болезни |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
|
|
|
|
| |
|
П |
Т° |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
140 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
41 |
|
|
|
|
|
|
|
|
|
|
|
|
|
-J |
п ■ |
|
|
|
| |
|
120 |
40 |
|
|
|
|
-* |
|
|
|
|
|
|
|
г—1 |
*~ |
|
|
|
|
|
|
ж |
|
А |
-/= |
|
|
|
|
|
-/ |
|
V |
|
|
|
|
|
| |||
|
100 |
39 |
|
—з |
f~ |
|
— |
Г |
|
|
д |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||
|
|
|
|
|
|
|
|
|
t |
t |
|
|
|
|
|
|
|
|
| ||
|
90 |
38 |
|
|
|
|
|
|
—; |
■— |
|
|
ц |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
/ |
|
|
|
|
|
| ||
|
80 |
37 |
|
|
/ |
|
'— |
|
|
|
|
|
|
|
|
|
г° |
|
|
|
|
|
|
|
|
|
|
|
|
|
—V |
— |
|
|
|
|
|
|
|
|
| ||
|
70 |
36 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кишечное кровотечение |
|
|
|
|
|
| ||||||
|
60 |
35 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 18
Брюшной тиф. «Чертов крест»
(эпигастральная область), боковых и передних отделах грудной клетки, реже — на спине. На лице сыпи нет. Высыпаний обычно немного, их легко можно сосчитать. Представляют они собой розовато-красные или бледно-розовые пятна с четкими границами, слегка выступающие над поверхностью кожи (roseola elevata), исчезающие при надавливании, но тут же появляющиеся снова. Розеолы сохраняются 3—4 дня, затем исчезают, не оставляя после себя следа. В течение всего лихорадочного периода розеолы «подсыпают», то есть появляются новые элементы. Располагаются розеолы на бледной коже. Сыпь с геморрагическим компонентом — признак тяжелого течения тифа. Розеолы могут отсутствовать у маленьких детей, стариков, у лиц с ослабленной иммунной системой, а также при раннем назначении антибиотиков.
Периферические лимфатические узлы при брюшном тифе не увеличены. Но иногда описывают увеличение миндалин и даже поверхностные язвочки на передней поверхности нёбных дужек (ангина Дюге) как проявление поражения лимфоидной ткани полости рта (2—3-я неделя болезни).
Головная боль — постоянный признак при брюшном тифе, наиболее
выраженный в первые дни болезни. Она упорная, разлитая, в большинстве случаев не сопровождается менингеальными знаками. Однако в разгар болезни может выявляться ригидность затылочных мышц в результате как менингизма, так и истинного брюшнотифозного менингита (при этом спинномозговая жидкость приобретает гнойный характер). Выраженное токсическое действие на ЦНС помимо головной боли может быть причиной развития истинного энцефалита, что проявляется амимией, оглушенностью, спутанностью сознания, бредом. Возможно, за счет того, что на фоне status typhosus больные меньше фиксируют свое внимание на головной боли, создается впечатление, что в разгар болезни (2—4-я неделя) интенсивность головной боли становится меньше. Обычно в этот период (2—4-я неделя) возникает и психоз, но иногда он появляется уже в первые дни болезни (инициальный психоз), что может послужить причиной ошибочного направления больного в психиатрическую больницу. Иногда наблюдают расстройство чувствительности. Есть сообщения о развитии преходящих моно- или ге-миплегий в разгар болезни за счет очаговых кровоизлияний и эмболии на высоте токсикоза. На фоне тифозного статуса иногда резко снижается слух. Все эти явления проходят в период реконвалесценции.
Ваготропное влияние эндотоксина — брадикардия, нарушение функции кишечника — особенно отчетливо проявляется в разгар болезни. При тяжелом течении может наблюдаться непроизвольное мочеиспускание или, наоборот, рефлекторная задержка мочи. Поэтому наблюдение за диурезом в разгар болезни обязательно, тем более, что больной мочится в это время редко, количество мочи уменьшается, так как жидкость задерживается в организме (несоответствие количеств введенной жидкости и выделенной мочи). В таком случае парадоксальную ишурию можно своевременно не диагностировать. В период реконвалесценции при снижении температуры на 1—2 °С значительно увеличивается количество мочи (мочевой криз), при этом в течение нескольких дней больной выделяет ее значительно больше, чем получает жидкости.
Стул в первые дни болезни задержан. На высоте заболевания может появляться понос, при этом стул принимает вид «горохового супа». Дополнительных лечебных мер такой симптом не требует за исключением коррекции водно-электролитного баланса. Обычно диарея бывает кратковременной, но раннее ее появление (с начала 2-й недели) и тем более появление крови в кале — свидетельство-тяжелого брюшнотифозного энтерита и даже энтероколита.
Несмотря на то что желчный пузырь закономерно вовлекается в патологический процесс (там идет активное размножение возбудителей), клинических признаков холецистита практически никогда не бывает. Увеличение печени обычно не сопровождается желтухой, ее появление -— грозный прогностический признак.
Начиная со 2-й недели, в патологический процесс могут вовлекаться не только ЦНС, но и другие системы и органы, при этом клиника поражения этих органов может быть настолько яркой, что такие варианты клинического течения получили свое название — «нефротиф», «пнев-мотиф» и т.д. Безусловно, в каждом конкретном случае следует убедиться, проявление ли это брюшного тифа или следствие присоединения вторичной инфекции.
Особенности течения брюшного тифа в зависимости от тяжести.
Легкое течение брюшного тифа характеризуется слабо выраженными явлениями общей интоксикации, непродолжительной умеренной лихорадкой, отсутствием тифозного статуса.
При среднетяжелом течении имеют место все типичные симптомы болезни — высокая лихорадка, интоксикация с адинамией, заторможенностью, нарушением сна. Но отсутствуют тяжелые гемодинамиче-ские расстройства, коллапс, бред, психоз. Длительность лихорадочного периода 2 нед и более.
Тяжелое течение отличается ранней и выраженной интоксикацией с длительным тифозным статусом, бредом, психозом, циркуляторными нарушениями, коллапсом, нарушением мочеиспускания, диареей, высокой постоянной температурой.
Особенно тяжело протекает брюшной тиф, если возникают гипер-пирексия, геморрагический синдром, ИТШ.
Атипичные формы брюшного тифа имеют такие варианты течения:
абортивный тиф, который вначале протекает в соответствии со всеми характерными для брюшного тифа закономерностями, а затем внезапно наступает перелом в ходе болезни, и больной быстро выздоравливает. Чаще это бывает при раннем назначении антибактериальной терапии и у вакцинированных;
тиф легчайшего течения, носивший в прошлом название «амбулаторный». Для него характерны субфебрильная кратковременная (несколько дней) температура, незначительная интоксикация, при которой больные к врачу не обращаются. Эти случаи обычно своевременно не распознают, диагноз устанавливают либо ретроспективно (серологические исследования), либо на основании случайно произведенных бактериологических исследований, а также при появлении таких осложнений, как кишечное кровотечение или перфорация кишечника.
У детей раннего возраста брюшной тиф начинается бурно, с быстрого подъема температуры тела, гиперпирексия может сопровождаться судорогами, потерей сознания, рвотой. Отказ ребенка от пищи в сочетании с высокой температурой, рвотой, диареей быстро приводит к эксикозу. Обычно появляется тахикардия, часто поражаются легкие. Типичные розеолезные высыпания отсутствуют. Кишечное кровотечение, перфорация не характерны, тем не менее летальность у этих детей выше, чем у детей других возрастных групп.
У детей старшего возраста клиника сходна с таковой у взрослых, но чаще (почти у половины детей) в начальный период бывает диарея, иногда — носовое кровотечение, сильнее выражена общая интоксикация (депрессия, бред, ступорозное состояние), реже регистрируется относительная брадикардия. В легких часто выслушивают сухие и влажные хрипы, что может служить причиной диагностических ошибок.
У лиц старческого возраста брюшной тиф, как правило, начинается постепенно (очень медленное «разогревание»), характерно длительное течение, реже бывают сыпь и диарея, но нередко вместо брадикардии возникает тахикардия. Редко бывает перфорация (инволюция лимфо-идной ткани), но чаще формируется бактерионосительство.
У лиц, проживающих в странах с жарким климатом, брюшной тиф нередко протекает как микст-патология (чаще в сочетании с ВГА, ши-геллезом, амебиазом, глистной инвазией, малярией), что существенно утяжеляет его течение и искажает клиническую картину. Микст-патология дает гораздо чаще (в 3—3,5 раза) рецидивы, осложнения, чаще формируется бактерионосительство.
Брюшной тиф может протекать с обострениями и рецидивами. О склонности этой инфекции к обострениям свидетельствует патогенез заболевания (периодически возникает очередной «выброс» возбудителей в кровь из очагов, где они накапливаются).
При обострениях после снижения температуры на несколько дней до субфебрильной и существенного улучшения самочувствия у больного снова поднимается температура до высоких показателей с последующим появлением всех ведущих клинических симптомов. В настоящее время причиной обострений чаще всего является ранняя отмена антибиотика или уменьшение его дозы.
Рецидивы могут наступить в любые сроки после нормализации температуры, но чаще на 2—3-й неделе нормальной температуры, то есть вскоре после отмены антибиотика. Однако описаны и более поздние, спустя 1—2 мес после нормализации температуры, рецидивы.
Наиболее частыми причинами возникновения рецидивов являются генетические особенности, иммунная недостаточность, ошибки в лечебной тактике (неправильный выбор антибиотика, его дозы, ранняя отмена препарата), образование в процессе лечения L-форм.
Иногда вероятность возникновения рецидива можно предвидеть, если в период реконвалесценции обратить внимание на следующие признаки:
— длительный субфебрилитет после снижения температуры тела; иногда «подсыпания» на этом фоне;
медленное сокращение размеров печени и селезенки;
стойкий метеоризм;
низкие титры антител в сыворотке крови;
отсутствие эозинофилов.
Брюшнотифозное бактерионосительство. Особым вариантом брюшнотифозной инфекции является носительство. Связь выявленного брюшнотифозного носительства с перенесенным брюшным тифом удается установить далеко не всегда, так как брюшной тиф мог протекать очень легко и даже субклинически, он мог быть не распознан и зафиксирован в истории болезни под другим диагнозом и наконец, как любое другое инфекционное заболевание, мог «оборваться» на любой фазе патогенеза, даже в инкубационный период, не дав клинических проявлений.
К формированию носительства предрасполагают способность возбудителя к внутриклеточному паразитированию и образованию L-форм, несостоятельность клеточного иммунитета, хронические заболевания (особенно желчевыводящих путей и печени), нерациональная антибактериальная терапия, пол (в 3 раза чаще носительство формируется у женщин), возраст (чаще у пожилых, чем у молодых), генетические факторы (например, группа крови А(П).
При установлении факта носительства давность его удается установить лишь в том случае, если имеются достоверные сведения о предшествовавшем заболевании брюшным тифом. При наличии таких данных можно говорить об остром носительстве (до 3 мес) и хроническом (более 3 мес), которое чаще носит перемежающийся характер. Возбудитель может задерживаться в лимфатических узлах, костном мозге, печени, селезенке, желчном пузыре, почках, а выделение его идет либо с мочой, либо с калом. Носительство может в течение всей жизни больного ничем клинически не проявляться, но при определенных условиях, прежде всего оказывающих угнетающее воздействие на иммунную систему, возможно возникновение заболевания.
Осложнения могут развиться в любой период болезни. Уже на 1 — 2-й неделе болезни возможны коллапс, тяжелая интоксикация вплоть до ИТШ, а также психоз, у маленьких детей — выраженная дегидратация, судороги.
Занос возбудителей в различные органы может привести к развитию местных очагов размножения возбудителей и некрозов с нарушением функции этих органов — пневмотиф, менинготиф, нефротиф и т.д., что чаще расценивается не как осложнения, а как особые формы брюшного тифа.
Может наступить тромбоз сосудов мозга с появлением очаговых симптомов. Поражение костного мозга сопровождается панцитопени-ей. Иногда развивается гемолитическая анемия.
В настоящее время сравнительно редко встречаются такие осложнения, как эндокардит, гнойный брюшнотифозный артрит, периферический неврит, поражение межпозвоночных хрящей, ценкеровский некроз — восковидное перерождение мышц, паротит, повреждение зрительного нерва.
Значительно чаще регистрируют различные осложнения на 3—4-й неделе болезни. К уже перечисленным ранее добавляются кровотечение, перфорация кишки, перитонит, аппендицит.
Кровотечение возникает чаще в период образования и очищения язв. Оно может быть незначительным и даже пройти незамеченным, а может сопровождаться массивной кровопотерей, тем более, что одновременно могут кровоточить несколько язв, а образование сгустка нарушено из-за наличия ДВС-синдрома, хотя и слабо выраженного. Характерно, что такое кровотечение может сопровождаться даже кратковременным снижением температуры, что врач расценивает как начинающееся выздоровление. Однако почти одновременно возникает тахикардия, а спустя сутки появляется мелена. В зависимости от локализации кровоточащих язв обнаруживают не только мелену, но иногда и алую кровь в кале. Кровотечения могут быть повторными, что существенно ухудшает прогноз.
Небольшое носовое кровотечение, кровоточивость десен могут появляться уже в начальный период болезни как проявление нарушения свертываемости крови.
Еще более грозным осложнением является перфорация кишечника, которая тоже наступает на 3—4-й неделе. Даже в том случае, когда перфоративное отверстие велико, боль редко бывает сильной, а «кинжальная» боль практически не встречается. Не всегда перфорация сочетается с кровотечением. Перфоративные отверстия могут быть единичными и множественными (3—4), локализуются они преимущественно в дистальных отделах подвздошной кишки. Размер дефекта может достигать 1 см. Заподозрить наличие перфорации позволяют такие симптомы:
защитное напряжение мышц живота;
отсутствие дыхательной экскурсии брюшной стенки;
— боль в животе (нерезкая, но более интенсивная по сравнению с той, которая наблюдалась в предыдущие дни);
исчезновение печеночной тупости при перкуссии;
тахикардия.
Следующее за перфорацией развитие перитонита сопровождается появлением положительного симптома Щеткина (не всегда отчетлив!), еще большим снижением АД, лейкоцитозом.
Перитонит может возникать и при наличии микроперфораций (до 1 мм в диаметре). В этих случаях боль вообще отсутствует, симптомы перитонита нарастают постепенно. S.typhi могут вызывать перитонит и без повреждения кишечной стенки, проникая в брюшную полость per diapedesem или в результате некроза мезентериальных лимфатических узлов. В связи с тем что желчный пузырь является местом размноже-
ния и накопления брюшнотифозных палочек, возможно возникновение желчного перитонита. В этих случаях возбудители проникают в брюшную полость либо per diapedesem, либо (реже) в результате перфорации желчного пузыря (особенно при наличии желчнокаменной болезни).
При брюшном тифе в процесс вовлекается червеобразный отросток, особенно богатый солитарными фолликулами. Это может сопровождаться появлением столь резко выраженных клинических признаков острого аппендицита, что больной попадает на операционный стол. Не исключается возможность и перфорации червеобразного отростка, наступающей, как и при перфорации другой локализации, на 3—4-й неделе болезни.
Безусловно, распознать катастрофу в брюшной полости у больного брюшным тифом, особенно находящегося в status typhosus, бывает непросто, многие симптомы острого живота могут быть смазаны. Поэтому при малейшем подозрении на перфорацию, перитонит, аппендицит необходимо обеспечить тщательное наблюдение за больным, особое внимание уделив такому симптому, как напряжение мышц живота. Этот признак наблюдается практически всегда, недаром Гаукес окрестил его «сверхпризнаком всех абдоминальных катастроф».
В любой период болезни возможно присоединение вторичной инфекции, особенно резистентной к применяемому антибиотику, обострение хронических заболеваний. Может развиться тромбофлебит вен нижних конечностей.
Длительное применение антибиотиков способствует развитию различных вариантов лекарственной болезни, дисбактериоза.
В период реконвалесценции, как уже указывалось, могут возникать поздний психоз, миокардит, длительно сохраняется астенизация.
Исходы. В большинстве случаев заболевание заканчивается полным выздоровлением с формированием длительного стойкого иммунитета. Повторные заболевания редки, но возможны.
Основной причиной смерти являются осложнения: кровотечение, перитонит, у маленьких детей — легочные осложнения, эксикоз, поражение ЦНС. В доантибиотиковый период летальность при брюшном тифе достигала 20 %. В настоящее время она не превышает 0,1—1,2 %.
У 2—4 % перенесших брюшной тиф формируется брюшнотифозное бактерионосительство.
Методы диагностики. Общеклинические методы исследования. При исследовании крови с 3—4-го дня болезни выявляют лейкопению, лимфоцитоз, анэозинофилию, тромбоцитопению. Но следует помнить, что в 1—2-й день болезни возможен даже небольшой лейкоцитоз или нормоцитоз. Для тяжелого и длительного течения характерна панцито-пения. В период реконвалесценции в крови появляются эозинофилы
(«заря выздоровления»). В разгар болезни может уменьшаться количество тромбоцитов. СОЭ умеренно увеличена.
В моче выявляется незначительная альбуминурия, появляются единичные эритроциты, лейкоциты. Число лейкоцитов значительно увеличивается при развитии специфического брюшнотифозного пиелонефрита или суперинфицировании.
При микроскопии кала обнаруживают иногда эритроциты. Даже при отсутствии признаков кровотечения у 20—25 % больных реакция на скрытую кровь с 3-й недели становится положительной (чаще — слабоположительной).
Биохимические методы могут оказать помощь в уточнении характера и степени электролитных и метаболических нарушений, выявить скрытый ДВС-синдром, определить степень функциональных нарушений при поражении почек.
Специфическая диагностика. Материалом для исследования служат кровь, моча, кал, желчь, можно выделить S.typhi и из розеол. Необходимо помнить о том, что диагностические возможности каждого метода различны в разные периоды болезни.
Кровь для исследования (гемокультура — ГК) берут с первого дня лихорадки до последнего, так как возбудитель может обнаруживаться в крови в течение всего лихорадочного периода. Наиболее часто S.typhi можно выделить в 1-ю неделю болезни, в дальнейшем вероятность обнаружения возбудителя в крови уменьшается, поэтому для посева берут большее количество крови. Положительная ГК — наиболее надежное подтверждение диагноза. Имеются данные, свидетельствующие о возникновении бактериемии у хронических бактерионосителей, умирающих от тяжелых заболеваний, сопровождающихся иммунодефицитом. Но обсуждается вопрос, не является ли бактериемия в этом случае проявлением активации брюшнотифозной инфекции, то есть речь идет о патологии-микст.
Копрокультуру и уринокультуру (КУК) можно выделить уже на 1-й неделе болезни, но вероятность подтверждения диагноза в эти сроки этим методом еще невелика. Гораздо чаще результаты этих исследований становятся положительными со 2-й недели болезни. Эти методы используют как для подтверждения диагноза в разгар болезни, так и для контроля за эффективностью лечения (при выписке из стационара), а также с целью выявления бактерионосительства. В отличие от положительной ГК выделение возбудителя из кала и мочи (положительная КУК) у лихорадящего больного не дает права безоговорочно ставить диагноз «брюшной тиф». Необходима тщательная оценка всех других методов исследования, в том числе серологических, чтобы исключить возможность бактерионосительства у больного с другим заболеванием.
В кишечник брюшнотифозная палочка попадает из желчного пузыря, где имеются наиболее благоприятные условия для ее размножения и накопления. Именно желчное — наиболее частый вариант носительства. Поэтому дуоденальное зондирование с последующим посевом желчи — обязательный компонент обследования брюшнотифозного реконвалесцента. Это исследование можно проводить только в период реконвалесценции, после стойкой нормализации температуры тела, отмены антибиотиков. Даже если рано наступила нормализация температуры, зондировать больного не следует ранее 5-й недели болезни (на 3—4-й неделе всегда имеется угроза перфорации и кровотечения).
Материалом для бактериологического исследования могут быть спинномозговая жидкость (при менинготифе), пунктат костного мозга, содержимое розеол, мокрота (при пневмотифе), материал из язвочек на нёбных дужках (при ангине Дюге).
Существуют различные среды, позволяющие выделять S.typhi, но наиболее часто посев крови производят на среду Раппопорта или 10—20 % желчный бульон. Соотношение объема взятой крови и среды 1:10. В 1-ю неделю для исследования достаточно взять 10 мл крови из вены, во 2-ю — 20, в 3-ю — 30. Материал как можно быстрее доставляют в лабораторию, помня о бактерицидных свойствах крови.
Испражнения также необходимо доставлять в лабораторию не позднее чем через 2 ч после забора их в стерильную посуду. Если это невозможно, применяют консерванты (чаще глицериновую смесь), соотношение объема испражнений и консерванта 1:3.
Для выделения возбудителя из мочи и желчи в лабораторию для исследования направляют взятый в стерильную посуду материал. В лаборатории производят посевы на среды Плоскирева, Эндо, Мюллера и др.
Процесс выделения и идентификации возбудителя довольно длителен. Окончательный результат можно получить не позднее 10-го дня с момента забора материала.
Отсутствие возбудителей в кале, моче, желчи, крови не противоречит диагнозу «брюшной тиф». Сроки назначения антибиотиков и поступления больного в стационар, правильность забора материала и его доставки в лабораторию — все это сказывается на результатах бактериологических исследований. Что касается копрокультуры, то отрицательные результаты могут быть связаны и с неравномерным выделением возбудителя из кишечника.
Для ускоренного выявления возбудителя в исследуемом материале можно использовать РФА в различных модификациях. Этот метод используют иногда и для определения чувствительности возбудителей к антибиотикам (С.И.Дьяков, 1982).
Серологические методы могут применяться для подтверждения диагноза со 2-й недели болезни, исследование обязательно проводят в динамике с интервалами 7—10 дней.
К настоящему времени предложено большое количество серологических методик, позволяющих определять антитела к S.typhi, к отдельным ее антигенам, различные классы антител к отдельным антигенам и т.д.
Наиболее старой и традиционной является РА (реакция Видаля). Она становится положительной со 2-й недели болезни, диагностические титры — 1:200, в дальнейшем происходит нарастание титров антител. Но реакция не является строго специфичной для брюшного тифа: за счет общности О-антигена для нескольких групп сальмонелл она может быть положительной при других сальмонеллезах. Возможны ложноположи-тельные реакции и при некоторых тяжелых септических и онкологических заболеваниях. Почти закономерно повышаются титры антител в реакции Видаля у привитых против брюшного тифа при развитии у них любых воспалительных заболеваний, что может привести к диагностическим ошибкам.
РНГА специфичнее, она становится положительной в более ранние (6—7-й день) сроки. Реакцию можно ставить с эритроцитарными моно-рецепторными диагностикумами (О, Vi).
Все шире используют РФА, который в 100 раз чувствительнее реакции Видаля. Он позволяет определить антитела различных классов (А, G, М) и таким образом прогнозировать вероятность исходов, в том числе и формирование бактерионосительства.
Vi-антитела появляются поздно, с конца 2—3-й недели, в невысоких титрах. Определение титров Vi-агглютининов используют для диагностики бактерионосительства. Диагностический титр 1:100 и выше.
На высоту титров в серологических реакциях помимо сроков исследования оказывает влияние лечение: рано начатое снижает активность иммунного ответа. Поэтому отрицательные серологические реакции при положительных ГК и КУК возможны.
Все серологические методы, независимо от исходного уровня антител, можно оценивать лишь при проведении соответствующих исследований в динамике. Четырехкратное нарастание титров антител — надежный критерий достоверности диагноза. Интервал между исследованиями — 10—12 дней.
Дополнительные методы диагностики. При необходимости больным производят рентгенографию легких (очаговые изменения при брюшнотифозной пневмонии), обзорную рентгенографию брюшной полости (при перфорации). ЭКГ позволяет контролировать деятельность сердца, выявлять миокардит.
При соответствующих показаниях делают спинномозговую пункцию (при менинготифе результаты исследования спинномозговой жидкости соответствуют критериям гнойного менингита).
УЗИ позволяет четче определить размеры печени и селезенки, что бывает затруднено при выраженном метеоризме.
Критерии диагноза. При установлении диагноза эпидемиологический анамнез помогает не всегда, особенно если это спорадический случай с длительным инкубационным периодом. Тем большее значение приобретает детальный опрос больного, изучение динамики и очередности возникновения клинических симптомов. Необходимо ориентироваться на следующие признаки:
постепенное начало заболевания;
длительную лихорадку, преимущественно постоянного типа;
наличие триады ведущих клинических симптомов в начальный период — лихорадки, бессонницы, головной боли; следует помнить слова Г.Ф.Вогралика: «Плохой сон, вскоре переходящий в бессонницу, является постоянным ранним спутником брюшнотифозных заболеваний. Нужно сказать, что ни при одной болезни бессонница не развивается так рано и не держится так упорно, как при брюшном тифе»;
адинамию, загруженность, в дальнейшем — развитие status typhosus;
бледность кожи;
брадикардию, иногда — дикротию пульса;
появление скудной мономорфной розеолезной сыпи не ранее 2-й недели болезни с характерной ее локализацией (кожа живота, груди);
характерные изменения языка (на 1-й неделе видны отпечатки зубов и белый налет, со 2-й — типичный «фулигинозный» язык);
увеличение печени и селезенки (отчетливое с конца 1-й недели);
метеоризм, задержку стула;
положительный симптом Падалки;
возможность развития метастатических специфических процессов в различных органах (пневмония, нефрит и др.) не ранее 2-й недели;
возможность возникновения кишечного кровотечения, перфорации (не ранее 3-й недели);
лейкопению, анэозинофилию, тромбоцитопению, в дальнейшем — анемию, анэозинофилию.
Когда речь идет об оценке выявленных у брюшнотифозного больного клинических симптомов, следует вспомнить слова Вундерлиха: «Даже при такой типичной болезни, как брюшной тиф, нельзя установить ни одного правила, которое не допускало бы исключения, но если в данном случае и встретится какое-нибудь отклонение от существующего правила, зато все другие, или по крайней мере, большинство все-таки вполне будут соответствовать типическому течению».
Абсолютным доказательством брюшного тифа является выделение возбудителя из крови (ГК +), тогда как положительная КУК может свидетельствовать не только о брюшном тифе, но и о носительстве. Однако при наличии убедительной клинической картины положительная КУК подтверждает наличие брюшного тифа у больного. Чтобы исключить возможность носительства брюшнотифозной палочки при неясном диагнозе, следует ставить реакцию с Vi-антигеном.
Брюшной тиф путем проведения комплекса соответствующих исследований следует исключать в каждом случае, когда у лихорадящего 5 дней больного диагноз остается неясным.
Дифференциальный диагноз. Дифференциальная диагностика брюшного тифа может быть достаточно сложной, при ее проведении необходимо учитывать период болезни, очередность возникновения клинических симптомов, помня о том, что для брюшного тифа, как и для многих других инфекционных заболеваний, характерна строгая цикличность. Так как при брюшном тифе могут поражаться легкие (пневмотиф), нередко приходится проводить дифференциальную диагностику с заболеваниями, сопровождающимися респираторным синдромом. И хотя брюшной тиф никогда не начинается с катаральных явлений, ошибки при постановке диагноза достаточно часты.
Иногда на 1-й неделе болезни больным брюшным тифом ставят диагноз «грипп», при этом ориентируются лишь на такие симптомы, как лихорадка и головная боль.
Однако в отличие от брюшного тифа:
— грипп начинается остро, иногда внезапно:
катаральный синдром (кашель, насморк) имеется с первых дней болезни;
лицо гиперемировано, склеры инъецированы, носовое дыхание затруднено;
головная боль локализуется преимущественно в лобной области;
в первые дни чаще бывает тахикардия;
печень и селезенка не увеличены;
заболевание длится не более 4—6 дней.
Аденовирусное заболевание, как и брюшной тиф, может протекать с длительной лихорадкой, увеличением печени и селезенки, диспепсическим синдромом.
Но для аденовирусного заболевания характерны:
— острое начало;
катаральные явления (насморк, першение или боль в горле) с первых дней болезни;
увеличение подчелюстных (иногда и шейных) лимфатических узлов;
— конъюнктивит (нередко односторонний), сопровождающийся жжением в глазах, слезотечением;
отсутствие сыпи;
нормоцитоз или даже умеренный лейкоцитоз. Инфекционный мононуклеоз сходен с брюшным тифом наличием
лихорадки (иногда длительной), гепатолиенального синдрома, иногда — сыпи.
Но для инфекционного мононуклеоза характерны:
— преимущественно острое начало;
— умеренно выраженный интоксикационный синдром (не бывает тифозного статуса);
— генерализованная лимфаденопатия;
катаральные изменения в ротоглотке с первых дней (гиперемия, гиперплазия фолликулов, миндалин, иногда наличие ангины);
разные, четко не определенные сроки появления сыпи, чаще ее появление бывает обусловлено приемом ампициллина; сыпь полиморфная, нередко обильная, может сопровождаться кожным зудом;
— нередко появление субиктеричности склер и даже кожи;
— появление в крови атипичных мононуклеаров (более 10 %), Головная боль, длительная лихорадка, бледность кожи, увеличение
печени и селезенки, брадикардия, лейкопения могут наблюдаться и при орнитозе. Но:
— орнитоз начинается обычно остро;
— рано, уже в первые дни, появляются кашель, одышка, колющая боль в грудной клетке;
— пневмония носит интерстициальный, а не очаговый характер;
отсутствуют признаки поражения пищеварительного тракта (запор, метеоризм);
рано (уже в 1-ю неделю болезни) бывает значительно увеличена СОЭ.
Тяжелая пневмония (крупозная, центральная) может протекать длительно, с упорной лихорадкой, интоксикацией. Отличают пневмонию от брюшного тифа:
— раннее (на 1-й неделе, а иногда и с первых дней) появление кашля;
— рано появляющиеся признаки дыхательной недостаточности (одышка, иногда цианоз);
тахикардия;
отсутствие признаков поражения пищеварительного тракта;
отсутствие гепатолиенального синдрома;
гиперемия лица, отсутствие сыпи;
нейтрофильный лейкоцитоз.
При милиарном туберкулезе, как и при брюшном тифе, могут наблюдаться длительная постоянная температура, тифозный статус, метеоризм, лейкопения.
Однако для туберкулеза характерны:
острое начало;
рано возникающая одышка;
потливость;
тахикардия;
в крови — эозинофилия (нередко значительная) с 1-й недели болезни;
— туберкулезные очаги в легких, обнаруживаемые на рентгенограммах;
— кашель с мокротой, нередко — кровь в мокроте.
Ку-лихорадка (пневмориккетсиоз) напоминает брюшной тиф наличием интоксикации, гепатолиенального синдрома, длительной лихорадки, а иногда и лейкопении.
Ку-лихорадку отличают:
острое начало;
гиперемия лица, инъекция сосудов склер;
потливость;
кашель, возникающий рано (не позднее 3—4-го дня);
нередко — боль в грудной клетке при дыхании;
отсутствие сыпи;
отсутствие метеоризма;
— при рентгенологическом исследовании, кроме очаговых изменений в легких, нередко обнаруживают увеличенные лимфатические узлы средостения.
Болезнь легионеров может напоминать брюшной тиф длительным упорным течением, выраженной интоксикацией, высокой температурой тела, полисистемностью поражения (в том числе печени, селезенки, пищеварительного тракта). Однако:
— болезнь легионеров начинается обычно остро, внезапно;
часто с первых дней наблюдаются тошнота, рвота, боль в животе, водянистый стул;
рано (со 2-го дня) появляется сильный сухой, не приносящий облегчения кашель;
в крови —• лейкоцитоз (иногда гиперлейкоцитоз), значительно увеличена СОЭ.
С выраженной интоксикацией, лихорадкой (иногда длительной) без респираторного синдрома могут протекать многие инфекционные и неинфекционные заболевания. Наиболее часто в различные периоды болезни (с 1-го дня и на протяжении всего лихорадочного периода) приходится проводить дифференциальную диагностику с такими заболеваниями, как сепсис, бруцеллез, иерсиниоз, малярия, сыпной тиф, сальмонеллез, лимфогранулематоз, злокачественные опухоли.
При сепсисе, как и при брюшном тифе, наблюдаются увеличение печени и селезенки, метастатическое поражение различных органов, бледность кожи, анемия. Особенности течения сепсиса в значительной мере определяются локализацией первичного септического очага, характером процесса (септицемия, септикопиемия), реактивностью организма.
Однако наиболее постоянными признаками, отличающими сепсис от брюшного тифа, являются:
лихорадка интермиттирующего или гектического характера;
ознобы;
потливость;
тахикардия;
лейкоцитоз, нейтрофилез;
значительно увеличенная СОЭ.
Острый бруцеллез, как и тиф, может протекать с длительной волнообразной лихорадкой, увеличением печени и селезенки, лейкопенией.
Отличают бруцеллез от брюшного тифа:
повторные ознобы, проливные поты;
длительная интермиттирующая лихорадка (иногда она сохраняется в течение нескольких месяцев);
удовлетворительное самочувствие больных, не соответствующее высоте и длительности лихорадки;
нередко наличие выраженного полиаденита;
отсутствие брадикардии (пульс соответствует температуре);
боль в суставах;
сыпь не характерна, но если она и появляется, то высыпания полиморфные, возникают без определенной закономерности.
Кишечный иерсиниоз может напоминать брюшной тиф длительной лихорадкой, головной болью, наличием высыпаний, увеличением печени и селезенки, возможными нарушениями функции кишечника.
Однако при иерсиниозе:
начало обычно острое;
часто наблюдаются тошнота и рвота;
стул водянистый, иногда со слизью;
нередко бывает фарингит с первых дней болезни;
возникает гиперемия и припухлость ладоней и стоп (симптом «перчаток и носков»);
возможно появление полиморфной сыпи;
иногда бывает умеренная желтуха;
при исследовании крови выявляют нейтрофильный лейкоцитоз и значительно увеличенную СОЭ.
При первичной малярии бывают лихорадка постоянного типа в первые дни, интоксикация, выявляют увеличение печени и селезенки. Но уже в это время имеются существенные отличия от брюшного тифа:
заболевание начинается остро, внезапно;
даже относительно небольшие перепады температуры в первые дни сопровождаются потрясающим ознобом и потом, а уже через несколько дней вырисовывается типичный малярийный приступ;
раньше, чем печень, и значительнее увеличивается селезенка;
нередко бывают герпетические высыпания;
с первых дней появляются иктеричность склер, тахикардия;
отсутствуют боль в животе, симптом Падалки;
— в крови повышается уровень непрямого билирубина, быстро нарастает анемия;
— при исследовании мазка крови выявляют малярийных паразитов. Не следует забывать, что в эндемичных районах малярия нередко
сочетается с брюшным тифом.
Лихорадка, тяжелая интоксикация с бредом и галлюцинациями, гепатолиенальный синдром, сыпь характерны как для брюшного, так и для сыпного тифа.
Но сыпной тиф отличают:
острое начало;
относительно кратковременное (не более 2—2,5 нед) течение;
тахикардия;
аритмия;
поведение больного (активность, агрессивность);
внешний вид (гиперемия лица, инъекция сосудов склер — «кроличьи глаза», симптом Киари—Авцына);
тремор языка, симптом Говорова—Годелье;
одномоментное появление сыпи, без подсыпаний, на фоне кратковременного снижения температуры на 4—5-й день болезни;
сыпь часто бывает петехиальной;
отсутствие рецидивов и обострений;
лейкоцитоз.
Сальмонеллез с тифоподобным течением бывает иногда очень трудно отличить от брюшного тифа без специальных исследований. Помогают иногда такие признаки:
острое начало, обычно с рвоты, боли в животе, диареи (эти явления обычно кратковременные, держатся 2—3 дня);
рано (на 4—6-й день) появляется сыпь, она более обильная и яркая, чем при брюшном тифе;
лейкоцитоз.
Но эти симптомы не всегда четко выражены.
Имеются и неинфекционные заболевания, клиника которых может напоминать брюшной тиф.
Так, для лимфогранулематоза характерны длительная волнообразная лихорадка, бледность кожи, увеличение печени и селезенки, лейкопения.
Но отличают лимфогранулематоз:
отсутствие тифозного статуса;
соответствие пульса температуре;
потливость;
кожный зуд (часто);
нередко выявляющееся увеличение лимфатических узлов (периферических, медиастинальных);
отсутствие метеоризма;
эозинофилия.
При злокачественных опухолях различной локализации на определенной стадии могут появляться длительная лихорадка, бледность, анемия. Наличие или отсутствие многих клинических симптомов (диарея или запоры, увеличение печени, селезенки, боль, кровотечения и др.) определяется локализацией опухоли. Тем не менее во всех случаях:
интоксикация не доходит до степени «тифозного статуса», хотя в терминальной стадии больной может впадать в коматозное состояние;
отсутствуют, как правило, головная боль, бессонница;
пульс соответствует температуре;
СОЭ обычно значительно увеличена.
Во всех случаях при проведении дифференциальной диагностики используют соответствующие специфические методы исследования.
Лечение. Все больные брюшным тифом независимо от тяжести течения подлежат обязательной госпитализации в инфекционные стационары.
Всем больным обеспечивают постельный режим в течение всего лихорадочного периода и еще 5—10 дней после нормализации температуры. При расширении режима очень серьезно оценивают вероятность возникновения таких осложнений, как коллапс, кровотечение, перфорация. Больным регулярно обрабатывают полость рта, кожу, при запорах назначают очистительные (не сифонные!) клизмы. Диету №2 назначают с 1-го дня пребывания в стационаре, расширение ее возможно после нормализации температуры, но не ранее чем с 5-й недели болезни (к этому времени наступает заживление язв). Пища должна содержать достаточное количество витаминов, солей калия. Не следует назначать минеральные воды, настой шиповника, желчегонные травы.
Этиотропная терапия. Антибиотики назначают немедленно, как только устанавливают (или даже подозревают) диагноз брюшного тифа. Наиболее эффективен левомицетин, который назначают по 2—3 г в сутки (чаще по 0,75 г 4 раза в сутки). Детям левомицетин назначают по 50 мг/кг массы тела в сутки. Предпочтительнее использовать левомицетин перорально, однако при бессознательном состоянии больного допустимо внутримышечное введение левомицетина сукцината растворимого (по 1 г 3 раза в сутки), переходя на пероральный прием, как только это становится возможным. В том случае, если больной не переносит левомицетин или в ходе лечения возникают какие-либо побочные реакции (например, выраженная лейкопения), можно перейти на ампициллин (до 4—6 г в сутки), однако он менее эффективен. После лечения ампициллином чаще формируется брюшнотифозное бактерионосительство.
Имеются сведения о возможности применения при брюшном тифе бисептола-480, обычная доза — по 2 таблетки 2 раза в сутки.
Антибактериальную терапию продолжают весь лихорадочный период и еще 10 дней нормальной температуры. Такой курс позволяет свести к минимуму вероятность рецидивов и обострений. Желательно в процессе лечения не уменьшать дозу препарата и после нормализации температуры.
К сожалению, наличие R-фактора (фактора устойчивости) у брюшнотифозных бактерий не гарантирует от возникновения резистентности ни к одному из применяющихся антибиотиков, в том числе и к ле-вомицетину. Эта резистентность может появиться и в ходе лечения, что потребует смены антибиотика.
При тяжелом течении брюшного тифа назначение препарата, действующего бактерицидно на брюшнотифозную палочку (левомицетин), может привести в первые дни даже к усилению токсикоза, вплоть до развития ИТШ. Поэтому при лечении левомицетином необходимо обеспечить одновременно и полноценную дезинтоксикационную терапию, а также не спешить с отменой препарата и заменой его другим по меньшей мере 3—5 дней.
Патогенетическая терапия. Учитывая наличие у больных токсических реакций, которые в первые дни могут даже усиливаться на фоне приема антибиотиков, существенное внимание следует уделять дезин-токсикационной терапии. Если необходимое количество жидкости (до 40 мл/кг массы тела в сутки) не удается обеспечить перорально, в том числе с пищей, можно назначить внутривенно солевые растворы («Ацесоль», «Трисоль» и др.), которые позволят компенсировать водно-электролитные нарушения, а также 5 % раствор глюкозы. При проведении дезинтоксикационной терапии необходимо следить за диурезом, учитывая способность жидкости задерживаться в организме и возможность возникновения у больных парадоксальной ишурии. Падение АД на фоне интоксикации, коллапс, особенно если эти явления возникают на фоне антибактериальной терапии, оправдывают назначение коротким курсом (2—4 дня) преднизолона (парентерально до 60—90 мг/сут).
Длительное применение антибиотиков может служить причиной развития кандидоза, дисбактериоза, следствием которых в свою очередь является дефицит витаминов группы В. Поэтому в течение всего курса антибиотикотерапии больные должны получать нистатин или ле-ворин. Аскорбиновую кислоту (до 1,5 г в сутки) можно назначать с первого дня лечения (лучше ее добавлять в капельницу с глюкозой или давать перорально), а с витаминами группы В спешить не следует, так как они могут увеличивать вероятность возникновения аллергических реакций в разгар болезни. В период реконвалесценции при наличии явных клинических проявлений дисбактериоза (сухая кожа, неустой
чивый стул) может оказаться целесообразным назначение витаминов группы В.
От введения в целях стимуляции иммунологической реактивности плазмы, цельной крови в настоящее время практически отказались, учитывая высокий риск заражения ВИЧ-инфекцией, ВГВ, ВГС, BrD, цитомегаловирусной инфекцией и др. Переливание крови и тромбо-цитной массы показано при возникновении кровотечения, при подготовке и в ходе операции по поводу перфорации и перитонита. При возникновении кишечных кровотечений больному обеспечиваются полный покой, голод, холод на живот. Постоянное наблюдение осуществляет хирург. Если кровотечение продолжается, может возникнуть необходимость в оперативном вмешательстве (ушивание язв).
В целях стимуляции неспецифической и иммунологической реактивности (угнетение ее обусловлено действием возбудителей, а также антибиотиками) можно назначить метилурацил, пентоксил.
При обострениях и рецидивах лечебная тактика такая же. Но целесообразно при этом использовать другой антибиотик.
Санация бактерионосителей — сложный, до конца не решенный вопрос. Предлагают лечить их ампициллином длительным курсом (иногда до 4—б нед) и даже удалять желчный пузырь. Но ни в одном случае нет стопроцентной гарантии успеха.
Порядок выписки из стационара. Реконвалесцентов выписывают на 21-й день нормальной температуры. Перед выпиской обязательно проводят контрольные исследования: через 2 дня после отмены антибиотика назначают 3 дня подряд посевы кала и мочи (КУК) и однократно — посев желчи (биликультура). При отрицательных результатах больного выписывают. Если в одном из посевов снова обнаруживаются S.typhi, проводят повторный курс лечения антибиотиком, к которому возбудитель чувствителен (10—14 дней), с дальнейшим обследованием перед выпиской, как указано выше.
Реконвалесценты подлежат диспансерному наблюдению в течение 2 лет, но работники предприятий общественного питания, пищевой промышленности, водопровода, детских дошкольных учреждений (декретированная группа) состоят на учете пожизненно. Порядок обследования различных категорий реконвалесцентов, допуска их на работу регламентируется специальными подробными инструкциями Министерства здравоохранения.
Профилактика. Важнейшим условием общей профилактики брюшного тифа является соблюдение личной гигиены (прежде всего чистоты рук), защиты от инфицирования продуктов питания, воды, предметов обихода; соблюдение условий приготовления и хранения пищи, выявление бактерионосителей путем регулярных обследований всех, кто относится к декретированным группам.
После госпитализации больного в очаге проводят заключительную
дезинфекцию. За контактными наблюдает участковый врач в течение 3 нед, всем однократно делают посев кала и мочи. Профилактическая медикаментозная санация контактных не показана.
Бактерионосители к работе на предприятиях общественного питания и в детских учреждениях не допускаются.
Специфическая профилактика. Вакцинацию проводят по показаниям (чаще это вспышка брюшного тифа на отдельной территории, поездка в местности, неблагоприятные по брюшному тифу). Брюшнотифозную вакцину в дозе 0,5 мл вводят подкожно однократно. Но поствакцинальный иммунитет в отличие от постинфекционного нестойкий, уже через 12—18 мес можно заболеть повторно. На территории, где регистрируется повышенная заболеваемость брюшным тифом, ревакцинацию проводят каждые 3 года.
Паратифы А и В
В 1896 г. клинику паратифозных заболеваний описали C.Achard и R.Bensaude под названием «легкие формы брюшного тифа». Они же предложили термин «паратиф». В 1898 г. N.Gwyn, а в 1900 г. H.Schott-mueller выделили возбудителей, которые отличались по некоторым свойствам от уже известной с 1880 г. палочки Эберта.
В 1902 г. A.Brion и Н.Kaiser доказали наличие двух родственных возбудителей паратифов, один из которых получил название «паратиф А», другой — «паратиф В».
В настоящее время эти заболевания встречаются повсеместно, соотношение между брюшным тифом и паратифами различно в различных регионах, но удельный вес паратифа А среди тифо-паратифозных заболеваний наименьший практически всюду.
Возбудитель паратифа А — единственный представитель сальмонелл группы А, возбудитель паратифа В — представитель сальмонелл многочисленной группы В.
По своим свойствам возбудители паратифов и брюшного тифа очень сходны, существуют лишь некоторые различия в биохимической активности. Они обладают теми же токсинами и ферментами, что и S.typhi, способны к внутриклеточному паразитированию. Как и S.typhi, возбудители паратифов имеют О- и Н-антигены, но они лишены Vi-ан-тигена.
Пути распространения и факторы передачи паратифов аналогичны таковым при брюшном тифе.
«Паратиф является в сущности более или менее полным воспроизведением классических картин брюшного тифа анатомически и гистологически» — это мнение И.В.Давыдовского (1956) полностью соответствует и современным представлениям о паратифах. В большинстве случаев на основании клинических проявлений провести дифференциальную диагностику между тифом и паратифом не представляется возможным. Тем не менее, определенная совокупность симптомов иногда может помочь в диагностике.
Паратиф А вызывает Salmonella paratyphi А. Как и брюшной тиф, паратиф А — антропоноз, источник инфекции — больные люди или бактерионосители.
Особенности паратифа А состоят в том, что:
— он значительно чаще, чем брюшной тиф (более чем в 50 % случаев), начинается остро;
— температура чаще ремиттирующая, иногда — гектическая;
нередко уже в первые дни у больных выявляют признаки поражения дыхательных путей (кашель, боль в горле, осиплость голоса), часто в сочетании с диспепсическими явлениями;
кожа обычно гиперемирована, склеры инъецированы; гиперемирована слизистая оболочка ротоглотки, нередко имеются признаки фарингита;
сыпь появляется раньше (у большинства больных уже на 5—7-й день болезни); она чаще розеолезно-папулезная, иногда кореподобная, нередко обильная, располагается не только на туловище, но и на сгиба-тельных поверхностях верхних конечностей;
запоры и расстройства стула в начальный период болезни встречаются с одинаковой частотой;
нередко бывают ознобы, потливость;
тифозный статус возникает редко;
чаще выявляют нормоцитоз или даже небольшой лейкоцитоз.
Паратиф А чаще, чем брюшной тиф, дает рецидивы, но реже осложнения в виде перфораций и кровотечений. Протекает легче, чем брюшной тиф, по тяжести течения занимая как бы промежуточное положение между брюшным тифом и паратифом В. Длительность течения заболевания может быть такая же, как при брюшном тифе.
Возбудитель паратифа В — Salmonella paratyphi В. Особенности паратифа В состоят в том, что:
это — зооантропоноз: паратифом В, кроме человека, болеют молодняк крупного рогатого скота, птицы;
короче, чем при брюшном тифе и паратифе А, инкубационный период (5—8 дней);
заболевание в большинстве случаев начинается остро, внезапно с гастроинтестинального синдрома — тошноты, рвоты, расстройства стула;
нередки в начальный период ознобы, потливость;
температура держится обычно 1—5 дней и бывает по своему характеру субфебрильной или ремиттирующей;
в связи с кратковременностью течения сыпь может отсутствовать; но иногда она появляется на 4—5-й день, может быть обильной, полиморфной, иногда бывает даже на лице;
при исследовании крови чаще обнаруживают лейкоцитоз, увеличенную СОЭ.
С учетом особенностей течения большинство случаев паратифа В проходят под диагнозами «пищевая токсикоинфекция», «острый гастроэнтерит». Но паратиф В может протекать и очень тяжело, с менингитом, септикопиемией.
В последние годы соотношение между брюшным тифом, паратифа-ми А и В еще больше изменилось за счет относительного роста послед-
него. Возможно, при этом имеет значение тот факт, что паратиф В протекает преимущественно в легкой форме и непродолжительно (иногда лишь 1—3 дня); такие случаи практически не диагностируют, а инфекция продолжает распространяться. Паратиф В чаще возникает и тяжелее протекает у лиц, имеющих В(III) группу крови, реже и легче — у лиц, имеющих А(П) группу крови.
Возможно сочетание брюшного тифа с паратифом А или В. Обычно это сопровождается большим полиморфизмом клинических проявлений, большей частотой рецидивов и обострений.
Лечение, правила выписки реконвалесцентов из стационара, профилактика при паратифозных заболеваниях аналогичны таковым при брюшном тифе.
Сальмонеллез
Сальмонеллез — острое зоонозное инфекционное заболевание с фекально-оральным механизмом передачи, вызываемое бактериями рода Salmonella, характеризующееся преимущественным поражением желудочно-кишечного тракта и протекающее чаще в виде гастроинтестиналь-ных форм различной степени тяжести, реже — в виде генерализованных форм (лат. — salmonellosis; англ. —-salmonellosis).
Краткие исторические сведения. Род Salmonella получил свое название в честь американского ветеринарного врача D.Salmon, описавшего в 1885 г. первого представителя этого рода микроорганизмов — Bact. hogcholera (современное название — S.cholerae suis). Но вначале этот возбудитель не связывали с заболеваниями человека, он был объявлен, как выяснилось позже, ошибочно возбудителем «свиной чумы». В 1888 г. A.Gaertner выделил из селезенки погибшего человека сходный микроорганизм, который был назван Bact.enteritidis. В последующие годы поток информации о возбудителях, вызывающих сходные заболевания, но различающихся по ряду биохимических признаков, нарастал. Уже к 1914 г. насчитывалось 12 представителей этого рода, к 1934 г. — 44, в настоящее время — более 2200.
Еще в 1934 г. Международная номенклатурная комиссия для всех этих возбудителей приняла родовое название — «Salmonella».
Классификация сальмонелл еще не упорядочена, хотя наиболее признанной считается классификация Кауффманна — Уайта (1966). Названия вновь открытым возбудителям дают совершенно произвольно (по имени исследователя, по названию местности, где они выделены, по виду животного, у которого возбудитель обнаружили впервые, и т.д.).
Заболевания, вызываемые S.typhi, S.paratyphi А и S.paratyphi В, регистрируют отдельно от вызываемых другими сальмонеллами, отдельно они рассматриваются и в этой книге (см. соответствующие разделы).
Актуальность. Сальмонеллез в настоящее время не только остается одной из важнейших гигиенических и эпидемиологических проблем, но и приобретает все большее значение в связи с экологическим и экономическим неблагополучием во многих регионах, интенсивной миграцией населения. Большинство сальмонелл патогенны не только для человека, но и для различных теплокровных животных, птиц, рыб, пресмыкающихся и т.д.
Убиквитарность сальмонелл, высокая устойчивость их в окружаю-
щей среде, способность вызывать не только манифестные, но и стертые формы заболевания затрудняют выявление и обезвреживание очагов инфекции.
Регистрация сальмонеллеза обязательна далеко не во всех странах, поэтому информации об истинной инфицированное™ населения в различных регионах нет. Даже в развитых странах, где заболеваемость сальмонеллезом относительно невысока, а каждый случай заболевания подтверждается развернутым бактериологическим исследованием и сопровождается тщательным эпидемиологическим расследованием, регистрируется лишь 5—15 % истинной заболеваемости.
Создание «пищевой индустрии» привело к росту числа групповых заражений, протекающих по типу пищевых токсикоинфекций. Среди возбудителей пищевых токсикоинфекций сальмонеллам принадлежит первое место.
В последние годы широкое распространение получили внутриболь-ничные (госпитальные) вспышки сальмонеллеза.
Возрастает резистентность сальмонелл к антибактериальным препаратам. Это связано с широким применением антибиотиков, в том числе добавкой их в пищевые продукты с профилактической целью. Дис-бактериозы, которые возникают на фоне применения антибиотиков, способствуют более тяжелому течению сальмонеллеза.
Надежных средств специфической профилактики (вакцин) сальмонеллеза нет, что связано с большим числом представителей рода сальмонелл и отсутствием перекрестного иммунитета между ними. Каждый год род сальмонелл пополняется новыми представителями.
До настоящего времени не изучены особенности патогенеза отдельных форм сальмонеллеза, характер взаимоотношений между возбудителем и макроорганизмом. Сложна идентификация сальмонелл, учитывая их многообразие.
Этиология. Сальмонеллы принадлежат к семейству Enterobacteria-сеае, роду Salmonella. Это грамотрицательные палочки с закругленными концами, имеющие размеры 1—3 мкм • 0,5—0,8 мкм. Они имеют перитрихиально расположенные жгутики, обеспечивающие им подвижность, но есть и неподвижные серотипы. Спор не образуют. Сальмонеллы — факультативные внутриклеточные паразиты.
Сальмонеллы достаточно устойчивы в окружающей среде: до 120 дней могут сохраняться в питьевой воде, до 18 мес — в комнатной пыли, до 13 мес — в замороженном мясе. Плохо переносят прямые солнечные лучи и кипячение, которое уничтожает их мгновенно. Но в кусках мяса весом около 400 г и толщиной около 20 см погибают при варке лишь через 2,5 ч. Выдерживают в течение 30 мин нагревание до 70 °С. Слабое действие на сальмонелл оказывают соление и копчение мяса: при содержании в них NaCl до 20 % выживают при комнатной температуре до 2 мес. Но различные штаммы сальмонелл различаются по степени резистентности к различным факторам внешней среды. 0,3 % осветленный раствор хлорной извести и 3 % раствор хлорамина убивают их через 30 мин. Могут размножаться в достаточно большом диапазоне температуры (от + 7 "С до +45 °С) и рН (от 4,1 до 9). Оптимум роста — температура +35 °С — +37 "С, рН 6,5—7,5. Растут на обычных питательных средах (Эндо, Плоскирева, висмут-сульфатном агаре и др.) в аэробных условиях.
Сальмонеллы обладают разнообразными ферментативными свойствами и высокой биохимической активностью. F.Kauffmann (1963) характеризует сальмонелл как «группы сероферментативных фаготипов».
Наиболее признанная в настоящее время классификация сальмонелл Кауффманна—Уайта достаточно сложна, в ней учитываются ферментативные свойства возбудителей, особенности их антигенной структуры и другие признаки.
Сальмонеллы имеют сложную антигенную структуру. По структуре О-антигена их делят на серогруппы, по Н-антигену — на серотипы. Кроме того, в пределах каждого серовара выделяют биовары (различаются по ферментации углеводов) и фаговары (по отношению к специфическому фагу).
Наибольшее значение для идентификации сальмонелл имеют 3 основных антигена — О, Н, К.
О-антиген — поверхностный антиген оболочки. Это термоустойчивый липидополисахаридный комплекс. По особенностям структуры главного О-антигена все сальмонеллы разделены на 50 серологических групп, а в пределах некоторых групп выделяют еще и подгруппы. Набор О-антигенов у каждого возбудителя индивидуален. Однако за счет общности отдельных антигенов, причем не только с сальмонеллами, но и с другими представителями семейства Enterobacteriaceae, возможны перекрестные реакции. Кроме того, О-антигенный состав нестабилен, возможны количественные и качественные изменения О-антигенов (О-вариации) у отдельных возбудителей, что может даже заканчиваться превращением одного серовара в другой. Известен феномен фазовой конверсии — изменение О-антигенов, вызываемое конвертирующим фагом. Для сальмонелл характерна высокая чувствительность к сальмонеллезному О-бактериофагу, который лизирует около 97% штаммов сальмонелл. Наиболее часто заболевания у человека вызывают сальмонеллы А—Е групп. Антитела против О-антигена обеспечивают антитоксический иммунитет.
Н-антиген — жгутиковый, белковый, термолабильный. Имеет 2 фазы — специфическую и неспецифическую (современное название их — I фаза и II фаза). Каждая фаза имеет серологические варианты (I — 80, II — 9). Есть серотипы, имеющие обе фазы, есть такие, которые имеют только одну, а неподвижные сальмонеллы вообще не имеют Н-антигена.
Сальмонеллы (не все) имеют также К-антигены (поверхностные, или капсульные), представленные различными вариантами (М, Vi и др.). К-антигены (белково-полисахаридный комплекс) повышают способность сальмонелл проникать внутрь макрофагов. Антитела против К-антигенов препятствуют внутриклеточному размножению сальмонелл.
Патогенность сальмонелл обеспечивается множеством факторов, главными их которых являются:
способность к внутриклеточному паразитированию;
наличие средств адгезии, обеспечивающих прикрепление к клетке;
— К-антигены, способствующие проникновению сальмонелл в клетку и размножению в ней;
— R-плазмиды, обеспечивающие резистентность к антибиотикам;
различные ферменты, облегчающие проникновение в клетку, повреждение ее (гиалуронидаза, нейраминидаза и др.);
способность сальмонелл выходить за пределы кишечника в кровяное русло, вызывая различной интенсивности бактериемию, септицемию;
способность размножаться в различных органах и тканях, вызывать полиорганные поражения;
способность конкурировать с нормальной кишечной микрофлорой и вызывать дисбактериоз;
способность образовывать L-формы, формировать резистентность к антибиотикам;
наличие токсических факторов — эндотоксина, а у некоторых штаммов и экзотоксина.
Существует мнение, что патогенность сальмонелл в значительной мере зависит от углеводного состава полисахаридов, входящих в состав эндотоксина.
Следует особо остановиться на токсических субстанциях сальмонелл, которые выделяются при их разрушении. Основным токсическим фактором является термостабильный эндотоксин (липополисахарид клеточной стенки). Всасываясь в кровь, он вызывает различные общетоксические реакции в результате воздействия на ЦНС, сосуды, вегетативную нервную систему и т.д. Эндотоксин вызывает пирогенный эффект, агрегацию тромбоцитов, опосредованно через макрофаги способствует выделению медиаторов воспаления, оказывает непосредственное цитоток-сическое действие, стимулирует ГЗТ и т.д. Эндотоксическим свойством, закрепленным в генах, обладают все сальмонеллы, хотя патогенность и степень вирулентности их очень варьируют.
Синтез термолабильного энтеротоксина (его основная часть — белок) кодируется плазмидами (клеточными структурами, не сцепленными с хромосомой бактерий). Плазмиды могут оказывать влияние на размножение бактерий в организме, повышать резистентность к факторам иммунной защиты. Плазмиды, несущие ген токсигенности, могут передаваться от клетки к клетке, то есть свойство энтеротоксиген-ности не является таким постоянным, как эндотоксигенность. Энтеро-токсин способен воздействовать на аденилатциклазную систему, вызывая нарушение функции кишечника, секреции и всасывания электролитов и жидкости.
Соотношение различных факторов патогенности у сальмонелл, зависящих прежде всего от хромосомных и плазмидных структур, в значительной мере определяет особенности течения болезни.
Эпидемиология. Источником инфекции при сальмонеллезах являются люди и различные теплокровные животные, птицы, пресмыкающиеся, рыбы. Особую опасность представляют инфицированные лица, относящиеся к декретированным группам (прежде всего работники предприятий общественного питания).
Больной человек в острый период болезни выделяет до 108 микробных тел в 1 г фекалий. После исчезновения клинических симптомов выделение возбудителя с калом или мочой может продолжаться еще от 2 до 10 нед, а у 1 % реконвалесцентов возможно более длительное (годы) носительство. Особенно длительно выделяются возбудители после лечения антибиотиками, что объясняется, с одной стороны, высокой резистентностью сальмонелл к антибиотикам, с другой — развитием на фоне антибиотикотерапии дисбактериоза, при котором существенно ослабевает антагонистическое действие нормальной микрофлоры на сальмонелл.
Источником инфекции могут быть сельскохозяйственные животные (свиньи, мелкий и крупный рогатый скот, овцы), у которых сальмонеллез может протекать в форме носительства, гастроэнтерита, септико-пиемии. Молоко и мясо таких животных содержит большое количество сальмонелл.
Важную роль в распространении инфекции играют птицы (утки, куры), при этом инфицированными могут оказаться как мясо, так и яйца.
Синантропные грызуны, дикие птицы (голуби, воробьи) могут также быть источником инфекции, загрязняя предметы окружающей среды. Источником инфекции могут быть и домашние животные ■— кошки, собаки.
Механизм передачи возбудителя — фекально-оральный, чаще сальмонеллы попадают в организм человека с инфицированной пищей. Но возможно инфицирование сальмонеллами предметов окружающей среды (дверные ручки, игрушки, посуда), и таким образом может реа-лизовываться бытовой путь передачи возбудителя.
Основным фактором передачи служат обсемененные сальмонеллами пищевые продукты, особенно часто мясные и (реже) молочные. Заражение может наступить при употреблении в пищу сырых или плохо прожаренных куриных и утиных яиц, в которые сальмонеллы могут
проникать даже через скорлупу при неправильном их хранении, но чаще яйца инфицируются при прохождении через яйцеводы больных птиц. В яйце сальмонеллы находятся главным образом в желтке, так как в нем нет бактерицидно действующего лизоцима, который содержится в белке. Сальмонеллы могут длительно сохраняться в яичном порошке. Кстати, если инфицированные яйца поместить в инкубатор, то и вылупившиеся цыплята будут заражены. Человек может заразиться, поедая и другие инфицированные продукты — плохо прожаренную рыбу (карп, щука и др.), сырые моллюски, заражение которых происходит при значительном загрязнении водоемов сточными водами, содержащими сальмонеллы.
Длительное время сальмонеллы сохраняются и даже размножаются в салатах, винегрете.
Вода как фактор передачи имеет меньшее значение, это возможно лишь при очень значительном загрязнении ее сточными водами, содержащими сальмонеллы.
В переносе инфекции на пищевые продукты немаловажная роль принадлежит мухам.
Заболеваемость сальмонеллезом регистрируется в виде спорадических случаев и вспышек, протекающих обычно по типу пищевых токсикоинфекций. В случаях нарушения санитарных правил на предприятиях и объектах общественного питания возможны крупные вспышки.
Для сальмонеллеза характерна сезонность: выше заболеваемость летом и осенью, что связано с более благоприятными условиями для сохранения сальмонелл и даже их накопления, наличием мух. В последние годы, тем не менее, такая сезонная закономерность более или менее отчетливо прослеживается лишь при спорадических случаях, эпидемические же вспышки возникают в любое время года.
Сальмонеллезом болеют люди различного возраста, но при заражении детей до 2 лет чаще развиваются манифестные формы с явлениями энтерита, гастроэнтерита. При заражении детей старшего возраста и взрослых нередко возникают стертые формы заболевания и носительство. Факторами, способствующими развитию болезни, являются прежде всего-хронические заболевания дигестивной системы, предшествовавшее лечение антибиотиками.
В последнее время сальмонеллез регистрируют в виде спорадических случаев и вспышек в лечебных учреждениях различного профиля (госпитальный сальмонеллез). Чаще всего источником таких вспышек сальмонеллеза (обычно среди детей до 2 лет) служат сотрудники отделений (больные или носители). Особенностью эпидемического процесса в очаге госпитального сальмонеллеза является длительное и вялое течение из-за постепенного вовлечения все новых лиц, выделение преимущественно резистентных к антибиотикам штаммов сальмонелл, течение заболевания по типу патологии-микст.
При изучении распространенности сальмонеллеза на отдельных территориях прослеживается обычно зависимость между ростом заболеваемости и носительства среди сельскохозяйственных животных и людей.
Классификация. Огромное число серотипов сальмонелл, особенности их взаимоотношений с организмом человека, проявляющиеся в разнообразии клинических симптомов, затрудняют создание стройной классификации. И до настоящего времени единой общепринятой классификации сальмонеллеза нет. В нашей стране с 1981 г. наибольшее распространение и применение получила классификация, разработанная под руководством В.И.Покровского (1981), в соответствии с которой выделяют следующие клинические формы сальмонеллеза:
гастроинтестинальная, локализованная (гастритический, гастро-энтеритический, гастроэнтероколитический, энтероколитический варианты);
генерализованная (тифоподобный и септикопиемический варианты) ;
бактерионосительство — острое (до 3 мес), хроническое (свыше 3 мес), транзиторное;
— субклиническая (бессимптомная).
При септикопиемическом варианте формируются гнойные очаги в различных органах. Но так как сальмонеллез, даже его гастроинтестинальная форма, практически всегда сопровождается кратковременной бактериемией, часто незначительной, то при этом возможно образование гнойных метастатических очагов в различных органах (практически во всех). В зарубежных руководствах (в частности, «Principles and Practice of infectious Diseases», 1985) помимо гастроинтестинальной и генерализованной форм выделяют еще и очаговые формы сальмонелле-зов:
менингит,
плевропульмональные заболевания,
абсцессы печени,
абсцессы легких и др.
Особенностью таких форм является то, что при обнаружении сальмонелл в содержимом абсцессов и флегмон не удается установить четкой связи с предшествовавшей манифестной сальмонеллезной инфекцией. Если же эта связь доказана, то речь идет о септикопиемическом варианте с соответствующей локализацией метастатического очага.
Необходимо также оценивать тяжесть течения сальмонеллезов (легкое, среднетяжелое, тяжелое).
Критериями тяжести заболевания могут быть либо степень интоксикации (см. Брюшной тиф), либо степень обезвоживания (см. Пищевые токсикоинфекций). Но в ряде случаев приходится учитывать оба эти фактора. Заболевание может начинаться с тяжелого токсикоза, вплоть до ИТШ, а затем присоединяется диарея с последующей гиповолемией.
Примерная формулировка диагноза. 1. Сальмонеллез, гастроинте-стинальная форма (гастроэнтерит), течение средней тяжести, дегидратация I—II степени.
Сальмонеллез, генерализованная форма (тифоподобный вариант), течение средней тяжести.
Сальмонеллез, генерализованная форма (септикопиемический вариант), абсцесс селезенки, тяжелое течение.
4. Сальмонеллезный гнойный артрит правого коленного сустава.
В последнем случае клинические проявления предшествовавшего сальмонеллеза (гастроинтестинальной или генерализованной формы) не были диагностированы.
Патогенез. «Ни при одном инфекционном заболевании мы не встречаемся с такими принципиально различными по своей патогенетической архитектонике процессами, как при сальмонеллезе», — эта краткая характеристика патогенеза сальмонеллеза академика А.Ф.Билиби-на (1960) объясняет отсутствие четкой логической схемы изложения этого раздела.
Особенности течения инфекционного процесса зависят от множества факторов: свойств и дозы попавшего в организм возбудителя, состояния макроорганизма (наличие и характер сопутствующих заболеваний) и т.д.
Так, лица с гемоглобинопатиями болеют тяжелее, заболевание часто протекает с выраженной бактериемией, образованием септических сальмонеллезных очагов.
Люди с пониженной желудочной секрецией, с удаленным желудком более подвержены сальмонеллезу, который у них возникает от меньшей дозы возбудителя и протекает более тяжело.
Тяжело болеют дети в возрасте до 5 лет из-за несовершенства гуморального и клеточного иммунитета, особенностей микрофлоры кишечника.
Нормальная микрофлора кишечника является антагонистом сальмонелл и других патогенных бактерий, поэтому дисбактериоз, развитию которого прежде всего способствует как предшествующая, так и применяющаяся нередко при различных формах сальмонеллезов антибио-тикотерапия, приводит к тяжелому затяжному течению, повышает вероятность генерализации процесса, формирования носительства.
Наличие местных очагов воспаления и повреждений различного ге-неза в организме человека (хроническая пневмония, гематома, травма костей и т.д.) повышает вероятность образования гнойных метастатических сальмонеллезных очагов.
При шистосомозе мочеполовой системы велика вероятность формирования мочевого носительства сальмонелл.
В значительной мере патогенетические особенности и характер клинических проявлений определяются свойствами самого возбудителя.
Так, S.anatum вызывает преимущественно бессимптомную форму заболевания, реже — умеренную диарею. При заражении S.cholerae suis практически всегда возникает генерализованная форма, протекающая по типу тифоподобного или септикопиемического варианта, а диарея при этом бывает редко; ведущий симптом — токсикоз.
Диарея — не обязательное проявление сальмонеллеза, так как не все сальмонеллы, а лишь энтеротоксигенные штаммы образуют энте-ротоксин.
Степень участия в развитии патологического процесса таких основных факторов, как эндотоксин и энтеротоксин, неодинакова у различных представителей рода сальмонелл, что сказывается на выраженности ведущих синдромов — интоксикации и диареи.
Антигенная структура сальмонелл существенно влияет на течение патологического процесса. Так, сальмонеллы, имеющие К-антиген, но лишенные О-антигена, способны проникать в макрофаги, размножаться в них, они не оказывают цитопатического действия. Наличие О-антигена при отсутствии К-антигена у сальмонелл приводит к выраженному цитопатическому действию. Штаммы, лишенные обоих антигенов, оказывают минимальное повреждающее действие, так как они легко перевариваются макрофагами.
При любой форме сальмонеллеза заражение происходит через пищеварительный тракт. Если в пищевом продукте произошло размножение возбудителя и его накопление в значительном количестве, при поступлении такой пищи в желудок массовая гибель сальмонелл сопровождается освобождением токсина. При этом первые проявления, как и при других пищевых токсикоинфекциях, будут обусловлены как местным действием токсина (тошнота, рвота, боль в эпигастрии), так и действием проникшего в кровь эндотоксина на сосуды, центр терморегуляции, надпочечники, вегетативную нервную систему, тромбоциты, лейкоциты. Циркулирующий эндотоксин уже в первые часы заболевания помимо лихорадочной реакции способен вызывать различные расстройства в организме вплоть до ИТШ.
Иногда заболевание может закончиться на этапе гибели возбудителей в желудке (гастритический вариант гастроинтестинальной формы сальмонеллеза).
Если возбудитель преодолевает защитные барьеры (кислотность желудочного сока, антагонистическое действие микрофлоры и ферментов кишечника, лизоцима, IgA и др.), сальмонеллы размножаются в просвете кишечника и благодаря своим адгезивным свойствам «прилипают» к эпителиальным клеткам кишечника, проникая затем в цитоплазму энтероцитов.
Эндотоксин, образующийся в просвете кишки при гибели сальмонелл, повышает проницаемость клеточных мембран, что облегчает проникновение сальмонелл в клетку. Не разрушая энтероциты, они могут продвигаться далее, достигая базальной мембраны, где захватываются макрофагами. Штаммы, вызывающие диарею, обусловливают лейкоцитарную инфильтрацию базальной мембраны, а далее инфекция обычно не распространяется, так как при этом наступает быстрая гибель и разрушение сальмонелл, повышение содержания гистамина и серотонина в слизистой оболочке, в результате чего усиливаются местные воспалительные процессы. Эндотоксин стимулирует также повышение синтеза простагландинов, влияющих на множественные ферментные системы кишечника, в том числе аденилатциклазную, вследствие этого повышается секреция воды и электролитов в кишечник, развивается диа-рейный синдром, который может сопровождаться значительной потерей электролитов, циркуляторными нарушениями (патогенез их сходен с таковым при пищевой токсикоинфекций). Но даже при гастроин-, тестинальной форме сальмонеллеза в начале заболевания наблюдают кратковременную перемежающуюся бактериемию.
В том случае, если заражение происходит неэнтеротоксигенными штаммами сальмонелл, диарейный синдром нередко отсутствует. Возможна рвота в первые часы болезни, может развиться коллапс и даже ИТШ в результате действия эндотоксина, но чаще заболевание развивается по тифоподобному варианту, при котором патогенетические механизмы развития болезни, выздоровления, формирования осложнений и носительства такие же, как при брюшном тифе.
Септикопиемический вариант генерализованной формы сальмонеллеза может возникнуть при заражении сальмонеллами, содержащими и не содержащими энтеротоксин. Основным условием его развития является неспособность реализовать местные и общие защитные механизмы, что чаще бывает у ослабленных людей (с иммунодефицитом, дисбактериозом и т.д.), у маленьких детей. При этом гнойные вторичные очаги чаще локализуются в тех местах, где имеется хронический воспалительный процесс, нарушено кровообращение и имеется гипоксия тканей (locus minoris resistentia). Сальмонеллы могут проникать через гематоэнцефалический барьер, вызывая гнойное воспаление мозговых оболочек. Практически нет органа, ткани, в которых бы не могли образовываться гнойные септические очаги. Такие формы сальмонеллеза сопровождаются высокой летальностью, тем более, что анти-биотикотерапия часто бывает неэффективной.
Взаимосвязь отдельных клинических форм сальмонеллеза можно условно представить следующим образом (рис. 19).
Роль экзотоксина в патогенезе сальмонеллезов еще недостаточно ясна. Полагают, что, кроме эндотоксина и энтеротоксина, существуют еще несколько токсических субстанций, роль их тоже еще изучается.
