
- •Предисловие
- •Химическая термодинамика, как теоретическая основа биоэнергетики Предмет, методы и основные понятия химической термодинамики
- •Термодинамические системы: изолированные, закрытые, открытые, гомогенные, гетерогенные
- •Термодинамические параметры
- •Внутренняя энергия системы
- •Форма обмена энергии с окружающей средой
- •Первое начало термодинамики. Тепловые эффекты химических реакций
- •1. В изолированной системе сумма всех видов энергии есть величина постоянная.
- •Изобарный и изохорный процессы. Энтальпия. Тепловые эффекты химических реакций
- •Термохимия. Закон Гесса
- •Влияние температуры и давления на тепловой эффект реакции
- •Использование закона Гесса в биохимических исследованиях
- •Энтропия. Второй закон термодинамики Энтропия
- •Второе начало термодинамики. Свободная энергия Гиббса
- •Принцип энергетического сопряжения
- •Химическое равновесие Обратимые и необратимые реакции. Константа равновесия
- •Смещение химического равновесия. Принцип Ле-Шателье
- •Учение о растворах Растворы
- •Физические свойства н2о и строение ее молекул
- •Механизм образования растворов
- •Растворимость веществ. Факторы, влияющие на растворимость
- •Влияние природы веществ на растворимость
- •Влияние давления на растворимость веществ
- •Влияние температуры на растворимость веществ
- •Влияние электролитов на растворимость веществ
- •Взаимная растворимость жидкостей
- •Способы выражения состава растворов
- •Термодинамические аспекты процесса растворения. Идеальные растворы
- •Коллигативные свойства разбавленных растворов
- •Диффузия и осмос в растворах
- •Роль осмоса в биологических процессах
- •Давление насыщенного пара растворителя над раствором. Закон Рауля
- •Следствия из закона Рауля
- •1) Растворы кипят при более высокой температуре, чем чистый растворитель;
- •2) Растворы замерзают при более низкой температуре, чем чистый растворитель.
- •Применение методов криоскопии и эбуллиоскопии
- •Коллигативные свойства растворов электролитов. Изотонический коэффициент Вант-Гоффа
- •Электролитическая диссоциация Электролиты и неэлектролиты. Теория электролитической диссоциации
- •Общая характеристика электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Диссоциация воды. Водородный показатель
- •Теория кислот и оснований. Буферные растворы Теория кислот и оснований
- •Буферные растворы Определение буферных систем и их классификация
- •Механизм действия буферных систем
- •Вычисление рН и рОн буферных систем. Уравнение Гендерсона-Гассельбаха
- •Буферная емкость
- •Буферные системы человеческого организма
- •Нарушения кислотно-оснóвного равновесия крови. Ацидоз. Алкалоз
- •Химическая кинетика и катализ Кинетика химических реакций
- •Понятие о скорости химической реакции. Закон действующих масс
- •Кинетическая классификация химических реакций. Понятие о молекулярности и порядке химической реакции Порядок и молекулярность простых химических реакций
- •Понятие о сложных химических реакциях
- •Классификация сложных реакций
- •Измерение скорости химической реакции
- •Влияние температуры на скорость химической реакции
- •Катализ Общие положения и закономерности катализа
- •Механизм гомогенного и гетерогенного катализа
- •Особенности каталитической активности ферментов
- •2. Другим важным отличием ферментов от катализаторов небелковой природы является их высокая специфичность, т.Е. Избирательность действия.
- •Физическая химия дисперсных систем Определение дисперсных систем
- •Классификация дисперсных систем и их общая характеристика
- •Классификация дисперсных систем по агрегатному состоянию вещества дисперсной фазы и дисперсионной среды
- •Классификация по взаимодействию между частицами дисперсной фазы или степени структурированности системы
- •Классификация по характеру взаимодействия дисперсной фазы с дисперсионной средой
- •Методы получения дисперсных систем
- •Диспергирование жидкостей
- •Диспергирование газов
- •Конденсационные методы
- •Методы физической конденсации
- •Методы химической конденсации
- •Очистка золей
- •Компенсационный диализ и вивидиализ
- •Молекулярно-кинетические свойства золей
- •Броуновское движение
- •Диффузия
- •Седиментация в золях
- •Осмотическое давление в золях
- •Оптические свойства золей
- •Рассеяние света (опалесценция)
- •Оптические методы исследования коллоидных систем Ультрамикроскоп
- •Механизм образования и строение коллоидной частицы – мицеллы
- •1. Получение золя берлинской лазури:
- •2. Получение с помощью гидролиза FeCl3 золя гидроксида железа (III).
- •3. Получение золя As2s3:
- •Электрокинетические свойства золей
- •Устойчивость гидрофобных коллоидных систем. Коагуляция золей Виды устойчивости золей
- •Теория коагуляции Дерягина-Ландау-Фервея-Овербека
- •Влияние электролитов на устойчивость золей. Порог коагуляции. Правило Шульца-Гарди
- •Чередование зон коагуляции
- •Коагуляции золей смесями электролитов
- •Скорость коагуляции
- •Коллоидная защита
- •Роль процессов коагуляции в промышленности, медицине, биологии
- •Растворы высокомолекулярных соединений
- •Общая характеристика высокомолекулярных соединений
- •Классификация полимеров
- •Набухание и растворение вмс
- •Термодинамические аспекты процесса набухания
- •Давление набухания
- •Свойства растворов высокомолекулярных соединений
- •Осмотическое давление растворов вмс
- •Онкотическое давление крови
- •Вязкость растворов полимеров
- •Свободная и связанная вода в растворах
- •Полиэлектролиты
- •Факторы, влияющие на устойчивость растворов полимеров. Высаливание
- •Электрохимия растворы электролитов как проводники второго рода. Электропроводность растворов электролитов
- •Эквивалентная электропроводность растворов
- •Практическое применение электропроводности
- •Равновесные электродные процессы
- •Металлический электрод
- •Измерение электродных потенциалов
- •Окислительно-восстановительные электроды
- •1. Переход окисленной формы в восстановленную и наоборот заключается только в обмене между ними электронами:
- •Диффузионный и мембранный потенциалы
- •Химические источники электрического тока. Гальванические элементы
- •Потенциометрия
- •Содержание
1. Получение золя берлинской лазури:
3 K4 [Fe(CN)6] + 4 FeCl3 → Fe4 [Fe(CN)6]3↓ + 12 KCl
Если в избытке взять комплексную соль K4 [Fe(CN)6], то потенциалопределяющими ионами будут являться ионы [Fe(CN)6]4–, а противоионами – K+. Гранула в этом случае будет иметь отрицательный заряд:
{m[Fe4[Fe(CN)6]3]n[Fe(CN)6]4– (4n – x) K+}–x xK+
При получении данного золя в условиях избытка FeCl3 потенциалопределяющими ионами станут ионы Fe3+, а противоионами – Cl–. Гранула при этом приобретет положительный заряд:
{m[Fe4[Fe(CN)6]3]nFe3+ (3n – x) Cl–}+x xCl–
2. Получение с помощью гидролиза FeCl3 золя гидроксида железа (III).
FeCl3 + 3 H2O Fe(OH)3↓ + 3HCl
Часть образовавшегося Fe(OH)3 в условиях проведения реакции прореагирует с соляной кислотой:
Fe(OH)3 + HCl → FeOCl + 2 H2O
В связи с этим в роли стабилизатора будет выступать FeOCl:
FeOCl ↔ FeO+ + Cl–
т.к. хлорид железа(III) расходуется полностью, то потенциалопределяющими будут являться ионы FeO+, т.к. именно они, а не ионы Fe3+, станут присутствовать в растворе в избытке.
Формула мицеллы (рис. 60а) при этом запишется следующим образом:
{m[Fe(OH)3] · nFeO+ (n – x) Cl–}+x xCl–
3. Получение золя As2s3:
2H3AsO3 + 3H2S → As2S3 ↓ + 6 H2O
избыток
Двухосновная сероводородная кислота является слабым электролитом, в растворе диссоциирует преимущественно по первой стадии
H2S ↔ HS– + H+,
поэтому потенциалопределяющими ионами в данном случае будут выступать ионы HS–. В связи с этим формулу образовавшейся мицеллы (рис. 60б) можно представить следующим образом:
{m[As2S3]n HS–(n – x) H+}–x xH+
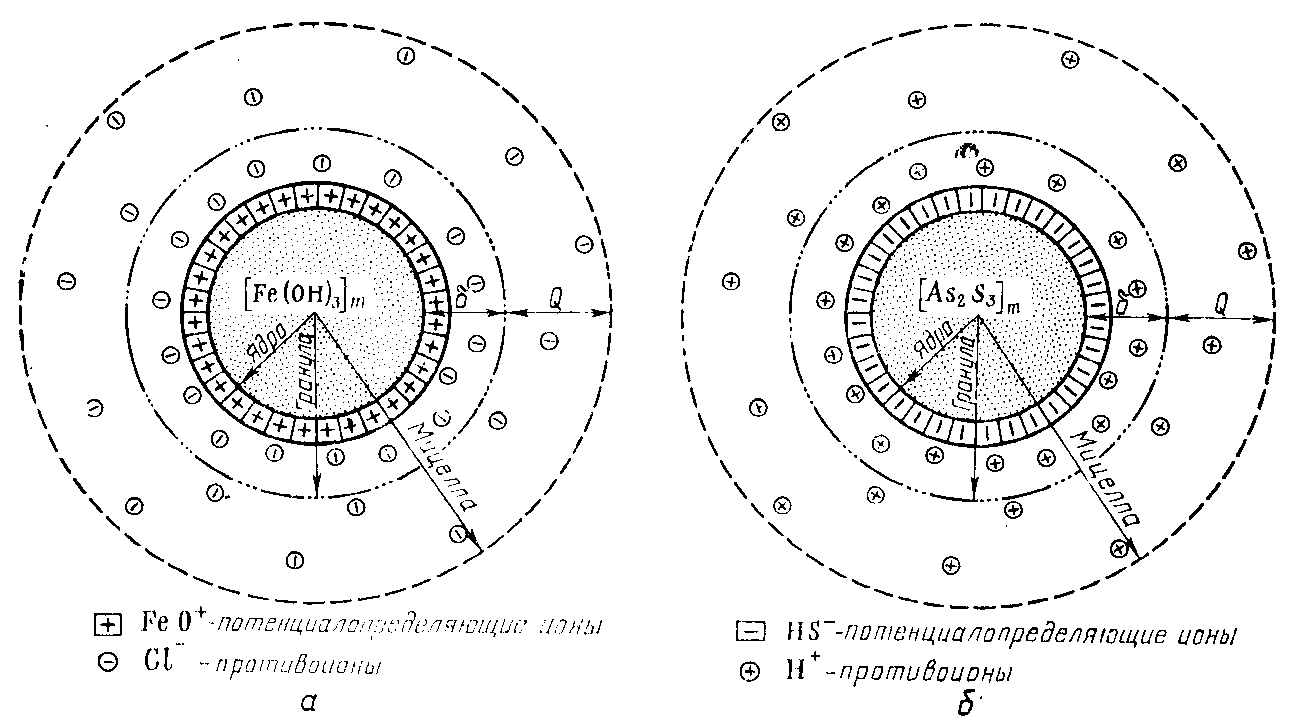
Рис. 60. Схема строения: a – мицеллы гидроксида железа (III); б – мицеллы сульфида мышьяка m – число молекул, образующих ядро; δ – адсорбционный слой (плотный); Q – диффузный слой противоионов
В качестве примера образования ДЭС путем поверхностной диссоциации можно рассмотреть строение мицеллы кремниевой кислоты, часть молекул которой, находясь на поверхности ядра, диссоциирует по уравнению:
H2SiO3 ↔ H+ + HSiO3–
Причем ионы HSiO3–, прочно связанные с ядром, являются потенциалопределяющими. Роль противоионов выполняют подвижные ионы Н+, которые распределяются как в адсорбционном, так и в диффузном слоях (рис. 61). Схематическое строение коллоидной частицы данного золя можно представить следующим образом:
{m[H2SiO3]n HSiO3– (n – x) H+} xH+
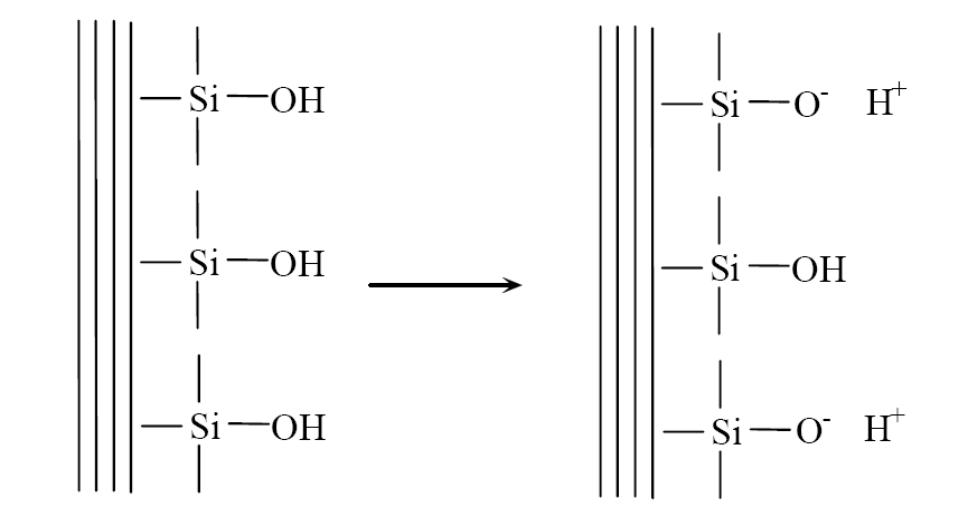
Рис. 61. Диссоциация поверхностных силанольных групп
Следует отметить, что мицеллы в золях не имеют строго определенного состава и обладают более сложным строением, которое предложенные нами формулы отражают со значительной степенью условности. Тем не менее, они позволяют интерпретировать многие свойства золей как в качественном, так и в количественном плане, и поэтому представляют определенный интерес.
Электрокинетические свойства золей
Доказательство того, что коллоидные частицы в золях состоят из двух разноименно заряженных частей, способных перемещаться друг относительно друга, можно получить, если воздействовать на дисперсную систему внешним электрическим полем.
Впервые это явление в 1809 г. наблюдал профессор Московского университета Ф. Рейс (рис. 62). В его опытах в кусок влажной глины (1) были вставлены две стеклянные трубки без дна (2), в которые до одинакового уровня наливали воду. В трубки были опущены электроды, присоединенные к соответствующим полюсам источника постоянного тока. Через некоторое время под влиянием электрического поля частицы глины, отрываясь от поверхности, стали двигаться в стеклянную трубку с положительно заряженным электродом (3), образуя в ней хорошо заметную суспензию (в виде мути) (рис. 62). Это свидетельствует о том, что сами частички глины заряжены отрицательно.
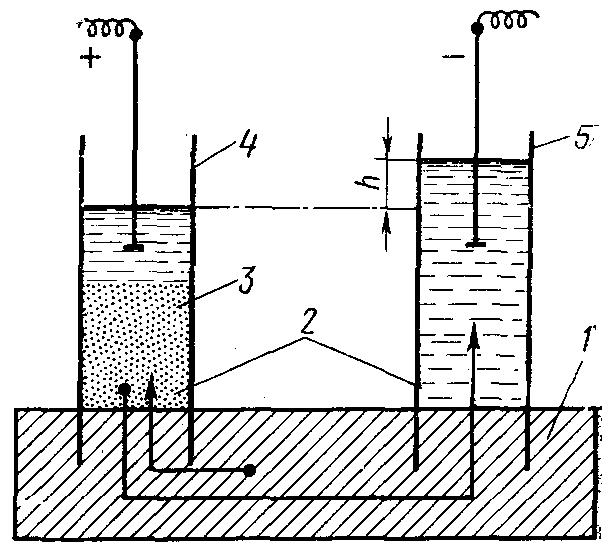
Рис. 62. Схема установки для проведения электрофореза и электроосмоса
Уровень жидкости в трубке с частицами глины при этом понизился, зато во второй трубке (с отрицательно заряженным электродом) (4), наоборот, увеличился на величину h (5). Сама жидкость при этом осталась прозрачной и, очевидно, приобрела положительный заряд.
При дальнейшем изучении этих явлений обнаружилось, что они характерны для многих коллоидно-дисперсных систем.
Движение твердых частиц дисперсной фазы во внешнем электрическом поле к одному из электродов получило название электрофореза.
Соответственно, перемещение жидкой дисперсионной среды к противоположно заряженному электроду назвали электроосмосом.
Оба эти явления относятся к так называемым электрокинетическим явлениям и наблюдаются при возникновении разности потенциалов в дисперсной системе.
Последующие исследования показали, что электрокинетические явления в золях наблюдаются не только при внесении их во внешнее электрическое поле. В 1859 г. Квинке обнаружил, что разность потенциалов в дисперсных системах возникает при механическом проталкивании воды через пористую диафрагму или через капилляр, т.е. при движении дисперсионной среды относительно неподвижной дисперсной фазы (рис. 63а). При этом протекание жидкости затрудняется.
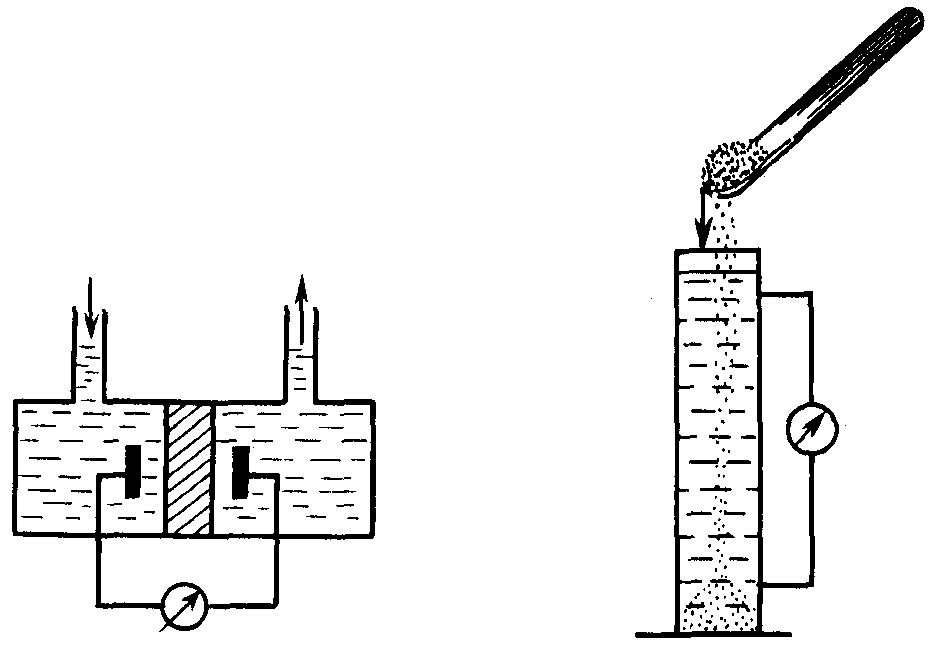
а б
Рис. 63. Схемы установки для наблюдения за: а – потенциалом протекания б – потенциалом седиментации
Это явление (обратное электроосмосу) получило название эффекта протекания или эффекта истечения, а возникающая разность потенциалов – потенциала протекания.
В 1878 г. Дорн обнаружил другое электрокинетическое явление, которое заключалось в возникновении разности потенциалов при механическом передвижении твердых частиц относительно неподвижной жидкой фазы (например, при оседании крупинок песка в воде) (рис. 63б). Данное явление обратно электрофорезу и получило название эффекта седиментации, возникающая разность потенциалов – потенциала седиментации.
Образование потенциалов протекания и седиментации наблюдается в производствах, в которых осуществляется транспортировка жидкости (перекачка технологических растворов, жидкого топлива), осаждение суспензий и эмульсий при разделении фаз. На концах трубопроводов и аппаратов возникают при этом высокие разности потенциалов, которые часто являются причиной искровых разрядов, вызывающих пожары и взрывы.
Электрокинетические явления можно объяснить существованием на поверхности частиц дисперсной фазы двойного электрического слоя, т.е. возникновением разности потенциалов между гранулой и диффузным слоем мицеллы.
Так как при этом гранулы в золе имеют заряды одного знака, а их диффузные слои – другого знака, то под действием внешнего электрического поля эти составные части мицеллы приходят в движение друг относительно друга (рис. 64).
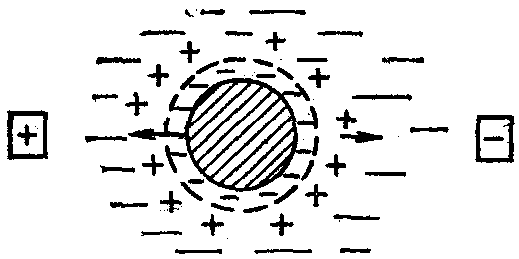
Рис. 64. Схема движения гранулы и диффузного слоя мицеллы во внешнем электрическом поле
Например, если гранула заряжена отрицательно, то во внешнем электрическом поле она будет перемещаться к аноду, положительно заряженные противоионы диффузного слоя вместе со своими гидратными оболочками станут накапливаться возле катода.
При движении твердой и жидкой фаз мицеллы друг относительно друга скольжение и разрыв их происходит не по поверхности гранулы, а на некотором расстоянии от нее, за пределами адсорбционного слоя по плоскости АВ (рис. 65). Поэтому противоионы, находящиеся в адсорбционном слое, будут неподвижны относительно гранулы и при электрофорезе станут перемещаться вместе с ней, увлекая за собой свои гидратные оболочки. Потенциал, возникающий на плоскости скольжения, является дзета-потенциалом (ζ-потенциалом), он определяет скорость перемещения гранулы и диффузного слоя друг относительно друга при наложении электрического поля, т.е. является причиной электрокинетических явлений. В связи с этим он и получил свое второе название – электрокинетический потенциал.
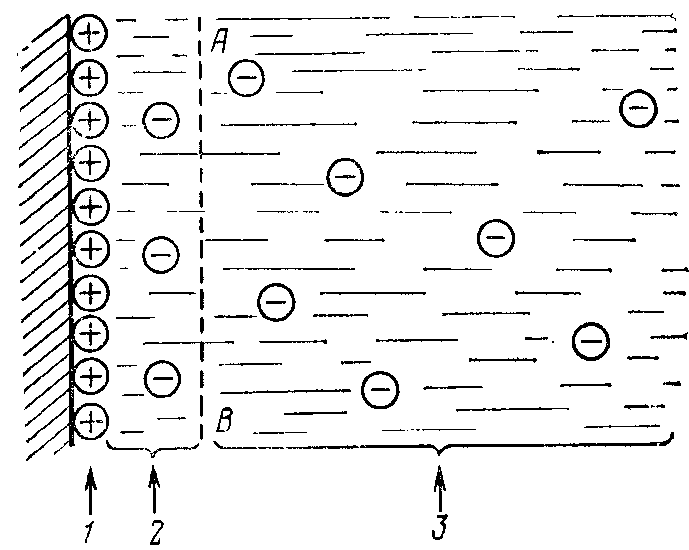
Рис 65. Строение двойного электрического слоя: 1 – потенциалопределяющие ионы; 2 – адсорбционный слой противоионов; 3 – диффузный слой противоионов; АВ – плоскость скольжения
Измеряя скорость движения заряженных гранул во внешнем электрическом поле, можно рассчитать величину их ζ-потенциала и тем самым оценить уровень устойчивости золя.
Возникновение потенциала протекания (течения), объясняется тем, что движущаяся жидкость увлекает за собой ионы диффузного слоя коллоидных частиц, находящихся в неподвижной твердой среде, и оказывается тем самым носителем электрического заряда, вследствие чего в ней возникает ток, называемый током течения.
Потенциал седиментации образуется из-за того, что в процессе осаждения ионы диффузного слоя в силу молекулярного трения и разности в массах отстают от более тяжелых движущихся гранул. При этом разные части системы приобретают электрические заряды противоположного знака.
Явления электрофореза и электроосмоса широко используются в промышленности, биологических исследованиях, медицине.
Электрофоретическое осаждение частиц золей на металлические поверхности применяют для нанесения защитных и декоративных покрытий. Так получают прочные и красиво окрашенные поверхности при электрофоретическом осаждении красок и лаков, электроизоляционные резиновые пленки при осаждении частиц каучука из его водных дисперсий, пленки оксидов щелочноземельных металлов на вольфрамовых нитях радиоламп. Электрофорез используют для очистки дыма в заводских трубах от частиц сажи и пыли.
Метод электроосмоса имеет большое практическое применение в процессах обезвоживания и сушки пористых материалов, осадков, или концентрированных (кашицеобразных) коллоидных систем. Для этой цели применяют, например, специальные электрофильтры – прессы (рис. 66).
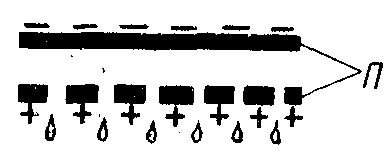
Рис. 66. Схема сушки методом электроосмоса
Основную часть их представляют 2 металлические пластины (П), расположенные одна над другой горизонтально. Нижняя пластина имеет множество отверстий. Подлежащую обезвоживанию кашицеобразную массу помещают между этими пластинами, которые подключают к разным полюсам источника постоянного тока.
При этом верхняя пластина должна иметь заряд, совпадающий по знаку с зарядом диффузного слоя коллоидных частиц, а нижняя – противоположный. Вследствие электроосмоса жидкость устремляется к нижней пластинке и удаляется через ее отверстия.
Электроосмос широко применяется для понижения уровня грунтовых вод, для осушения глинистых осадочных слоев (рис. 67). Частицы коллоидно-дисперсных грунтов заряжены, как правило, отрицательно. Если в такой грунт ввести два металлических электрода, один из которых (отрицательно заряженный) опустить в специально пробуренную скважину (1), то вода под действием электрического поля будет перемещаться в скважину, откуда ее можно откачивать специальными насосами.

Рис. 67. Схема установки для обезвоживания грунтов методом электроосмоса: 1 – скважина с вставленным в нее металлическим фильтром; 2 – глубинный насос; 3 – генератор постоянного тока; 4 – металлический стержень
Электрофорез является эффективным средством для изучения фракционного состава сложных биологических жидкостей (особенно крови), содержащих белковые молекулы, энзимы, вирусы, бактерии, различные другие клеточные структуры (форменные элементы крови). Все эти частицы имеют в биологических жидкостях, как правило, отрицательный заряд различной величины. Следовательно, они будут обладать неодинаковой электрофоретической подвижностью во внешнем электрическом поле и их можно разделить на различные фракции.
В медицине для диагноза и контроля за ходом болезней таким образом получают электрофореграммы белков сыворотки крови. Они имеют специфические различия для каждого заболевания, по сравнению с таковыми у здоровых организмов.
Электрофоретические методы находят широкое применение в иммунологических исследованиях (в частности, для оценки клеточного иммунитета у онкологических больных), для определения изоэлектрической точки белков.
В фармацевтической промышленности электрофорез применяют для очистки лекарственных препаратов, выделенных из животных и растительных клеток, а также для контроля степени их чистоты и однородности.
В практической медицине широко используется электрофоретический метод местного введения через неподвижную кожу лекарственных препаратов при лечении самых различных заболеваний. При этом проницаемость клеток кожи увеличивается. Во многих случаях, как побочный эффект, наблюдается уменьшение болевых ощущений, ослабление чувства тревоги и усталости.
