
- •Предисловие
- •Химическая термодинамика, как теоретическая основа биоэнергетики Предмет, методы и основные понятия химической термодинамики
- •Термодинамические системы: изолированные, закрытые, открытые, гомогенные, гетерогенные
- •Термодинамические параметры
- •Внутренняя энергия системы
- •Форма обмена энергии с окружающей средой
- •Первое начало термодинамики. Тепловые эффекты химических реакций
- •1. В изолированной системе сумма всех видов энергии есть величина постоянная.
- •Изобарный и изохорный процессы. Энтальпия. Тепловые эффекты химических реакций
- •Термохимия. Закон Гесса
- •Влияние температуры и давления на тепловой эффект реакции
- •Использование закона Гесса в биохимических исследованиях
- •Энтропия. Второй закон термодинамики Энтропия
- •Второе начало термодинамики. Свободная энергия Гиббса
- •Принцип энергетического сопряжения
- •Химическое равновесие Обратимые и необратимые реакции. Константа равновесия
- •Смещение химического равновесия. Принцип Ле-Шателье
- •Учение о растворах Растворы
- •Физические свойства н2о и строение ее молекул
- •Механизм образования растворов
- •Растворимость веществ. Факторы, влияющие на растворимость
- •Влияние природы веществ на растворимость
- •Влияние давления на растворимость веществ
- •Влияние температуры на растворимость веществ
- •Влияние электролитов на растворимость веществ
- •Взаимная растворимость жидкостей
- •Способы выражения состава растворов
- •Термодинамические аспекты процесса растворения. Идеальные растворы
- •Коллигативные свойства разбавленных растворов
- •Диффузия и осмос в растворах
- •Роль осмоса в биологических процессах
- •Давление насыщенного пара растворителя над раствором. Закон Рауля
- •Следствия из закона Рауля
- •1) Растворы кипят при более высокой температуре, чем чистый растворитель;
- •2) Растворы замерзают при более низкой температуре, чем чистый растворитель.
- •Применение методов криоскопии и эбуллиоскопии
- •Коллигативные свойства растворов электролитов. Изотонический коэффициент Вант-Гоффа
- •Электролитическая диссоциация Электролиты и неэлектролиты. Теория электролитической диссоциации
- •Общая характеристика электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Диссоциация воды. Водородный показатель
- •Теория кислот и оснований. Буферные растворы Теория кислот и оснований
- •Буферные растворы Определение буферных систем и их классификация
- •Механизм действия буферных систем
- •Вычисление рН и рОн буферных систем. Уравнение Гендерсона-Гассельбаха
- •Буферная емкость
- •Буферные системы человеческого организма
- •Нарушения кислотно-оснóвного равновесия крови. Ацидоз. Алкалоз
- •Химическая кинетика и катализ Кинетика химических реакций
- •Понятие о скорости химической реакции. Закон действующих масс
- •Кинетическая классификация химических реакций. Понятие о молекулярности и порядке химической реакции Порядок и молекулярность простых химических реакций
- •Понятие о сложных химических реакциях
- •Классификация сложных реакций
- •Измерение скорости химической реакции
- •Влияние температуры на скорость химической реакции
- •Катализ Общие положения и закономерности катализа
- •Механизм гомогенного и гетерогенного катализа
- •Особенности каталитической активности ферментов
- •2. Другим важным отличием ферментов от катализаторов небелковой природы является их высокая специфичность, т.Е. Избирательность действия.
- •Физическая химия дисперсных систем Определение дисперсных систем
- •Классификация дисперсных систем и их общая характеристика
- •Классификация дисперсных систем по агрегатному состоянию вещества дисперсной фазы и дисперсионной среды
- •Классификация по взаимодействию между частицами дисперсной фазы или степени структурированности системы
- •Классификация по характеру взаимодействия дисперсной фазы с дисперсионной средой
- •Методы получения дисперсных систем
- •Диспергирование жидкостей
- •Диспергирование газов
- •Конденсационные методы
- •Методы физической конденсации
- •Методы химической конденсации
- •Очистка золей
- •Компенсационный диализ и вивидиализ
- •Молекулярно-кинетические свойства золей
- •Броуновское движение
- •Диффузия
- •Седиментация в золях
- •Осмотическое давление в золях
- •Оптические свойства золей
- •Рассеяние света (опалесценция)
- •Оптические методы исследования коллоидных систем Ультрамикроскоп
- •Механизм образования и строение коллоидной частицы – мицеллы
- •1. Получение золя берлинской лазури:
- •2. Получение с помощью гидролиза FeCl3 золя гидроксида железа (III).
- •3. Получение золя As2s3:
- •Электрокинетические свойства золей
- •Устойчивость гидрофобных коллоидных систем. Коагуляция золей Виды устойчивости золей
- •Теория коагуляции Дерягина-Ландау-Фервея-Овербека
- •Влияние электролитов на устойчивость золей. Порог коагуляции. Правило Шульца-Гарди
- •Чередование зон коагуляции
- •Коагуляции золей смесями электролитов
- •Скорость коагуляции
- •Коллоидная защита
- •Роль процессов коагуляции в промышленности, медицине, биологии
- •Растворы высокомолекулярных соединений
- •Общая характеристика высокомолекулярных соединений
- •Классификация полимеров
- •Набухание и растворение вмс
- •Термодинамические аспекты процесса набухания
- •Давление набухания
- •Свойства растворов высокомолекулярных соединений
- •Осмотическое давление растворов вмс
- •Онкотическое давление крови
- •Вязкость растворов полимеров
- •Свободная и связанная вода в растворах
- •Полиэлектролиты
- •Факторы, влияющие на устойчивость растворов полимеров. Высаливание
- •Электрохимия растворы электролитов как проводники второго рода. Электропроводность растворов электролитов
- •Эквивалентная электропроводность растворов
- •Практическое применение электропроводности
- •Равновесные электродные процессы
- •Металлический электрод
- •Измерение электродных потенциалов
- •Окислительно-восстановительные электроды
- •1. Переход окисленной формы в восстановленную и наоборот заключается только в обмене между ними электронами:
- •Диффузионный и мембранный потенциалы
- •Химические источники электрического тока. Гальванические элементы
- •Потенциометрия
- •Содержание
Измерение скорости химической реакции
Для экспериментального определения скорости химической реакции необходимо иметь данные об изменении концентрации исходных или конечных веществ во времени. Методы, с помощью которых это можно сделать, подразделяются на химические и физико-химические.
Химические методы основаны на непосредственном определении количества вещества или его концентрации в реакционном сосуде.
Чаще всего для этих целей используют такие виды количественного анализа, как титриметрия и гравиметрия. Если реакция протекает медленно, то для контроля за расходованием реагентов через определённые промежутки времени из реакционной среды осуществляют отбор пробы. Затем определяют в них содержание нужного вещества. Например, титрованием щёлочью определяют количество кислоты в системе по мере протекания реакции
R1 – COOH + R2 – OH → R1 – COO – R2 + H2O
Если реакция протекает с большой скоростью, то для отбора пробы её останавливают с помощью резкого охлаждения, быстрого удаления катализатора, разбавления либо перевода одного из реагентов в нереакционное состояние.
Химические методы анализа отличает простота, доступность и хорошая точность.
В современной экспериментальной кинетике чаще всего используют физико-химические методы анализа. Они позволяют контролировать изменение концентрации вещества непосредственно в ходе протекания реакции, не останавливая её и не делая отбора пробы. Эти методы основаны на измерении какого-либо физического свойства системы, меняющегося во времени и зависящего от количественного содержания в ней определённого соединения; например: давления (если в реакции участвуют газы), электропроводности, показателя преломления, спектра поглощения реагента или продукта реакции в ультрафиолетовой, видимой либо инфракрасной областях. Широко используются спектры электронного парамагнитного резонанса (ЭПР) и ядерного магнитного резонанса (ЯМР).
Применение спектральных методов основано на том, что поглощение электромагнитного излучения пропорционально количеству вещества или его концентрации в системе.
Обычно экспериментально изучают реакции в замкнутой системе (т.е. при постоянном объёме) и представляют результаты графически в виде так называемой кинетической кривой, выражающей зависимость концентрации реагента или продукта реакции от времени t. Аналитический вид этой зависимости называется уравнением кинетической кривой. В отличие от основного кинетического уравнения, уравнения кривых расходования реагирующих веществ (или накопления продуктов реакции) содержат в качестве параметров начальные концентрации компонентов (С0) в момент времени t=0.
Из этих уравнений выводят формулы для расчёта константы скорости реакции и времени полупревращения (t½) – промежутка времени, в течение которого расходуется половина взятого исходного вещества, т.е. его концентрация уменьшится в 2 раза и станет равной Со/2.
В реакциях нулевого порядка концентрация исходного вещества линейно уменьшается со временем (рис. 37)
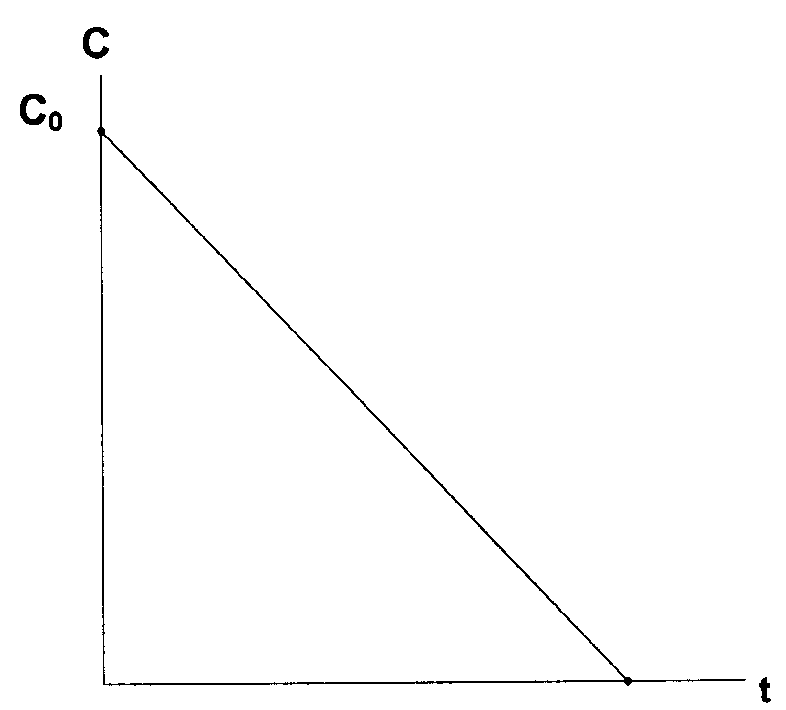
Рис. 37. Изменение концентрации исходного вещества от времени в реакции нулевого порядка
Математически данная линейная зависимость запишется следующим образом
С = С0 – kt
где k – константа скорости, С0 – начальная молярная концентрация реагента, С – концентрация в момент времени t.
Из неё можно вывести формулу для расчёта константы скорости химической реакции нулевого порядка.
k
=
![]() (C0
– C).
(C0
– C).
Константа скорости нулевого порядка измеряется в моль/л ∙ с (моль · л-1· с-1).
Время полупревращения для реакции нулевого порядка пропорционально концентрации исходного вещества
t½
=
![]()
Для реакций первого порядка кинетическая кривая в координатах С, t носит экспоненциальный характер и выглядит следующим образом (рис. 38) Математически данная кривая описывается следующим уравнением
С = С0e-kt

Рис. 38. Изменение концентрации исходного вещества от времени в реакции первого порядка
На практике для реакций первого порядка кинетическую кривую чаще всего строят в координатах ℓnC, t. В этом случае наблюдается линейная зависимость ℓnС от времени (рис. 39)
ℓn С = ℓnС0 – kt
ℓn
С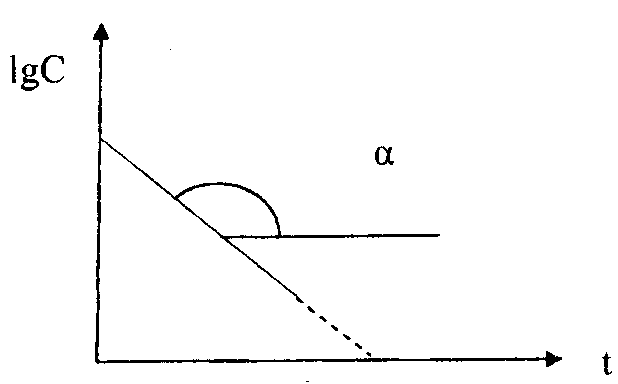
Рис. 39. Зависимость логарифма концентрации реагента от времени протекания для реакции первого порядка
Соответственно, величину константы скорости и время полупревращения можно рассчитать по следующим формулам
k
=
ℓn
![]() или k = 2,303
ℓg
или k = 2,303
ℓg
(при переходе от десятичного логарифма к натуральному).
t½
=
![]()
Константа скорости реакции первого порядка имеет размерность t –1 , т.е. 1/с и не зависит от единиц измерения концентрации. Она показывает долю, которую составляют молекулы, вступившие в реакцию за единицу времени, от общего числа молекул реагента в системе. Таким образом, в реакциях первого порядка за одинаковые промежутки времени расходуются одинаковы доли взятого количества исходного вещества.
Второй отличительной особенностью реакций первого порядка является то, что t½ для них не зависит от начальной концентрации реагента, а определяется только константой скорости.
Вид уравнения зависимости концентрации от времени для реакций второго порядка рассмотрим только для простейшего случая, когда в элементарном акте участвуют 2 одинаковые молекулы, или молекулы разных веществ, но начальные концентрации их (С0) равны. При этом линейная зависимость наблюдается в координатах 1/С, t (рис. 40). Математическое уравнение этой зависимости запишется следующим образом
![]() =
=
![]() + kt
+ kt
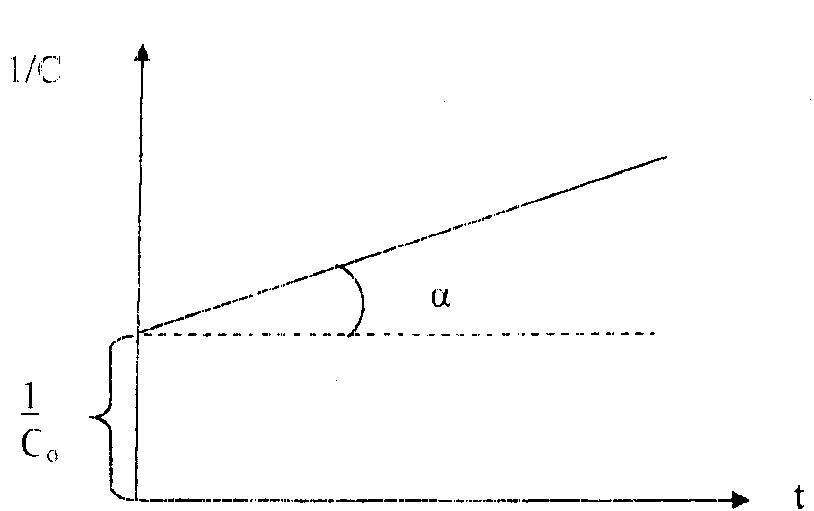
Рис. 40. Зависимость величины обратной концентрации реагента от времени для реакции второго порядка
Константа скорости вычисляется по формуле
k = ( – )
и измеряется в л∙с-1∙моль-1, т.е. ее численное значение зависит от того, в каких единицах измеряется концентрация вещества.
Период полупревращения реакций второго порядка обратно пропорционален начальной концентрации реагента
t½=
![]()
Это связано с тем, что скорость реакций второго порядка в сильной мере зависит от числа столкновений между молекулами реагирующих веществ в единицу времени, которое, в свою очередь, пропорционально числу молекул в единице объема, т.е. концентрации вещества. Таким образом, чем больше концентрация вещества в системе, тем чаще сталкиваются молекулы между собой и тем за меньший промежуток времени половина их успеет прореагировать.
Реакции третьего порядка, как уже было сказано ранее, встречаются крайне редко и не представляют практического интереса. Поэтому в связи с этим мы их не будем рассматривать.
