
- •Предисловие
- •Химическая термодинамика, как теоретическая основа биоэнергетики Предмет, методы и основные понятия химической термодинамики
- •Термодинамические системы: изолированные, закрытые, открытые, гомогенные, гетерогенные
- •Термодинамические параметры
- •Внутренняя энергия системы
- •Форма обмена энергии с окружающей средой
- •Первое начало термодинамики. Тепловые эффекты химических реакций
- •1. В изолированной системе сумма всех видов энергии есть величина постоянная.
- •Изобарный и изохорный процессы. Энтальпия. Тепловые эффекты химических реакций
- •Термохимия. Закон Гесса
- •Влияние температуры и давления на тепловой эффект реакции
- •Использование закона Гесса в биохимических исследованиях
- •Энтропия. Второй закон термодинамики Энтропия
- •Второе начало термодинамики. Свободная энергия Гиббса
- •Принцип энергетического сопряжения
- •Химическое равновесие Обратимые и необратимые реакции. Константа равновесия
- •Смещение химического равновесия. Принцип Ле-Шателье
- •Учение о растворах Растворы
- •Физические свойства н2о и строение ее молекул
- •Механизм образования растворов
- •Растворимость веществ. Факторы, влияющие на растворимость
- •Влияние природы веществ на растворимость
- •Влияние давления на растворимость веществ
- •Влияние температуры на растворимость веществ
- •Влияние электролитов на растворимость веществ
- •Взаимная растворимость жидкостей
- •Способы выражения состава растворов
- •Термодинамические аспекты процесса растворения. Идеальные растворы
- •Коллигативные свойства разбавленных растворов
- •Диффузия и осмос в растворах
- •Роль осмоса в биологических процессах
- •Давление насыщенного пара растворителя над раствором. Закон Рауля
- •Следствия из закона Рауля
- •1) Растворы кипят при более высокой температуре, чем чистый растворитель;
- •2) Растворы замерзают при более низкой температуре, чем чистый растворитель.
- •Применение методов криоскопии и эбуллиоскопии
- •Коллигативные свойства растворов электролитов. Изотонический коэффициент Вант-Гоффа
- •Электролитическая диссоциация Электролиты и неэлектролиты. Теория электролитической диссоциации
- •Общая характеристика электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Диссоциация воды. Водородный показатель
- •Теория кислот и оснований. Буферные растворы Теория кислот и оснований
- •Буферные растворы Определение буферных систем и их классификация
- •Механизм действия буферных систем
- •Вычисление рН и рОн буферных систем. Уравнение Гендерсона-Гассельбаха
- •Буферная емкость
- •Буферные системы человеческого организма
- •Нарушения кислотно-оснóвного равновесия крови. Ацидоз. Алкалоз
- •Химическая кинетика и катализ Кинетика химических реакций
- •Понятие о скорости химической реакции. Закон действующих масс
- •Кинетическая классификация химических реакций. Понятие о молекулярности и порядке химической реакции Порядок и молекулярность простых химических реакций
- •Понятие о сложных химических реакциях
- •Классификация сложных реакций
- •Измерение скорости химической реакции
- •Влияние температуры на скорость химической реакции
- •Катализ Общие положения и закономерности катализа
- •Механизм гомогенного и гетерогенного катализа
- •Особенности каталитической активности ферментов
- •2. Другим важным отличием ферментов от катализаторов небелковой природы является их высокая специфичность, т.Е. Избирательность действия.
- •Физическая химия дисперсных систем Определение дисперсных систем
- •Классификация дисперсных систем и их общая характеристика
- •Классификация дисперсных систем по агрегатному состоянию вещества дисперсной фазы и дисперсионной среды
- •Классификация по взаимодействию между частицами дисперсной фазы или степени структурированности системы
- •Классификация по характеру взаимодействия дисперсной фазы с дисперсионной средой
- •Методы получения дисперсных систем
- •Диспергирование жидкостей
- •Диспергирование газов
- •Конденсационные методы
- •Методы физической конденсации
- •Методы химической конденсации
- •Очистка золей
- •Компенсационный диализ и вивидиализ
- •Молекулярно-кинетические свойства золей
- •Броуновское движение
- •Диффузия
- •Седиментация в золях
- •Осмотическое давление в золях
- •Оптические свойства золей
- •Рассеяние света (опалесценция)
- •Оптические методы исследования коллоидных систем Ультрамикроскоп
- •Механизм образования и строение коллоидной частицы – мицеллы
- •1. Получение золя берлинской лазури:
- •2. Получение с помощью гидролиза FeCl3 золя гидроксида железа (III).
- •3. Получение золя As2s3:
- •Электрокинетические свойства золей
- •Устойчивость гидрофобных коллоидных систем. Коагуляция золей Виды устойчивости золей
- •Теория коагуляции Дерягина-Ландау-Фервея-Овербека
- •Влияние электролитов на устойчивость золей. Порог коагуляции. Правило Шульца-Гарди
- •Чередование зон коагуляции
- •Коагуляции золей смесями электролитов
- •Скорость коагуляции
- •Коллоидная защита
- •Роль процессов коагуляции в промышленности, медицине, биологии
- •Растворы высокомолекулярных соединений
- •Общая характеристика высокомолекулярных соединений
- •Классификация полимеров
- •Набухание и растворение вмс
- •Термодинамические аспекты процесса набухания
- •Давление набухания
- •Свойства растворов высокомолекулярных соединений
- •Осмотическое давление растворов вмс
- •Онкотическое давление крови
- •Вязкость растворов полимеров
- •Свободная и связанная вода в растворах
- •Полиэлектролиты
- •Факторы, влияющие на устойчивость растворов полимеров. Высаливание
- •Электрохимия растворы электролитов как проводники второго рода. Электропроводность растворов электролитов
- •Эквивалентная электропроводность растворов
- •Практическое применение электропроводности
- •Равновесные электродные процессы
- •Металлический электрод
- •Измерение электродных потенциалов
- •Окислительно-восстановительные электроды
- •1. Переход окисленной формы в восстановленную и наоборот заключается только в обмене между ними электронами:
- •Диффузионный и мембранный потенциалы
- •Химические источники электрического тока. Гальванические элементы
- •Потенциометрия
- •Содержание
Физические свойства н2о и строение ее молекул
При комнатных условиях чистая вода – жидкость без запаха и вкуса. Температура кипения Н2О (при р=101,325 кПа) равна 100оС, температура замерзания 0оС. В тонком слое вода бесцветна, однако при толщине более двух метров приобретает голубоватый оттенок. Вода является хорошим растворителем для многих веществ, поэтому чистой Н2О в природе нет. Она всегда содержит многочисленные примеси растворенных веществ. Для очистки от них воду доводят до кипения, а образовавшиеся при этом водяные пары путем охлаждения вновь конденсируют в жидкость. Этот процесс называют «перегонкой», а получившуюся Н2О – дистиллированной водой.
Молекулы Н2О состоят из двух атомов водорода Н и одного атома кислорода О, соединенных между собой ковалентными полярными связями. На атоме О, как на более электроотрицательном, сосредоточен частичный отрицательный заряд |δ–| < 1, а на атомах Н – частичный положительный заряд |δ+| < 1. Молекула Н2О имеет угловую форму. Атомы водорода, связанные одинарными δ-связями с атомами кислорода, образуют угол, равный 104,5о (рис. 16). Он несколько отличается от тетраэдрического (109о28′), хотя атом О в молекуле Н2О находится в состоянии sp3-гибридизации. Отклонение угла связи от тетраэдрического связано с взаимным отталкиванием двух неподеленных электронных пар, находящихся на гибридных орбиталях атома кислорода.
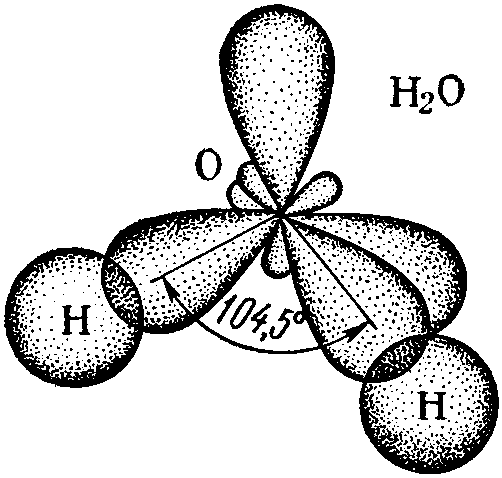
Рис. 16. Схема образования молекулы Н2О
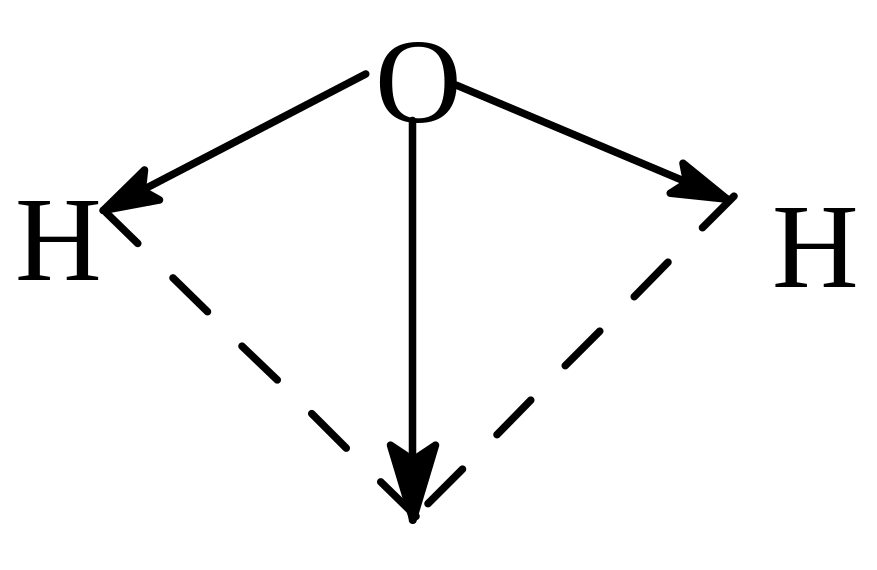
Вследствие своего строения молекула Н2О обладает значительным дипольным моментом (рис. 17) и является сильнополярной. В связи с этим вода имеет большую диэлектрическую проницаемость и в ее среде значительно уменьшаются (приблизительно в 80 раз) кулоновские силы взаимодействия между электрическими зарядами. Это приводит к тому, что прочность связей в ионной кристаллической решетке, а также между полярными молекулами твердых и жидких веществ и между атомами в самих этих молекулах тоже понижается ≈ в 80 раз.
-
![]() ≠ 0
≠ 0
Рис. 17. Дипольный момент молекулы Н2О
Благодаря этому свойству, вода хорошо растворяет вещества, образованные ионными и ковалентными полярными связями, вызывая при этом электролитическую диссоциацию электролитов и реакции гидролитического разложения веществ.
Вода по сравнению с другими водородными соединениями элементов IVA – VIIA групп (HCl, H2S, CH4, HF, NH3) имеет аномально высокие температуры кипения и плавления, обладает высокой теплоемкостью и удельной теплотой испарения.
Эти свойства воды объясняются способностью ее молекул образовывать друг с другом прочные водородные связи. Причем одна молекула Н2О может образовать водородные связи с четырьмя другими молекулами воды. Это создает возможность построения сложной трехмерной пространственной структуры из ассоциированных молекул Н2О, в которой имеется много пустот. Благодаря этому плотность льда меньше плотности жидкой воды, т.к. в последнем случае вследствие теплового движения происходит частичное разрушение водородных связей и образовавшиеся свободные молекулы воды могут заполнять имеющиеся полости, увеличивая тем самым плотность жидкости.
Водородные связи молекулы Н2О могут образовывать не только между собой, но и с полярными функциональными группами органических веществ: спиртов, аминов, карбоновых кислот, различных гетеро- и полифункциональных соединений, способствуя тем самым их растворению.
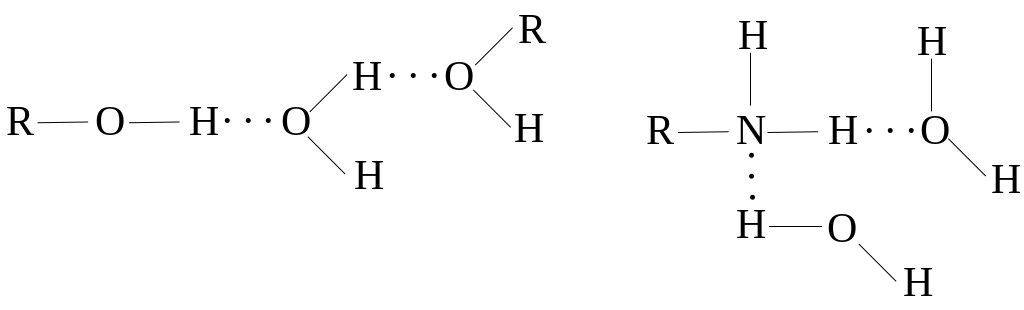
Таким образом, вода является универсальным растворителем и способна растворять в себе как многочисленные неорганические, так и органические соединения.
