
- •Предисловие
- •Химическая термодинамика, как теоретическая основа биоэнергетики Предмет, методы и основные понятия химической термодинамики
- •Термодинамические системы: изолированные, закрытые, открытые, гомогенные, гетерогенные
- •Термодинамические параметры
- •Внутренняя энергия системы
- •Форма обмена энергии с окружающей средой
- •Первое начало термодинамики. Тепловые эффекты химических реакций
- •1. В изолированной системе сумма всех видов энергии есть величина постоянная.
- •Изобарный и изохорный процессы. Энтальпия. Тепловые эффекты химических реакций
- •Термохимия. Закон Гесса
- •Влияние температуры и давления на тепловой эффект реакции
- •Использование закона Гесса в биохимических исследованиях
- •Энтропия. Второй закон термодинамики Энтропия
- •Второе начало термодинамики. Свободная энергия Гиббса
- •Принцип энергетического сопряжения
- •Химическое равновесие Обратимые и необратимые реакции. Константа равновесия
- •Смещение химического равновесия. Принцип Ле-Шателье
- •Учение о растворах Растворы
- •Физические свойства н2о и строение ее молекул
- •Механизм образования растворов
- •Растворимость веществ. Факторы, влияющие на растворимость
- •Влияние природы веществ на растворимость
- •Влияние давления на растворимость веществ
- •Влияние температуры на растворимость веществ
- •Влияние электролитов на растворимость веществ
- •Взаимная растворимость жидкостей
- •Способы выражения состава растворов
- •Термодинамические аспекты процесса растворения. Идеальные растворы
- •Коллигативные свойства разбавленных растворов
- •Диффузия и осмос в растворах
- •Роль осмоса в биологических процессах
- •Давление насыщенного пара растворителя над раствором. Закон Рауля
- •Следствия из закона Рауля
- •1) Растворы кипят при более высокой температуре, чем чистый растворитель;
- •2) Растворы замерзают при более низкой температуре, чем чистый растворитель.
- •Применение методов криоскопии и эбуллиоскопии
- •Коллигативные свойства растворов электролитов. Изотонический коэффициент Вант-Гоффа
- •Электролитическая диссоциация Электролиты и неэлектролиты. Теория электролитической диссоциации
- •Общая характеристика электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Диссоциация воды. Водородный показатель
- •Теория кислот и оснований. Буферные растворы Теория кислот и оснований
- •Буферные растворы Определение буферных систем и их классификация
- •Механизм действия буферных систем
- •Вычисление рН и рОн буферных систем. Уравнение Гендерсона-Гассельбаха
- •Буферная емкость
- •Буферные системы человеческого организма
- •Нарушения кислотно-оснóвного равновесия крови. Ацидоз. Алкалоз
- •Химическая кинетика и катализ Кинетика химических реакций
- •Понятие о скорости химической реакции. Закон действующих масс
- •Кинетическая классификация химических реакций. Понятие о молекулярности и порядке химической реакции Порядок и молекулярность простых химических реакций
- •Понятие о сложных химических реакциях
- •Классификация сложных реакций
- •Измерение скорости химической реакции
- •Влияние температуры на скорость химической реакции
- •Катализ Общие положения и закономерности катализа
- •Механизм гомогенного и гетерогенного катализа
- •Особенности каталитической активности ферментов
- •2. Другим важным отличием ферментов от катализаторов небелковой природы является их высокая специфичность, т.Е. Избирательность действия.
- •Физическая химия дисперсных систем Определение дисперсных систем
- •Классификация дисперсных систем и их общая характеристика
- •Классификация дисперсных систем по агрегатному состоянию вещества дисперсной фазы и дисперсионной среды
- •Классификация по взаимодействию между частицами дисперсной фазы или степени структурированности системы
- •Классификация по характеру взаимодействия дисперсной фазы с дисперсионной средой
- •Методы получения дисперсных систем
- •Диспергирование жидкостей
- •Диспергирование газов
- •Конденсационные методы
- •Методы физической конденсации
- •Методы химической конденсации
- •Очистка золей
- •Компенсационный диализ и вивидиализ
- •Молекулярно-кинетические свойства золей
- •Броуновское движение
- •Диффузия
- •Седиментация в золях
- •Осмотическое давление в золях
- •Оптические свойства золей
- •Рассеяние света (опалесценция)
- •Оптические методы исследования коллоидных систем Ультрамикроскоп
- •Механизм образования и строение коллоидной частицы – мицеллы
- •1. Получение золя берлинской лазури:
- •2. Получение с помощью гидролиза FeCl3 золя гидроксида железа (III).
- •3. Получение золя As2s3:
- •Электрокинетические свойства золей
- •Устойчивость гидрофобных коллоидных систем. Коагуляция золей Виды устойчивости золей
- •Теория коагуляции Дерягина-Ландау-Фервея-Овербека
- •Влияние электролитов на устойчивость золей. Порог коагуляции. Правило Шульца-Гарди
- •Чередование зон коагуляции
- •Коагуляции золей смесями электролитов
- •Скорость коагуляции
- •Коллоидная защита
- •Роль процессов коагуляции в промышленности, медицине, биологии
- •Растворы высокомолекулярных соединений
- •Общая характеристика высокомолекулярных соединений
- •Классификация полимеров
- •Набухание и растворение вмс
- •Термодинамические аспекты процесса набухания
- •Давление набухания
- •Свойства растворов высокомолекулярных соединений
- •Осмотическое давление растворов вмс
- •Онкотическое давление крови
- •Вязкость растворов полимеров
- •Свободная и связанная вода в растворах
- •Полиэлектролиты
- •Факторы, влияющие на устойчивость растворов полимеров. Высаливание
- •Электрохимия растворы электролитов как проводники второго рода. Электропроводность растворов электролитов
- •Эквивалентная электропроводность растворов
- •Практическое применение электропроводности
- •Равновесные электродные процессы
- •Металлический электрод
- •Измерение электродных потенциалов
- •Окислительно-восстановительные электроды
- •1. Переход окисленной формы в восстановленную и наоборот заключается только в обмене между ними электронами:
- •Диффузионный и мембранный потенциалы
- •Химические источники электрического тока. Гальванические элементы
- •Потенциометрия
- •Содержание
Факторы, влияющие на устойчивость растворов полимеров. Высаливание
Истинные растворы полимеров, как и растворы низкомолекулярных соединений, являются агрегативно устойчивыми и в отличие от золей могут существовать длительное время без добавок стабилизаторов. Нарушить устойчивость растворов полимеров можно путем уменьшения их растворимости. Это можно сделать за счет уменьшения температуры или добавления большого количества другого растворителя (неограниченно смешивающегося с первым), по отношению к которому высокомолекулярное соединение обладает плохим сродством. Для водных растворов белков такими растворителями являются, например, этиловый спирт или ацетон.
очень часто для высаждения полимеров из водных растворов используют электролиты. Протекающий при этом процесс называется высаливанием (т.к. чаще всего в качестве электролитов используют соли). Внешне он напоминает коагуляцию электролитами золя, но отличается от нее по механизму действия.
Во-первых, если коагуляция золей протекает уже при добавлении небольшого количества электролита, то для выделения из раствора полимера требуются в сотни раз большие концентрации электролитов.
Во-вторых, при высаливании полимеров из водных растворов основное значение имеет не только заряд ионов электролита и их размер, как при коагуляции золя, а, в первую очередь, способность иона к гидратации. При этом наблюдается неподчинение правилу Шульца-Гарди. Кроме того, высаливающее действие оказывает весь электролит, а не только какие-то его определенные ионы.
В-третьих, высаливание в отличие от коагуляции является обратимым процессом. После удаления электролита образовавшийся осадок снова легко растворяется в чистом растворителе.
В основе высаливания полимера лежит процесс дегидратации. Ионы электролита связывают в гидратные оболочки сперва имеющуюся в растворе свободную воду, а затем начинают отрывать от макромолекул связанную воду. В результате этих процессов молекулы полимеров объединяются друг с другом в кинетически неустойчивые ассоциаты, которые за счет действия силы тяжести оседают на дно раствора.
При высаждении белков их обычно до либо после добавления электролита переводят в изоэлектрическое состояние.
Высаливание из водных растворов можно проводить не только электролитами, но и органическими веществами, способными лучше гидратироваться водой чем макромолекулы полимера.
Чем выше степень гидратации ионов электролита и прочнее его гидратные оболочки, тем меньшее количество его потребуется для высаждения полимера из раствора.
Высаливание ВМС имеет большое практическое значение. Его применяют для фракционирования белков, полисахаридов и других полимеров.
В процессе добавления электролита растворимость полимера изменяется неравномерно. В первую очередь в осадок выпадают наиболее длинные его макромолекулы, имеющие максимальную массу молекулы полимера с наименьшей молярной массой высаждаются последними, после прибавления гораздо больших порций электролита.
Электрохимия растворы электролитов как проводники второго рода. Электропроводность растворов электролитов
В зависимости от способности проводить электрический ток все вещества делятся на 3 основных типа: проводники, полупроводники и диэлектрики.
Вещества первого типа могут проводить электрический ток при наложении на них внешнего электрического поля, последнего – нет. Полупроводники занимают промежуточное положение между проводниками и диэлектриками.
Под прохождением электрического тока через вещество подразумевают направленное движение (перенос) электрических зарядов. В зависимости от природы их носителя различают проводники первого рода и проводники второго рода.
В проводниках первого рода перенос электрического заряда осуществляется за счет направленного движения электронов. К ним относятся главным образом сплавы металлов, металлы и их расплавы.
В проводниках второго рода перенос электрического заряда осуществляется за счет направленного движения ионов. К ним относятся все электролиты. Причем в большинстве случаев используются растворы или расплавы данных соединений, так как именно в таких системах за счет действия растворителя или высокой температуры образуются в достаточных количествах свободные ионы, способные перемещаться под действием внешнего электрического поля.
Способность вещества проводить электрический ток количественно характеризуется электропроводностью L, которую можно предсказать как величину, обратную сопротивлению проводника R:
![]()
Единицей измерения электропроводности в системе СИ является Сименс (См) или Ом–1.
Электропроводность представляет собой суммарный электрический заряд, проходящий через вещество за единицу времени, при приложении к нему разности потенциалов в 1 В.
Как и для обычных металлических проводников, сопротивление растворов рассчитывается по формуле:
![]()
где – удельное сопротивление, зависящее от природы раствора и его температуры; l – длина проводника (в случае раствора в её роли выступает расстояние между опущенными в него электродами); S – площадь поперечного сечения проводника (для растворов в его роли выступает площадь поверхности электродов).
Величина, обратная , называется удельной электропроводностью ϰ (греческая буква «каппа»):
ϰ
![]()
Удельная электропроводность характеризует электропроводность объема раствора, заключенного между двумя параллельными электродами, имеющими площадь поверхности 1 м2 каждый и расположенными на расстоянии 1 м друг от друга.
Удельная электропроводность растворов в системе СИ измеряется в См ∙ м–1 или в Ом–1 ∙ м–1.
Удельная электропроводность чистой дистиллированной воды при 291 K равна 5 ∙ 10–9 См ∙ м–1. Т.е., если мы опустим в эту воду два электрода площадью 1 м2 каждый, то при расстоянии между ними 1 м и разности потенциалов в 1 В сила тока будет равна 5 ∙ 10–9 А. Такое маленькое значение удельной электропроводности воды объясняется слабой диссоциацией ее молекул
Н2О Н+ + ОН–
и низкой концентрацией положительно (Н+) и отрицательно (ОН–) заряженных ионов.
Удельная электропроводность растворов электролитов значительно выше и зависит от общего числа ионов в единице их объема, а значит и от концентрации самого электролита (табл. 18) и его степени диссоциации (если электролит слабый).
Таблица 18. Удельная электропроводность растворов некоторых электролитов в зависимости от их концентрации при 291 K, См ∙ м–1
Концентрация раствора, % |
KCl |
NaOH |
H2SO4 |
NaCl |
5 |
6,9 |
13,0 |
21,0 |
6,7 |
10 |
14,0 |
19,0 |
39,0 |
12,0 |
15 |
20,0 |
– |
54,0 |
16,0 |
Причем с увеличением концентрации как сильных, так и слабых электролитов удельная электропроводность раствора увеличивается до некоторого определенного предела, а затем уменьшается (рис. 81).
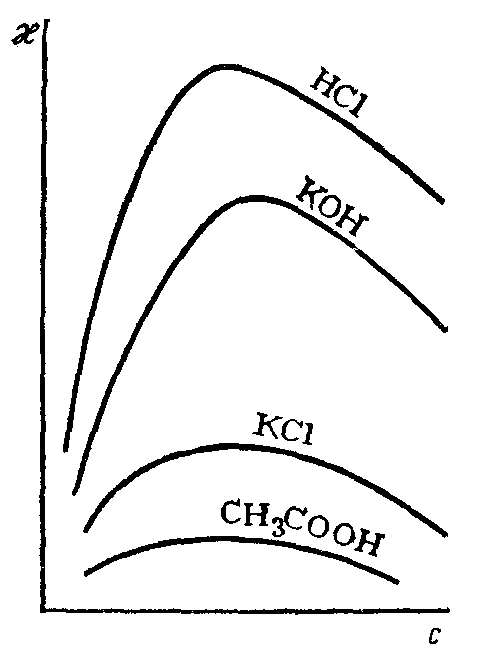
Рис. 81. Зависимость удельной электропроводности растворов от их концентрации
В разбавленных растворах сильных электролитов первоначальный рост электрической проводимости с повышением их концентрации обусловлен увеличением числа ионов. Однако в области концентрированных растворов одновременно с ростом количества ионов увеличиваются и силы электростатического притяжения между ними, интенсифицируется процесс образования ионных атмосфер и ассоциатов (ионных двойников, тройников и т.д.), и как следствие, уменьшается скорость движения ионов во внешнем электрическом поле. Все эти факторы и приводят в конечном итоге к снижению электропроводности.
В растворах слабых электролитов (как разбавленных, так и концентрированных) силы электростатического взаимодействия между ионами являются незначительными из-за малой концентрации последних и большого расстояния между ними. Поэтому они не оказывают существенного влияния на электропроводность. Но при повышении концентрации вещества до определенных пределов происходит уменьшение степени диссоциации электролита и, соответственно, концентрации самих ионов.
Удельная электропроводность растворов электролитов (в отличие от металлов) возрастает с повышением температуры (табл. 19). Причин, вызывающих данное явление, может быть несколько.
Таблица 19. Зависимость удельной электропроводности 0,1 М раствора KCl от температуры
T, K |
ϰ ∙ 10–1, См ∙ м–1 |
273 |
7,13 |
283 |
9,32 |
293 |
10,66 |
303 |
14,10 |
Во-первых, это связано с увеличением скорости движения самих ионов из-за уменьшения вязкости среды; во-вторых, с возрастанием степени диссоциации слабых электролитов.
Опытным путем было установлено, что повышение температуры на 1о ведет к возрастанию проводимости раствора на 1,5-2,7% (в зависимости от его концентрации и вида содержащегося в нем электролита).
Удельная электропроводность растворов зависит также от индивидуальных свойств ионов: величины их заряда, радиуса, степени гидратации, скорости движения во внешнем электрическом поле.
В таблице 20 приведены значения абсолютной скорости движения некоторых ионов к соответствующему электроду при приложенной разности потенциалов 1 В/м.
Таблица 20. Абсолютные скорости движения ионов (м/с) в воде при Т = 291 K
Катионы |
Скорость ∙ 10–6, м/с |
Анионы |
Скорость ∙ 10–6, м/с |
H+ |
32,7 |
OH– |
18,7 |
Li+ |
3,5 |
Cl– |
6,85 |
Na+ |
4,6 |
NO3– |
6,40 |
K+ |
6,75 |
I– |
6,95 |
NH4+ |
6,70 |
MnO4– |
5,60 |
Как видно из таблицы 20, скорости перемещения ионов при прохождении через раствор электрического тока достаточно малы по сравнению со скоростями движения молекул в газообразных средах и электронов в металлических проводниках (различаются более чем в миллион раз). Соответственно, и удельная электропроводность растворов примерно во столько же раз меньше по сравнению с металлическими проводниками.
Низкая подвижность ионов в водных растворах объясняется тем, что они окружены гидратными оболочками и при движении испытывают существенное сопротивление со стороны растворителя.
Значительно большей скоростью движения в водной среде, по сравнению с другими ионами, обладают ионы Н+ и ОН–. Это связано с тем, что механизм перемещения данных ионов отличается от механизма перемещения других ионов.
В водных растворах ион водорода находится в виде иона гидроксония Н3О+. В электрическом поле Н+ переходит от иона гидроксония к ближайшей молекуле Н2О. Вновь образовавшийся ион Н3О+ передает свой протон следующей молекуле Н2О (рис. 82а). Аналогично перемещается протон от молекулы воды к гидроксид-иону (рис. 82б).
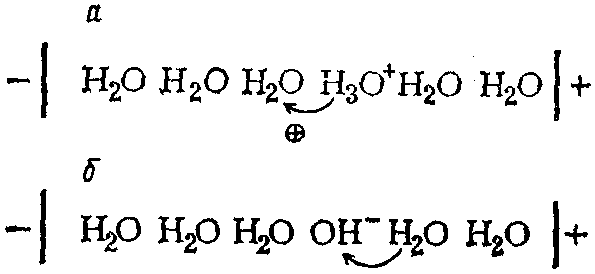
Рис. 82. Схема механизма электропроводимости ионов Н+ (а) и ОН– (б)
В обоих случаях перенос электрического заряда осуществляется не за счет движения самих ионов, а в результате перескока протона от одной частицы к другой. Поскольку протон в молекуле воды связан прочнее, чем в Н3О+, то скорость перемещения гидроксид-иона почти в 2 раза меньше, чем катиона водорода. Такой способ перемещения ионов называется иначе «эстафетным».
Таким образом, на удельную электропроводность растворов оказывают влияние достаточно много самых различных факторов, рассмотренных нами выше. На основе ее определения сложно сделать какие-то обобщающие выводы при сравнивании свойств растворов разных веществ.
В связи с этим ввели понятие об эквивалентной электропроводности.
