
- •Предисловие
- •Химическая термодинамика, как теоретическая основа биоэнергетики Предмет, методы и основные понятия химической термодинамики
- •Термодинамические системы: изолированные, закрытые, открытые, гомогенные, гетерогенные
- •Термодинамические параметры
- •Внутренняя энергия системы
- •Форма обмена энергии с окружающей средой
- •Первое начало термодинамики. Тепловые эффекты химических реакций
- •1. В изолированной системе сумма всех видов энергии есть величина постоянная.
- •Изобарный и изохорный процессы. Энтальпия. Тепловые эффекты химических реакций
- •Термохимия. Закон Гесса
- •Влияние температуры и давления на тепловой эффект реакции
- •Использование закона Гесса в биохимических исследованиях
- •Энтропия. Второй закон термодинамики Энтропия
- •Второе начало термодинамики. Свободная энергия Гиббса
- •Принцип энергетического сопряжения
- •Химическое равновесие Обратимые и необратимые реакции. Константа равновесия
- •Смещение химического равновесия. Принцип Ле-Шателье
- •Учение о растворах Растворы
- •Физические свойства н2о и строение ее молекул
- •Механизм образования растворов
- •Растворимость веществ. Факторы, влияющие на растворимость
- •Влияние природы веществ на растворимость
- •Влияние давления на растворимость веществ
- •Влияние температуры на растворимость веществ
- •Влияние электролитов на растворимость веществ
- •Взаимная растворимость жидкостей
- •Способы выражения состава растворов
- •Термодинамические аспекты процесса растворения. Идеальные растворы
- •Коллигативные свойства разбавленных растворов
- •Диффузия и осмос в растворах
- •Роль осмоса в биологических процессах
- •Давление насыщенного пара растворителя над раствором. Закон Рауля
- •Следствия из закона Рауля
- •1) Растворы кипят при более высокой температуре, чем чистый растворитель;
- •2) Растворы замерзают при более низкой температуре, чем чистый растворитель.
- •Применение методов криоскопии и эбуллиоскопии
- •Коллигативные свойства растворов электролитов. Изотонический коэффициент Вант-Гоффа
- •Электролитическая диссоциация Электролиты и неэлектролиты. Теория электролитической диссоциации
- •Общая характеристика электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Диссоциация воды. Водородный показатель
- •Теория кислот и оснований. Буферные растворы Теория кислот и оснований
- •Буферные растворы Определение буферных систем и их классификация
- •Механизм действия буферных систем
- •Вычисление рН и рОн буферных систем. Уравнение Гендерсона-Гассельбаха
- •Буферная емкость
- •Буферные системы человеческого организма
- •Нарушения кислотно-оснóвного равновесия крови. Ацидоз. Алкалоз
- •Химическая кинетика и катализ Кинетика химических реакций
- •Понятие о скорости химической реакции. Закон действующих масс
- •Кинетическая классификация химических реакций. Понятие о молекулярности и порядке химической реакции Порядок и молекулярность простых химических реакций
- •Понятие о сложных химических реакциях
- •Классификация сложных реакций
- •Измерение скорости химической реакции
- •Влияние температуры на скорость химической реакции
- •Катализ Общие положения и закономерности катализа
- •Механизм гомогенного и гетерогенного катализа
- •Особенности каталитической активности ферментов
- •2. Другим важным отличием ферментов от катализаторов небелковой природы является их высокая специфичность, т.Е. Избирательность действия.
- •Физическая химия дисперсных систем Определение дисперсных систем
- •Классификация дисперсных систем и их общая характеристика
- •Классификация дисперсных систем по агрегатному состоянию вещества дисперсной фазы и дисперсионной среды
- •Классификация по взаимодействию между частицами дисперсной фазы или степени структурированности системы
- •Классификация по характеру взаимодействия дисперсной фазы с дисперсионной средой
- •Методы получения дисперсных систем
- •Диспергирование жидкостей
- •Диспергирование газов
- •Конденсационные методы
- •Методы физической конденсации
- •Методы химической конденсации
- •Очистка золей
- •Компенсационный диализ и вивидиализ
- •Молекулярно-кинетические свойства золей
- •Броуновское движение
- •Диффузия
- •Седиментация в золях
- •Осмотическое давление в золях
- •Оптические свойства золей
- •Рассеяние света (опалесценция)
- •Оптические методы исследования коллоидных систем Ультрамикроскоп
- •Механизм образования и строение коллоидной частицы – мицеллы
- •1. Получение золя берлинской лазури:
- •2. Получение с помощью гидролиза FeCl3 золя гидроксида железа (III).
- •3. Получение золя As2s3:
- •Электрокинетические свойства золей
- •Устойчивость гидрофобных коллоидных систем. Коагуляция золей Виды устойчивости золей
- •Теория коагуляции Дерягина-Ландау-Фервея-Овербека
- •Влияние электролитов на устойчивость золей. Порог коагуляции. Правило Шульца-Гарди
- •Чередование зон коагуляции
- •Коагуляции золей смесями электролитов
- •Скорость коагуляции
- •Коллоидная защита
- •Роль процессов коагуляции в промышленности, медицине, биологии
- •Растворы высокомолекулярных соединений
- •Общая характеристика высокомолекулярных соединений
- •Классификация полимеров
- •Набухание и растворение вмс
- •Термодинамические аспекты процесса набухания
- •Давление набухания
- •Свойства растворов высокомолекулярных соединений
- •Осмотическое давление растворов вмс
- •Онкотическое давление крови
- •Вязкость растворов полимеров
- •Свободная и связанная вода в растворах
- •Полиэлектролиты
- •Факторы, влияющие на устойчивость растворов полимеров. Высаливание
- •Электрохимия растворы электролитов как проводники второго рода. Электропроводность растворов электролитов
- •Эквивалентная электропроводность растворов
- •Практическое применение электропроводности
- •Равновесные электродные процессы
- •Металлический электрод
- •Измерение электродных потенциалов
- •Окислительно-восстановительные электроды
- •1. Переход окисленной формы в восстановленную и наоборот заключается только в обмене между ними электронами:
- •Диффузионный и мембранный потенциалы
- •Химические источники электрического тока. Гальванические элементы
- •Потенциометрия
- •Содержание
Классификация по характеру взаимодействия дисперсной фазы с дисперсионной средой
По характеру взаимодействия между частицами дисперсной фазы и молекулами дисперсионной среды коллоидные и грубодисперсные системы подразделяются на лиофильные (от греческого lyo – растворяю, philia – люблю) и лиофобные (phobia – страх, нелюбовь).
Системы, в которых дисперсионной средой является вода, называются, соответственно, гидрофильными и гидрофобными.
Лиофильные (гидрофильные) системы характеризуются сильно выраженным взаимодействием частиц дисперсной фазы с молекулами дисперсионной среды. Результатом такого взаимодействия является образование на поверхности частиц сольватных оболочек из молекул растворителя, которые препятствуют их слипанию и уменьшают поверхностную энергию. Лиофильные системы термодинамически устойчивы, могут образовываться самопроизвольно и не требуют добавок стабилизаторов. Они немногочисленны и в природе встречаются редко. К ним можно отнести растворы некоторых поверхностно-активных веществ, определенные сорта глин.
На начальном этапе коллоидной химии к лиофильным золям отнесли растворы высокомолекулярных соединений. Однако в дальнейшем было доказано, что данные системы являются молекулярно-дисперсными и гомогенными. Но вследствие того, что макромолекулы полимеров по своим размерам совпадают с коллоидными частицами, их растворы по многим свойствам схожи с золями.
Большинство так называемых классических дисперсных систем являются гидрофобными. Они характеризуются очень слабым взаимодействием частиц дисперсной фазы с молекулами дисперсионной среды, вследствие чего защитная сольватная оболочка на их поверхности не образуется. Такие системы термодинамически неустойчивы, самопроизвольно не получаются, могут существовать лишь непродолжительное время, в связи с чем для увеличения времени жизни требуют специальных методов стабилизации, например, добавок соответствующих веществ.
Методы получения дисперсных систем
Для получения дисперсных систем необходимо решить следующие задачи:
1) в зависимости от поставленной цели подобрать такие компоненты системы, чтобы вещество дисперсной фазы не растворялось самопроизвольно в дисперсионной среде с образованием истинного раствора;
2) довести размеры частиц дисперсной фазы до соответствующей величины;
3) равномерно распределить дисперсные частицы по всему объему раствора, не превышая заданного уровня их концентрации;
4) определенным способом стабилизировать дисперсную систему, чтобы сохранить ее степень дисперсности и свойства в течение достаточно длительного времени (например, ввести добавки специальных веществ – стабилизаторов).
Сложнее всего выполнить вторую задачу. Дисперсные частицы, в том числе и коллоидные, могут быть образованы двумя способами:
1) путем дробления (диспергирования) более крупных образований веществ;
2) путем агрегации (конденсации) молекул и ионов истинных растворов.
В соответствии с этим различают диспергационные и агрегационные (конденсационные) методы получения дисперсных частиц.
Диспергационные методы используют в основном для получения грубодисперсных частиц от 10–6 м и выше. С помощью специальных приспособлений или устройств удается снизить их размеры до 10–7 м, но в промышленных процессах диспергирования обычно получают более крупные частицы.
Для диспергирования твердых тел используют механические, ультразвуковые, химические методы, взрывы.
Эти процессы широко применяют в народном хозяйстве: при производстве цементов, для помола зерна и других продуктов, измельчения угля в энергетике, при изготовлении красок, наполнителей и т.п. Мировое производство порошков для вышеперечисленных целей превышает 1 млрд. т в год.
Механическое измельчение твердых веществ осуществляется в соответствующих установках: дробильных аппаратах, мельницах различного типа и т.п. В них измельчаемый материал подвергается сильным механическим нагрузкам (растяжению, сжатию, ударам), которые приводят к разрушению больших образцов вещества на мелкие частицы (рис. 49).
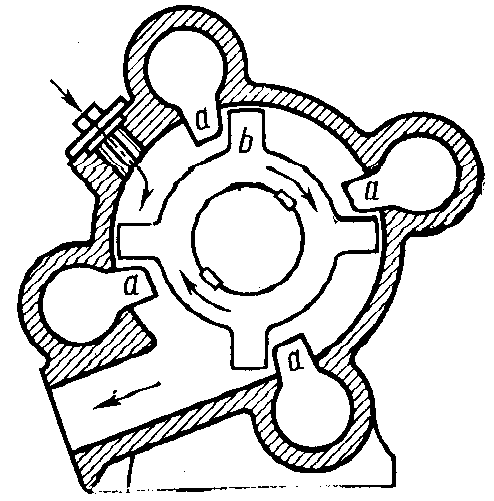
Рис. 49. Схема коллоидной мельницы. Измельчение вещества происходит в зазорах между лопастями ротора b и выступами а внутри корпуса в результате быстрого вращения вала
В случае хрупких материалов, имеющих атомную или ионную кристаллическую решетки (многие минералы, керамика, стекло и т.д.), процесс измельчения идет достаточно эффективно.
Пластичные материалы (металлы) диспергировать гораздо труднее. Механические нагрузки вызывают вначале большую пластическую деформацию и только после этого происходит их разрушение. Поэтому механическое диспергирование таких веществ до достаточно мелких частиц требует особо больших энергетических затрат.
Ультразвуковой метод используют для диспергирования твердых веществ, помещенных в жидкость. Для этих целей воздействуют на систему звуковыми волнами с частотой колебаний более 20 000 Гц. Ультразвук создает резкие чередования сжатия и расширения, в результате чего появляются разрывающие силы, ведущие к раздроблению образца.
Химическое диспергирование или метод пептизации заключается в раздроблении свежеприготовленных рыхлых осадков на отдельные частицы при добавлении к ним растворов электролитов или поверхностно-активных веществ. Данные соединения (их иначе называют пептизаторами, по аналогии с ферментом пепсином, вызывающим гидролиз белковых макромолекул) уменьшают взаимодействие между частицами осадка и облегчают их переход в состояние золя. При этом степень дисперсности вещества фактически не изменяется, т.к. частицы рыхлого осадка уже имеют нужные размеры, но находятся в связанном состоянии за счет сил межмолекулярного взаимодействия и разделены тонкими прослойками из молекул дисперсионной среды.
Слежавшиеся осадки со слипшимися частицами, лишенными прослоек из растворителя, не поддаются диспергированию путем пептизации. Фактически в данном методе происходит не диспергирование, а дезагрегация уже имеющихся частичек.
Пептизация имеет биологическое значение: рассасывание атеросклеротических бляшек в кровеносных сосудах, почечных и печеночных камней, действие антикоагулянтов при тромбофлебитах сводится, в сущности, к явлению пептизации.
