
- •170034, Г. Тверь, пр. Чайковского, д. 9, оф. 504,
- •Список сокращений
- •Характеристика системы гемостаза
- •Морфологические компоненты системы гемостаза:
- •Сосудистая стенка
- •Эндотелий
- •Продукты эндотелиоцитов, участвующие в гемостазе
- •Контроль активности тромбоцитов
- •Тромбомодулин
- •Прокоагулянтная роль эндотелия, регуляция сосудистого тонуса
- •Роль эндотелия в регуляции сосудистого тонуса
- •Сосудистая стенка
- •Тканевой фактор
- •Коллаген
- •Тромбоциты
- •Рецепторы мембраны тромбоцитов
- •Рецепторы для высокомолекулярных белков
- •Интегрины
- •Фактор роста тромбоцитов (pdgf)
- •Фактор XIII
- •Адгезия тромбоцитов
- •Тромбоциты
- •Активация тромбоцитов
- •Агрегация тромбоцитов
- •Ретракция сгустка крови
- •Участие моноцитов в свертывании крови
- •Плазменные белки гемостаза
- •1) Многоступенчатый этап, приводящий к акти вации протромбина и превращению его в ак тивный фермент - тромбин;
- •Роль кофакторов и микроокружения в процессе свертывания крови
- •Роль кальция в гемостатических реакциях
- •Ингибиторы ферментов системы гемостаза
- •Антитромбин и гепарин
- •Протеин s
- •Система фибринолиза
- •Активатор плазминогена тканевого типа
- •Внутренний путь активации фибринолиза
- •Внешний путь активации фибринолиза
- •Ингибиторы тканевого активатора плазминогена (pai)
- •Активируемый тромбином ингибитор фибринолиза (tafi)
- •Другие элементы системы фибринолиза
- •Реологические аспекты гемостаза
- •Функция тромбоцитов в различных гемодинамических условиях
- •Современная теория свертывания крови
- •Особенности физиологии и исследования гемостаза у плодов, новорожденных и детей раннего возраста
- •Тромбоциты
- •О собенности физиологии и исследования гемостаза у женщин при менструации и беременности
- •Клинический пример 1
- •Обеспечение диагностики нарушении гемостаза в
- •Подбор антикоагулянтов
- •Динамический анализ функции тромбоцитов
- •2 Агонистов (индукторов агрегации) возможно селективное выделение аспириновых тромбоцитопа-тий. По типу измерения pfa-100 является динамическим агрегометром.
- •Тромбоцитокрит (рст)
- •Агрегация тромбоцитов
- •Клинический пример 2
- •Исследования агрегации тромбоцитов в образцах цельной крови
- •Молекулярно-биологические методы
- •Коагуляционные методы
- •Ручные методы
- •Автоматизированные коагулометры
- •Оптико-механические коагулометры
- •Турбидиметрические коагулометры
- •Нефелометрические коагулометры
- •Преимущества и недостатки различных методов обнаружения сгустка
- •Иммунохимические методы
- •Скрининговые тесты оценки плазменного звена гемостаза
- •Диагностическое значение ачтв
- •Использование ачтв для выявления волчаночного антикоагулянта
- •Контроль лечения гирудином
- •Скрининговый тест на основе ачтв для оценки антикоагулянтной активности протеина с
- •Протромбиновое время
- •3) Протромбиновое отношение (по), которое определяется как
- •Тканевые тромбопластины
- •Протромбиновый тест (пт) по Квику
- •0,5 Г/л (врожденная или приобретенная гипо/
- •Рептилазное время (батроксобиновое время)
- •Турбидиметрический метод
- •Интерпретация результатов
- •Определение фактора Виллебранда (vWf)
- •Определение фактора VII с использованием хромогенного субстрата
- •Определение протромбина (фактора II) с использованием хромогенного субстрата
- •Определение фактора XIII
- •Преаналитические факторы, влияющие на результаты определения гепарина
- •Определение протеина с
- •Определение протеина s
- •Определение антитромбина
- •Тесты аля исслелования фибринолитической системы
- •Определение α2-антиплазмина
- •Опрелеление ингибитора активатора плазминогена типа 1 (pai-1)
- •Паракоагуляционные тесты
- •Стандарты воз
- •Внутрилабораторный контроль качества
- •Патология гемостаза
- •Без правильных современных лабораторных исследований невозможно лечение и профилактика нарушений гемостаза.
- •Гемофилия а
- •Коагулограмма при гемофилии а
- •Исследование восстановления фактора VIII в крови
- •Клинический пример 3
- •500 Me 1 раз в 2 дня. Исследование коагулог-раммы через год показало отсутствие ингибитора к ф.VIII у пациента.
- •Клинический пример 4
- •Патология гемостаза
- •VWf:Ag - антиген фактора Виллебранда, vWf:rCo - коллаген-связывающая активность фактора Виллебранда, ф.VIII - фактор коагуляции VIII, а-д - аутосомно-доминантное, а-р - аутосомно-рецессивное.
- •Клинический пример 5
- •Клинический пример 6
- •Иммунная тромбоцитопеническая пурпура (итп)
- •Клинический пример 7
- •3 Недель.
- •Приобретенный ингибитор к фактору VIII (приобретенная гемофилия а)
- •Клинический пример 8
- •Приобретенный ингибитор к фактору V
- •Приобретенные ингибиторы к протромбину, факторам VII и X
- •Приобретенные ингибиторы к фибриногену, фибрину, ф.Хiii и промежуточным продуктам
- •Приобретенный дефицит витамина к
- •Лечение антикоагулянтами непрямого действия, отравление антагонистами витамина к
- •Клинический пример 9
- •Лабораторные тесты при тромбофилии
- •Клинический пример 10
- •Дефицит протеина с
- •Клинический пример 11
- •Дефицит протеина s
- •Мутация протромбина 20210а
- •Дефицит антитромбина
- •Гипергомоцистеинемия
- •Клинический пример 12
- •Высокая активность фактора VIII и фактора Виллебранда
- •Дисфибриногенемия
- •Антифосфолипидный синдром и волчаночный антикоагулянт
- •Клинический пример 14
- •110%, Ачтв 45,9 с (норма 28-40 с), активность ф.Iх 68%, ф.Хi 80%, ф.Хii 96%, ф.VIII 120%, скринин-говый тест на волчаночный антикоагулянт положительный.
- •Клинический пример 15
- •Клинический пример 16
- •Фибринолитическая терапия
- •Этиология и патогенез двс
- •Виды двс-синдрома
- •Тромбоцитарно-сосудистый гемостаз при двс-синдроме
- •Плазменный гемостаз при двс-синдроме
- •И фазы двс-синдрома
- •Клинический пример 18
- •Наиболее значимые факторы патологического тромбообразования у детей первого полугодия жизни
- •Приложение
- •Новорожденных в первые 6 месяцев жизни
- •В течение первых 6 месяцев жизни
- •У детей первых 6 месяцев жизни
- •По сравнению с взрослыми
- •По сравнению с взрослыми
- •Обеспечение качества лабораторной
- •Вторичные комплексные нарушения
Внутренний путь активации фибринолиза
Внутренний путь активации фибринолиза начинается в комплексе реакций контактной активации свертывания крови. Калликреин активирует проурокиназу с образованием активного фермента урокиназы. Кроме калликреина, активация проурокиназы до активной двухцепочеч-ной формы u-РА происходит под воздействием ф.ХIIа и -ХIа, плазмина (положительная обратная связь) и усиливается при связывании с уроки-назным рецептором. В связи с этим у пациентов с дефицитом прекалликреина, XII фактора (болезнь Хагемана) или высокомолекулярного кини-ногена (ВМК), у которых, казалось бы, из-за не-
достатка плазменных факторов должна быть склонность к кровотечениям, наоборот, в результате неполноценной активации фибринолиза имеется тенденция к тромбозам.
Определение u-РА для диагностики нарушений гемостаза практически не проводится, так как диагностическое значение этого фермента пока недостаточно ясно. Однако u-РА является опухолевым маркером карциномы яичника и, вероятно, других опухолей, поэтому имеются коммерческие ELISA-наборы, которые используются для определения u-РА как опухолевого маркера.
Внешний путь активации фибринолиза
Плазминоген имеет высокое сродство к выпавшему фибрину за счет присутствия на фибрине специфических лизин-связывающих участков (сайтов). Эндотелиальные клетки синтезируют и освобождают в систему циркуляции тканевой активатор плазминогена (t-PA). Изучение процесса высвобождения t-PA из клеток показало, что основным стимулятором этого является брадики-нин, который отщепляется от высокомолекулярного кининогена калликреином. Таким образом, процесс активации факторов контактной фазы является основным физиологическим пусковым механизмом фибринолиза. Этот процесс резко усиливается при остановке кровотока и образовании фибрина. t-PA обладает высоким сродством к фибрину. На фибрине формируется комплекс фибрин -тканевой активатор - плазминоген (рис. 58) - наиболее специфическое и эффективное действующее начало фибринолиза. Фибрин, особенно частично деградированный фибрин, служит кофактором t-PA-индуцированной протеолитической активации плазминогена. В результате образования это-
го комплекса плазминоген переходит в активный плазмин, который разрушает пептидные связи в фибрине/фибриногене.
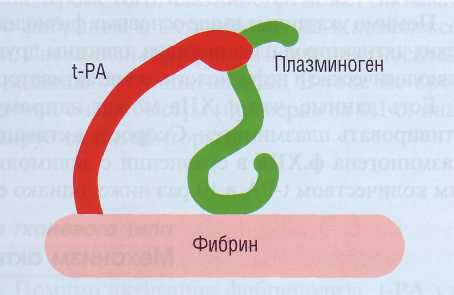
Рис. 58. Активация плазминогена при формировании комплекса фибрин - тканевой активатор - плазминоген на фибрине. Фибрин служит кофактором t-PA-индуцированной протеолитической активации плазминогена. На поверхности фибрина присутствует лизин-связывающий сайт, необходимый для активации плазминогена тканевым активатором
Система фибринолиза
Ингибиторы фибринолиза
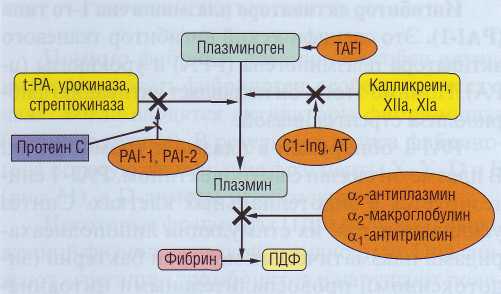
Рис. 59. Ингибиторы фибринолиза, показаны участки основного ингибирующего эффекта, Практически все ингибиторы фибринолиза являются белками острой фазы. TAFI - тромбин-активируемый ингибитор фибринолиза, t-PA- тканевой активатор плазминогена, Cl-Ing -ингибитор 1-го компонента комплемента, AT - антитромбин III, PAI-1, PAI-2 - ингибиторы тканевого активатора плазминогена (тип 1 и 2), ПДФ - продукты деградации фибрина/фибриногена
αг-антиплазмин, αг-макрогло6улин, αгантитрипсин
αг-антиплазмин (αг-АП) в физиологических условиях быстро инактивирует плазмин, образуя неактивные комплексы. оц-АП имеет высокое сродство к плазмину, взаимодействует с ним, удаляя свободный плазмин из системы циркуляции. В результате время полужизни свободного плаз-мина составляет всего 0,1 секунды. Если же плазмин успевает соединиться с выпавшим фибрином, то взаимодействие плазмин-αг-АП резко снижается (примерно в 50 раз). Недостаточность αг-АП проявляется кровотечениями, так как накапливающийся активный плазмин ускоренно разрушает фибрин и фибриноген. αг-АП - белок острой фазы, однако при массивной активации фибринолиза, в частности при ДВС-синдроме, может наблюдаться истощение αг-АП. Приобретенная недостаточность αг-АП встречается значительно чаще, чем врожденная.
αг-макроглобулин. Этот ингибитор был описан в разделе «Ингибиторы системы свертывания крови». Это неспецифический ингибитор. При активации фибринолиза образующийся из плазминогена (концентрация в плазме свыше 1,5 мкмоль) плазмин в первую очередь связывается αг-антиплазми-ном (концентрация в плазме около 1 мкмоль). После полного насыщения αг-антиплазмина дальнейшая нейтрализация плазмина осуществляется за счет αг-макроглобулина. Кроме того, αг-макро-глобулин инактивирует другие ферменты систе-
мы фибринолиза: урокиназу (u-РА), тканевой активатор плазминогена (t-PA), плазменный каллик-реин, компоненты комплемента, бактериальные и лейкоцитарные протеазы, такие, как эластаза и ка-тепсины.
α1-aHmumpuncuH. На его долю приходится более 80% антипротеазной активности крови. В сыворотке α1 -антитрипсин содержится в концентрации 1,4-3,2 г/л, или около 52 ммоль/л. Это основной ингибитор сериновых протеаз: трипсина, хи-мотрипсина. Помимо этого, он принимает участие в инактивации плазмина, калликреина, ренина, урокиназы. Благодаря небольшим размерам он может проникать и функционировать в тканях (легкие, бронхи). α1-антитрипсин - белок острой фазы, его выработка увеличивается при реакциях, запускаемых через фактор некроза опухолей, ин-терлейкин-1, интерлейкин-6, а также при высокой концентрации эстрогена в сыворотке в последнем триместре беременности, при приеме эстроген-со-держащих противозачаточных препаратов.
Все 3 описанных ингибитора совместно предупреждают появление плазмина в системе циркуляции в свободном виде, исключая его деградирующий эффект на фибриноген, а также на факторы свертывания VIII, V и другие плазменные белки. Деятельность этих ингибиторов является важным условием поддержания гемостати-ческого баланса.
Система фибринолиза
