
- •170034, Г. Тверь, пр. Чайковского, д. 9, оф. 504,
- •Список сокращений
- •Характеристика системы гемостаза
- •Морфологические компоненты системы гемостаза:
- •Сосудистая стенка
- •Эндотелий
- •Продукты эндотелиоцитов, участвующие в гемостазе
- •Контроль активности тромбоцитов
- •Тромбомодулин
- •Прокоагулянтная роль эндотелия, регуляция сосудистого тонуса
- •Роль эндотелия в регуляции сосудистого тонуса
- •Сосудистая стенка
- •Тканевой фактор
- •Коллаген
- •Тромбоциты
- •Рецепторы мембраны тромбоцитов
- •Рецепторы для высокомолекулярных белков
- •Интегрины
- •Фактор роста тромбоцитов (pdgf)
- •Фактор XIII
- •Адгезия тромбоцитов
- •Тромбоциты
- •Активация тромбоцитов
- •Агрегация тромбоцитов
- •Ретракция сгустка крови
- •Участие моноцитов в свертывании крови
- •Плазменные белки гемостаза
- •1) Многоступенчатый этап, приводящий к акти вации протромбина и превращению его в ак тивный фермент - тромбин;
- •Роль кофакторов и микроокружения в процессе свертывания крови
- •Роль кальция в гемостатических реакциях
- •Ингибиторы ферментов системы гемостаза
- •Антитромбин и гепарин
- •Протеин s
- •Система фибринолиза
- •Активатор плазминогена тканевого типа
- •Внутренний путь активации фибринолиза
- •Внешний путь активации фибринолиза
- •Ингибиторы тканевого активатора плазминогена (pai)
- •Активируемый тромбином ингибитор фибринолиза (tafi)
- •Другие элементы системы фибринолиза
- •Реологические аспекты гемостаза
- •Функция тромбоцитов в различных гемодинамических условиях
- •Современная теория свертывания крови
- •Особенности физиологии и исследования гемостаза у плодов, новорожденных и детей раннего возраста
- •Тромбоциты
- •О собенности физиологии и исследования гемостаза у женщин при менструации и беременности
- •Клинический пример 1
- •Обеспечение диагностики нарушении гемостаза в
- •Подбор антикоагулянтов
- •Динамический анализ функции тромбоцитов
- •2 Агонистов (индукторов агрегации) возможно селективное выделение аспириновых тромбоцитопа-тий. По типу измерения pfa-100 является динамическим агрегометром.
- •Тромбоцитокрит (рст)
- •Агрегация тромбоцитов
- •Клинический пример 2
- •Исследования агрегации тромбоцитов в образцах цельной крови
- •Молекулярно-биологические методы
- •Коагуляционные методы
- •Ручные методы
- •Автоматизированные коагулометры
- •Оптико-механические коагулометры
- •Турбидиметрические коагулометры
- •Нефелометрические коагулометры
- •Преимущества и недостатки различных методов обнаружения сгустка
- •Иммунохимические методы
- •Скрининговые тесты оценки плазменного звена гемостаза
- •Диагностическое значение ачтв
- •Использование ачтв для выявления волчаночного антикоагулянта
- •Контроль лечения гирудином
- •Скрининговый тест на основе ачтв для оценки антикоагулянтной активности протеина с
- •Протромбиновое время
- •3) Протромбиновое отношение (по), которое определяется как
- •Тканевые тромбопластины
- •Протромбиновый тест (пт) по Квику
- •0,5 Г/л (врожденная или приобретенная гипо/
- •Рептилазное время (батроксобиновое время)
- •Турбидиметрический метод
- •Интерпретация результатов
- •Определение фактора Виллебранда (vWf)
- •Определение фактора VII с использованием хромогенного субстрата
- •Определение протромбина (фактора II) с использованием хромогенного субстрата
- •Определение фактора XIII
- •Преаналитические факторы, влияющие на результаты определения гепарина
- •Определение протеина с
- •Определение протеина s
- •Определение антитромбина
- •Тесты аля исслелования фибринолитической системы
- •Определение α2-антиплазмина
- •Опрелеление ингибитора активатора плазминогена типа 1 (pai-1)
- •Паракоагуляционные тесты
- •Стандарты воз
- •Внутрилабораторный контроль качества
- •Патология гемостаза
- •Без правильных современных лабораторных исследований невозможно лечение и профилактика нарушений гемостаза.
- •Гемофилия а
- •Коагулограмма при гемофилии а
- •Исследование восстановления фактора VIII в крови
- •Клинический пример 3
- •500 Me 1 раз в 2 дня. Исследование коагулог-раммы через год показало отсутствие ингибитора к ф.VIII у пациента.
- •Клинический пример 4
- •Патология гемостаза
- •VWf:Ag - антиген фактора Виллебранда, vWf:rCo - коллаген-связывающая активность фактора Виллебранда, ф.VIII - фактор коагуляции VIII, а-д - аутосомно-доминантное, а-р - аутосомно-рецессивное.
- •Клинический пример 5
- •Клинический пример 6
- •Иммунная тромбоцитопеническая пурпура (итп)
- •Клинический пример 7
- •3 Недель.
- •Приобретенный ингибитор к фактору VIII (приобретенная гемофилия а)
- •Клинический пример 8
- •Приобретенный ингибитор к фактору V
- •Приобретенные ингибиторы к протромбину, факторам VII и X
- •Приобретенные ингибиторы к фибриногену, фибрину, ф.Хiii и промежуточным продуктам
- •Приобретенный дефицит витамина к
- •Лечение антикоагулянтами непрямого действия, отравление антагонистами витамина к
- •Клинический пример 9
- •Лабораторные тесты при тромбофилии
- •Клинический пример 10
- •Дефицит протеина с
- •Клинический пример 11
- •Дефицит протеина s
- •Мутация протромбина 20210а
- •Дефицит антитромбина
- •Гипергомоцистеинемия
- •Клинический пример 12
- •Высокая активность фактора VIII и фактора Виллебранда
- •Дисфибриногенемия
- •Антифосфолипидный синдром и волчаночный антикоагулянт
- •Клинический пример 14
- •110%, Ачтв 45,9 с (норма 28-40 с), активность ф.Iх 68%, ф.Хi 80%, ф.Хii 96%, ф.VIII 120%, скринин-говый тест на волчаночный антикоагулянт положительный.
- •Клинический пример 15
- •Клинический пример 16
- •Фибринолитическая терапия
- •Этиология и патогенез двс
- •Виды двс-синдрома
- •Тромбоцитарно-сосудистый гемостаз при двс-синдроме
- •Плазменный гемостаз при двс-синдроме
- •И фазы двс-синдрома
- •Клинический пример 18
- •Наиболее значимые факторы патологического тромбообразования у детей первого полугодия жизни
- •Приложение
- •Новорожденных в первые 6 месяцев жизни
- •В течение первых 6 месяцев жизни
- •У детей первых 6 месяцев жизни
- •По сравнению с взрослыми
- •По сравнению с взрослыми
- •Обеспечение качества лабораторной
- •Вторичные комплексные нарушения
Адгезия тромбоцитов
На рис. 22 показаны адгезированные тромбоциты на участке деэндотелизации. Через несколько минут после повреждения сосудистой стенки формируется сплошной слой адгезиро-ванных и агрегированных тромбоцитов, которые являются основой тромбоцитарного тромба (рис. 23).
В процессе адгезии важную роль играют 2 механизма. Один из них - непосредственная адгезия тромбоцитов через рецепторы GPIa-IIa и GPVI к коллагену субэндотелия. Однако это взаимодействие недостаточно для удержания тромбоцитов в местах воздействия высоких скоростей кровотока - артериях и артериолах. Другой ме-
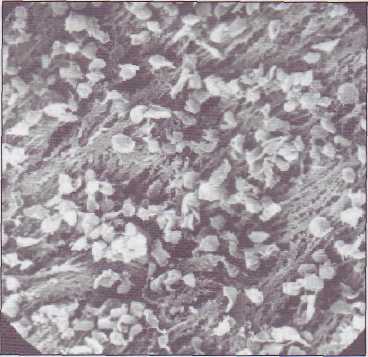
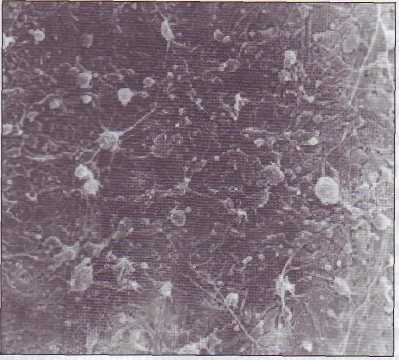
Рис. 23. Тромбоцитарный тромб, сформированный на поврежденной сосудистой стенке
ханизм, эффективно удерживающий тромбоциты при высокой скорости кровотока, включает адгезию тромбоцитов, опосредованную молекула-ми адгезии - фактором Виллебранда, фибронек-тином, витронектином, ламинином, тромбоспон-дином и др. In vivo оба эти механизма работают параллельно. Возможно, что первичный контакт тромбоцитов с субэндотелием осуществляется благодаря первому механизму, тогда как окончательная фиксация тромбоцитов происходит за счет формирования связей субэндотелий - фак-тор Виллебранда - GPIb-V-IX и связей, опосредованных другими молекулами адгезии.
Молекулы адгезии
Фактор Виллебранда (vWF) - один из самых больших гликопротеидов плазмы, имеет молекулярную массу от 540 до нескольких тысяч кДа, содержит в цепочке более 2000 аминокислот.
Ген фактора Виллебранда находится на коротком плече 12-й хромосомы. Синтез фактора Виллебранда происходит в эндотелиоцитах и мегака-риоцитах. Фактор Виллебранда из эндотелиоци-гов секретируется или в плазму, или в субэндоте-лиальное пространство; кроме того, он может содержаться в тельцах Вейбла-Палада эндотелиоци-тов (пулы хранения) и секретироваться после стимуляции эндотелиальных клеток. Фактор Виллебранда, синтезированный мегакариоцитами, содержится в альфа-гранулах тромбоцитов.
Информация о синтезе фактора Виллебранда получена в основном при изучении его в культурах эндотелиальных клеток. Первичный продукт синтеза, обозначаемый как пpe-пpo-vWF, найден в эндотелии и тромбоцитах, он иммуно-логически отличается от зрелого фактора Виллебранда. Его уровень снижен у пациентов с болезнью Виллебранда.
Пре-про-vWF содержит 2813 аминокислотных остатков. В эндоплазматическом ретикулу-ме после гликозилирования npe-npo-vWF преобразуется в пpo-vWF, который превращается в зрелый vWF после отщепления пептида, состоящего из 741 аминокислотного остатка. Этот полипептид идентифицируется как антиген II vWF (vWF:AgII).
Процесс димеризации и полимеризации vWF происходит одновременно. Зрелая субъединица
vWF содержит 2050 аминокислотных остатков, 169 из которых - цистеин, сгруппированный в областях, расположенных в амино- и карбокси-концах молекулы (N- и С-концы). Процесс димеризации связан с образованием дисульфидных мостиков между С-концами молекулы, а дальнейшая полимеризация происходит за счет образования дисульфидных связей между N-концами. Конечный продукт накапливается в тельцах Вейбла-Палада в эндотелиоцитах и в α-гранулах тромбоцитов.
Фактор Виллебранда состоит из ряда полимеров прогрессивно увеличивающейся молекулярной массы: разделяют легкие, средние, тяжелые и сверхтяжелые мультимеры. Молекулярная масса vWF варьирует от 540 кДа у димеров до 20 тысяч кДа у самых крупных мультимеров, содержащих от 50 до 100 субъединиц. Самым большим тромбоген-ным потенциалом обладают молекулы vWF с наибольшей молекулярной массой.
В плазме нет мономеров фактора Виллебранда, он всегда образует комплексы. Концентрация vWF в плазме составляет примерно 10 мкг/мл.
При исследовании vWF, содержащегося в пулах хранения, было выявлено, что его молекулярная масса, а следовательно, и тромбогенный потенциал существенно выше, чем у vWF, содержащегося в плазме, и наиболее высок в а-гранулах тромбоцитов (так называемый сверхвысокомолекулярный фактор Виллебранда). После сильной стимуляции тромбоцитов и эндотелиоцитов сверхвысокомолекулярный фактор Виллебранда некоторое время обнаруживается в плазме. Однако потом в сосудистом русле молекулярная масса vWF довольно быстро снижается до «нормальной» под воздействием кальпаиновых про-теаз плазмы. Такое распределение позволяет создавать высокий тромбогенный потенциал в местах повреждения эндотелия при выбросе vWF из пулов хранения, в то же время сохраняя тромбогенный потенциал на «обычном» уровне в интак-тном сосудистом русле.
Фактор Виллебранда имеет два пути секреции: непосредственная секреция после синтеза и полимеризации, которая создает определенный уровень vWF в крови, и регуляторная секреция из пулов хранения в ответ на различную стимуляцию. Фоновая активность vWF в крови у каждого человека может меняться в значительных
Тромбоциты
пределах. Реализация vWF из тромбоцитарных гранул возникает при активации тромбоцитов под воздействием различных физиологических и нефизиологических индукторов (АДФ, коллаген, адреналин, вазопрессин, серотонин, тромбин, простагландин Е1, тромбоксан А2 и др.), и в том числе плазменного vWF. Уровень vWF в крови возрастает при воспалении различного генеза, повреждении эндотелия сосудов при васкулитах, стрессе, у женщин во время беременности. Повышение активности vWF в патологических ситуациях может способствовать развитию тромбозов.
Вторичные изменения структуры vWF и его активности являются следствием иммунных процессов, тромботической тромбоцитопенической пурпуры, гемолитико-уремического синдрома и др. Описаны заболевания (болезнь Виллебран-да, тип Виченза; врожденная тромботическая тромбоцитопеническая пурпура), при которых дефект этих ферментов приводит к накоплению сверхвысокомолекулярных мультимеров vWF и преждевременной секвестрации тромбоцитов из кровотока.
Основными функциями фактора Виллебранда являются:
опосредование адгезии тромбоцитов к субэн- дотелиальным структурам, в первую очередь к коллагену, и последующей агрегации тром боцитов (участие в первичном сосудисто- тромбоцитарном гемостазе);
связывание свободного фактора VIII и защи та его молекулы от преждевременной инак тивации (участие во вторичном плазменном гемостазе).
Опосредование адгезии и агрегации тромбоцитов. Роль фактора Виллебранда в адгезии и агрегации тромбоцитов наиболее велика в условиях воздействия высоких скоростей кровотока. Молекулы vWF специфически связываются с рецепторами тромбоцитов GPIb-V-IX и коллагеном субэндотелия. Это обеспечивает прочную фиксацию тромбоцитов к субэндотелиальным структурам в тех участках сосудистого русла, где сила потока крови существенно мешает формированию гемостатической пробки и другие механизмы адгезии не могут обеспечить надежной фиксации тромбоцитов. В частности, известно, что vWF является ключевым при формировании
тромба в мелких артериях, артериолах и артериальных капиллярах. В местах, где интенсивность кровотока невелика, роль vWF уменьшается, преобладающим становится взаимодействие, опосредованное другими молекулами, в том числе прямая адгезия тромбоцитов к коллагену посредством GPIa-IIa.
Агрегация тромбоцитов в условиях воздействия активного тока крови тоже происходит с участием фактора Виллебранда. Помимо GPIb-V-IX, с фактором Виллебранда также связывается GPIIb-IIIа. Возможно, что это взаимодействие является ключевым в процессе агрегации в местах сосудистого русла с высокой скоростью тока крови.
Тест агрегации, опосредованный фактором Виллебранда, в лабораторных условиях может быть выполнен с использованием фиксированных тромбоцитов. Видимо, эта реакция не требует энергетических затрат. Однако стимуляция рецептора Ib-V-IX приводит к активации тромбоцита.
Учитывая особенности фактора Виллебранда, можно сказать, что он выполняет функцию «биологического клея», фиксируя тромбоциты на поврежденной сосудистой стенке (рис. 24).
Другая функция фактора Виллебранда - защита ф.VIII от протеолитической деградации системой протеин С - протеин S. В плазме vWF является белком-носителем фактора VIII.

Рис. 24. Фактор Виллебранда (vWF) выполняет роль «биологического клея», прикрепляя к коллагену субэндотелия адгезированные тромбоциты через гликопротеиновый комплекс GPIb-V-IX, Тромб увеличивается в размерах по мере адгезии и агрегации новых тромбоцитов, скрепление которых в агрегат обеспечивает фибриноген, имеющий дива-лентную структуру и взаимодействующий с рецепторами GPIIb-llla
Тромбоциты
Молярная концентрация vWF примерно в 50 раз выше, чем молярная концентрация фактора VIII. Фактор VIII практически весь связан с vWF (рис. 25). Это предупреждает быструю деградацию ф.VШ под влиянием протеина С. Связанный с vWF фактор VIII защищен от протео-литической инактивации в плазме, поскольку у него заблокированы сайты связывания с фос-фолипидной матрицей и заблокированы сайты связывания с протеином С. Поэтому недостаток vWF часто вызывает вторичный дефицит ф.VIII.
В области повреждения сосуда, в процессе vWF-опосредованной адгезии тромбоцитов происходит контакт комплекса vWF-ф.VIII и тромбина (ф.Па), который активирует ф.III, освобождая его из комплекса с фактором Виллебранда.
Фибронектин (плазматический, субэндоте-лиальный и тромбоцитарный) - гранулярный контактный белок, который способен образовывать комплексы с GPIc-Па-рецепторами тромбоцитов и коллагеном. Сродство фибронектина к коллагену и тромбоцитам меньше, чем у фактора Виллебранда, однако молекулярная концентрация его выше. Видимо, фибронектин является основной молекулой адгезии в венозной и капиллярной сети, образуя ось: тромбоцитарный рецептор GPIc-IIa - фибронектин - коллаген. Гликопротеиновый комплекс GPIc-IIa распознает в фибронектине RGD последовательность и осуществляет рецепторную функцию как в интактных, так и в активированных тромбоцитах. Характерная аминокислотная последовательность RGD - трипептид Arg-Gly-Asp имеется во всех адгезивных белках крови, белках а-гранул тромбоцитов, фибриногене, факторе Виллебранда, фибронектине, витронектине и других белках. Наличие RGD-последовательно-сти на фибронектине определяет зависимость процесса его взаимодействия со своим рецептором на тромбоцитах от двухвалентных катионов Са2+ и Mg2+.
Витронектин - гликопротеин плазмы, субэндотелия и а-гранул тромбоцитов. Имеет значение в гемостатических реакциях и в восстановлении поврежденных тканей сосудистой стенки. Витронектин, как и другие адгезивные белки, содержит трипептид RGD, распознающийся интегриновыми рецепторами эндотели-альных клеток и тромбоцитов. Витронектино-
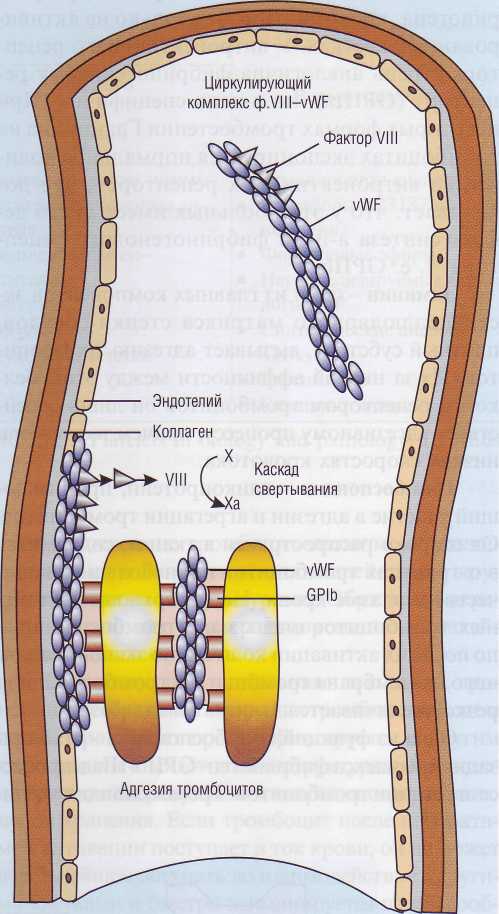
Рис. 25. Комплекс фактор VIII - фактор Виллебранда (ф.Vlll—vWF) состоит из 2 отдельных белков, которые выполняют в гемостазе разные функции, имеют разную химическую и иммунологическую структуру. Фактор VIII необходим для активации фактора X в каскаде свертывания крови, его дефицит вызывает гемофилию А. Фактор Виллебранда (vWF) - полимерный белок, который составляет основную массу комплекса. Он необходим для адгезии тромбоцитов к поврежденной стенке сосудов, обеспечивая взаимодействие коллагена с гликопротеиновым комплексом тромбоцитов GPIb-V-IX. Кроме того, он участвует в агрегации тромбоцитов, взаимодействуя с интегринами GPIIb-llla. Недостаток vWF приводит к болезни Виллебранда
