
- •170034, Г. Тверь, пр. Чайковского, д. 9, оф. 504,
- •Список сокращений
- •Характеристика системы гемостаза
- •Морфологические компоненты системы гемостаза:
- •Сосудистая стенка
- •Эндотелий
- •Продукты эндотелиоцитов, участвующие в гемостазе
- •Контроль активности тромбоцитов
- •Тромбомодулин
- •Прокоагулянтная роль эндотелия, регуляция сосудистого тонуса
- •Роль эндотелия в регуляции сосудистого тонуса
- •Сосудистая стенка
- •Тканевой фактор
- •Коллаген
- •Тромбоциты
- •Рецепторы мембраны тромбоцитов
- •Рецепторы для высокомолекулярных белков
- •Интегрины
- •Фактор роста тромбоцитов (pdgf)
- •Фактор XIII
- •Адгезия тромбоцитов
- •Тромбоциты
- •Активация тромбоцитов
- •Агрегация тромбоцитов
- •Ретракция сгустка крови
- •Участие моноцитов в свертывании крови
- •Плазменные белки гемостаза
- •1) Многоступенчатый этап, приводящий к акти вации протромбина и превращению его в ак тивный фермент - тромбин;
- •Роль кофакторов и микроокружения в процессе свертывания крови
- •Роль кальция в гемостатических реакциях
- •Ингибиторы ферментов системы гемостаза
- •Антитромбин и гепарин
- •Протеин s
- •Система фибринолиза
- •Активатор плазминогена тканевого типа
- •Внутренний путь активации фибринолиза
- •Внешний путь активации фибринолиза
- •Ингибиторы тканевого активатора плазминогена (pai)
- •Активируемый тромбином ингибитор фибринолиза (tafi)
- •Другие элементы системы фибринолиза
- •Реологические аспекты гемостаза
- •Функция тромбоцитов в различных гемодинамических условиях
- •Современная теория свертывания крови
- •Особенности физиологии и исследования гемостаза у плодов, новорожденных и детей раннего возраста
- •Тромбоциты
- •О собенности физиологии и исследования гемостаза у женщин при менструации и беременности
- •Клинический пример 1
- •Обеспечение диагностики нарушении гемостаза в
- •Подбор антикоагулянтов
- •Динамический анализ функции тромбоцитов
- •2 Агонистов (индукторов агрегации) возможно селективное выделение аспириновых тромбоцитопа-тий. По типу измерения pfa-100 является динамическим агрегометром.
- •Тромбоцитокрит (рст)
- •Агрегация тромбоцитов
- •Клинический пример 2
- •Исследования агрегации тромбоцитов в образцах цельной крови
- •Молекулярно-биологические методы
- •Коагуляционные методы
- •Ручные методы
- •Автоматизированные коагулометры
- •Оптико-механические коагулометры
- •Турбидиметрические коагулометры
- •Нефелометрические коагулометры
- •Преимущества и недостатки различных методов обнаружения сгустка
- •Иммунохимические методы
- •Скрининговые тесты оценки плазменного звена гемостаза
- •Диагностическое значение ачтв
- •Использование ачтв для выявления волчаночного антикоагулянта
- •Контроль лечения гирудином
- •Скрининговый тест на основе ачтв для оценки антикоагулянтной активности протеина с
- •Протромбиновое время
- •3) Протромбиновое отношение (по), которое определяется как
- •Тканевые тромбопластины
- •Протромбиновый тест (пт) по Квику
- •0,5 Г/л (врожденная или приобретенная гипо/
- •Рептилазное время (батроксобиновое время)
- •Турбидиметрический метод
- •Интерпретация результатов
- •Определение фактора Виллебранда (vWf)
- •Определение фактора VII с использованием хромогенного субстрата
- •Определение протромбина (фактора II) с использованием хромогенного субстрата
- •Определение фактора XIII
- •Преаналитические факторы, влияющие на результаты определения гепарина
- •Определение протеина с
- •Определение протеина s
- •Определение антитромбина
- •Тесты аля исслелования фибринолитической системы
- •Определение α2-антиплазмина
- •Опрелеление ингибитора активатора плазминогена типа 1 (pai-1)
- •Паракоагуляционные тесты
- •Стандарты воз
- •Внутрилабораторный контроль качества
- •Патология гемостаза
- •Без правильных современных лабораторных исследований невозможно лечение и профилактика нарушений гемостаза.
- •Гемофилия а
- •Коагулограмма при гемофилии а
- •Исследование восстановления фактора VIII в крови
- •Клинический пример 3
- •500 Me 1 раз в 2 дня. Исследование коагулог-раммы через год показало отсутствие ингибитора к ф.VIII у пациента.
- •Клинический пример 4
- •Патология гемостаза
- •VWf:Ag - антиген фактора Виллебранда, vWf:rCo - коллаген-связывающая активность фактора Виллебранда, ф.VIII - фактор коагуляции VIII, а-д - аутосомно-доминантное, а-р - аутосомно-рецессивное.
- •Клинический пример 5
- •Клинический пример 6
- •Иммунная тромбоцитопеническая пурпура (итп)
- •Клинический пример 7
- •3 Недель.
- •Приобретенный ингибитор к фактору VIII (приобретенная гемофилия а)
- •Клинический пример 8
- •Приобретенный ингибитор к фактору V
- •Приобретенные ингибиторы к протромбину, факторам VII и X
- •Приобретенные ингибиторы к фибриногену, фибрину, ф.Хiii и промежуточным продуктам
- •Приобретенный дефицит витамина к
- •Лечение антикоагулянтами непрямого действия, отравление антагонистами витамина к
- •Клинический пример 9
- •Лабораторные тесты при тромбофилии
- •Клинический пример 10
- •Дефицит протеина с
- •Клинический пример 11
- •Дефицит протеина s
- •Мутация протромбина 20210а
- •Дефицит антитромбина
- •Гипергомоцистеинемия
- •Клинический пример 12
- •Высокая активность фактора VIII и фактора Виллебранда
- •Дисфибриногенемия
- •Антифосфолипидный синдром и волчаночный антикоагулянт
- •Клинический пример 14
- •110%, Ачтв 45,9 с (норма 28-40 с), активность ф.Iх 68%, ф.Хi 80%, ф.Хii 96%, ф.VIII 120%, скринин-говый тест на волчаночный антикоагулянт положительный.
- •Клинический пример 15
- •Клинический пример 16
- •Фибринолитическая терапия
- •Этиология и патогенез двс
- •Виды двс-синдрома
- •Тромбоцитарно-сосудистый гемостаз при двс-синдроме
- •Плазменный гемостаз при двс-синдроме
- •И фазы двс-синдрома
- •Клинический пример 18
- •Наиболее значимые факторы патологического тромбообразования у детей первого полугодия жизни
- •Приложение
- •Новорожденных в первые 6 месяцев жизни
- •В течение первых 6 месяцев жизни
- •У детей первых 6 месяцев жизни
- •По сравнению с взрослыми
- •По сравнению с взрослыми
- •Обеспечение качества лабораторной
- •Вторичные комплексные нарушения
Протеин s
Протеин S (ПS) - витамин-К-зависимый белок, синтезируемый в печени. Протеин S присутствует в плазме частично в свободном состоянии, частично в комплексе с С4-связывающим протеином (С4-СП), который доставляет протеин S на фосфолипидную мембрану. Это важно учитывать, так как комплекс протеин S - С4-СП не обладает кофакторной активностью по отношению к протеину С. Только свободный протеин S является кофактором АПС. Активность АПС в кооперации со свободным протеином S значительно выше, чем без него.
Дефицит nS, так же как и дефицит ПС, приводит к развитию тромбозов. Тяжесть течения тромбофилии при дефиците nS также пропорциональна степени снижения его активности, а гомозиготные формы дефицита nS неизвестны.
На рис. 53 схематично представлена последовательность взаимодействий компонентов системы протеин С - протеин S при инактивации фактора Va.
С4-связывающий протеин
С4-связывающий протеин (С4-СП) - острофазный белок, синтезируется в печени. В плазме присутствует в виде молекулы, содержащей 7 идентичных ос-цепей и одну β-цепь (рис. 54). Сниженный уровень С4-СП имеет место у новорожденных и лиц, принимающих непрямые антикоагулянты. Повышение С4-СП наблюдается при воспалении, активации аутоиммунных реакций, при беременности, у женщин, принимающих стероидные контрацептивы; при этом происходит избыточное связывание протеина S. Дефицит свободной формы протеина S рассматривается как фактор риска тромбофилии. С4-СП способен также регулировать активность системы комплемента, образовывать Са-зависимые комплексы с амилоидным
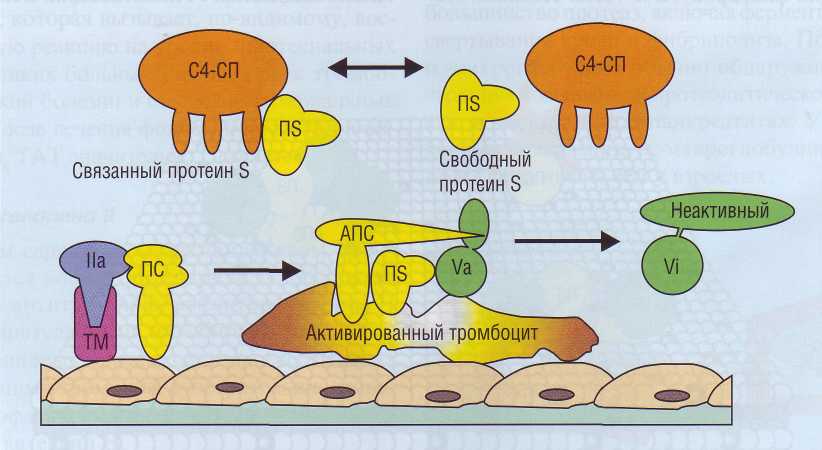
Рис. 53. Система протеина С. Активированный протеин С (АПС), сопрягаясь с теназным комплексом на фосфолипид-ной поверхности (активированный тромбоцит), вызывает деградацию фактора V. ТМ - тромбомодулин, С4-СП - связывающий протеин, F1S - протеин S, ПС - протеин С, На, Va - активированные плазменные факторы, Vi - деградированный фактор V
Плазменные белки гемостаза
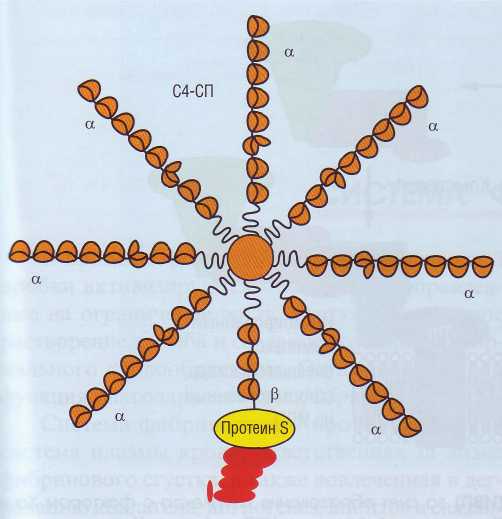
Рис. 54. Схематическое изображение α- и β-цепей С4-cвязывающего протеина и участок связывания протеина S
Р-белком сыворотки. Определение С4-СП возможно методом иммунотурбидиметрии или ELISA. Концентрация С4-СП в сыворотке составляет в норме около 200 мкг/мл.
Тромбомодулин был описан ранее в разделе, посвященном функции эндотелия.
Нарушения в системе протеина С (рис. 55), среди которых выделяют дефицит протеина С, дефицит тромбомодулина, дефицит протеина S и особенно резистентность к активированному протеину С (РАПС), - наиболее изученная па-тоология, значительно увеличивающая риск па-тоологического тромбообразования - тромбо-филии.
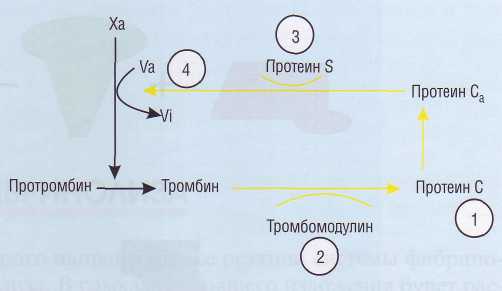
Рис. 55. Нарушения в системе протеина С, способствующие развитию тромбофилий: 1 -дефицит протеина С, 2 -дефицит тромбомодулина, 3 - дефицит протеина S, 4 - резистентность к активированному протеину С
Система протеина С активно реагирует на развитие воспаления в организме. Известно, что развитие воспаления, особенно в условиях грамнега-тивного сепсиса значительно воздействует на гемо-статический баланс, вызывая гиперкоагуляцию. Это связано с несколькими эффектами в системе протеина С. Во-первых, медиаторы воспаления подавляют синтез тромбомодулина, что ведет к уменьшению активации протеина С. Во-вторых, в крови повышается активность комплемента, следствием этого является относительное увеличение количества связанного и уменьшение активного несвязанного протеина S. В-третьих, фагоцитарные ферменты могут отщеплять тромбомодулин от эндо-телиальной поверхности. Он появляется в свободной циркуляции, но его активность в этих условиях значительно ниже, чем у фиксированного на мембране. В-четвертых, стимуляция синтеза и экспрессии тканевого фактора на мембране клеток в зоне воспаления ведет к усилению синтеза факторов IХа и Ха и нарастанию дисбаланса.
Ингибиторы активных комплексов
Ингибитор пути тканевого фактора, или ин-гибитор внешнего пути
Открытие в последнее десятилетие ингиби-тора пути тканевого фактора (ИПТФ, ИВП, TFPI) стало важным шагом в пересмотре классического каскада свертывания крови и создания современной каскадно-матричной теории гемостаза.
ИВП ограничивает синтез тромбина комплексом ТФ-ф.VII-ф.Ха, блокируя его вскоре после образования. Один из ингибирующих доменов ИВП связывается с ф.Ха, после чего другой домен реагирует с активным центром ф.VII, когда последний связан с тканевым фактором. Аффинность ИВП к ф.VIIа значительно повышается в присутствии гепарина (рис. 56). Образуется пол-
Плазменные белки гемостаза
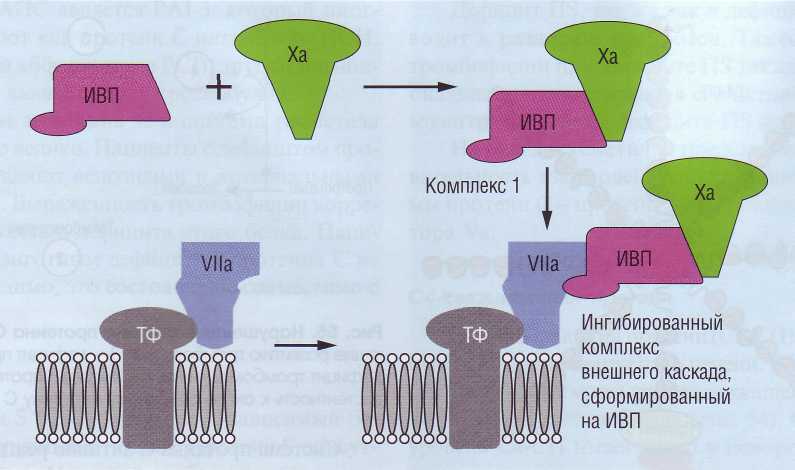
Рис. 56. Механизм действия ингибитора внешнего пути (ИВП) за счет образования комплекса с фактором Ха и формирования четырехкомпонентного комплекса - фактор Vila + тканевой фактор + ИВП + фактор Ха
ностью неактивный тетрамолекулярный комплекс ТФ-ф.VII-ИВП ф.Х. Помимо ингибирова-ния, ИВП способствует поглощению и деградации этого комплекса. Таким образом, во внешнем каскаде плазменного гемостаза формируется отрицательная обратная связь.
ИВП, по-видимому, ответственен при лечении гепарином за удлинение ряда тестов коагу-лограммы, в частности АЧТВ. ИВП в плазме частично связан с липопротеидами низкой и очень низкой плотности (ЛПНП и ЛПОНП). В таком комплексе ИВП более устойчив к инактивации. Появились сообщения, что тромбин способен стимулировать освобождение ИВП из эндотелия и ЛПНП, тем самым формируется обратная от-
рицательная связь для снижения образования тромбина.
Определение ИВП в плазме проводят методом ELISA или методом с образованием фактора Ха, который определяется в тесте с хромоген-ным субстратом. Определение ИВП в плазме выявляет не более 5-10% общего количества ИВП в сосудистой системе, так как основное его количество депонируется в сосудистой стенке. Повышение ИВП в плазме обнаружено после лечения нефракционированным или низкомолекулярным гепарином, при диабете и у больных с инфарктом миокарда. Есть сообщения о снижении ИВП при тромботической тромбопенической пурпуре и ишемическом инсульте.
Система фибринолиза
