
Марини. Медицина критических ситуаций
.pdf601
нилциклидин. У большинства больных из группы риска удается поставить диагноз перед началом синдрома с помощью биопсии мышцы и провоцирующего теста.
Диагноз Диагноз должен быть поставлен по клиническим данным, распознаваемым по воз-
никновению: а) мышечной ригидности; б) высокой и быстро развивающейся лихорадки (часто 41—45 °С); в) тахикардии. Чрезвычайно интенсивная мышечная активность вызы- вает увеличение потребления кислорода и продукции СО2. Злокачественная гипертермия вызывает гипоксию, гиперкапнию и метаболический ацидоз, который в свою очередь мо- жет обусловить появление аритмии и пятен на коже. Дифференциальный диагноз злока- чественной гипертермии включает "тиреоидный криз" и феохромоцитому. Ни поясничная пункция, ни электроэнцефалограмма (ЭЭГ) не позволяют объяснить нарушения сознания. В результате острого некроза скелетных мышц обычно повышается содержание фосфатов, мочевой кислоты и мышечных ферментов (КФК, лактатдегидрогеназы [ЛДГ], альдолазы).
Осложнения Значительное увеличение уровня метаболизма в большом проценте случаев стано-
вится причиной гиперкапнии, гипоксемии и гипогликемии. Если злокачественная гипер- термия быстро не излечивается, она может вызвать тяжелое повреждение мышц с некро- зом и кальцинозом мягких тканей. Циркулирующий миоглобин приводит к почечной не- достаточности. В таких случаях повреждение почек предотвращают ощелачиванием мочи и поддержанием артериального давления и канальцевого потока. Высокий сердечный вы- брос с низким общепериферическим сосудистым сопротивлением приводит к гипотензии, но допамин или α-агонисты следует применять осторожно, потому что вазоконстрикция может замедлить теплоотдачу. Гипоксия ткани более интенсивна при злокачественной ги- пертермии, чем при тепловом ударе или нейролептическом злокачественном синдроме, что объясняет большую частоту аритмий сердца и повреждения мышц.
Собственно тепловая токсичность приводит к гибели нейронов. Особенно ранимы гиппокамп и клетки Пуркинье мозжечка, что объясняет высокую частоту двигательных нарушений после излечения. Профилактические противосудорожные средства помогают предотвращать судорожные припадки, которые почти всегда встречаются при злокачест- венной гипертермии. Показано профилактическое применение блокаторов гистамина или антацидов для противодействия тенденции желудочно-кишечного кровотечения. Некроз печени и холестаз отмечаются редко. Поздние осложнения включают увеличение числа лейкоцитов и тромбоцитов, коагулопатию как результат ухудшения функции печени и не-
посредственную тепловую активацию тромбоцитов и факторов свертывающей системы крови.
Лечение Злокачественная гипертермия — реальная опасность; смертность непосредственно
связана с величиной и продолжительностью максимальной температуры. Даже краткая за- держка терапии может оказаться фатальной. Анестезия должна быть немедленно законче- на, и элементы дыхательного контура должны быть заменены. Как можно скорее необхо- димо начать внешнее охлаждение и специфическое лечение дантроленом (2—10 мг/кг). Дантролен может нарушить механизмы возбуждения — сокращения и помешать выходу кальция из клеток, чтобы остановить продукцию тепла, но реакция на дантролен не может служить диагностической (тепловой удар и нейролептический злокачественный синдром также могут поддаваться этим препаратам). Кортикостероиды не улучшают прогноз, их применять не следует. Средства, которые считают безопасными при злокачественной ги- пертермии, включают закись азота, барбитураты, диазепам, панкуроний и опиаты. В отли- чие от пациентов с тепловым ударом напряжения, которые обычно обезвожены, пациенты со злокачественной гипертермией обычно имеют нормальный ОЦК.
602
НЕЙРОЛЕПТИЧЕСКИЙ ЗЛОКАЧЕСТВЕННЫЙ СИНДРОМ Определение
Подобно злокачественной гипертермии, нейролептический злокачественный син- дром — редкий вызванный лекарственными средствами гипертермический синдром, ха- рактеризующийся лихорадкой, ригидностью мышц, нарушением сознания и часто сопро- вождаемый дисфункцией легких и неустойчивостью ауторегуляции. Он отличается, одна- ко, причинами, основным механизмом, длительностью течения, прогнозом и характери- стиками групп больных. Все нарушения, выявленные лабораторными методами, не- специфичны и включают повышение КФК, лейкоцитоз и повышенные показатели, полу- чаемые при функциональных пробах печени. Люмбальная пункция и компьютерная томо- графия (КТ) головы бесполезны для диагностики. При дифференциальной диагностике нейролептического злокачественного синдрома следует иметь в виду тепловой удар, фео- хромоцитому, антихолинергическую токсичность и криз ингибитора моноаминоксидазы.
Причины Нейролептический злокачественный синдром встречается меньше чем у 1 % всех
больных, получающих нейролептические средства. С этим синдромом ассоциируются фе- нотиазины, бутирофеноны и тиоксантины, но единственная наиболее часто отмечаемая корреляция — это галоперидол. Интересно, что лишь изредка поступают сообщения о нейролептическом злокачественном синдроме у пациентов ОИТ, которые получали внут- ривенно галоперидол для устранения возбуждения. У большинства больных признаки развиваются в пределах 4 нед после начала терапии или увеличения дозировки лекарст- венного препарата, однако синдром может возникнуть и после единственной дозы и в лю- бое время в течение лечения.
Также сообщали о нейролептическом злокачественном синдроме, который развива- ется после того, как резко прекращают введение допаминергических препаратов при бо- лезни Паркинсона. Независимо от этиологии признаки возникают более чем за 24—72 ч и обычно продолжаются приблизительно от 10 до 14 дней. (Большая продолжительность может сопровождать более длительно действующие нейролептические средства). Причи- ны нейролептического злокачественного синдрома не установлены, но, вероятно, он воз- никает из-за блокады допаминергических рецепторов в полосатом теле. В качестве второ- го потенциального механизма предполагают блокаду ацетилхолиновых рецепторов. К нейролептическому злокачественному синдрому предрасполагают дегидратация и мы- шечное истощение больных.
Клинические особенности Синдром характеризуют быстрое начало выраженной лихорадки, ригидность мышц,
измененная чувствительность, нестабильность ауторегуляции и экстрапирамидные двига- тельные нарушения. Очевидно, что только клинические особенности не позволяют отли- чить этот синдром от злокачественной гипертермии (особенно у больного, которому сразу после операции вводят галоперидол для снятия возбуждения).
Лабораторные исследования Все нарушения, выявленные путем лабораторных исследований, неспецифичны и
включают повышение КФК, увеличенный креатинин, лейкоцитоз и повышенные показа- тели функциональных проб печени. Люмбальную пункцию и КТ головы выполнять бес- полезно.
Осложнения Даже при соответствующем лечении нейролептический злокачественный синдром
фатален в 20—30 % случаев и часто осложнен острым некрозом скелетных мышц, острым
603
инфарктом миокарда и остаточными нарушениями движений. Не у всех больных нейро- лептический злокачественный синдром рецидивирует при повторном воздействии подоб- ных нейролептических средств. Хотя степень корреляции между злокачественной гипер- термией и нейролептическим злокачественным синдромом неизвестна, то обстоятельство, что некоторые пациенты, перенесшие злокачественную гипертермию, безболезненно вы- держивают терапию нейролептическими средствами, свидетельствует, что злокачест- венная гипертермия и нейролептический злокачественный синдром, несмотря на сходные клинические проявления, имеют различную этиологию.
Лечение Как и при злокачественной гипертермии, лечение нейролептического злокачествен-
ного синдрома требует отмены причиняющего страдание лекарственного средства и внут- ривенного применения дантролена в дозах до 10 мг/кг.
Хотя эффективность внешнего охлаждения не доказана, оно представляется разум- ной мерой. Для устранения мышечной ригидности также можно применять бромокрип- тин, амантадин и миорелаксант панкуроний.
КЛЮЧЕВЫЕ МОМЕНТЫ
1.Температура тела — результат баланса между генерируемым теплом и его потеря- ми. В принципе потеря тепла — намного более эффективный процесс, чем продукция теп- ла, когда под влиянием окружающей среды температура тела отклоняется от нормальной.
2.Для выявления лихорадки или гипотермии важно, каким методом измеряется тем- пература. Многие термометры не позволяют обнаружить температуру ниже 34,4 СС или выше 40,5 °С. В ОИТ термопара на катетере, введенном в легочную артерию для мони- торного контроля температуры центральной крови, наиболее точно определяет внутрен- нюю температуру, но это явно инвазивный метод. Измерения температуры во рту и на по- верхности тела гораздо менее точны соответственно из-за проблем тахипноэ и слабого контакта термометра с телом. Наиболее целесообразно контролировать температуру у па- циентов ОИТ в прямой кишке.
3.Гипотермия обычно бывает вызвана многими причинами, включая пребывание при низкой температуре окружающей среды, а также инфекцию,
гипотиреоз или интоксикацию лекарственным средством или алкоголем. Понижен- ная температура изменяет функцию всех главных систем организма. Хотя это и спорно, пассивное внешнее согревание, вероятно, лучший метод для большинства пациентов с на- чальной температурой, равной 33,3 °С или выше. Пассивное согревание может быть до- полнено промыванием желудка нагретой водой, подачей респиратором нагретого и ув- лажненного газа и внутривенным введением нагретой жидкости. Перитонеальный лаваж или экстракорпоральное кровообращение необходимы редко.
4.Классический тепловой удар и тепловой удар напряжения прежде всего связаны с окружающей средой, но часто осложнены основными сердечнососудистыми заболевания- ми и медикаментозной терапией, а, также использованием наркотиков Наиболее эффек- тивные методы быстрого охлаждения — понижение температуры окружающего воздуха и воздействие на пациента потоком воздуха с аэрозолем воды. Восполнение жидкости носит дополнительный характер, дефицит жидкости намного более заметен у пациентов с теп- ловым ударом напряжения, чем с классическим тепловым ударом.
5.Злокачественная гипертермия — потенциально смертельный синдром, вызывае- мый ингаляционными анестетиками и миорелаксантами, которые должны рассматривать- ся как причина лихорадки в операционном и послеоперационном периодах. Когда выяв- лены характерная ригидность мышц и высокая лихорадка, следует прекратить введение провоцирующего лекарственного средства и приступить к внешнему охлаждению в соче- тании с назначением дантролена.

604
6. Нейролептический злокачественный синдром, другое фармакологически индуци- рованное гипертермическое состояние, может быть вызван лекарственным нейролептиче- ским средством или отменой допаминергического агента. Синдром может начаться в про- цессе применения любого нейролептического средства, но чаще в начале терапии или при изменении дозы лекарственного препарата. Показаны отмена причиняющего страдание лекарственного средства и лечение дантроленом.
ГЛАВА 29
Острая почечная недостаточность и диализ
Поскольку выделительная функция почек может быть "протезирована" гемодиали- зом и их метаболические функции можно скомпенсировать фармакологически или функ- цией легких и печени, почки являются единственным органом, чья полная недостаточ- ность не обязательно фатальна. Со времени опубликования первого издания этой книги
стало более понятно значение поддержания адекватной перфузии и отказа от применения нефротоксических соединений, благодаря чему, возможно, уменьшились частота и тя- жесть острой почечной недостаточности. Кроме того, заметно улучшился диализ и другие поддерживающие технологии, применяемые в случаях, когда вследствие острого пораже- ния почки перестают функционировать.
ОЦЕНКА ФУНКЦИИ ПОЧЕК Так как почки — основной орган, выделяющий азотсодержащие отходы, концентра-
ция азота мочевины крови (АМК) и креатинина характеризует их функцию. Значительная
изменчивость выделения мочи и способности канальцев абсорбировать фильтрованную мочу делают исследование АМК для этой цели менее надежным, чем исследование креа- тинина. В качестве общего положения можно считать, что после острого прекращения ра- боты почек АМК увеличивается на 10—15 мг/дл/день, а креатинин — на 1—2,5 мг/дл/день. Калий плазмы обычно повышается меньше чем на 0,5 мэкв/л в день, а НСО3~ падает приблизительно на 1 мэкв/л в день. При катаболических нагрузках вследствие ожо- гов, травм, острого некроза скелетных мышц, введения стероидов, сепсиса или голодания скорость изменения этих параметров может удвоиться. В отличие от АМК ежедневная продукция креатинина относительно постоянна. Повышение креатинина указывает, что скорость продукции превышает скорость его выведения гломерулярной фильтрацией.
605
Следовательно, стабильное повышение креатинина означает, что было достигнуто новое состояние гомеостаза при уменьшенной скорости гломерулярной фильтрации (СГФ).
ТАБЛИЦА 29.1 ЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ ОСТРОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНО-
СТИ
Показатели |
Внепочечные |
Почечные |
|
|
|
АМК и креатинин |
> 10:1 |
≈10:1 |
|
|
|
Концентрация Na* в |
< 20 мэкв/л |
> 40 мэкв/л |
моче |
|
|
Осмоляльность мочи |
>500 мосм/л |
< 300—400 мосм/л |
|
|
|
Креатинин в моче и |
>40 |
<20 |
креатинин в плазме |
|
|
Na+ в моче и клиренс |
< 1 |
> 2 |
креатинина |
|
|
Выведение Na* и клиренс |
< 1 |
> 1 |
креатинина |
|
|
(FeNa) |
|
|
Осаждение мочи |
Нормальное |
Активное |
|
|
|
До стабилизации креатинина тяжесть острой почечной дисфункции и выведение креатинина надежно оценить невозможно. Поскольку рост креатинина плазмы отстает от ухудшения СГФ, во время развития острой почечной недостаточности дозы лекарственно- го средства часто бывают, завышенными.
Если отказ почек продолжается, креатинин обычно выравнивается приблизительно до уровня 12— 15 мг/дл в зависимости от катаболического статуса. (Острый некроз ске- летных мышц может заставить креатинин временно превысить эту величину.) Кетоны, до- бутамин, флюцитозин и цефокситин иногда вызывают искусственное завышение креа- тинина, измеряемого в плазме.
Объем мочи обычно отражает почечную перфузию, в то время как удельный вес мо- чи пропорционален концентрационной способности (функция канальцев). Следовательно, у больных без олигурии почечный кровоток, вероятно, адекватен.
Кроме того, у пациентов, выделяющих концентрированную мочу, существенное по- вреждение канальцев маловероятно. Отделить проблемы перфузии от канальцевой дис- функции помогают некоторые расчетные показатели (табл. 29.1).
ЭТИОЛОГИЯ ОСТРОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ Приблизительно у 20 % критически больных развивается острая почечная недоста-
точность; ее частота в этой группе пациентов в пять раз выше, чем среди всех пациентов стационара. Как и при пневмонии, этиология почечной недостаточности значительно раз- личается в зависимости от того, развивается ли это осложнение в больнице или вне ее, и от того, насколько процесс является хроническим.
Например, неконтролируемая артериальная гипертония и сахарный диабет — наибо- лее частые причины хронической или медленно развивающейся почечной недоста- точности вне больницы, а гломерулонефрит, васкулит и обструктивная уропатия лежат в основе внебольничной острой почечной недостаточности. Если последняя возникает в
606
больнице, в качестве этиологических факторов намного более вероятны токсичность ле- карственных средств или недостаточность перфузии.
Острая почечная недостаточность бывает олигурической (менее 15 мл/ч) или неоли- гурической. Летальность при недостаточности первого вида (приблизительно 50 %) по крайней мере вдвое выше. По-видимому, дело в большой частоте шока и сепсиса, которые
ведут к олигурической форме. Так как 25—50 % случаев острой почечной недостаточности вызвано сниже-
нием ОЦК или применением нефротоксичных лекарственных средств, ключевую роль иг- рает профилактика. Острая почечная недостаточность может быть следствием разнооб- разных причин, действующих посредством одного из трех механизмов: 1) недостаточной перфузии (преренальный механизм); 2) препятствия оттоку (постренальный механизм); 3) заболевания паренхимы (интраренальный механизм) (рис. 29.1).
ПРЕРЕНАЛЬНАЯ НЕДОСТАТОЧНОСТЬ Недостаточная перфузия считается причиной половины всех случаев острой по-
чечной недостаточности; следовательно, предотвращение гипотензии или ее быстрое устранение — вероятно, единственная наиболее эффективная терапия. Хотя одна только длительная почечная ишемия может привести к острой почечной недостаточности, в большинстве случаев она имеет многофакторную этиологию (например, сепсис, ле- карственные средства и гипотензия). В целом среднее артериальное давление ниже 60—70 мм рт. ст., некорригируемое более 30 мин, связано с риском повреждения почек. Недос- таточная перфузия почек может быть обусловлена циркуляторной недостаточностью, ги- потензией, обструкцией сосудов (например, стенозом почечной артерии, васкулитом или эмболией, мягким тромбом или сгустком холестерина) или же неправильным распределе- нием сердечного выброса (как при сепсисе). Значительное увеличение давления внутри брюшной полости, обычно превышающее 40 мм рт. ст., в результате накопления асцити- ческой жидкости, крови или послеоперационного отека также может воздействовать на преренальный механизм. Гепаторенальный синдром и почечная реакция на положитель- ное давление в конце выдоха (ПДКВ) напоминают преренальный механизм, снижая кро- воток в фильтрующих клубочках.
Преренальные причины: гипотензия, аневризма аорты, стеноз почечной артерии,
тромбоз почечной вены Ренальные причины: острый тубулярный некроз, интерстициальный нефрит, гломе-
рулонефрит. лекарственные средства Постренальные причины: камни, опухоли, гипертрофия простаты
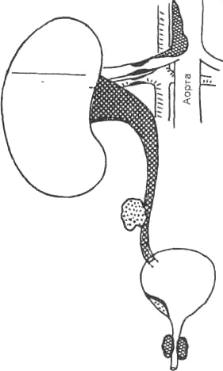
607
Рис. 29.1. Частые причины острой почечной недостаточности в отделении интенсив- ной терапии.
Показатели объема циркулирующей крови / Ортостатические изменения артериального давления служат клиническим показате-
лем состояния ОЦК у здоровых людей. Но у большинства больных в критическом состоя- нии этим способом проверить ОЦК не удается. Недостаточность ауторегуляции может сделать эти изменения менее надежным признаком у больных диабетом, у пожилых или прикованных к постели пациентов. Сухие слизистые оболочки, вялость кожи и ее недос- таточная влажность также могут быть признаками гиповолемии. К сожалению, на эти при- знаки нельзя положиться у пациентов с гиперпноэ и людей преклонного возраста.
Поскольку атравматичные методы оценки жидкостного баланса (рентгенография легких и эхокардиография) не обладают чувствительностью для оценки снижения ОЦК, часто предпринимается инвазивный мониторинг (см. главу 2 "Мониторинг ге- модинамики"). Потребность в таком контроле, однако, спорна, так как никакие специфи- ческие значения давления заклинивания, сердечного выброса или общепериферического
сосудистого сопротивления определенно не указывают на достаточный или неадекватный почечный кровоток. Таким образом, давление и кровоток на уровне клубочков плохо оце- ниваются гемодинамическими показателями, полученными с помощью введенного в ле- гочную артерию измерительного катетера.
В случае преренальной недостаточности анализ мочи нормален или характеризуется минимальной патологией в виде гиалиновых цилиндров и других неспецифических пара- метров осадка.
Преренальные нарушения побуждают канальцы усиленно реабсорбировать натрий и воду, вследствие чего моча отличается высокой концентрацией и низким содержанием на- трия. Обычно натрий мочи меньше 20 мэкв/л, осмоляльность превышает 500 мосм/л, а удельный вес мочи выше 1,015. Для идентификации преренального нарушения часто ис- пользуют такой показатель, как фракционное выделение натрия (FeNa). Его рассчитывают
как отношение произведения концентрации натрия в моче и концентрации креатинина в плазме к произведению концентрации натрия в плазме и концентрации креатинина в моче.
FeNa = 100 х {[(натрий в моче) х (креатинин в плазме)] [(натрий в плазме) х (креатинин в моче)]}
608
Величина FeNa менее чем 1 % вообще показательна для преренального нарушения, в то время как значение выше 3 % обычно отражает острые канальцевые нарушения типа острого канальцевого некроза. Для того чтобы измерения натрия в моче или FeNa были достоверными, основная способность реабсорбции натрия почечным канальцем не должна быть повреждена.
По этой причине хроническая почечная недостаточность, гипоальдостеронизм и ме- таболический алкалоз могут сделать проверку натрия мочи бессмысленной.
Аналогичным образом, по крайней мере на 24 ч после введения диуретической тера- пии определение натрия в моче будет неточно. Осмотические средства (глюкоза, манни- тол, рентгеноконтрастный материал) также могут нарушить интерпретацию биохимиче- ского состава мочи из-за ее разбавления.
Хотя AM К может быть несоразмерно высоким из-за увеличенного производства мо- чи, являющегося следствием воздействия тетрациклина, кортикостероидов или желудоч- но-кишечного кровотечения, повышенное соотношение «АМК/креатинин» чаще возника- ет из-за уменьшения канальцевого потока мочи и увеличения канальцевой реабсорбции азота мочевины. Следовательно, это соотношение обычно повышено при преренальных нарушениях (более 10:1).
ТАБЛИЦА 29.2 РАЗМЕР ПОЧЕК КАК ПРИЗНАК ЭТИОЛОГИИ ПОЧЕЧНОЙ НЕДОСТА-
ТОЧНОСТИ
Нормальный
Острый гломерулонефрит Острый канальцевый некроз Острый кортикальный некроз Острый интерстициальный нефрит Гепаторенальный синдром
Злокачественная артериальная гипертензия Обструкция почечной артерии Склеродермия
Увеличенный
Амилоидоз Острый гломерулонефрит
Обструктивная уропатия Острый интерстициальный нефрит Тромбоз почечной вены
Острое отторжение трансплантата
Уменьшенный
Хроническая почечная недостаточность Хроническая артериальная гипертензия
Так как почечные канальцы не могут абсорбировать креатинин, уменьшенная ско- рость канальцевого потока не влияет на концентрацию креатинина, если СГФ сохранена. Сравнение выделения мочи с клиренсом креатинина позволяет определить, является ли причиной высокого AM К увеличенное производство мочи или ее уменьшенное выде- ление. Если отношение клиренс мочи/клиренс креатинина превышает 1, вероятная этио- логия — увеличенное производство мочи. Чаще всего клиническая задача состоит в том, чтобы дифференцировать преренальные нарушения от острого канальцевого некроза. В табл. 29.1 сравниваются наиболее частые показатели почечных функций при этих Двух состояниях. Анализ изображения почек при использовании КТ и УЗТ также помогает по- нять причины острой почечной недостаточности (табл. 29.2). В случае чистой прере- нальной азотемии почки должны иметь нормальные размеры при КТ-сканировании, на
609
изображении, полученном при ультразвуковой томографии или методами радиоизотоп- ного исследования. Уменьшенные почки указывают на хронический процесс.
ПОСТРЕНАЛЬНАЯ НЕДОСТАТОЧНОСТЬ После того как были исключены преренальные причины, необходимо рассмотреть
обструктивную или постренальную этиологию (например, мочевые камни, опухоль, ги- пертрофия предстательной железы, сгусток крови, забрюшинное кровотечение). Даже ес- ли обструктивная причина вызывает заболевание только в 1 — 10 % случаев острой по- чечной недостаточности, эту поддающуюся лечению проблему не следует упускать из ви- ду. Характер снижения потока мочи может дать ценный ключ к наличию обструктивного заболевания. Как при преренальной, так и при интраренальной недостаточности олигурия
или анурия обычно развиваются постепенно в течение периода от нескольких часов до нескольких дней, в то время как резкое прекращение выделения мочи часто встречается в случае обструктивной уропатии. (Ясно, что наиболее распространенная причина анурии
— это уретральная обструкция, вызванная увеличением предстательной железы, травмой или сгустком крови.) Обструкция верхней части мочевыводящих путей вызывает анурию только тогда, когда преграда двусторонняя или если она встречается у больного с единст- венной почкой или с дренажем.
Уретральная обструкция может быть немедленно исключена или подтверждена по- пыткой ввести мочевой катетер в мочевой пузырь. Однако из-за высокой частоты патоло- гии мочевыводящих путей сама по себе катетеризация мочевого пузыря никогда не ис- ключает возможности проксимальной обструктивной уропатии. При наличии постоянных катетеров не следует упускать из виду возможность их засорения как потенциальную при- чину внезапной анурии. УЗТ- или КТ-сканирование почек позволяют обнаружить гидро- нефроз и мочевую преграду внутри или проксимальнее мочевого пузыря, а радиоизотоп- ное изображение почек дает возможность оценить поток или функцию канальцев. Внут- ривенная пиелография вряд ли будет полезна при обструктивной уропатии, если не подоз- реваются камни или травма. Кроме того, применяемое для этого исследования контра- стное вещество обладает потенциальной нефротоксичностью.
При обструктивной уропатии анализ мочи обычно бывает нормальным, по крайней мере первоначально, а биохимический анализ редко дает нужную информацию. Извест- ным исключением было бы выявление гематурии, которое предполагает сосочковый нек- роз или обструкцию почечным камнем или сгустком.
ИНТРАРЕНАЛЬНАЯ НЕДОСТАТОЧНОСТЬ Анализ мочи и ее биохимический состав обеспечивают возможность отличить ин-
траренальные причины острой почечной недостаточности (табл. 29.3; см. табл. 29.1) от преренальных. Однако ни один из отдельных показателей почечной функции определенно не указывает на наличие острой почечной недостаточности.
Например, хотя при интраренальной недостаточности фракционное выделение на- трия (FeNa) обычно больше единицы, диуретики, глюкозурия, маннитол и длительная об- струкция мочевых путей могут привести к идентичным показателям.
ТАБЛИЦА 29.3 ОСАДОК МОЧИ ПРИ ОСТРОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ
Осадок мочи |
Этиология почечной недостаточности |
|
|
|
|
Выщелоченные эритроци- |
Гломерулонефрит, васкулит, |
|
ты |
травма |
|
Гемопигментированные |
Гемоглобинурия, миоглобинурия |
|
цилиндры |
|
|
|
610 |
Лейкоцитарные цилиндры |
Пиелонефрит, сосочковый некроз |
Канальцевые цилиндры |
Острый канальцевый некроз |
Мутный зернистый осадок |
Острый канальцевый некроз |
Лейкоциты |
Инфекция мочевого тракта, интерстициальный нефрит |
Эозинофилы |
Интерстициальный нефрит |
Кристаллы |
Ураты, оксалаты (этиленгликоль) |
Подобным же образом, анализ мочи может быть очень информативен, если выявляет эритроцитарные цилиндры, эозинофилы или кристаллы, но он редко дает однозначные результаты. Размер почек также может служить ключом к пониманию этиологии почеч- ной недостаточности: при хронической патологии почки обычно небольшие; напротив,
при острой почечной недостаточности намного чаще отмечаются почки нормального или увеличенного размера. Увеличение почек показательно для ограниченного числа острых заболеваний, включающих обструкцию, тромбоз почечной вены и отторжение трансплан- тата (см. табл. 29.2).
Существует три категории острой интраренальной недостаточности: 1) нарушения канальцев; 2) интерстициальный нефрит; 3) гломерулонефрит или васкулит мелких сосу- дов.
Нарушения функции канальцев После преренальной азотемии нефротоксичные лекарственные средства — наиболее
частая причина острой почечной недостаточности. Риску лекарственной почечной не- достаточности особенно подвержены пожилые или обезвоженные пациенты, страдающие гипертонией, диабетом, а также больные с умеренной дисфункцией почек и миеломой в качестве основного заболевания. Аминогликозиды, контрастные вещества, циклоспорин, содержащие платину препараты, ингибиторы ангиотензинпреобразующего фермента (АПФ) и нестероидные противовоспалительные средства (НСПВС) — наиболее часто ус- танавливаемые причины нарушения канальцев.
Аминогликозиды вызывают почечную недостаточность у 10—20 % всех больных, которые их получают, связывая и повреждая клеточные протеины в проксимальной части канальцев. Вследствие этого возникает острый канальцевый некроз, который наиболее вероятен, когда поддерживается повышенный уровень лекарственного средства в плазме. (Пиковые уровни аминогликозидов коррелируют с антибактериальной эффективностью, в то время как минимальные уровни указывают на токсичность.) Токсичность усугубляется предшествующим почечным заболеванием, снижением ОЦК и сопутствующим приемом других нефротоксичных средств.
В связи с наиболее часто применяемыми аминогликозидами риск развития острой почечной недостаточности отличается весьма незначительно. Поскольку на повреждение почек влияет длительное выделение лекарственного средства почечными канальцами, а Не его пиковые уровни, риск нефротоксичности уменьшают, назначая аминогликозиды один раз в день (обычно 5 мг/кг). Эта схема дозирования также более удобна и стоит де- шевле. Так как продолжительность выделения — наиболее существенный фактор риска токсичности, ограничение продолжительности терапии и более редкая дозировка снижают риск. Частые ошибки при использовании аминогликозидов состоят в их многократном
ежедневном введении и эмпирическом длительном лечении больных с высоким риском токсичности без четких к тому показаний. Эта тенденция не ограничивается аминоглико-
