
2683
.pdf
городке открыты. Поскольку |
площадь первого отверстия |
S 2 , а площадь второго - S |
S , влиянием отверстия 1 на |
1 |
|
процессы переноса по отношению ко второму отверстию можно пренебречь. В стационарном состоянии системы потоки молекул через отверстие 2 слева – направо и справа – налево
будут одинаковы, |
а давления в половинах сосуда равны, |
||||||||
p1 p2 . Отсюда получаем: |
|
|
|
|
|
||||
|
m1RT1 |
|
m2RT2 |
|
|
|
~ |
~ |
|
|
|
|
|
|
m1T1 |
m2T2 n1mT1 |
n2mT2 |
||
|
VM |
VM |
|||||||
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
n1T1 n2T2 |
|
T1 |
|
(1) |
||
|
|
|
|
||||||
|
|
|
n2 T |
n1 . |
|||||
~ |
|
|
|
|
2 |
|
|
||
|
|
|
|
|
|
|
|
||
Здесь m - масса молекулы. |
|
|
|
|
|||||
Теперь перейдем к случаю, |
когда большое отверстие 2 |
||||||||
перекрывается. Число молекул, самопроизвольно переходящих в единицу времени через отверстие 1 из первой половины сосуда во вторую равно
1
N1 4 1 n1S,
А с противоположной стороны
1
N2 4 2 n2S,
В стационарном состоянии N1 N2 т.е.
|
2 |
|
1 n1 |
n2 . |
(2)
(3)
(4)
Отсюда имеем:
|
|
T1 |
|
|
|
|
|
n2 |
|
|
|
T1 |
|
|
|
n1 |
|
T2 |
n2 |
|
T2 n1 . |
(5) |
|
Сравнительное изменение концентрации молекул во второй половине сосуда определим отношением, следующим из
(1) и (5):
|
|
T2 |
|
|
|
|
n2 |
|
|
n1 |
. |
(6) |
|
n2 |
T1 |
|
||||
|
|
n1 |
|
|||
|
181 |
|
|
|
|
|

Далее воспользуемся балансом частиц:
|
|
|
|
|
|
|
|
|
|
|
T1 |
|
|
|
|
|
|
T1 |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
T |
|||||||||||||||||||||
n1 n2 n1 |
n2 n1 T |
n1 n1 |
n1 |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
2 |
|
|
|||||||
|
|
|
n1 |
|
|
|
|
|
|
T1 T2 |
|
. |
|
|
|
|
(7) |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
n1 |
|
T2 ( T1 T2 ) |
|
|
|
|
|
|||||||||||||||||||
Подставляя (7) в (6), получаем: |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
T1 T2 |
|
|
|
|
|
|
|
|
1 T2 |
/T1 |
|
|
|
|
||||||||||||
|
n2 |
|
|
|
|
|
|
|
|
|
|
. |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
n2 |
|
|
T2 T1T2 |
1 T2 /T1 |
|
|
|
|
|
||||||||||||||||||||
По условию T2 /T1 , следовательно, |
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
n2 |
|
|
|
1 |
. |
|
|
|
|
|
|
(8) |
|||||||||||
|
|
|
|
|
|
|
n2 |
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
6.207. Из формул для вязкости и коэффициента диффузии
|
|
1 |
и D |
1 |
|
, |
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
||||||||
а также соотношений |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
и |
nM |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
, |
|
8RT |
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
2 |
n |
|
|
|
|
|
|
|
|
|
|
|
|
M |
|
|
|
|
|
|
|
|
|
|
N |
A |
|||||||||||
|
|
|
|
|
2 d |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Получаем: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D |
T |
|
3/2 |
|
|
p |
|
|
|||||||||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
T |
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
, |
|
|
2 |
|
|
2 |
|
|
|
|
|
|
|
|
1 |
. |
|
|
|
||||||||||||
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
T |
|
D |
|
|
T |
|
|
|
|
|
|
|
|
p |
2 |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
1 |
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
По условию |
2 |
|
, |
|
D2 |
|
|
. Тогда |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
1 |
|
D1 |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3/2 |
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
p2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
p |
|
|
|
|
T |
|
/ |
|
|
|
. |
|
|
|
|
|
|||||||||||||||||
Для 2 |
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
и 4 давление газа увеличилось в 2 раза. |
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
182 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
6.208. Выясним как изменяется коэффициент диффузии D и вязкость идеального газа при увеличении его объема в r раз в процессе:
а) изотермического расширения. Воспользуемся формулами
|
|
|
|
|
D |
1 |
, |
1 |
, |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
а также |
|
|
|
|
3 |
|
|
|
|
3 |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
~ |
nM |
|
||||
|
|
|
|
|
|
|
|
|
, |
8RT |
. |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
и nm |
|
|
||||||||
|
|
|
|
|
2 |
|
|
M |
N |
|
|||||||||||||||
|
|
|
|
|
n |
|
|
|
|
A |
|
||||||||||||||
2 |
|
d |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
При этом получим |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
D2 |
|
2 |
|
|
|
n1 |
|
N /V1 |
r ,увеличивается, |
|
||||||||||||||
|
|
1 |
|
|
n2 |
|
|
||||||||||||||||||
|
D1 |
|
|
|
|
|
|
|
N /V2 |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
2 |
|
2 2 |
|
r |
1 |
1 ( const). |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
1 |
1 1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
r |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
б) изобарического расширения: |
|
|
|
|
|
|
|
|
|
|
|
3/2 |
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
D2 |
|
|
2 2 |
|
|
n1 |
|
|
|
T2 |
|
|
|
|
|
N /V1 |
|
|
V2 |
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
V2 |
|
|
|
r3/2 |
; |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
N /V V |
|
|
|
|
||||||||||||||||||||||||||||||||||
|
D n T |
|
|
|
|
|
|
|
|
|
V |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
1 |
|
1 1 |
2 |
|
1 |
|
|
|
|
|
|
|
2 |
|
|
1 |
|
|
|
|
1 |
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
2 |
|
2 2 2 |
|
n1 |
|
|
|
|
|
|
|
n2 |
|
|
|
|
|
|
|
|
|
|
|
|
. |
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
T2 |
|
|
|
T2 |
|
|
|
V2 |
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
r |
|
|||||||||||||||||||||||||||||||||
|
|
1 |
|
|
1 1 1 |
|
|
|
n2 |
|
|
|
|
T1 |
|
|
n1 |
|
|
|
T1 |
|
|
|
|
|
V1 |
|
|
|
|
||||||||||||||||
6.209. Объем двухатомного идеального газа адиабатически уменьшается в r 10 раз. Выяснить, как изменяются D и
Изменение величин D и будем характеризовать отно-
шениями |
D2 |
и |
2 |
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
D1 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
D2 |
|
2 2 |
|
n1 |
|
|
|
|
|
N /V1 |
|
|
|
|
|
V2 |
|
|
|
|
||||
|
|
|
|
|
T2 |
|
|
T2 |
|
|
T2 |
|
|||||||||||||
|
D1 |
|
|
T1 |
N /V2 |
T1 |
|
T1 |
|
||||||||||||||||
|
|
|
1 1 n2 |
|
|
|
|
|
|
|
V1 |
|
|
|
|||||||||||
183

|
|
|
|
|
T2 |
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
V1 |
|
|
, находим |
|
|
|
|
|
|
|
|||||||||||
Учитывая, что T |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
V |
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
1 |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
D2 |
|
( 3)/2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
V1 |
|
|
|
|
|
|
|
|
r( 3)/2 r(1 i)/i 1/r(1 i)i . |
|||||||||||||||
|
|
|
D |
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
V |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
1 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
2 |
|
2 2 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
( 1)/2 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
n1 |
|
|
T2 |
|
|
n2 |
|
|
T2 |
|
|
V1 |
|
. |
|||||||||||
|
|
|
|
|
|
|
T |
|
||||||||||||||||||||
|
|
|
|
|
n |
2 |
|
|
T n |
|
|
V |
|
|
||||||||||||||
1 |
|
1 |
1 |
|
|
1 |
|
|
|
|
|
|
|
1 1 |
|
1 |
|
2 |
|
|
||||||||
r( 1)/2 r1/i .
При r 10 и i 5
D1 104/5 6,3; 2 101/5 1,6.
D2 |
1 |
6.210. Найдем показатель политропы n процесса, совершаемого идеальным газом, в котором неизменны:
а) коэффициент диффузии;
Из условия D 1 const следует: 
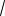 T const
T const
3

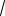 T /n const . Поскольку n N/V , где N – число молекул, V
T /n const . Поскольку n N/V , где N – число молекул, V 
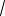 T const , т.е. TV 2 const . Сравнивая с уравнением полит-
T const , т.е. TV 2 const . Сравнивая с уравнением полит-
ропы TVn 1 const |
, получаем n 1 2, т.е. n 3. |
||||||||
б) вязкость; |
|
|
|
|
|
|
|
||
|
1 |
|
|
|
T |
~ |
|
|
|
|
|
|
|
|
|
||||
|
|
const |
|
|
|
(nm const) T const |
|||
3n
процесс изотермический; TVn 1 const . Так как T const,
то величина V n 1 |
не должна зависеть от n, тогда n 1 0 и |
||||||||
n=1. |
|
|
|
|
|
|
|||
в) теплопроводность; |
|
|
|
||||||
|
1 |
C |
const |
1 |
|
|
n const T const |
||
|
T |
||||||||
|
|
||||||||
3 |
|
V |
|
n |
|
|
|
||
|
|
|
|
|
|
||||
Следовательно, как и в пункте б) n=1.
184
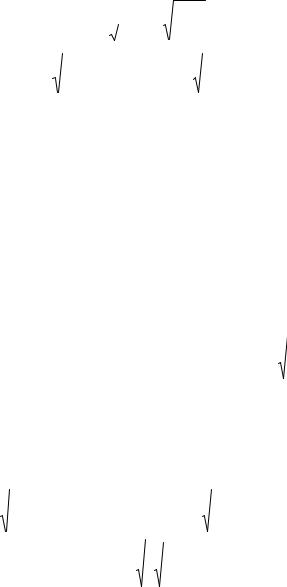
6.211. Вязкость гелия при нормальных условиях известна. Вычислить эффективный диаметр его атома.
|
1 |
|
1 |
|
|
|
|
8RT |
|
nM |
|
|
||||||||||
|
|
|
|
|
|
|
M |
|
||||||||||||||
3 |
|
|
|
|
|
|
|
|
2 |
n |
|
|
N |
A |
||||||||
|
|
|
|
|
|
|
|
3 2 d |
|
|
|
|
|
|
||||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
2 |
|
|
|
1/2 |
||||||
|
|
|
|
8RT |
|
|
|
|
|
|
|
MRT |
||||||||||
|
|
|
|
|
|
d |
|
|
|
|
|
|
|
|
|
|
||||||
3 d2NA |
|
|
3 NA |
3 |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Для гелия 18,9мкПа с , M=4 10-3 кг/моль.
При Т=273 К d=0,18 нм.
6.212. Величинам, относящимся к гелию, присвоим знак 1, к аргону – 2. По условию 1 / 2 r 8,7 Требуется найти отношение эффективных диаметров молекул d2 /d1 .
На основании формулы для теплопроводности идеального газа можно написать
|
|
|
|
|
|
|
|
1 |
|
|
|
|
1 |
1 1CV |
r . |
|
|
|
|
|
|
(1) |
|||
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
2 |
|
2 2 2CV21 |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
d2n |
|
|
|
d |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
2 |
|
|
2 |
|
|
|
|
|
M |
2 |
|
|
|||||||||||
Здесь |
|
1 |
|
2 |
|
|
|
|
|
, т.к. n1 n2 |
; |
|
1 |
|
|
|
|
при |
|||||||
|
2 |
d2n |
|
|
d |
1 |
|
|
2 |
|
M |
1 |
|
||||||||||||
|
|
|
1 1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Т1=Т2=Т, М1, М2 – молярные массы газов;
|
|
|
1 |
|
|
M1 |
|
; |
CV1 |
|
CV / M1 |
|
M2 |
|
, i=3 для обоих газов. |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
2 |
M2 |
CV 2 |
CV /M2 |
M1 |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
Учитывая указанные отношения, получаем: |
||||||||||||||||||||||||||||||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|||||||
2 |
|
|
|
M2 |
|
|
M1 |
|
M2 |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
d |
|
|
|
|
|
|
|
r |
|
d2 |
|
|
|
|
|
M2 |
|
r, т.е. |
|||||||||||||||||||
d |
1 |
|
|
|
|
M |
1 |
|
|
|
M |
2 |
|
M |
1 |
|
|
|
|
d |
|
|
|
|
|
|
M |
1 |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
d2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
r |
|
|
|
M1 |
. |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
d1 |
|
|
|
|
|
M2 |
|
|
|
|
|
|
|
|
|||
185

Для гелия M1=4 г/моль, аргона M2=40 г/моль. При r=8,7 отношение эффективных диаметров молекул аргона и гелия
равно d2 1,7. d1
6.213. Описание движения жидкости или газа между стенками вращающихся коаксиальных цилиндров представляет собой сложную задачу. Поэтому мы будем исходить из простейших моделей движения частицы газа при вычислении сил трения между его частями.
Введем обозначения: R1 – радиус внутреннего цилиндра, R2 - внешнего, R R2 R1 – зазор между стенками цилинд-
ров; R R1 R2 - средний радиус зазора.
2
Молекулы газа при соударениях со стенкой внешнего цилиндра приобретают дополнительную касательную скорость, обусловленную вращением этого цилиндра, равную u R2 . Молекулы у поверхности внутреннего цилиндра не получают такой скорости, поскольку он находится в покое. Так какR R1,R2 , то можно воспользоваться линейной зависимостью ротационной скорости u при переходе от поверхности внутреннего цилиндра к поверхности внешнего и тем самым определить градиент направленной скорости:
grad(u) |
u(R2) u(R1) |
|
R2 0 |
|
R2 |
0. |
|
R2 R1 |
R |
R |
|||||
|
|
|
|
Сила трения F и момент N этой силы, действующие на поверхность внутреннего цилиндра, численно соответственно равны:
F grad(u) S R2 2 R1 (для 1),
R
N R1F 2 R2R12 .
R
186

Полагая R2R12 R3 , для момента сил трения, действующего на внутренний цилиндр, найдем:
N |
2 R3 |
. |
(1) |
|
R
Сила F действует в направлении вращения внешнего цилиндра.
Теперь перейдем ко второму случаю, когда при уменьшении давления газа момент сил трения N 2 уменьшается в r
раз по сравнению с N1 в первом случае. Так как r = 10 – сравнительно большая величина, то следует предположить, что газ во втором случае будет находится в состоянии вакуума, в котором длина свободного пробега молекул и ширина зазора R - величины одного порядка. В этом случае молекулы после отражения от стенки внешнего цилиндра без столкновений будут двигаться к стенке внутреннего цилиндра.
При столкновении со стенками внешнего вращающегося
цилиндра |
~ |
молекула |
получает |
момент |
импульса |
|
~ |
2 |
. Число ударов молекул на единицу площади |
||||
m( R2)R2 |
m R2 |
|||||
стенки за единицу времени равно
1 n (точнее 1 n ),
64
ана цилиндрическую поверхность радиуса R2 и единичной
длины число ударов q 2 R2 nR2 /3. При этом передаваемый за единицу времени момент импульса
dL |
~ 3 |
1 |
3 |
, |
(2) |
|
|
(mR2 ) q |
|
nR2 |
|||
dt |
3 |
|||||
|
|
|
|
~ ~
где mn , m – масса молекулы.
В стационарном состоянии и при отсутствии столкновений молекул между собой систему газа можно рассматривать как изолированную систему. Молекулы, отразившись от стенки вращающегося цилиндра и свободно пролетая промежутокR , ударяются о неподвижную стенку внутреннего цилиндра, полностью передавая ей момент импульса. Таким образом, для
187

момента сил трения на поверхности внутреннего цилиндра (на единицу длины) получаем выражение
N |
|
|
dL |
|
1 |
nR3 |
. |
(3) |
|
|
|
||||||
|
2 |
|
dt 3 |
2 |
|
|
||
Обозначая момент N, определяемый формулой (1) через
N1 , для отношения N1 получим:
N2
|
N1 |
|
6 |
|
|
6 |
|
|
|
|
2 |
|
2 |
|
|
1 |
|
|
||||||||||
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
N |
2 |
|
R |
|
|
R |
|
R |
R |
2 |
n |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 d |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
kT |
. |
|
|
|
|
|
|
||||||||
|
|
|
|
|
2 |
|
2 |
|
|
|
|
|
(4) |
|||||||||||||||
|
|
|
|
|
d2n R |
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
d2 p R |
|
|
|
|
|
|
|
||||||||||||||
При условии N1 / N2 r совместно с (4) находим, что |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
kT |
. |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
p |
|
2 |
|
|
|
|
|
(5) |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
d2r R |
|
|
|
|
|
|
|
|
|
|
|
|||||||
При Т=273 К, d=0,27 нм, r=10, R 6мм давление р=0,7 Па.
6.214. В формуле для поверхностной плотности сил тре-
ния
r , (1)
r
перейдем к линейной круговой скорости цилиндрических слоев газа:
r |
u |
u |
|
u |
|
|||||
|
|
|
|
|
|
|
|
. |
(2) |
|
|
|
|
|
|||||||
|
r r |
r |
|
r |
|
|||||
Представим равенство (2) через новую независимую переменную x r R1:
188

|
|
u x |
|
u |
|
|
u |
|
u |
|
|
|||
(x) |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
||||||
x r |
x R |
x |
x R |
(3) |
||||||||||
|
|
|
. |
|||||||||||
|
|
|
|
|
1 |
|
|
|
1 |
|
|
|||
Поскольку угловая скорость вращения внешнего цилиндра мала, можем на промежутке (R1,R2) по переменной x определить градиент круговой скорости выражением
|
u |
|
u(R2) u(R1) |
|
R2 |
|
, т.к. u(R ) 0. |
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
|
x |
|
|
R2 R1 |
|
|
|
R2 R1 |
|
1 |
|
|||||
|
|
|
|
|
|
|
|
|
||||||||
Вместо (3) имеем: |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
R2 |
|
|
|
u |
|
|
|
|||
|
|
|
|
(x) |
|
|
|
|
|
|
(4) |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
R R x R |
. |
|||||||||||
|
|
|
|
|
|
2 |
|
|
1 |
|
|
|
|
1 |
|
|
Для x 0 |
и r R , (x) |
R2 |
. |
|
|
|
||||||||||
|
|
|
|
|||||||||||||
|
|
1 |
|
|
|
R2 R1 |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
При этом сила трения F и ее момент, действующие на поверхность внутреннего покоящегося цилиндра единичной длины, соответственно равны
|
|
2 R R |
, N R F |
2 R2R |
|
|||
F 2 R |
1 |
2 |
1 |
2 |
. |
(5) |
||
|
|
|||||||
1 |
1 |
R R |
1 1 |
R R |
|
|||
|
|
2 |
1 |
|
2 |
1 |
|
|
Из равенства (5) находим коэффициент вязкости газа:
|
N1(R2 R1) |
|
N1 |
|
1 |
|
1 |
|
|
|
|
|
|
|
|
(6) |
|||||
2 R2R |
2 |
|
R R |
|||||||
R2 |
. |
|||||||||
|
1 2 |
|
|
|
1 |
|
1 2 |
|
|
|
Если положить, что R 
 R1R2 есть средний радиус, то
R1R2 есть средний радиус, то
|
N1 |
|
1 |
|
1 |
|
|
|
|
|
|
|
(7) |
||||
2 |
|
R2 |
||||||
R2 |
. |
|||||||
|
|
|
1 |
|
|
|
|
|
189

6.215. Здесь градиент круговой скорости u между слоями газа зависит от расстояния r до оси дисков. Градиент этой скорости вдоль оси вращения z определим выражением
du u(r) r , dz h h
где h - ширина зазора между дисками. Сила трения dF и момент dN, действующие на кольцевой элемент поверхности неподвижного диска, равны:
dF du dS r 2 rdr 2 r2dr ,
dz |
h |
h |
dN rdF 2 r3dr . h
Полный момент сил трения, действующий на неподвижный диск равен
|
2 |
a |
a |
4 |
|
N |
r3dr |
|
. |
||
h |
2h |
|
|||
|
0 |
|
|
6.216. В этом случае молекулы газа свободно, без столкновений с другими молекулами, летают между внутренними
поверхностями |
со |
средней |
тепловой |
скоростью |
|
|
8RT / M |
. Молекулы ультраразреженного газа, ударя- |
|||
ясь о стенку вращающегося диска и получая круговую скорость, переносят момент импульса на неподвижный диск.
При столкновении с поверхностью вращающегося диска
молекула получает момент импульса, равного |
~ |
~ |
2 |
, где |
mur m r |
|
|||
~ – масса молекулы. На кольцевой элемент этого диска ра- m
диуса r и ширины dr ударяется за единицу времени d 1 n 2 rd 1 n rdr молекул.
6 |
3 |
|
|
|
|
|
|
|
|
|
Эти же молекулы получают за единицу времени момент |
||||||||||
импульса |
|
|
|
|
|
|
|
|
|
|
dL |
~ |
2 |
|
|
1 |
|
3 |
|
||
d |
|
|
m r |
|
d |
|
|
r |
|
dr |
|
|
3 |
|
|||||||
dt |
|
|
|
|
|
|
|
|||
|
|
|
|
190 |
|
|
|
|
|
|
