
2683
.pdf
Постоянная b характеризует ту часть объема V, которая не доступна для движения молекул и равна нескольким значениям суммарного объема молекул, содержащихся в моле газа.
При значительном расширении газа поправки a/Vm2 и b
по сравнению с основными величинами p и Vm будут малыми величинами, которыми можно пренебречь, в результате чего уравнение (2) переходит в уравнение (1).
Рассмотрим следующий пример. Имеется некоторый газ при нормальных условиях, для которого постоянная b 40см3 / моль. Найдем среднюю длину свободного пробега молекул газа.
Средняя длина свободного пробега |
вычисляется по |
||||||
формуле |
1 |
|
|
|
|||
|
|
. |
(3) |
||||
|
|
|
|
|
|||
|
|
|
2 d2n |
|
|||
В заданных условиях плотность молекул газа равна |
|||||||
n |
p0 |
, |
|
(4) |
|||
kT0 |
|
||||||
|
|
|
|
|
|||
где p0 и T0 – давление и температура газа при н.у.
Полагая, что форма молекулы сферическая радиуса r d/2, а также и то, что постоянная b примерно равна четырем значениям полного объема самих молекул, можем написать:
b 4VM NA |
4 |
4 |
r3NA |
|
2 |
d3NA . |
(5) |
|
|
||||||
|
3 |
|
3 |
|
|
||
Здесь VM – объем молекулы, NA - число Авогадро. Из равенства (5) имеем:
|
|
|
|
|
2 |
|
|
|
|
|
|
|
3b |
|
|
|
|
|
2 |
|
3 |
|
||||
d |
|
|
|
|
|
(6) |
||
|
|
|||||||
|
|
|
. |
|||||
|
|
|
|
2 NA |
|
|||
Подставляя (4) и (6) в (3), получим:
1 |
|
2 N |
2 |
kT |
|
|
|
kT |
2 N |
|
|
2 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
A |
3 |
|
|
A |
3 |
|
||||||||||||||
|
|
|
|
|
|
|
|
0 |
|
|
|
0 |
|
|
. |
||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
2 |
|
3b |
|
|
|
p0 |
|
|
|
2 p0 |
|
3b |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
||||||||||||
171
6.197. Пусть - средняя длина свободного пробега молекул азота при заданных p0 и T0, - длина звуковой волны. При этом
|
|
1 |
(1), |
c |
(2). |
|
|
|
|
|
|||
|
|
2 d2n |
|
|||
где c 
 RT0 /M - скорость волны, - частота волны. По условию . Получаем:
RT0 /M - скорость волны, - частота волны. По условию . Получаем:
|
1 |
|
RT0 |
|
|
|
|
1 |
|
|
|
d2n |
2 RT0 |
|
|
|
|||||||
|
|
M |
|
|
|
|
|
|
|
|
|
M |
|||||||||||
|
|
|
|
2 d2n |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
p0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
d2 |
|
|
|
2 RT0 |
|
d2 |
N |
|
|
|
2 |
, |
|||||||||
|
|
|
|
A |
MRT |
||||||||||||||||||
|
|
|
|
|
kT |
|
|
M |
0 |
|
|
|
|
|
|||||||||
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|||||
где k R/ NA . |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Для азота М=28 10-3 |
кг/моль ; 1,4; |
|
d 0,37нм. При |
||||||||||||||||||||
нормальных условиях p0 105 Па , T0 300К . Частота волны
0 5,5Гц.
6.198. Кислород находится при T0 273К в сосуде с ли-
нейным размером . Требуется найти:
а) давление газа, ниже которого средняя длина свободного пробега молекул :
|
1 |
|
|
kT0 |
, |
||
|
|
|
|
|
|
||
|
2 d2n |
|
|
2 d2 p |
|||
где n p/kT0 . Отсюда имеем:
|
|
|
p |
|
kT0 |
. |
|
|||
|
|
|
|
|
|
|||||
|
|
|
|
|
2 d2 |
|
|
|||
Для O2 |
d 0,35нм, тогда |
|
|
|||||||
p |
|
|
1,38 10 23 273 |
Па, т.е. |
p 0,7Па . |
|||||
|
|
|
|
|
|
0,7 |
||||
|
|
|
|
|
|
|||||
|
|
2 (0,35 10 9 )2 10 2 |
|
|
||||||
|
172 |
|
|
|
|
|
|
|||

б) среднюю концентрацию молекул. В формуле (1) заменяем р на nkT0 и получаем:
|
|
1 |
|
|
1 |
|
20 |
|
м |
3 |
14 |
см |
3 |
||
n |
|
|
|
|
|
|
|
2 10 |
|
(1/ |
|
) 2 10 |
|
||
|
|
d2 |
|
|
(0,35 10 9)2 10 2 |
|
|
|
|||||||
|
2 |
2 |
|
|
|
||||||||||
в) среднее расстояние между молекулами. Полное число молекул в сосуде N nV n 3 . Среднее расстояние между
молекулами газа должно удовлетворять условию s |
|
1 |
|
, т.е. |
|||||||||
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
3 |
N |
|||
s |
1 |
|
|
|
1 |
|
0,17 10 4 |
17мкм. |
|||||
|
|
|
|
|
|
||||||||
|
3 n |
10 2 3 2 1020 |
|
|
|
|
|
|
|
||||
Итак, s 20мкм.
6.199. Среднее число столкновений молекулы за одну секунду определяется выражением
|
|
|
|
|
2 d2 n, |
(1) |
где |
8RT |
- |
средняя скорость |
молекулы, |
||
|
||||||
|
|
M |
|
|
||
n p/kT NA / RT – плотность молекул газа в заданном состоянии p, V, T. Для азота d 0,37нм. Для T 273К и p 105 Па число 0,74 1010 c 1.
Перед тем как определить число всех столкновений между молекулами в заданном объеме за одну секунду, заметим: 1) столкновения молекул носят парный характер, событие одновременного столкновения какой-либо молекулы с двумя другими чрезвычайно редкое, не говоря уже о столкновении с большим число молекул; 2) столкновения – случайные и независимые события.
Теперь допустим, что произошло столкновение двух некоторых молекул. Каждой из двух молекул можно приписать 1/2 столкновения. Это условие необходимо учесть при расчете
173
общего числа столкновений молекул между собой в заданном объеме V за одну секунду. Это число равно
|
z |
1 |
nV |
1 |
|
|
d2n2 V |
|
|||||
|
|
2 |
|
||||||||||
|
|
|
|
||||||||||
или |
2 |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
z d2n2 |
V / |
|
, |
|
|
(2) |
||||||
|
2 |
||||||||||||
где d 0,37нм, |
n NA / RT , |
|
|
|
8RT |
|
, |
T 273К , |
|||||
|
|
|
|||||||||||
V 1см3 , М=28 10-3 кг/моль. |
|
|
|
|
|
|
M |
|
|||||
|
|
|
|
|
|
|
|
|
|
||||
6.200. Покажем зависимость средней длины свободного пробега и числа столкновений молекулы в единицу времени от температуры Т идеального газа в следующих процессах:
а) изохорическом;
|
|
|
|
|
|
|
|
|
|
|
|
1 |
, |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
2 d2n |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
n |
p |
|
NA |
|
NA |
|
|
mRT |
|
mNA |
|
|
c const |
|
|||||
|
|
|
|
|
|
|
|
||||||||||||
|
kT |
|
RT RT |
|
|
|
MV |
|
|
MV |
|
1 |
|
||||||
|
|
|
|
|
|
|
|
|
V |
|
|||||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
1 |
|
|
|
|
c const. |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
2 d2c |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
Длина не зависит от Т (остается постоянной). Число столкновений
|
|
|
1 |
|
8RT |
const |
|
, |
|
|
T |
||||||||
|
|
|
M
const
где const |
1 |
|
8R |
. |
|
|
|||
|
|
M |
||
б) изобарическом;
n |
p |
, |
|
|
kT |
|
|
|
cT , |
|
|
|
|
|
|
|
|||||
|
kT |
|
|
2 d2 |
p |
|
p const |
|||
|
|
|
174 |
|
|
|||||
|
|
|
|
|
|
|
|
|||
где c |
|
|
k |
|
const , ~T . |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
2 d2 p |
|
|
|
|
|
|
|
|
|
|
|
||||||
Число столкновений |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
/cT |
const |
|
, т.е. ~ |
|
|
|
|
||
|
|
|
|
|
|
8RT |
|
1 |
|
. |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
M |
T |
|
T |
|||||||||
6.201. Идеальный газ совершил определенный процесс так, что давление возросло в раз. Выяснить, как и во сколько раз изменились средняя длина свободного пробега и число столкновений молекулы за единицу времени, если:
а) процесс изохорический;
|
|
|
1 |
, n |
p |
|
NA |
, RT |
MV |
|
|
|
|
|
|
|
|||||
|
|
2 d2n |
|
kT RT |
|
m |
||||
1MV

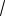 2 d2 mNA V const c1 const
2 d2 mNA V const c1 const
Средняя длина пробега не зависит от давления. Число столкновений
|
|
|
1 |
|
|
8RT |
|
|
1 |
|
|
|
|
8 |
|
|
|
pMV |
|
|
|
c2 |
|
||||||||||
|
|
|
|
|
|
|
|
|
p |
||||||||||||||||||||||||
|
|
|
|
|
M |
|
|
|
|
|
|
|
m |
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
M |
|
|
|
,V const |
||||||||||||||||||
б) давление р: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1/ |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
1 |
|
|
|
, n |
|
N |
, V |
V |
|
p1 |
|
c p1/ ; |
||||||||||||||||||
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
2 d |
|
n |
|
|
|
|
|
|
V |
|
|
|
|
|
p |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
p |
1/ |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
n |
|
|
|
|
|
c2 p |
1/ |
; |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
V |
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
p |
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
||||||
175

|
|
1 |
c p 1/ . |
(1) |
|
|
|
|
|||
|
|
2 d2c2 p1/ |
3 |
|
|
|
|
|
|
||
Число столкновений: |
|
|
|||
|
|
|
|
8RT |
|
|
p1/ |
c p1/ |
|
; |
|
|
T |
||||||||||
|
|
|
|||||||||
|
|
M c3 |
4 |
|
|
||||||
|
|
|
|
||||||||
|
pV |
|
|
p1 |
1/ |
c p( 1)/ , |
|
|
T |
pV |
|
|
(2) |
||||
|
|
|||||||
|
R |
1 |
|
p |
|
5 |
|
|
|
|
|
|
|
|
1/ ( 1)/ 1/2 * ( 1)/2
c4 p c5 p c p
Для 1,4 ~ p6/7 .
в) температуры Т:
1V

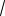 2 d2 N c6V ,
2 d2 N c6V ,
|
|
|
N |
|
|
1 |
|
|
|
|
c |
|
|
|
|
|
|
|
|
|
|
||||
|
|
1 |
|
|
|
|
|
|
) |
|
|
|
|
5/2 |
|
||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
V V |
|
|
1 |
|
|
|
|
|
7 |
|
c T1/(1 |
|
c T |
, |
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
1 |
|
N |
|
|
|
T |
1/( 1) |
7 |
|
|
1,4 |
7 |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
1 |
T |
1 |
c T |
|
|
|
|
||||||||||
|
|
|
|
8RT |
|
( 1)/2( 1) |
|
|
c T3 . |
||||||||||||||||
|
|
|
|
|
|
1 |
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
M |
|
|
c7 |
8 |
|
|
|
|
1,4 |
8 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
По пункту в) получим:
~ T 5/2 , ~T3 .
6.202. На основании формул для средней длины свободного пробега и частоты столкновений молекул идеального газа
|
|
1 |
|
c1 |
(1), |
|
|
8RT |
c |
|
T |
(2), а также эк- |
||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
||||||||
|
|
2 d2n n |
|
|
M |
2 |
|
|||||||
вивалентных |
уравнений |
адиабаты |
|
pV const |
(3), |
|||||||||
TV 1 |
const (4) и уравнения состояния газа pV mRT /M (5), |
|||||||||||||
получим решения вопросов задачи. При этом условимся в следующих обозначениях:
176
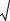
p0,V0,T0 - параметры начального состояния газа и 0, 0 -
соответствующие характеристики движения молекул;
p ,V ,T и , - для последующего состояния газа в ходе
осуществления адиабатического процесса. Установим зависимости:
а) (V) и (V) .
Согласно (1) и (2), сначала найдем зависимости n(V) и
T(V) . Концентрация молекул n N/V , где N – полное число молекул газа. Из соотношения TV 1 T0V0 1 следует соотно-
шение T T (V /V) 1 c V1 . Обращаясь к (1) и (2), получим: |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
0 |
|
0 |
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
c |
|
V |
c V , т.е. ~V ; |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
1 |
N |
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
c |
|
|
1 |
|
|
|
|
|
(V /V)( 1)/2 c V ( 1)/2 c V 1,2 |
c V 6/5 , |
||||||||||||||||||||||
|
|
|
|
|
|
T |
|||||||||||||||||||||||||||
2 c V |
|
||||||||||||||||||||||||||||||||
|
|
|
0 |
|
|
0 |
|
|
|
|
|
5 |
|
|
|
5 |
|
|
|
|
5 |
|
|
||||||||||
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
т.е. ~V 6/5 . |
|
|
i 2 |
|
|
|
5 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
Здесь |
|
|
1,4. |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
б) (p) и (p). |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
Из уравнения |
pV |
p V |
имеем V V ( |
p0 |
)1/ |
c |
|
p 1/ . |
||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 0 |
|
|
|
|
|
0 |
|
p |
|
|
6 |
|
||||
Концентрация молекул |
|
n |
N |
|
N |
p1/ c p1/ , |
длина пробега |
||||||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V |
c6 |
7 |
|
|
|
|
|
|
|
|
||||
|
c1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
p 1/ |
|
c p 1/ |
c p 5/7 , т.е. ~ |
p 5/7 . |
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
c7 |
|
|
|
|
|
8 |
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T(p). |
|
|
|
|
|
|
|
|
|||
|
Далее |
|
|
|
находим |
|
зависимость |
Из |
соотношения |
||||||||||||||||||||||||
TV 1 TV |
1 |
|
|
|
|
|
|
следует |
T( |
mRT |
) 1 |
T V 1 |
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
0 |
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
pM |
|
|
0 |
|
0 |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
T T V 1 |
( |
pM |
) 1 c |
|
p 1 T c p( 1)/ . |
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
0 0 |
|
|
|
mRT |
|
|
9 |
|
|
|
|
|
|
|
9 |
|
|
|
|
|
|
|
|
|
|||||||||
Для частоты столкновений молекул получаем следующее выражение:
177

c |
1 |
p1/ |
|
|
|
|
p( 1)/2 c p( 1)/2 |
c p6/7 , |
|||||||||
c |
|
|
|
||||||||||||||
|
|
|
|
|
|||||||||||||
2 |
|
c |
10 |
|
|
|
11 |
|
11 |
|
|||||||
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
т.е. ~ p6/7 . |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
в) (T) и (T). |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
В этом случае |
V V T 1/( 1) |
T1/(1 ) c T1/(1 ) , |
средняя |
||||||||||||||
|
|
|
|
|
|
|
|
|
0 |
0 |
|
12 |
|
|
|||
длина пробега |
|
c1 |
|
c1 |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
T1/(1 ) |
c T1/(1 ) |
c |
T 5/2 |
, |
|||||||||
|
N/V |
|
Nc12 |
|
|
|
|
|
13 |
13 |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
частота столкновений молекул |
|
|
|
|
|||||||||||||
|
c2 |
|
T1/(1 ) |
|
|
|
c |
T( 1)/ 2( 1) |
c T3 . |
|
|||||||
|
|
|
T |
|
|||||||||||||
|
|
|
c13 |
|
|
|
|
|
|
14 |
|
|
14 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Т.о. ~ T 5/2 , ~ c14T3 .
6.203. Решение данной задачи следует из результатов, полученных в задаче 6.202, заменой показателя адиабаты на показатель n политропы.
а) c1V , c2 /V(n 1)/2 ; б) c3 p 1/n , c* p(n 1)/2n ;
в) c7T1/(1 n) , c8T(n 1)/2(n 1) .
Здесь ci – постоянные.
6.204. Найти молярную теплоемкость двухатомного газа, совершающего политропический процесс, при котором число столкновений между молекулами в единицу времени остается неизменным:
а) в единице объема; Сначала выясним, что вытекает из условия постоянства
столкновений молекул ze.o. |
в единице объема: |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
d2n 4 |
|
|
|
d2n; |
||
|
|
8RT |
|
|
RT |
|
||||||||
|
2 |
|||||||||||||
|
|
|
||||||||||||
|
|
M |
M |
|||||||||||
|
|
|
|
178 |
|
|
|
|
|
|
|
|||

z |
e.o. |
|
1 |
n 2 |
|
RT |
d2n const . |
||||||||||
|
|
|
|
||||||||||||||
|
2 |
|
|
|
|
|
|
|
|
M |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Это означает, что |
|
Tn |
2 |
|
T |
|
NA |
|
const , т.е. |
||||||||
|
|
|
|||||||||||||||
|
|
V |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
M |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
|
const. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1) |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Молярная теплоемкость газа, совершающего политропи- |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ческий процесс, определим выражением |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
C |
QM |
|
|
dUM pdVM |
C |
p |
dVM |
. |
|
|
|
(2) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
dT |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dT |
|
|
|
|
|
|
|
|
|
|
V |
|
|
|
|
|
|
|
|
dT |
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
Из равенства (1) получим: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
1 |
|
|
|
1 |
|
|
|
|
dT |
2 |
|
|
|
|
|
|
|
|
dV |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
T |
|
|
0 |
dVM |
|
|
VM |
. |
(3) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
VM2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dT |
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
2 T |
|
|
|
|
|
|
|
|
|
|
|
|
|
VM3 |
|
|
|
|
|
|
|
M |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4T |
|
|
|||||||||||||||||||||||||||
Подставим (3) в (2): |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
C C |
|
|
VM |
|
|
|
C |
|
|
|
RT |
|
|
|
i |
|
R |
R |
(1 2i)R/4. |
(4) |
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
V |
|
|
|
|
4T |
|
|
|
|
|
|
|
|
V |
|
|
|
|
4T |
|
2 |
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
б) во всем объеме: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
1 |
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
z |
N |
|
|
|
|
|
N |
|
|
|
|
|
8RT |
|
|
|
|
|
|
d |
2nN |
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
A |
|
A |
|
|
|
|
|
2 |
A |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2 |
|
|
|
|
|
|
|
M |
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
RT |
d |
|
2N2 |
/V |
M |
|
const |
|
|
|
|
|
const |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
M |
|
|
|
|
|
|
|
|
|
|
|
A |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
VM |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
1 |
|
1 |
|
|
|
|
|
dT |
|
|
|
|
|
|
|
|
|
0 |
dVM |
|
VM |
; |
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
T |
|
|
dV |
M |
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
VM2 |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
VM 2 T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dT |
|
2T |
|
|
||||||||||||||||||||||||||||||||||
|
|
C C p |
dVM |
C |
pVM |
C |
RT |
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
V |
|
|
|
|
|
|
|
|
|
dT |
|
|
|
|
|
|
|
|
|
|
V |
|
|
|
2T |
|
V |
|
|
|
|
|
2T |
|
|
|
|
|||||||||||||||||||||||||||
Ci R R (i 1)R /2.
2 2
179
6.205. Молекулы газа, находясь в непрерывном тепловом движении, ударяются о стенку сосуда и, отражаясь от нее, создают давление на стенку сосуда. Среднее число ударов на единичную площадку стенки за единицу времени равно
z n /4. |
(1) |
Следовательно, число ударов, совершаемых о поверхность стенки площади S за время dt, будет равно
dN zSdt nS dt/4. |
(2) |
Теперь представим, что часть стенки сосуда площади S, за которой с внешней стороны был вакуум, удалили. В этом случае молекулы беспрепятственно (свободно) будут вылетать наружу. При этом приращение числа молекул в объеме будет равно
dN d(nV)V const Vdn.
Равенства (2) и (3) дают:
Vdn |
1 |
nS dt или |
dn |
|
S |
dt . |
|
n |
|
||||
4 |
|
|
4V |
|||
Решением уравнения (4) является функция
n const e t/ ,
где 4V /S , 
 8RT .
8RT .
M
При t=0, n=n0, тогда
n n0 e t/ .
(3)
(4)
(5)
(6)
6.206. Исходное состояние частей газа, находящихся в равных половинах сосуда, отображено на рисунке.
|
|
|
|
|
|
Сперва рассмотрим случай, |
|
|
|
|
|
|
когда оба отверстия 1 и 2 в пере- |
T1 T 1 |
|
|
S T2 T |
|||
|
|
|||||
|
|
|
||||
2 |
|
|
|
|
S1 S |
180 |
V1 V |
|
|
|
V2 V |
|
|
|
|
|
||||
