
Zakpita travma jivota
.pdfтрікторів) і настає параліч капілярів, у яких депонується до 10% ОЦК (у нормі
5% ) . Це - секвестрація крові в систему мікроциркуляції.
Пр и пролонгованому геморагічному шоці внаслідок гіповолемії, гіпотонії знижується серцевий викид. Для забезпечення кровопостачання найбільш важливих органів - головного мозку та міокардуосновний потік крові за рахунок п о р у ш е н н я кровотоку в інших органах направляється саме до цих органів - виникає "централізація" кровообігу як механізм тимчасової компенсації гіповолемії і довгий час підтримується їх адекватне кровопостачання. Із-за циркуляційної гіпоксії і кисневого голоду виникають врешті-решт пору- ш е н н я не л и ш е функцій, а й структури органів. При значній крововтраті, особливо геморагічному шоці, кров, як орган, пошкоджується - значно порушуються її функції: транспортна, буферна, імунного захисту, системи коагуляції (згортання і фібринолізу). Змінюється реологія крові: знижується швидкість току крові і коли AT падає до 80 мм рт. ст, кровотік на периферії зупиняється повністю [А.И. В о р о б ь е в 2002]. Зразу ж розпочинається процесс згортання,
тобто виникає гіперкоагуляційний синдром (перша фаза ДВЗ-синдрому): с к о р о ч у є т ь с я час згортання крові, рекальцифікації плазми, підвищується рівень фібриногену, відбувається агрегація тромбоцитів, "сладж"-синдром, наступає генералізоване мікротромбування, секвестрація значної кількості крові у мікросудинному руслі ("непряма крововтрата"), знижується фібринолітична активність крові. Все це приводить до блокади мікроциркуляції, дистрофік н е к р о з у паренхіми багатьох органів, ПОН.
Д л я у т в о р е н н я тромбів (дисеміноване тромбоутворення) витрачаються всі фактори згортання, зокрема зменшується вміст фібриногену, кількість тромбоцитів, протромбіну. Коли фактори згортання виснажилися, активується фібриноліз з у т в о р е н н я м плазміну, я к и й розчиняє фібрин і фибриноген. Продукти деградації, розпаду фібрину розчиняють тромби, тобто діють як антикоагулянти. Отже, т р о м б с а м себе розчинює. Саме тому це явище названо "тромбогеморагічним синдромом". Наступає друга фаза ДВЗ-синдрому | гіпокоагуляційна.
С.С. Б е с с м е л ь ц е в [2005] в в а ж а є практично доцільним у перебігу ДВЗ - с и н д р о м у виділяти 4 стадії.
ДВ З І - гіперкоагуляція.
ДВ З 1 - перехідна з н а р о с т а ю ч о ю коагулопатією та тромбоцитопенією (гіпокоагуляція б е з генералізованого підвищення фібринолізу). Це вже коагулопатична стадія, під час я к о ї виділяється тканевий фактор, після чого зни-
ж у є т ь с я р і в е н ь фібриногену і кількість тромбоцитів.
Д В З III І глибока гіпокоагуляція з т я ж к о ю полікомпонентною гемостазіопатією, з п і д в и щ е н н я м фібринолітичної активності (коагулопатія витрачання, р о з п о ч и н а є т ь с я генералізація фібринолізу), пошкодження клітин з п о р у ш е н н я м п р о н и к н о с т і капілярів.
Д В З I V - п о в н е незгортання крові (генералізований фібриноліз).
П р и великій, а т и м б і л ь ш е масивній крововтраті (більше 25-30% ОЦК), в т.ч. операційній, н е м и н у ч е п о р у ш у ю т ь с я згортаючі властивості плазми крові, оскільки, по-перше, з п л а з м о ю крові втрачаються і плазматичні фактори;
71
по-друге, кров розводиться плазмозаміщуючими розчинами (коагулопатія розведення); по-третє, виникають ознаки ДВЗ -синдрому з витрачанням факторів коагуляції.
Отже, масивна крововтрата, шок будь якої етіології, політравма завжди супроводжуються ДВЗ-синдромом, який розпізнається, як правило, не в першій, а в другій фазі.
Діагностика ДВЗ -синдрому ситуаційна, клінічна (синдромна), лабораторна. Клінічні симптоми ДВЗ-синдрому складаються із ознак основного захворювання чи пошкодження, шоку, тромбозів і геморагій, гіповолемії, анемії, дисфункції органів і систем, метаболічних порушень. Про першу фазу (гіперкоагуляції) ДВЗ-синдрому свідчить тромбування голки при заборі крові із вени для аналізів, швидке згортання крові в пробірці, поява немотивованих тромбозів і ознак ПОН внаслідок порушення мікроциркуляції в органах: в нирках (олігурія), в легенях (хрипи, неефективне дихання), в мозку (заторможеність), наднирниках (зниження AT повторне), в печінці (біль у підребер'ї, жовтуха, білірубінемія). Але перша фаза надто часто не діагностується. Можно сказати, що ДВЗ-синдром виявляють, як правило, при появі геморагічних ускладнень (дифузна кровоточивість на місці ін'єкцій, носові та шлунковокишкові кровотечі). Гіперкоагуляційна фаза дещо проявляється клінічно: пацієнт до цього активно відповідав на питання, на щось скаржився, раптово став заторможеним, безучасним, замовчав або відповіді стали короткі, уривчасті, обличчя зробилося байдужим, амімічним. Це - перша фаза ДВЗ-синдро- му [А.И. Воробьев, 2002].
Для діагностики ДВЗ-синдрому найбільш важливі його лабораторні ознаки/які випереджають клінічну маніфестацію і типові прояви (кровоточивість). З метою експрес-діагностики коагулопатичної кровотечі і щоб вчасно проводити її корекцію до чи під час втручання, регулярно проводять лабораторні дослідження: визначають час згортання крові за Лі-Уайтом, концентрацію фібриногену, кількість тромбоцитів, їх агрегаційні властивості.
Для ДВЗ-синдрому патогномонічними є зниження рівня тромбоцитів та фібриногену, збільшення протромбінового та тромбінового часу.
Об'єктивним маркером ДВЗ-синдрому вважається феномен фрагментизаціївиявлення в мазках крові фрагментів еритроцитів.
Лабораторна діагностика ДВЗ-синдрому найбільше значення має в початковій стадії, коли корекція ще порівняно не складна.
Досвід свідчить, що чим гостріший початок ДВЗ-синдрому, тим коротша фаза гіперкоагуляції і тим більш тяжка фаза гіпокоагуляціїі кровоточивості.
Досить швидко наростає фібриноліз і час згортання крові збільшується до 15 хв і навіть 30 хв, наростає фібриногенопенія, тромбоцитопенія (< 1004 109/л), протромбіновий індекс знижується до 40-50%, кровоточивість стає генералізованою (слизових, летехії на шкірі, операційної рани, ШКК). Якщо утворюється невеликий згусток крові, то швидко настає його лізис.
Доцільна, хоча і проста, але досить інформативна, проба виявлення згустка крові в пробірці - якщо згусток утворюється, то, незважаючи на кровоточивість, гіпокоагуляції ще немає.
72
При крововтраті і гіповолемії згустками крові, агресивними метаболітами і агрегатами забивається також капілярний фільтр легень (вони перетворюються в "еритроцитне болото", коли еритроцитів надлишок, а не нестача) - наступає набряк інтерстицію, порушується альвеолярно-капілярна дифузія (альвеолярне шунтування). Посилюється гіпоксія тканин. Але кисневе голодания виникає не стільки із-за гемічної, скільки внаслідок циркуляторної гіпоксії. Включаються компенсаторні механізми, зокрема еритропоез, завдяки чому в кровотік негайно поступають ще не зовсім зрілі еритроцити. Оскільки мало кисню, обмін речовин стає анаеробним. Такий гліколіз у 15 разів менше дає енергії, ніж аеробний. Накопичується молочна кислота і виникає метаболічний ацидоз. Збільшується проникнення мембран і трансудація рідини із капіляр у тканини, ОЦК ще більше зменшується.
Які ж клінічні ознаки масивної крововтрати і геморагічного шоку, тобто критичного стану? Це, по-перше, класична тріада: холодна, блідо-ціанотична, навіть мармурова шкіра, покрита липким потом; частий ниткоподібний пульс; низький тиск ("шокові ножиці"); по-друге, депресія центральної нервової системи (адинамія, апатія, а нерідко затемнена свідомість, розширені зіниці), у травмованого часте дихання, нестерпна спрага. Про порушення мікроциркуляції свідчать також симптом "білої плями", знижений діурез (менше 0,5 мл/ хв або ЗО мл/год), значний градієнт температури шкіри і ректальної (більше 4°С). Не слід, забувати, що колір і температура шкіри хоча і прості, але досить важливі показники периферичного кровотоку. Так, якщо AT навіть низький, але шкіра тепла і рожева - периферичний кровотік ще не порушений. Якщо ж шкіра бліда, холодна, а після надавлювання на ніготь капіляри його ложа наповнюються кров'ю дуже повільно - це, безсумнівно, свідчить про глибокі порушення мікроциркуляції, про "централізацію" кровообігу.
Тому перша і найголовніша задача не в тім, щоб поповнити втрачений гемоглобін, а щоб нормалізувати мікроциркуляцію і запобігти ПОН.
1.11. Допомога. Реанімаційні заходи.
Реанімаційні маніпуляції поєднуються з діагностичними. Отримані дані про тяжкість стану потерпілого і тяжкість пошкодження постійно співставляють, пам'ятаючи - чим тяжчий шок, тим менше виражені ознаки абдомінальної катастрофи. Основний принцип реанімації - виявлення і усунення в першу чергу тих патологічних станів, які безпосередньо загрожують життю в данний момент. Реанімаційно-діагностичний комплекс проводять [Н.К. Голобородько, 1983] передусім в певній послідовності в залежності від стану травмованого за дещо зміненою схемою в декілька етапів:
I етап: а) визначення простих показників гомеостазу (дихання, пульсу, артеріального тиску); б) загальний огляд потерпілого для оцінки стану (забарвлення шкіри, слизових, температура тіла на дотик); в) закритий масаж серця, штучна вентиляція легень (за необхідністю).
II етап проводиться за правилом "трьох катетерів" (катетеризація центральної вени, сечового міхура, шлунка) або навіть "п'яти катетеризацій": а) ка-
73

тетеризація центральної вени; 6) інтубація трахеї; в) евакуація вмісту шлунка; г) катетеризація сечового міхура; д) лапароцентез.
III етап: а) забір крові для аналізів (гемоглобін, еритроцити, гематокрит, лейкоцити, цукор, амілаза, білок і фракції, коагулограма, обсяг крововтрати); аналіз сечі; б) вимірювання центрального венозного тиску; в) інфузій- но-трансфузійна терапія (струменеве введення поліглюкіну, розчинів електролітів, білкових препаратів); штучна вентиляція легень.
IV етап: 1) корекція гемодинаміки, газообміну, метаболізму згідно даних лабораторних досліджень; 2) клінічне обстеження; 3) ультразвукове обстеження; 4) рентгенологічна діагностика (рентгенографія, комп'ютерна томографія грудей, живота, таза для виявлення переломів, пошкодження паренхіматозних органів і крові в порожнинах); 5) застосування інструментальних методик (лапароцентез і діагностичний перитонеальний лаваж, лапароскопія).
Для з'ясування величини крововтрати визначають дефіцит ОЦК.
Належний ОЦК дорівнює:
учоловіків - маса тіла х на 70;
ужінок - маса тіла х на 60;
vвагітних - 75 мл/кг.
HtH (належний) - показник гематокриту в нормі (для чоловіків - 45%, для жінок - 42%),
Нtф (фактичний) - показник гематокриту у даного пацієнта.
Отже, крововтрата у травмованої жінки 1200 мл.
Дефіцит ОЦК тісно корелює з тяжкістю шоку і визначає об'єм інфузійної терапії.
Стверджується [Е.А. Вагнер и соавт., 1986; А.І. Воробйов, 2001], що при гострій, особливо масивній, крововтраті організм страждає не стільки від зменшення кількості еритроцитів і гемоглобіну, скільки від зниження ОЦК і гіповолемії.
74
Відомо, що організм залишається життєздатним при втраті навіть 65% еритроцитів, але він в небезпеці, коли втрачається 30% плазми. Тому вижи-
вання визначається дефіцитом рідкої частини крові.
В гострому періоді травматичної хвороби, тобто в перші 1-2 години після травми (а саме у цей термін доставляють у стаціонар більшість потерпілих) в організмі виникають значні зміни ~ централізація кровообігу, різноманітні гуморальні та метаболічні розлади,
В цей час навіть при значній крововтраті достовірно зясувати її величину, орієнтуючись на традиційні «інертні» показники аналізів крові (еритроцити, гемоглобін, гематокрит), неможливо, оскільки вони не віддзеркалюють важкість стану травмованого.
Впротилежність існуючим поглядам, гематокрит не може служити надійним показником наявності кровотечі і ступеня крововтрати. Це тому, що, по-перше, величина гематокриту часто залишається без змін, оскільки при гострій внутрішній кровотечі організм рівномірно втрачає і форменні елементи крові, і плазму; по-друге, при інфузійній терапії зменшення гематокритного числа свідчить лише про поповнення ОЦП, а збільшення показника гематокриту - про недостатню інфузію. До того ж не кожна лабораторія із-за дефіциту реактивів в останні роки може визначити гематокрит.Отримані псевдоблагополучні результати дезорієнтують лікаря.
Вперші години після травми найбільш реальний показник гомеостазу - питома щільність крові, що визначається гравіметричним методом Ван- Слайка-Барашкова [С.В. Гаврилин и соавт., 2005].
Величину крововтрати і ступінь важкості шоку пропонується [С.А. Гешелин, 2003] визначати показниками пульсу, систолічного артеріального тиску, шокового індексу та центрального венозного тиску (табл. 11).
Доречі, А.П. Зильбер [2001] вважає, що при крововтраті вимірювання ЦВТ більш вагомий критерій, ніж артеріальна тонометрія.
|
ОбЛєм |
крововтрати і ступінь геморагічного |
шоку |
Таблиця 11 |
|
||||
|
|
|
|
||||||
Ступінь |
Пульс, |
Систол, тиск |
ЦВТ, |
|
|
Об'єм |
|
|
|
ШІ |
|
крововтрати |
|
|
|||||
шоку |
уд/хв |
мм рт.ст. |
мм рт.ст. |
|
|
|
|||
|
|
мл |
% ОЦК |
|
|
||||
|
|
|
|
|
|
|
|
||
1 |
90-100 |
100-130 |
> + 2,0 |
< 1 |
|
< 1000 |
15-20 |
|
< |
II |
101-120 |
80-99 |
>-1,0 |
|
|
< 1500 30 |
|
||
|
|
|
|
||||||
III |
121-140 |
70-79 |
>-3,0 |
<2 |
|
<2000 |
40 |
|
|
IY |
1140 |
<70 |
> - 4,0 |
>2 |
|
>2000 >40 |
|
|
|
Тяжкість гемодинамічних порушень можна оцінювати шоковим індексом (Ш І) Алговера-Бурри. Це відношення частоти серцевих скорочень (ЧСС) до систоличного артеріального тиску (AT сист.)
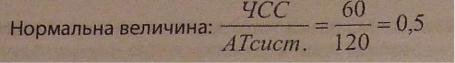
Ш о к І ступеня - LLI I |
0,8 та нижче; |
Ш о к II ступеня - Ш I |
0,9-1,2; |
Ш о к III ступеня - Ш I |
1,3 та вище. |
Ступінь важкості геморагічного ш о к у
(за Baker у модифікації П.Г. Брюсова)
І ступінь (помірний) ЧСС - 90 - 100 уд/хв;
АТсист. - більше 100 мм рт. ст.; Центральний венозний тиск (ЦВТ) - N; Діурез - N;
Ш 1-0,78; О б ' є м крововтрати £ 1000 мл (10-20%)
IIступінь (виражений)
ЧС С - д о 120 уд/хв;
АТсист. - м е н ш е 100 мм рт. ст.; Ц В Т - з н и ж е н и й ; Діурез - олігурія;
ШІ - 0,99;
Об ' є м крововтрати < 1500 мл (21-30%) III ступінь (тяжкий)
ЧС С - до 140 уд/хв;
АТсист. - м е н ш е 70 мм рт. ст.; ЦВТ - понижений до 0; Діурез - анурія;
Ш1-1,1;
Об ' є м крововтрати < 2000 мл (31-40%)
IVступінь (позамежний/потойбічний) ЧСС - більше 140 уд/хв; АТсист. - м е н ш е 50 мм рт. ст.; ЦВТ - від'ємний; Діурез - анурія;
111 І - 1,4 та більше; О б ' є м крововтрати більше 2000 м л (41 % та більше).
Величину крововтрати називають по-різному. Так, Е.А. Вагнер и соавт. [1977] невеликою крововтратою вважають 100-500 мл, п о м і р н о ю - 501-1000 мл., масивною - 1001-2500 мл. А.І. В о р о б й о в [2001; 2003] масивною кро-
вовтратою називає втрату крові близько 3 0 % її обсягу. Оскільки крововтрата вимірюється л и ш е приблизно, академік радить гостру м а с и в н у крововтрату визначати за клінічними ознаками: втрата протягом хвилин, десятків хвилин
76
більше 1 л крові (інколи менше, але швидко), що супроводжується блідістю, спадінням вен, падінням AT, тахікардією, задишкою. П.Г. Брюсов [19973 розрізняє середню крововтрату (500-1000 мл) і легку ступінь гіповолемії; велику крововтрату (1100-2000 мл) і помірну гіповолемію; масивну крововтрату (21003500 мл) і тяжку гіповолемію; смертельну крововтрату (> 3500 мл) і вкрай тяжку гіповолемію. В .А. Климанский и соавт. [1984] виділяють три ступені крововтрати: 1 - помірну ( не більше 25% ОЦК); 2 - велику (30-40 % ОЦК); 3 - масивну (більше 40% ОЦК). Ступені крововтрати розрізняються і по-іншому: легка ступінь крововтрати (до 500 мл), середньої важкості (до 1000 мл), важка (до 1500 мл), дуже важка (більше 1500 мл).
Якщо немає даних за пошкодження внутрішніх органів, необхідно енергійно проводити пошук позачеревних причин шоку і гіпоциркуляци. Продовжують вивчати характер рідини в черевній порожнині (із катетера), зокрема кількість лейкоцитів на предмет пошкодження порожнистих органів.
Для ранньої топічної діагностики, зменшення числа діагностичних помилок, зниження частоти ускладнень і рівня летальності необхідно розумно поєднувати ретельне фізикальне обстеження, лапароцентез з діагностичним лаважем, КТ і УЗД.
В останні роки при травмах живота з метою діагностики і лікування впроваджуються мініінвазивні хірургічні технології. В деяких клініках вони використовуються у 82,0% потерпілих [В.М. Тимербулатов и соавт., 2002], що дає можливість у 36,0% не проводити діагностичну лапаротомію.
Оскільки у багатьох пацієнтів з травмою живота явища шоку і внутрішньої кровотечі, то терміново потрібно вирішити головне питання - оперувати травмованого зразу ж, чи спочатку вивести його із шоку? Для зниження ризику втручання абсолютно показана, як життєво необхідна, повноцінна (короткочасна і максимально інтенсивна) доопераційна підготовка. ЇЇ тривалість і якість залежить від періоду, в якому травмованого госпіталізовано. В перші години після травми живота з пошкодженнями паренхіматозного органа доопераційна підготовка необхідна для корекції травматичного та/або геморагічного шоку.
Танатогенез шоку досить складний. В його основі, як критичного стану, лежить різке зниження перфузії органів [М. Мун и соавт., 1998]. Такий шок ізза некомпенсованої, або несвоєчасно відшкодованої масивної (більше 30% ОЦК) крововтрати вважають [А.П. Зильбер, 1999] ПОН.
Компоненти ПОН: а) гіповолемія з порушенням реологічних властивостей крові і її секвестрацією в капілярах. При геморагічному шоці саме із-за секвестрації крові після крововтрати, наприклад, 1000 мл, початковий ОЦК з 5л дорівнюватиме не 4л, а 3-3,5л; 6) метаболічний ацидоз; в) ішемія і розлади функції органів (нирок, печінки, легенів, міокарду та інше); г) гнійно-септичні ураження; д) коагулопатія.
Із-за гіповолемії дефіциту ОЦК і артеріальної гіпотензії настає гемоконцентрація, знижуються реологічні властивості крові, порушується макро- і мікроциркуляція. Тому шок ще називають "кризисом мікроциркуляції" Внаслідок низького перфузійного тиску страждає перфузія тканин, не забез-
77
печується доставка в клітини кисню і енергетичних матеріалів,розвивається тканьова гіпоксія. Доставка кисню тканинам при травматичному шоці нижче норми у 2,8 рази [Е.К. Гуманенко и соавт., 2004]. Гіпоксія активує анаеробне окислення глюкози. Накопичується кінцевий продукт анаеробного гліколізу І лактат і розвивається некомпенсований метаболічний ацидоз (лактатацидемія). Саме неадекватна оксигенація тканин вважається центральною проблемою шоку.
В нормалізації процесів перфузії тканин організму важливу роль відіграють ендотеліальні клітини судин.
Як доведено Z.F. Ва et al. [2001] досить складними експериментальними дослідженнями на щурах під час геморагічного посттравматичного шоку (втрата крові сягала 60% загального ОЦК з терміном кровотечі 90 хв) у тва- рин-самців (у протилежність самкам) виникала виражена імунна депресія. Дослідники тваринам уводили підшкірно антагоніст рецептора тестостерона флутамід по 25 мг/кг маси. Зроблеоно висновок, що завдяки блокаді рецептора тестостерона флутамідом відновлюється імунна функція до нормального стану, поліпшується послаблена функція ендотеліальних клітин, попереджається звуження кровоносних судин, компенсується кровообіг, перфузія тканин, транспорт до них кисню і його засвоєння у печінці, тонкій кишці, нирках щурів-самців. Автори припускають, що флутамід зменшує також продукцію фактору некрозу пухлин (ФНП), який пригнічує функцію ендотеліальних клітин і підвищує тонус судин. Отже функція клітин ендотелію поліпшується.
Подібна дія виявлена і у пентоксифіліну.
Тому, коли у травмованого геморагічний шок, вже не досить ліквідувати крововтрату - потрібна ефективна профілактика і терапія ПОН.
В основі ПОН лежить феномен "подвійного удару". "Перший удар"- це механічне травматичне пошкодження органів і тканин, кровотеча, дефіцит ОЦК. "Другий удар"- додаткове травмування під час транспортування; хірургічне втручання. Друге пошкодження розвивається по типу каскаду: ішемія 1 синдром системної запальної реакції І ПОН. Крім того, на перебіг негативно впливає і третій тип пошкодження - компресивний синдром: компресія серця (внаслідок гемомедіастінума), легень (гемоторакс), головного або спинного мозку гематомою, органів черевної порожнини, м'язів кінцівок (гематома, набряк).
Сучасна концепція надання кваліфікованої допомоги тяжко травмованим базується на настанові"... дії реаніматолога повинні встигнути "обігнати" смерть, а скальпель хірурга 1 асфіксію, крововтрату, тампонаду серця" [Н.К. Голобородько и соавт., 2003]. Але при наявності внутрішньої кровотечі реанімаційні засоби проводяться в умовах "відкритого крану".
Реанімація потерпілих полягає в максимально швидкій нормалізації газообміну (інтубація трахеї, штучна вентиляція легень, адекватна оксигенація) та в адекватній інфузійно-трансфузійній терапії, яка посідає провідне місце. У пацієнтів з геморагічним шоком її потрібно проводити як при ПОН [А.П. Зильбер, 1999].
Синдром відмови множинних органів після тупої травми зустрічаєть-
78
ся нерідко. Згідно даних D. Nast-Kolb et al. [2001] за 1975-1999 рр із 1361 потерпілого синдром виявлено у 325 (24%). За цей період впроваджена нова лікувальна тактика, яка полягала у збільшені об'єму реанімаційної допомоги; посиленні легеневої вентиляції (open lung conceps І концепція відкритих легень); стабілізації переломів; damage control травматичних пошкоджень; ранньому ентеральному харчуванні. Завдяки застосуванню нової стратеги лікування смертність з синдромом відказу множинних органів за 25-річний період зменшилася з 8 5 % до 33% .
При знекровленні пацієнта реанімаційну допомогу необхідно проводити поетапно [Г.Н. Цыбуляк и соавт., 1999]:
операція і радикальний гемостаз;
фузій;
Задачі першого рівня на догоспітальному етапі чи зразу ж після госпіталізації.
Терміново, як першорядна задача | відновити ОЦК і підтримувати його на рівні, що попереджає зупинку "пустого" серця (ліквідація критичної гіповолеми). При цьому виходять з того, що ч и м більша крововтрата та глибина шоку, тим більша необхідність у введенні великих об'ємів рідини за короткий термін [П.Г. Брюсов, 1997]. Якщо AT не визначається, то інфузії необхідно проводити зі швидкістю не м е н ш е 250 мл/хв (нерідко і швидше), причому не просто вливанням, а нагнітанням під тиском в дві-три вени чи в артерію. Про ефективність такої " о ж и в л ю ю ч о ї інфузії" свідчить AT, який повинен визначатися вже через 5-10 хв.
В процесі відновлення гемодинаміки всі препарати необхідно вводити тільки довенно!, тому що вони із-за порушення кровообігу депонують в місцях ін'єкції, а після нормалізації кровообігу всмоктують і можуть визвати ускладнення: морфій - пригнічення дихання, адреналін - фібриляцію шлуночків серця та інше.
Оскільки на цьому етапі вводять значну кількість розчинів, реальна небезпека гіперінфузій, порушення згортання крові і виникнення гемодилюційної коагулопатіїта ДВЗ синдрому [П.В. Мирютин и соавт., 1998]. Крім того, із-за введення переважно сольових розчинів, тобто 0,9% розчину натрія хлориду, нерідко розвивається гіперхлоремічний ацидоз; внаслідок великої кількості йонів натрію клітини втрачають калій; знижується колоїдно-онкотичний тиск плазми.
Задача другого рівня і в перші ж одну-дві години після зупинки кровотечі нормалізувати якісний склад та функції крові гемотрансфузіями і вве-
денням препаратів крові.
Задача третього рівня - до кінця першої доби адекватно корегувати мікроциркуляцію і периферичний кровотік з відновленням газообміну в тканинах, зокрема транспорт кисню.
Ефективність такої терапії залежить від об'єму, якісного складу інфузій,
79
своєчасності ліквідації макро- і мікроциркуляторних порушень гемодинаміки. До повного відновлення ОЦК серцево-судинні препарати та діуретики протипоказані [Ч. Апрахамен, 1998*].
Особлива увага приділяється способу і швидкості введення рідини та препаратів [В.А. Пронин и соавт., 2006]. При компенсованому шоці катетеризують дві вени (одна із них центральна, наприклад v. jugularis чи v. subclavia), що забезпечує необхідний темп інфузії і постійний контроль ЦВТ. При декомпенсованому шоці автори вважають доцільним крім вен катетеризувати ще й a.radialis для внутрішньоартеріального нагнітання колоїдних розчинів і компонентів крові (але недопустимо в артерію вводити гіперосмолярні розчини і симлатоміметики!). Ефекти внутрішньоартеріальних інфузій: поліпшується коронарний кровотік, стимулюється гомеометричний механізм Анрепа і збільшується серцевий викид, попереджається блокада легеневого фільтру клітинними елементами крові.
Це давало можливість знизити дозу симпатоміметиків, в короткий термін стабілізувати центральну гемодинаміку і поліпшити органний кровотік. Авторами доведено, що із збільшенням тяжкості гемодинамічних розладів зростає кількість ускладнень і летальність (до 30%), в основному, від декомпенсованого незворотнього шоку. Автори зробили висновки: у потерпілих без шоку або коли він компенсований об'єм втручання може бути повним; якщо ж шок некомпенсований, інтраопераційна корекція пошкоджень повинна бути мінімізована до зупинки кровотечі і тимчасової герметизації травмованих порожнистих органів.
Тільки після виведення потерпілого із шоку і стабілізації вітальних функцій можливе, при необхідності, проведення релапаротомії для адекватної корекції пошкоджень, тобто оперування за принципом damage control.
Зметою якнайшвидшого відновлення ОЦК при масивній крововтраті
востаннє десятиріччя посилено розробляється (переважно у США) і широко впроваджується програма малооб'ємної інфузійної терапії - метод екстренної довенної інфузії малих об'ємів ("small volume resuscitation") гіпертонічних розчинів, що є найбільш доцільним.
Послідовність інфузії:
Ікристалоїдні розчини (зокрема гіпертонічний розчин);
Іколоїдні розчини (препарати гідроксиетилкрохмалю); - свіжозаморожена плазма;
- еритроцитна маса.
Для корекції компенсованого і некомпенсованого шоку вводять [ВА Пронин и соавт., 2005] препарати за наступною схемою (Табл. 12).
При цьому дуже важливо розрізняти поняття «дегідратація» (дефіцит рідини в організмі, що корегують уведення кристалоїдів) та «гіповолемія» (дефіцит внутрішньосудинного об'єму, для корекції якого необхідні колоїди).
80
