
- •Предисловие
- •Программа курса «Молекулярная физика. Термодинамика.»
- •2. Учебно-тематический план
- •3. Содержание курса
- •4. Примерная тематика семинарских занятий
- •5. Средства обеспечения дисциплины
- •Введение
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •Глава 1 Термодинамика
- •§1. Температура и термодинамическое равновесие
- •Давление
- •§2. Уравнение состояния идеального газа
- •§3. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Закон Авогадро
- •Закон Дальтона
- •§4. Первое начало термодинамики
- •§5. Макроскопическая работа
- •I начало термодинамики для системы в адиабатической оболочке
- •§6. Внутренняя энергия
- •§7. Количество теплоты. Математическая формулировка первого начала термодинамики
- •§8. Различные приложения I начала термодинамики. Теплоёмкость
- •§9. Внутренняя энергия идеального газа. Закон Джоуля
- •Уравнение Роберта Майера
- •§10. Адиабатический процесс. Уравнение Пуассона
- •Работа при адиабатическом изменении объёма газа
- •§11. Политропический процесс
- •Вопросы и задания для самостоятельной работы студентов Основы термодинамики. I начало термодинамики
- •§12. II начало термодинамики
- •Различные формулировки основного постулата, выражающего II начало термодинамики
- •§13. Равновесные состояния
- •§14. Обратимые и необратимые процессы
- •Необратимость и вероятность
- •§15. Цикл Карно
- •Коэффициент полезного действия в цикле Карно
- •§16. Холодильная машина
- •§17. Свободная энергия
- •§18. Энтропия
- •§19. Некоторые термодинамические соотношения
- •§20. Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •§21. Энтропия и вероятность
- •§22. Энтропия и беспорядок
- •§23. Третье начало термодинамики
- •Вопросы для контроля самостоятельной работы студентов
- •II начало термодинамики. Энтропия.
- •Глава 2. Неравновесная термодинамика §1. Основные принципы линейной термодинамики
- •§2. Нелинейная термодинамика
- •§3. Принцип синергетики
- •Свойства и примеры самоорганизации диссипативных структур
- •Глава 3. Статистическая физика и её применение к идеальному газу
- •§1. Давление газа с точки зрения молекулярно – кинетической теории
- •§2. Температура как мера средней энергии хаотичного движения молекул
- •Скорость газовых молекул
- •§3. Броуновское движение
- •§4. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •§5. Классическая теория теплоёмкости и её недостатки
- •§6. Барометрическая формула
- •Закон Больцмана
- •§7. Распределение молекул по скоростям
- •§8. Функция распределения
- •§9. Формула Максвелла
- •§10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •§11. Среднее число молекул, сталкивающихся со стенкой сосуда
- •Вопросы для контроля знаний студентов Молекулярно-кинетическая теория
- •Глава 4. Явления переноса §1. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •§4. Явление переноса в газах. Уравнение переноса
- •§5. Диффузия
- •§6. Нестационарная диффузия
- •§7. Теплопроводность газов
- •§8. Вязкость газов (внутреннее трение)
- •§9. Соотношения между коэффициентами переноса
- •§10. Физические явления в разреженных газах
- •Вопросы для самостоятельного контроля знаний студентов Явления переноса
- •Глава 5 §1. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •Уравнение Ван-Дер-Ваальса
- •§2. Учет сил отталкивания между молекулами
- •§3. Учет сил притяжения между молекулами
- •§4. Изотермы Ван-дер-Ваальса
- •§5. Критическая температура и критическое состояние
- •§6. Недостатки уравнения Ван-дер-Ваальса
- •§7. Внутренняя энергия газа Ван-дер-Ваальса
- •§8. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •§9. Сжижение газов
- •Эффект Джоуля-Томсона
- •Вопросы для самоконтроля изученного материала Реальные газы
- •Глава 6. Жидкое состояние §1.Строение жидкостей
- •§2. Поверхностное натяжение
- •§3. Условия равновесия на границе двух сред. Краевой угол
- •§4. Граница жидкости и твердого тела
- •§5. Силы, возникающие на кривой поверхности жидкости
- •§6. Капиллярные явления
- •§7. Упругость насыщенного пара над кривой поверхностью жидкости
- •Вопросы для самоконтроля знаний студентов
- •Глава 7. Жидкие растворы §1. Свойства растворов
- •§2. Упругость насыщенного пара над идеальным раствором
- •§3. Закон Генри
- •§4. Осмотическое давление
- •Глава 8. Кристаллическое состояние §1. Отличительные черты кристаллического состояния
- •§2. Классификация кристаллов
- •§3. Физические типы кристаллических решеток
- •§4. Тепловое движение в кристаллах
- •Глава 9. Фазовые переходы §1. Фаза и фазовые равновесия
- •§2. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
- •Вопросы для самоконтроля знаний студентов
- •Содержание
§4. Первое начало термодинамики
Первое начало термодинамики выражает закон сохранения энергии для тех макроскопических явлений, где одним из ведущих параметров, определяющих состояние тел, является температура.
В механике доказывается, что для изолированной системы полная механическая энергия сохраняется. Но это справедливо не всегда, и только в тех случаях, когда все действующие силы консервативны. При наличии диссипативных сил - силы трения – механическая энергия уменьшается. Работа диссипативных сил превращается в тепло. Оказалось, что принцип сохранения энергии остаётся справедливым и при наличии диссипативных сил, если только расширить понятие энергии введением её новой формы – внутренней энергии, называемой тепловой энергией.
Нарушение механического закона сохранения энергии объясняется тем, что макроскопическое механическое движение не учитывает все виды движения. Из ее поля зрения ускользает внутреннее движение атомов и молекул, а также взаимодействия между ними.
Прежде чем сформулировать I начало термодинамики, введём некоторые важные величины термодинамики.
§5. Макроскопическая работа
Р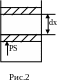 ассмотрим
газ в цилиндре с поршнем. Пусть под этим
поршнем находится сжатый газ (рис.2).
Вычислим бесконечно малую или элементарную
работу A,
совершаемую газом при бесконечно малом
расширении, в котором его объём
увеличивается на dV.
Сила давления газа на поршень равна
F=PS,
где S
– площадь поршня. Если поршень переместить
на расстояние dx,
то газ совершит работу δA=Fdx=PSdx.
Учитывая, что Sdx=dV,
имеем следующее выражение для элементарной
работы
ассмотрим
газ в цилиндре с поршнем. Пусть под этим
поршнем находится сжатый газ (рис.2).
Вычислим бесконечно малую или элементарную
работу A,
совершаемую газом при бесконечно малом
расширении, в котором его объём
увеличивается на dV.
Сила давления газа на поршень равна
F=PS,
где S
– площадь поршня. Если поршень переместить
на расстояние dx,
то газ совершит работу δA=Fdx=PSdx.
Учитывая, что Sdx=dV,
имеем следующее выражение для элементарной
работы
A=PdV. (1.9)
В том случае, когда над газом совершается работа внешними силами, то
A=-PdV.
Формула (1.9) верна не только для газов, но и для любых тел.
Е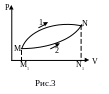 сли
тело переходит из состояния 1 в состояние
2, то совершённая во время этого процесса
работа определяется путём интегрирования
уравнения (1.9)
сли
тело переходит из состояния 1 в состояние
2, то совершённая во время этого процесса
работа определяется путём интегрирования
уравнения (1.9)
![]() (1.10)
(1.10)
Интеграл
![]() можно
определить графически. Это связано с
тем, что состояние тела характеризуется
точкой на кривой P=f(V).
Поэтому, если зависимость P(V)
построена графически, то
можно
определить графически. Это связано с
тем, что состояние тела характеризуется
точкой на кривой P=f(V).
Поэтому, если зависимость P(V)
построена графически, то
![]() равен площади
под данной кривой.
равен площади
под данной кривой.
Пусть система переходит из состояния M в состояние N вдоль кривой M1N (рис.3). Эта кривая определяет давление P, как вполне определённую функцию объёма V. После этого работа системы A определяется однозначно. Она численно равна площади криволинейной трапеции N1M1M1NN1. Если систему заставить переходить из того же начального состояния M в то же конечное состояние N вдоль другой кривой M2N, то соответствующая работа A1 изобразится площадью M1M2NN1. Как видно из рисунка AA1. Это означает, что работа, совершаемая системой, при переходе из одного состояния в другое зависит от того, через какую последовательность состояний она проходит, т. е. зависит от формы пути перехода. Про такие величины говорят, что они не являются функциями состояния. Величины, которые не зависят от формы пути перехода, а зависят только от начального и конечного состояния системы являются функциями состояния.
Вычислим работу, совершаемую идеальным газом при различных изопроцессах. При изохорическом процессе dV=0, соответственно работа равна нулю. При изобарическом процессе P=const, тогда
 .
.
При изотермическом процессе Т=const,
![]() ,
,
работа будет равна
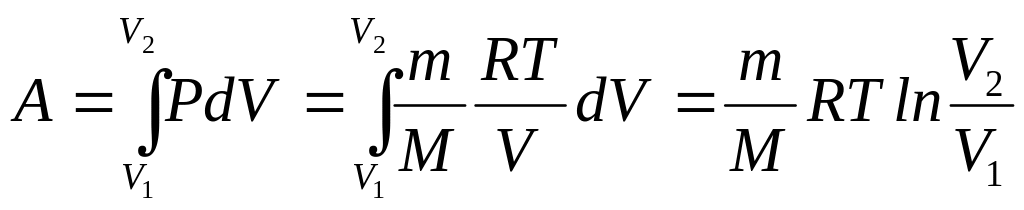 .
(1.11)
.
(1.11)
