
- •Предисловие
- •Программа курса «Молекулярная физика. Термодинамика.»
- •2. Учебно-тематический план
- •3. Содержание курса
- •4. Примерная тематика семинарских занятий
- •5. Средства обеспечения дисциплины
- •Введение
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •Глава 1 Термодинамика
- •§1. Температура и термодинамическое равновесие
- •Давление
- •§2. Уравнение состояния идеального газа
- •§3. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Закон Авогадро
- •Закон Дальтона
- •§4. Первое начало термодинамики
- •§5. Макроскопическая работа
- •I начало термодинамики для системы в адиабатической оболочке
- •§6. Внутренняя энергия
- •§7. Количество теплоты. Математическая формулировка первого начала термодинамики
- •§8. Различные приложения I начала термодинамики. Теплоёмкость
- •§9. Внутренняя энергия идеального газа. Закон Джоуля
- •Уравнение Роберта Майера
- •§10. Адиабатический процесс. Уравнение Пуассона
- •Работа при адиабатическом изменении объёма газа
- •§11. Политропический процесс
- •Вопросы и задания для самостоятельной работы студентов Основы термодинамики. I начало термодинамики
- •§12. II начало термодинамики
- •Различные формулировки основного постулата, выражающего II начало термодинамики
- •§13. Равновесные состояния
- •§14. Обратимые и необратимые процессы
- •Необратимость и вероятность
- •§15. Цикл Карно
- •Коэффициент полезного действия в цикле Карно
- •§16. Холодильная машина
- •§17. Свободная энергия
- •§18. Энтропия
- •§19. Некоторые термодинамические соотношения
- •§20. Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •§21. Энтропия и вероятность
- •§22. Энтропия и беспорядок
- •§23. Третье начало термодинамики
- •Вопросы для контроля самостоятельной работы студентов
- •II начало термодинамики. Энтропия.
- •Глава 2. Неравновесная термодинамика §1. Основные принципы линейной термодинамики
- •§2. Нелинейная термодинамика
- •§3. Принцип синергетики
- •Свойства и примеры самоорганизации диссипативных структур
- •Глава 3. Статистическая физика и её применение к идеальному газу
- •§1. Давление газа с точки зрения молекулярно – кинетической теории
- •§2. Температура как мера средней энергии хаотичного движения молекул
- •Скорость газовых молекул
- •§3. Броуновское движение
- •§4. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •§5. Классическая теория теплоёмкости и её недостатки
- •§6. Барометрическая формула
- •Закон Больцмана
- •§7. Распределение молекул по скоростям
- •§8. Функция распределения
- •§9. Формула Максвелла
- •§10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •§11. Среднее число молекул, сталкивающихся со стенкой сосуда
- •Вопросы для контроля знаний студентов Молекулярно-кинетическая теория
- •Глава 4. Явления переноса §1. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •§4. Явление переноса в газах. Уравнение переноса
- •§5. Диффузия
- •§6. Нестационарная диффузия
- •§7. Теплопроводность газов
- •§8. Вязкость газов (внутреннее трение)
- •§9. Соотношения между коэффициентами переноса
- •§10. Физические явления в разреженных газах
- •Вопросы для самостоятельного контроля знаний студентов Явления переноса
- •Глава 5 §1. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •Уравнение Ван-Дер-Ваальса
- •§2. Учет сил отталкивания между молекулами
- •§3. Учет сил притяжения между молекулами
- •§4. Изотермы Ван-дер-Ваальса
- •§5. Критическая температура и критическое состояние
- •§6. Недостатки уравнения Ван-дер-Ваальса
- •§7. Внутренняя энергия газа Ван-дер-Ваальса
- •§8. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •§9. Сжижение газов
- •Эффект Джоуля-Томсона
- •Вопросы для самоконтроля изученного материала Реальные газы
- •Глава 6. Жидкое состояние §1.Строение жидкостей
- •§2. Поверхностное натяжение
- •§3. Условия равновесия на границе двух сред. Краевой угол
- •§4. Граница жидкости и твердого тела
- •§5. Силы, возникающие на кривой поверхности жидкости
- •§6. Капиллярные явления
- •§7. Упругость насыщенного пара над кривой поверхностью жидкости
- •Вопросы для самоконтроля знаний студентов
- •Глава 7. Жидкие растворы §1. Свойства растворов
- •§2. Упругость насыщенного пара над идеальным раствором
- •§3. Закон Генри
- •§4. Осмотическое давление
- •Глава 8. Кристаллическое состояние §1. Отличительные черты кристаллического состояния
- •§2. Классификация кристаллов
- •§3. Физические типы кристаллических решеток
- •§4. Тепловое движение в кристаллах
- •Глава 9. Фазовые переходы §1. Фаза и фазовые равновесия
- •§2. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
- •Вопросы для самоконтроля знаний студентов
- •Содержание
Глава 8. Кристаллическое состояние §1. Отличительные черты кристаллического состояния
Подавляющее большинство твердых тел в природе имеет кристаллическое строение. Характерная черта кристаллического состояния, отличающее его от жидкого и газообразного состояний, заключается в наличии анизотропии, т.е. зависимости ряда физических свойств (механических, тепловых, оптических, электрических) от направления. Причиной анизотропии кристаллов является упорядоченное расположение частиц (атомов, молекул), из которых они построены. Упорядоченное расположение частиц проявляется в правильной внешней огранке кристаллов. Кристаллы ограничены плоскими гранями, пересекающимися под некоторыми углами. Правильность геометрической формы и анизотропия кристаллов обычно не проявляются по той причине, что кристаллические тела встречаются, как правило, в виде поликристаллов, т.е. конгломератов множества сросшихся между собой беспорядочно ориентированных мелких кристалликов. В поликристаллах анизотропия наблюдается только в пределах каждого отдельно взятого кристаллика, тело же вследствие беспорядочной ориентации кристалликов анизотропии не обнаруживает.
Упорядоченность расположения атомов кристалла заключается в том, что атомы размещаются в узлах геометрически правильной пространственной решетки. Весь кристалл может быть получен путем многократного повторения в трех различных направлениях одного и того же структурного элемента, называемого элементарной кристаллической ячейкой (рис.1).
Д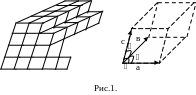 лины
ребер
лины
ребер
![]() кристаллической
ячейки называются периодами идентичности
кристалла. Кристаллическая ячейка
представляет собой параллелепипед,
построенный на трех векторах
кристаллической
ячейки называются периодами идентичности
кристалла. Кристаллическая ячейка
представляет собой параллелепипед,
построенный на трех векторах
![]() ,
модули которых равны периодам идентичности.
Этот параллелепипед, кроме ребер
характеризуется
так же углами
,
модули которых равны периодам идентичности.
Этот параллелепипед, кроме ребер
характеризуется
так же углами
![]() и
и
![]() между ребрами.
Величины
между ребрами.
Величины
![]() и
и
однозначно
определяют элементарную ячейку и
называются ее параметрами. Элементарную
ячейку можно выбрать различными
способами. Кристаллическая ячейка,
включающая наименьшее число атомов,
характеризующих химический состав
кристаллического вещества (например,
один атом кислорода и два атома водорода
для кристаллов льда) называется
примитивной ячейкой. Однако обычно
вместо примитивной выбирают элементарную
ячейку с большим числом атомов, но
обладающую такой же симметрией, как и
весь кристалл в целом.
и
и
однозначно
определяют элементарную ячейку и
называются ее параметрами. Элементарную
ячейку можно выбрать различными
способами. Кристаллическая ячейка,
включающая наименьшее число атомов,
характеризующих химический состав
кристаллического вещества (например,
один атом кислорода и два атома водорода
для кристаллов льда) называется
примитивной ячейкой. Однако обычно
вместо примитивной выбирают элементарную
ячейку с большим числом атомов, но
обладающую такой же симметрией, как и
весь кристалл в целом.
§2. Классификация кристаллов
Кристаллическая решетка может обладать различными видами симметрии. Под симметрией кристаллической решетки понимается свойство решетки
совпадать с самой
собой при некоторых пространственных
перемещениях. Всякая решетка, прежде
всего, обладает трансляционной
симметрией, т.е. совпадает сама собой
при перемещении (трансляции) на величину
периода идентичности. Из других видов
симметрии отметим симметрию по отношению
к поворотам вокруг некоторых осей, а
также к зеркальному отражению относительно
определенных плоскостей. Если решетка
совпадает само собой при повороте вокруг
некоторой оси на угол
![]() ,
т.е. за один поворот вокруг оси решетка
совпадает сама с собой
раз, то эта ось называется осью симметрии
-го
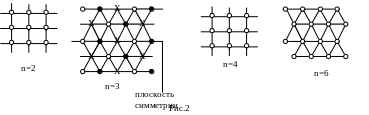
порядка. Примеры структур, обладающих
такими осями симметрии, показаны на
рисунке 2 (белыми кружками, черными
кружками и крестиками обозначены атомы
разных сортов).
,
т.е. за один поворот вокруг оси решетка
совпадает сама с собой
раз, то эта ось называется осью симметрии
-го
порядка. Примеры структур, обладающих
такими осями симметрии, показаны на
рисунке 2 (белыми кружками, черными
кружками и крестиками обозначены атомы
разных сортов).
Плоскости, при зеркальном отражении от которых решетка совпадает само с собой, называется плоскостями симметрии.
Различные виды симметрии называются элементами симметрии кристаллической решетки.
Кристаллическая решетка, как правило, обладает одновременно несколькими видами симметрии. Однако не всякое сочетание элементов симметрии оказывается возможным. Как показал выдающийся русский ученый Е.С.Федоров, возможны 230 комбинаций элементов, получивших название пространственных групп. Эти 230 пространственные группы разбиваются по признакам симметрии на 32 класса. Наконец, по форме элементарной ячейки все кристаллы делятся на семь кристаллографических систем (или сингоний), каждая из которых включает в себя несколько классов симметрии. В порядке возрастающей симметрии кристаллографические системы располагаются следующим образом:
Триклинная система. Для нее характерно, что
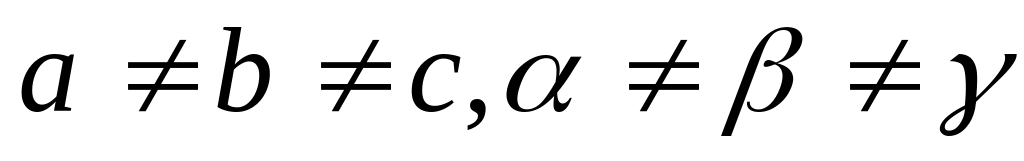 .
Элементарная ячейка имеет форму
косоугольного параллелепипеда.
.
Элементарная ячейка имеет форму
косоугольного параллелепипеда.Моноклинная система. Два угла - прямые, третий (в качестве которого принято выбирать угол
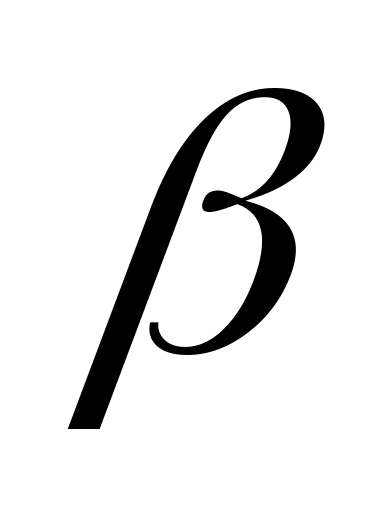 ),
отличен от нуля. Элементарная ячейка
имеет форму прямой призмы, в основании
которой лежит параллелограмм (т.е. форму
прямого параллелепипеда).
),
отличен от нуля. Элементарная ячейка
имеет форму прямой призмы, в основании
которой лежит параллелограмм (т.е. форму
прямого параллелепипеда).Ромбическая система. Все углы прямые, все ребра разные:
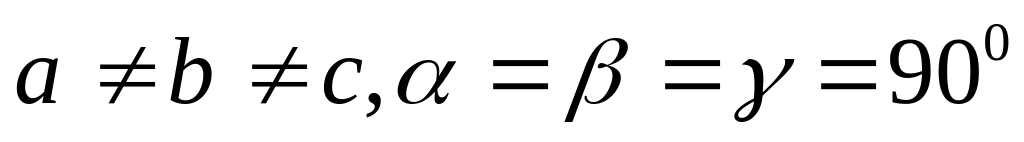 .
Элементарная ячейка имеет форму
прямоугольного параллелепипеда.
.
Элементарная ячейка имеет форму
прямоугольного параллелепипеда.Тетрогональная система. Все углы прямые, два ребра одинаковые:
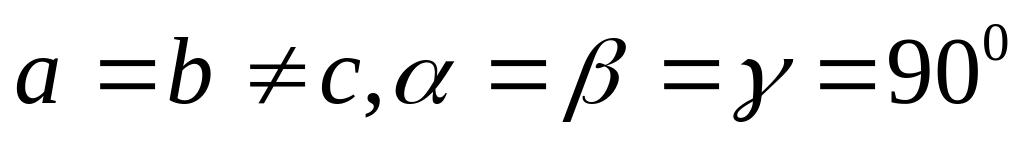 .
Элементарная ячейка имеет форму прямой
призмы с квадратным основанием.
.
Элементарная ячейка имеет форму прямой
призмы с квадратным основанием.Ромбоэдрическая (или тригональная) система. Все ребра одинаковые, все углы также одинаковые и отличные от прямого
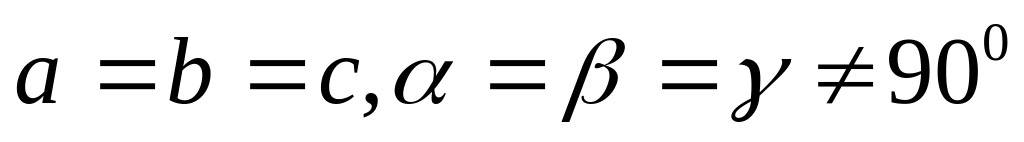 .
Элементарная ячейка имеет форму куба,
деформированного сжатием или растяжением
вдоль диагонали.
.
Элементарная ячейка имеет форму куба,
деформированного сжатием или растяжением
вдоль диагонали.Гексогональная система. Ребра и углы между ними удовлетворяют условиям:
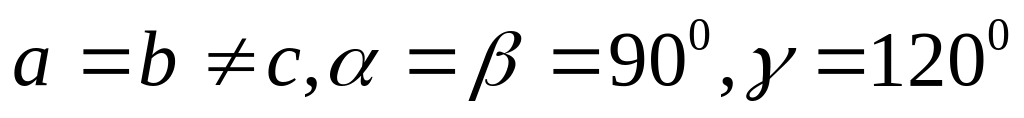 .
.Кубическая система. Все ребра одинаковые, все углы прямые
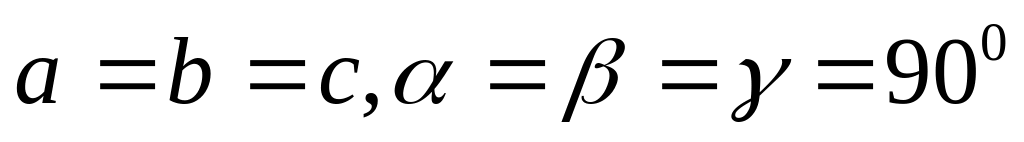 .
Элементарная ячейка имеет форму куба.
.
Элементарная ячейка имеет форму куба.
