
- •Предисловие
- •Программа курса «Молекулярная физика. Термодинамика.»
- •2. Учебно-тематический план
- •3. Содержание курса
- •4. Примерная тематика семинарских занятий
- •5. Средства обеспечения дисциплины
- •Введение
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •Глава 1 Термодинамика
- •§1. Температура и термодинамическое равновесие
- •Давление
- •§2. Уравнение состояния идеального газа
- •§3. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Закон Авогадро
- •Закон Дальтона
- •§4. Первое начало термодинамики
- •§5. Макроскопическая работа
- •I начало термодинамики для системы в адиабатической оболочке
- •§6. Внутренняя энергия
- •§7. Количество теплоты. Математическая формулировка первого начала термодинамики
- •§8. Различные приложения I начала термодинамики. Теплоёмкость
- •§9. Внутренняя энергия идеального газа. Закон Джоуля
- •Уравнение Роберта Майера
- •§10. Адиабатический процесс. Уравнение Пуассона
- •Работа при адиабатическом изменении объёма газа
- •§11. Политропический процесс
- •Вопросы и задания для самостоятельной работы студентов Основы термодинамики. I начало термодинамики
- •§12. II начало термодинамики
- •Различные формулировки основного постулата, выражающего II начало термодинамики
- •§13. Равновесные состояния
- •§14. Обратимые и необратимые процессы
- •Необратимость и вероятность
- •§15. Цикл Карно
- •Коэффициент полезного действия в цикле Карно
- •§16. Холодильная машина
- •§17. Свободная энергия
- •§18. Энтропия
- •§19. Некоторые термодинамические соотношения
- •§20. Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •§21. Энтропия и вероятность
- •§22. Энтропия и беспорядок
- •§23. Третье начало термодинамики
- •Вопросы для контроля самостоятельной работы студентов
- •II начало термодинамики. Энтропия.
- •Глава 2. Неравновесная термодинамика §1. Основные принципы линейной термодинамики
- •§2. Нелинейная термодинамика
- •§3. Принцип синергетики
- •Свойства и примеры самоорганизации диссипативных структур
- •Глава 3. Статистическая физика и её применение к идеальному газу
- •§1. Давление газа с точки зрения молекулярно – кинетической теории
- •§2. Температура как мера средней энергии хаотичного движения молекул
- •Скорость газовых молекул
- •§3. Броуновское движение
- •§4. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •§5. Классическая теория теплоёмкости и её недостатки
- •§6. Барометрическая формула
- •Закон Больцмана
- •§7. Распределение молекул по скоростям
- •§8. Функция распределения
- •§9. Формула Максвелла
- •§10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •§11. Среднее число молекул, сталкивающихся со стенкой сосуда
- •Вопросы для контроля знаний студентов Молекулярно-кинетическая теория
- •Глава 4. Явления переноса §1. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •§4. Явление переноса в газах. Уравнение переноса
- •§5. Диффузия
- •§6. Нестационарная диффузия
- •§7. Теплопроводность газов
- •§8. Вязкость газов (внутреннее трение)
- •§9. Соотношения между коэффициентами переноса
- •§10. Физические явления в разреженных газах
- •Вопросы для самостоятельного контроля знаний студентов Явления переноса
- •Глава 5 §1. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •Уравнение Ван-Дер-Ваальса
- •§2. Учет сил отталкивания между молекулами
- •§3. Учет сил притяжения между молекулами
- •§4. Изотермы Ван-дер-Ваальса
- •§5. Критическая температура и критическое состояние
- •§6. Недостатки уравнения Ван-дер-Ваальса
- •§7. Внутренняя энергия газа Ван-дер-Ваальса
- •§8. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •§9. Сжижение газов
- •Эффект Джоуля-Томсона
- •Вопросы для самоконтроля изученного материала Реальные газы
- •Глава 6. Жидкое состояние §1.Строение жидкостей
- •§2. Поверхностное натяжение
- •§3. Условия равновесия на границе двух сред. Краевой угол
- •§4. Граница жидкости и твердого тела
- •§5. Силы, возникающие на кривой поверхности жидкости
- •§6. Капиллярные явления
- •§7. Упругость насыщенного пара над кривой поверхностью жидкости
- •Вопросы для самоконтроля знаний студентов
- •Глава 7. Жидкие растворы §1. Свойства растворов
- •§2. Упругость насыщенного пара над идеальным раствором
- •§3. Закон Генри
- •§4. Осмотическое давление
- •Глава 8. Кристаллическое состояние §1. Отличительные черты кристаллического состояния
- •§2. Классификация кристаллов
- •§3. Физические типы кристаллических решеток
- •§4. Тепловое движение в кристаллах
- •Глава 9. Фазовые переходы §1. Фаза и фазовые равновесия
- •§2. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
- •Вопросы для самоконтроля знаний студентов
- •Содержание
§19. Некоторые термодинамические соотношения
Энтропия, будучи функцией состояния тела, может служить таким же параметром состояния тела как T,V,P. Энтропия S может быть выражена через любые из двух параметров P,V,T. Рассмотрим, как это делается. Это тем более интересно, поскольку S нельзя измерить на эксперименте.
Из термодинамического тождества (1.39) имеем
![]() ,
,
![]()
![]() .
.
Из любых из четырёх величин T,S,P и V, входящих в это уравнение, можно выбрать в качестве независимых переменных две, через которые можно выразить остальные. Выберем в качестве независимых переменных T и Р, то есть состояние системы изменяется в результате изменения T и Р. Вычислим изменение dS. Поскольку энтропия является функцией состояния, ее полный дифференциал dS можно представить в виде
![]() .
(1.40)
.
(1.40)
Учитывая, что,
![]() где
СР
–теплоемкость при постоянном давлении,
выражение (1.40) имеет вид
где
СР
–теплоемкость при постоянном давлении,
выражение (1.40) имеет вид
![]() .
(1.41)
.
(1.41)
Для расчета
производной
![]() воспользуемся
методом термодинамических потенциалов.
Одним из потенциалов термодинамики
является внутренняя энергия U,
дифференциал
которой равен
воспользуемся
методом термодинамических потенциалов.
Одним из потенциалов термодинамики
является внутренняя энергия U,
дифференциал
которой равен
dU=TdS-PdV (1.42)
Введем еще потенциалы:
H= U+PV- энтальпия или теплосодержание;
F=U-TS- cвободная энергия;
Ф=U-TS+PV- большой термодинамический потенциал.
Дифференциалы этих потенциалов с учетом (1.42) имеют вид:
dH=TdS+VdP
dF=-SdT-PdV
dФ=-SdT+VdP.
Поскольку все термодинамические потенциалы являются функциями состояния и имеют полные дифференциалы, для них справедливы соотношения
![]() ,
(1.43)
,
(1.43)
![]() ,
(1.44)
,
(1.44)
![]() ,
(1.45)
,
(1.45)
![]() .
(1.46)
.
(1.46)
Из (1.43) с учетом выражения (1.42) для dU имеем
![]() .
(1.47)
.
(1.47)
Из (1.44) с учетом выражения для dH получим
![]() .
(1.48)
.
(1.48)
Из (1.45) с учетом выражения для dF получим
![]() .
(1.49)
.
(1.49)
Из (1.46) и выражения для dФ имеем
![]() .
(1.50)
.
(1.50)
Выражения (1.47)-(1.50) называют соотношениями Максвелла.
Формулу (1.41), используя соотношение (1.47), перепишем в виде
![]() .
(1.51)
.
(1.51)
Считая, что энтропия является функцией температуры и объема, используя соотношение (1.49), можно записать следующее выражение для дифференциала энтропии
![]() .
.
Поскольку
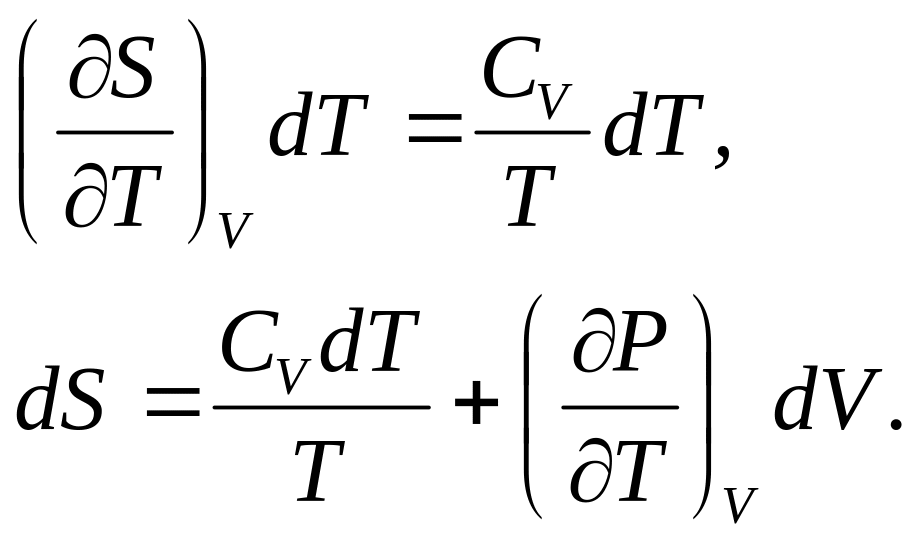 (1.52)
(1.52)
Используя (1.51) и (1.52) можно вычислить энтропию для данной массы вещества при данных значениях объема V и температуры Т, которую обозначим S(T,V), или при данных значениях давления Р и температуры Т S(P,T), если известны значения энтропии S(T0,V0) и S(T0,P0) при каких-нибудь других значениях этих параметров V0 и Т0 или Р0 и Т0..
П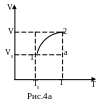 усть
система переходит из состояния 1 в
состояние 2 по пути, указанной на рис.
4а. Поскольку энтропия является функцией
состояния и ее изменение не зависит от
формы пути, а определяется конечным и
начальным состоянием,
усть
система переходит из состояния 1 в
состояние 2 по пути, указанной на рис.
4а. Поскольку энтропия является функцией
состояния и ее изменение не зависит от
формы пути, а определяется конечным и
начальным состоянием,
![]() по пути 12 совпадет со значением изменения
энтропии
по пути 12 совпадет со значением изменения
энтропии
![]() по пути 1а2, т.е.
по пути 1а2, т.е.
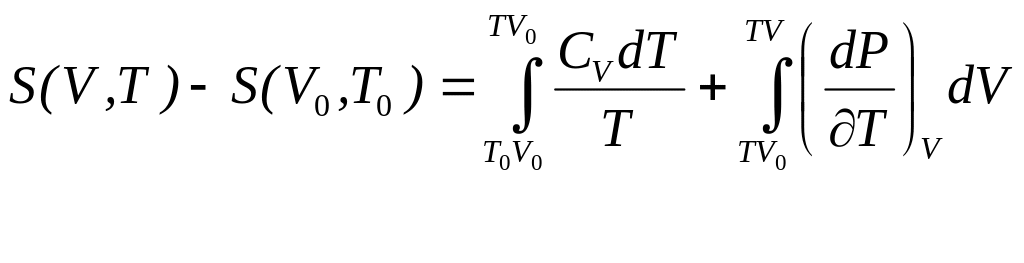 .
.
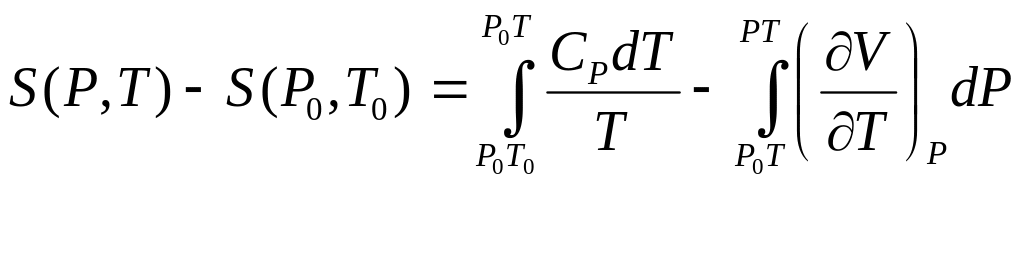 .
.
В частности для 1 моля идеального газа
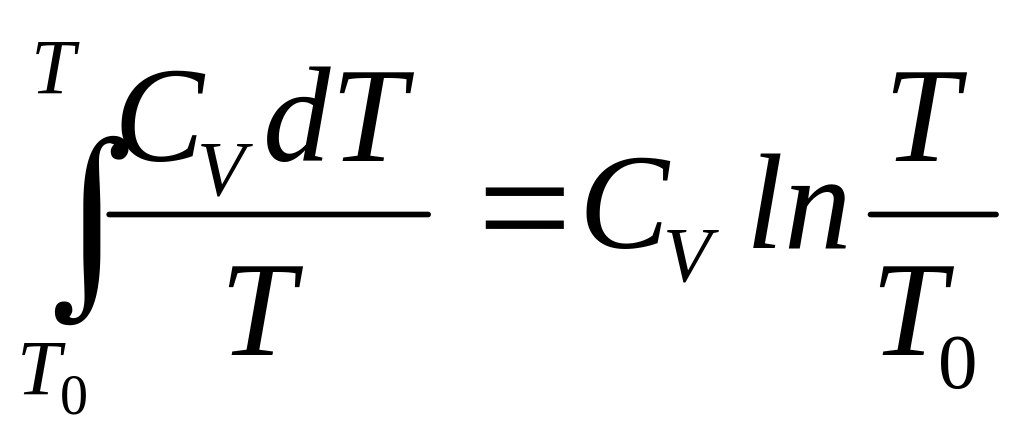 ,
,
а
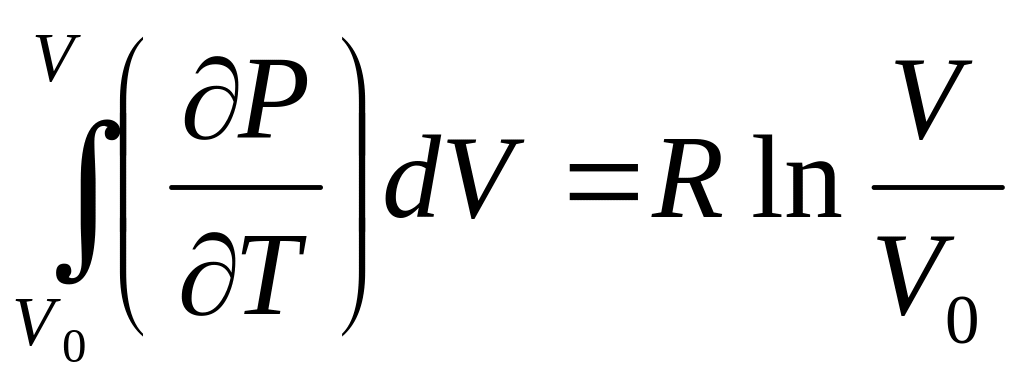 так как
так как
![]() .
.
Таким образом, для идеального газа
![]() .
.
Это значит, что энтропия идеального газа возрастает с увеличением объема и температуры.
