
- •Предисловие
- •Программа курса «Молекулярная физика. Термодинамика.»
- •2. Учебно-тематический план
- •3. Содержание курса
- •4. Примерная тематика семинарских занятий
- •5. Средства обеспечения дисциплины
- •Введение
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •Глава 1 Термодинамика
- •§1. Температура и термодинамическое равновесие
- •Давление
- •§2. Уравнение состояния идеального газа
- •§3. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Закон Авогадро
- •Закон Дальтона
- •§4. Первое начало термодинамики
- •§5. Макроскопическая работа
- •I начало термодинамики для системы в адиабатической оболочке
- •§6. Внутренняя энергия
- •§7. Количество теплоты. Математическая формулировка первого начала термодинамики
- •§8. Различные приложения I начала термодинамики. Теплоёмкость
- •§9. Внутренняя энергия идеального газа. Закон Джоуля
- •Уравнение Роберта Майера
- •§10. Адиабатический процесс. Уравнение Пуассона
- •Работа при адиабатическом изменении объёма газа
- •§11. Политропический процесс
- •Вопросы и задания для самостоятельной работы студентов Основы термодинамики. I начало термодинамики
- •§12. II начало термодинамики
- •Различные формулировки основного постулата, выражающего II начало термодинамики
- •§13. Равновесные состояния
- •§14. Обратимые и необратимые процессы
- •Необратимость и вероятность
- •§15. Цикл Карно
- •Коэффициент полезного действия в цикле Карно
- •§16. Холодильная машина
- •§17. Свободная энергия
- •§18. Энтропия
- •§19. Некоторые термодинамические соотношения
- •§20. Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •§21. Энтропия и вероятность
- •§22. Энтропия и беспорядок
- •§23. Третье начало термодинамики
- •Вопросы для контроля самостоятельной работы студентов
- •II начало термодинамики. Энтропия.
- •Глава 2. Неравновесная термодинамика §1. Основные принципы линейной термодинамики
- •§2. Нелинейная термодинамика
- •§3. Принцип синергетики
- •Свойства и примеры самоорганизации диссипативных структур
- •Глава 3. Статистическая физика и её применение к идеальному газу
- •§1. Давление газа с точки зрения молекулярно – кинетической теории
- •§2. Температура как мера средней энергии хаотичного движения молекул
- •Скорость газовых молекул
- •§3. Броуновское движение
- •§4. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •§5. Классическая теория теплоёмкости и её недостатки
- •§6. Барометрическая формула
- •Закон Больцмана
- •§7. Распределение молекул по скоростям
- •§8. Функция распределения
- •§9. Формула Максвелла
- •§10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •§11. Среднее число молекул, сталкивающихся со стенкой сосуда
- •Вопросы для контроля знаний студентов Молекулярно-кинетическая теория
- •Глава 4. Явления переноса §1. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •§4. Явление переноса в газах. Уравнение переноса
- •§5. Диффузия
- •§6. Нестационарная диффузия
- •§7. Теплопроводность газов
- •§8. Вязкость газов (внутреннее трение)
- •§9. Соотношения между коэффициентами переноса
- •§10. Физические явления в разреженных газах
- •Вопросы для самостоятельного контроля знаний студентов Явления переноса
- •Глава 5 §1. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •Уравнение Ван-Дер-Ваальса
- •§2. Учет сил отталкивания между молекулами
- •§3. Учет сил притяжения между молекулами
- •§4. Изотермы Ван-дер-Ваальса
- •§5. Критическая температура и критическое состояние
- •§6. Недостатки уравнения Ван-дер-Ваальса
- •§7. Внутренняя энергия газа Ван-дер-Ваальса
- •§8. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •§9. Сжижение газов
- •Эффект Джоуля-Томсона
- •Вопросы для самоконтроля изученного материала Реальные газы
- •Глава 6. Жидкое состояние §1.Строение жидкостей
- •§2. Поверхностное натяжение
- •§3. Условия равновесия на границе двух сред. Краевой угол
- •§4. Граница жидкости и твердого тела
- •§5. Силы, возникающие на кривой поверхности жидкости
- •§6. Капиллярные явления
- •§7. Упругость насыщенного пара над кривой поверхностью жидкости
- •Вопросы для самоконтроля знаний студентов
- •Глава 7. Жидкие растворы §1. Свойства растворов
- •§2. Упругость насыщенного пара над идеальным раствором
- •§3. Закон Генри
- •§4. Осмотическое давление
- •Глава 8. Кристаллическое состояние §1. Отличительные черты кристаллического состояния
- •§2. Классификация кристаллов
- •§3. Физические типы кристаллических решеток
- •§4. Тепловое движение в кристаллах
- •Глава 9. Фазовые переходы §1. Фаза и фазовые равновесия
- •§2. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
- •Вопросы для самоконтроля знаний студентов
- •Содержание
§12. II начало термодинамики
I начало термодинамики не даёт указаний относительно направления, в котором могут происходить процессы в природе. Для изолированной системы I закон термодинамики требует только то, чтобы при всех процессах энергия системы оставалась постоянной. Если 1 и 2 – два состояния такой системы, то I закон ничего не может сказать, будет ли система переходить из состояния 1 в состояние 2, или из состояния 2 в состояние 1. Пусть два тела находятся в адиабатической оболочке и взаимодействуют между собой. Тогда Q1=-Q2, т.е. тепло Q1 полученное одним телом, равно теплу Q2, отданному другим телом. В каком направлении будет переходить тепло, I закон термодинамики не отвечает. Согласно I закону тепло может переходить от менее нагретого к более нагретому, хотя в действительности такой процесс самопроизвольно не идёт. I закон термодинамики не даёт количественную меру температуры.
II начало термодинамики, наоборот, позволяет судить о направлении процесса. Кроме того, II закон термодинамики позволяет решить вопрос о количественной мере температуры и позволяет построить температурную шкалу, не зависящую от произвола выбора термометрического тела и устройства термометра.
Различные формулировки основного постулата, выражающего II начало термодинамики
Чтобы прийти к формулировке постулата II закона термодинамики, рассмотрим схематически работу тепловой машины (рис.1). В цилиндре помещается газ или какое – либо другое вещество, называемое рабочим телом.
П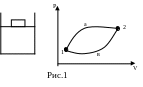 усть
начальное состояние тела 1.
Приведем дно цилиндра в тепловой контакт
с нагревателем, т. е. с телом, температура
которого выше температуры газа в
цилиндре. Газ будет нагреваться и
расширяться по кривой 1а2.
Рабочее вещество получит от нагревателя
тепло Q1
и совершит положительную работу.
Согласно I
закону термодинамики
усть
начальное состояние тела 1.
Приведем дно цилиндра в тепловой контакт
с нагревателем, т. е. с телом, температура
которого выше температуры газа в
цилиндре. Газ будет нагреваться и
расширяться по кривой 1а2.
Рабочее вещество получит от нагревателя
тепло Q1
и совершит положительную работу.
Согласно I
закону термодинамики
![]() .
(1.30)
.
(1.30)
Теперь надо вернуть поршень в исходное положение. Это надо сделать так, чтобы работа A2 затраченная на сжатие была меньше A1 (в этом случае мы получим полезную работу). С этой целью приведём дно цилиндра в тепловой контакт с холодильником, температура которого ниже температуры газа в цилиндре и сожмём газ по пути 2в1. При этом газ вернётся в исходное положение 1 и отдаст холодильнику тепло Q2.
![]() .
(1.31)
.
(1.31)
Отсюда в комбинации с (1.30) имеем
![]() .
.
Таким образом, тепловая машина совершила круговой процесс, в результате которого нагреватель отдал тепло Q1, холодильник получил тепло Q2, а тепло Q1-Q2 – пошёл на производство полезной работы A1-A2. Отношение
![]() (1.32)
(1.32)
называется коэффициент полезного действия. Возникает вопрос нельзя ли построить периодически действующую тепловую машину без холодильника, т. е. чтоб Q2=0 и =1. В этом случае тепловая машина превратила бы в работу всю теплоту, полученную от теплового резервуара. Возможность её построение не противоречит закону сохранения энергии. Такую машину Оствальд назвал вечным двигателем II рода. Опытные данные говорят против возможности двигателя II рода и это возведен в постулат и является постулатом II начала термодинамики.
Томсон дал такую формулировку постулаты II начала термодинамики: невозможен круговой процесс, единственным результатом которого было бы производство работы за счёт охлаждения теплового резервуара.
Планк сформулировал постулату II начало термодинамики следующим образом: невозможно построить периодически действующую машину, единственным результатом которой было бы поднятие груза за счёт охлаждения теплового резервуара.
Формулировка Клаузиуса: «Теплота не может самопроизвольно переходить от тела менее нагретого к более нагретому, при условии, что во всех окружающих телах никаких изменений нет.
Прежде чем как перейти к подробному изучению II начало термодинамики рассмотрим некоторые термодинамические понятия.
