
- •Предисловие
- •Программа курса «Молекулярная физика. Термодинамика.»
- •2. Учебно-тематический план
- •3. Содержание курса
- •4. Примерная тематика семинарских занятий
- •5. Средства обеспечения дисциплины
- •Введение
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •Глава 1 Термодинамика
- •§1. Температура и термодинамическое равновесие
- •Давление
- •§2. Уравнение состояния идеального газа
- •§3. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Закон Авогадро
- •Закон Дальтона
- •§4. Первое начало термодинамики
- •§5. Макроскопическая работа
- •I начало термодинамики для системы в адиабатической оболочке
- •§6. Внутренняя энергия
- •§7. Количество теплоты. Математическая формулировка первого начала термодинамики
- •§8. Различные приложения I начала термодинамики. Теплоёмкость
- •§9. Внутренняя энергия идеального газа. Закон Джоуля
- •Уравнение Роберта Майера
- •§10. Адиабатический процесс. Уравнение Пуассона
- •Работа при адиабатическом изменении объёма газа
- •§11. Политропический процесс
- •Вопросы и задания для самостоятельной работы студентов Основы термодинамики. I начало термодинамики
- •§12. II начало термодинамики
- •Различные формулировки основного постулата, выражающего II начало термодинамики
- •§13. Равновесные состояния
- •§14. Обратимые и необратимые процессы
- •Необратимость и вероятность
- •§15. Цикл Карно
- •Коэффициент полезного действия в цикле Карно
- •§16. Холодильная машина
- •§17. Свободная энергия
- •§18. Энтропия
- •§19. Некоторые термодинамические соотношения
- •§20. Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •§21. Энтропия и вероятность
- •§22. Энтропия и беспорядок
- •§23. Третье начало термодинамики
- •Вопросы для контроля самостоятельной работы студентов
- •II начало термодинамики. Энтропия.
- •Глава 2. Неравновесная термодинамика §1. Основные принципы линейной термодинамики
- •§2. Нелинейная термодинамика
- •§3. Принцип синергетики
- •Свойства и примеры самоорганизации диссипативных структур
- •Глава 3. Статистическая физика и её применение к идеальному газу
- •§1. Давление газа с точки зрения молекулярно – кинетической теории
- •§2. Температура как мера средней энергии хаотичного движения молекул
- •Скорость газовых молекул
- •§3. Броуновское движение
- •§4. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •§5. Классическая теория теплоёмкости и её недостатки
- •§6. Барометрическая формула
- •Закон Больцмана
- •§7. Распределение молекул по скоростям
- •§8. Функция распределения
- •§9. Формула Максвелла
- •§10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •§11. Среднее число молекул, сталкивающихся со стенкой сосуда
- •Вопросы для контроля знаний студентов Молекулярно-кинетическая теория
- •Глава 4. Явления переноса §1. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •§4. Явление переноса в газах. Уравнение переноса
- •§5. Диффузия
- •§6. Нестационарная диффузия
- •§7. Теплопроводность газов
- •§8. Вязкость газов (внутреннее трение)
- •§9. Соотношения между коэффициентами переноса
- •§10. Физические явления в разреженных газах
- •Вопросы для самостоятельного контроля знаний студентов Явления переноса
- •Глава 5 §1. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •Уравнение Ван-Дер-Ваальса
- •§2. Учет сил отталкивания между молекулами
- •§3. Учет сил притяжения между молекулами
- •§4. Изотермы Ван-дер-Ваальса
- •§5. Критическая температура и критическое состояние
- •§6. Недостатки уравнения Ван-дер-Ваальса
- •§7. Внутренняя энергия газа Ван-дер-Ваальса
- •§8. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •§9. Сжижение газов
- •Эффект Джоуля-Томсона
- •Вопросы для самоконтроля изученного материала Реальные газы
- •Глава 6. Жидкое состояние §1.Строение жидкостей
- •§2. Поверхностное натяжение
- •§3. Условия равновесия на границе двух сред. Краевой угол
- •§4. Граница жидкости и твердого тела
- •§5. Силы, возникающие на кривой поверхности жидкости
- •§6. Капиллярные явления
- •§7. Упругость насыщенного пара над кривой поверхностью жидкости
- •Вопросы для самоконтроля знаний студентов
- •Глава 7. Жидкие растворы §1. Свойства растворов
- •§2. Упругость насыщенного пара над идеальным раствором
- •§3. Закон Генри
- •§4. Осмотическое давление
- •Глава 8. Кристаллическое состояние §1. Отличительные черты кристаллического состояния
- •§2. Классификация кристаллов
- •§3. Физические типы кристаллических решеток
- •§4. Тепловое движение в кристаллах
- •Глава 9. Фазовые переходы §1. Фаза и фазовые равновесия
- •§2. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
- •Вопросы для самоконтроля знаний студентов
- •Содержание
§7. Упругость насыщенного пара над кривой поверхностью жидкости
 Испарение
жидкости происходит с ее поверхности.
Поэтому изменение свойств поверхностного
слоя должно изменить условия равновесия
между жидкостью и паром над ней. В
частности, на условиях равновесия, а
значит и на упругости насыщенного пара
должна сказаться кривизна поверхности
жидкости. Это значит, упругость насыщенного
пара над кривой поверхностью должна
отличаться от упругости его над плоской
поверхностью. Вычислим, насколько
упругость насыщенного пара над кривой
и плоской поверхностями отличаются
друг от друга.
Испарение
жидкости происходит с ее поверхности.
Поэтому изменение свойств поверхностного
слоя должно изменить условия равновесия
между жидкостью и паром над ней. В
частности, на условиях равновесия, а
значит и на упругости насыщенного пара
должна сказаться кривизна поверхности
жидкости. Это значит, упругость насыщенного
пара над кривой поверхностью должна
отличаться от упругости его над плоской
поверхностью. Вычислим, насколько
упругость насыщенного пара над кривой
и плоской поверхностями отличаются
друг от друга.
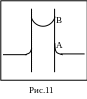
Представим себе замкнутый сосуд с жидкостью, в которую частично погружена капиллярная трубка К, полностью смачиваемая жидкостью (рис.11).
Под действием капиллярных сил жидкость в трубке поднимается на высоту , определяемую формулой
![]() .
(6.18)
.
(6.18)
Упругость пара в точке. В, т.е. над вогнутой поверхностью можно определить, пользуясь барометрической формулой
![]() .
(6.19)
.
(6.19)
Поставив в (6.19) значение из (6.18), получим:
![]() (6.20)
(6.20)
или
![]() .
(6.21)
.
(6.21)
Разложив в (6.20) экспоненту в ряд Тейлора и, ограничиваясь первыми двумя членами разложения, имеем:
![]() .
(6.22)
.
(6.22)
Если учесть, что насыщенный пар подчиняется уравнению состояния идеального газа
![]() ,
,
где
![]() - плотность
насыщенного пара, уравнение (6.22) можно
переписать в виде:
- плотность
насыщенного пара, уравнение (6.22) можно
переписать в виде:
![]() .
(6.23)
.
(6.23)
Таким образом,
упругость насыщенного пара над вогнутой
поверхностью меньше, чем над плоской
на величину
![]() .
Очевидно, что точно таким же образом
можно показать, что над выпуклой
поверхностью упругость насыщенного
пара больше, чем под плоской на ту же
величину
.
Очевидно, что точно таким же образом
можно показать, что над выпуклой
поверхностью упругость насыщенного
пара больше, чем под плоской на ту же
величину
![]() .
.
Вопросы для самоконтроля знаний студентов
Запишите выражение для коэффициента сжимаемости.
Чем объясняется малая сжимаемость жидкостей?
Как зависит коэффициент сжимаемости жидкостей от давления и температуры?
Запишите выражение для коэффициента объемного расширения жидкостей.
Каковы особенности теплоемкости жидкостей?
Чем объясняется низкое значение коэффициента диффузии в жидкостях?
Каков физический смысл коэффициента поверхностного натяжения?
Что такое сила поверхностного натяжения?
Наблюдаются случаи удержания на поверхности жидкости тела, плотность которого больше, чем плотность жидкости. Чем это объясняется?
Как объясняется явление, когда тело с плотностью, меньшей плотности жидкости, погружается в жидкость?
Что такое капиллярное давление?
Что такое краевые углы?
Запишите условие равновесия жидкости на границе двух сред.
Запишите условие равновесия жидкости на границе с твердым телом.
Как определяется сила сцепления между смачиваемыми пластинами?
Молекулы жидкости, подобно частицам твердого тела, совершают колебания около некоторых положений равновесия. В чем же отличие в поведении молекул жидких тел от поведения молекул в газах и в твердых телах?
В чем причина малой сжимаемости жидкостей и особых свойств поверхностного слоя?
В опыте Плато капля оливкового масла помещается в смесь спирта с водой такой плотности, что капля масла находится во взвешенном состоянии. Какова форма капли масла и почему?
Каким должен быть наибольший диаметр стальной иголки, чтобы смазанная жиром, она могла держаться в горизонтальном положении на поверхности воды?
Как изменяются размеры больших и малых капель, находящихся рядом при испарении.
Что можно говорить о соотношении между теплоемкостями Ср и Cv для жидкостей?
Какие факторы делают структуру жидкостей промежуточной между твердыми телами и жидкостями?
3а счет каких физических факторов сжимаемость реального газа при малом давлении больше, чем идеального, а при большом — меньше?
С какими факторами на молекулярном уровне связана скрытая теплота перехода?
Какие соображения позволяют выбрать давление, при котором должна быть проведена горизонтальная изотерма реального газа, соответствующая двухфазному состоянию?
Как наглядно объяснить зависимость знака дифференциального эффекта Джоуля-Томсона от давления газа?
Каким физическим условиям в газе соответствует точка инверсии дифференциального эффекта Джоуля-Томсона?
Поверхностное натяжение не зависит от геометрических размеров сосудов или объема жидкости. Почему же его существование наиболее четко проявляется лишь в узких трубках и маленьких каплях?
Чем свойства пара отличаются от свойств газа? При каких условиях к пару можно применить газовые законы?
Изменяется ли температура поверхностной пленки жидкости при ее растяжении?
Как зависит поверхностное натяжение жидкости от температуры?
При каких условиях жидкость смачивает твердое тело?
Как связано избыточное давление поверхностной пленки жидкости с кривизной ее поверхности?
Как рассчитать высоту капиллярного подъема жидкости?
