
- •Предисловие
- •Программа курса «Молекулярная физика. Термодинамика.»
- •2. Учебно-тематический план
- •3. Содержание курса
- •4. Примерная тематика семинарских занятий
- •5. Средства обеспечения дисциплины
- •Введение
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •Глава 1 Термодинамика
- •§1. Температура и термодинамическое равновесие
- •Давление
- •§2. Уравнение состояния идеального газа
- •§3. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Закон Авогадро
- •Закон Дальтона
- •§4. Первое начало термодинамики
- •§5. Макроскопическая работа
- •I начало термодинамики для системы в адиабатической оболочке
- •§6. Внутренняя энергия
- •§7. Количество теплоты. Математическая формулировка первого начала термодинамики
- •§8. Различные приложения I начала термодинамики. Теплоёмкость
- •§9. Внутренняя энергия идеального газа. Закон Джоуля
- •Уравнение Роберта Майера
- •§10. Адиабатический процесс. Уравнение Пуассона
- •Работа при адиабатическом изменении объёма газа
- •§11. Политропический процесс
- •Вопросы и задания для самостоятельной работы студентов Основы термодинамики. I начало термодинамики
- •§12. II начало термодинамики
- •Различные формулировки основного постулата, выражающего II начало термодинамики
- •§13. Равновесные состояния
- •§14. Обратимые и необратимые процессы
- •Необратимость и вероятность
- •§15. Цикл Карно
- •Коэффициент полезного действия в цикле Карно
- •§16. Холодильная машина
- •§17. Свободная энергия
- •§18. Энтропия
- •§19. Некоторые термодинамические соотношения
- •§20. Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •§21. Энтропия и вероятность
- •§22. Энтропия и беспорядок
- •§23. Третье начало термодинамики
- •Вопросы для контроля самостоятельной работы студентов
- •II начало термодинамики. Энтропия.
- •Глава 2. Неравновесная термодинамика §1. Основные принципы линейной термодинамики
- •§2. Нелинейная термодинамика
- •§3. Принцип синергетики
- •Свойства и примеры самоорганизации диссипативных структур
- •Глава 3. Статистическая физика и её применение к идеальному газу
- •§1. Давление газа с точки зрения молекулярно – кинетической теории
- •§2. Температура как мера средней энергии хаотичного движения молекул
- •Скорость газовых молекул
- •§3. Броуновское движение
- •§4. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •§5. Классическая теория теплоёмкости и её недостатки
- •§6. Барометрическая формула
- •Закон Больцмана
- •§7. Распределение молекул по скоростям
- •§8. Функция распределения
- •§9. Формула Максвелла
- •§10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •§11. Среднее число молекул, сталкивающихся со стенкой сосуда
- •Вопросы для контроля знаний студентов Молекулярно-кинетическая теория
- •Глава 4. Явления переноса §1. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •§4. Явление переноса в газах. Уравнение переноса
- •§5. Диффузия
- •§6. Нестационарная диффузия
- •§7. Теплопроводность газов
- •§8. Вязкость газов (внутреннее трение)
- •§9. Соотношения между коэффициентами переноса
- •§10. Физические явления в разреженных газах
- •Вопросы для самостоятельного контроля знаний студентов Явления переноса
- •Глава 5 §1. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •Уравнение Ван-Дер-Ваальса
- •§2. Учет сил отталкивания между молекулами
- •§3. Учет сил притяжения между молекулами
- •§4. Изотермы Ван-дер-Ваальса
- •§5. Критическая температура и критическое состояние
- •§6. Недостатки уравнения Ван-дер-Ваальса
- •§7. Внутренняя энергия газа Ван-дер-Ваальса
- •§8. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •§9. Сжижение газов
- •Эффект Джоуля-Томсона
- •Вопросы для самоконтроля изученного материала Реальные газы
- •Глава 6. Жидкое состояние §1.Строение жидкостей
- •§2. Поверхностное натяжение
- •§3. Условия равновесия на границе двух сред. Краевой угол
- •§4. Граница жидкости и твердого тела
- •§5. Силы, возникающие на кривой поверхности жидкости
- •§6. Капиллярные явления
- •§7. Упругость насыщенного пара над кривой поверхностью жидкости
- •Вопросы для самоконтроля знаний студентов
- •Глава 7. Жидкие растворы §1. Свойства растворов
- •§2. Упругость насыщенного пара над идеальным раствором
- •§3. Закон Генри
- •§4. Осмотическое давление
- •Глава 8. Кристаллическое состояние §1. Отличительные черты кристаллического состояния
- •§2. Классификация кристаллов
- •§3. Физические типы кристаллических решеток
- •§4. Тепловое движение в кристаллах
- •Глава 9. Фазовые переходы §1. Фаза и фазовые равновесия
- •§2. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
- •Вопросы для самоконтроля знаний студентов
- •Содержание
§4. Кинетическая теория теплоты Внутренняя энергия идеального газа
С точки зрения
молекулярно – кинетической теории
внутренняя энергия вещества определяется
суммой кинетических энергий всех молекул
вещества и потенциальной энергией их
взаимодействия. В случае идеального
газа потенциальная энергия взаимодействия
молекул равна нулю, соответственно
внутренняя энергия будет определяться
кинетической энергией всех молекул
газа. При учёте только поступательного
движения молекул средняя кинетическая
энергия
![]() молекулы
определяется основным уравнением
молекулярно – кинетической теории
(3.11)
молекулы
определяется основным уравнением
молекулярно – кинетической теории
(3.11)
![]()
 .
.
Но кроме
поступательного движения молекул газа,
совершает и другие виды движений
(вращательные, колебательные). Для
расчета средней кинетической энергии
молекул, с учётом различных видов
движений воспользуемся классической
теорией о равномерном распределении
энергии по степеням свободы. Эту теорему
можно сформулировать так: Если
система молекул находиться в тепловом
равновесии при температуре T,
средняя кинетическая энергия молекулы
равномерно распределена между всеми
степенями свободы, причём для каждой
степени свободы молекулы она равна
![]() .
.
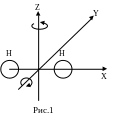
Число степеней свободы – это число независимых координат, определяющих положение тела в пространстве. Если вещество состоит из атомов, атомы можно представить как материальную точку, положение которой можно определить, задав три координаты X,Y,Z центра атома. Если обозначим через n число атомов в молекуле, и через i число степеней свободы, то при n=1 i=3. Если рассмотреть простейший случай двухатомной молекулы её можно представить в виде системы состоящей из двух атомов, расположенных на некотором расстоянии друг от друга (рис.1).
Рис.1
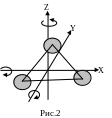 Если
же молекула состоит из 3-х и более атомов,
то она имеет 3 степени свободы, связанных
с поступательным движением центра масс
и 3 степени свободы с вращательным
движение вокруг осей X,Y,Z
(рис.2), т.е. при n³3
i=6.
Если
же молекула состоит из 3-х и более атомов,
то она имеет 3 степени свободы, связанных
с поступательным движением центра масс
и 3 степени свободы с вращательным
движение вокруг осей X,Y,Z
(рис.2), т.е. при n³3
i=6.
Но атомы в молекулах не всегда жёстко связано друг с другом и могут совершать колебания друг относительно друга. Тогда требуется ещё одна координата для определения конфигурации молекулы – это расстояние между атомами. В общем случае двухатомные молекулы обладают 6 степенями свободы: тремя поступательными, двумя вращательными и одной колебательной. Если молекула состоит из n атомов не жёстко связанных, то она имеет 3n степеней свободы (каждый атом имеет 3 степени свободы). Из этого числа 3 степени свободы поступательные, 3 степени свободы вращательные (за исключением случая когда атомы расположены по одной прямой), 3n-6 колебательные.
В случае, когда
амплитуда колебаний меньше, чем расстояние
между атомами, то такие колебания
называют гармоническими, атомы в этом
случае являются гармоническими
осцилляторами. Но осциллятор обладает
не только кинетической, но и потенциальной
энергией. Для гармонического осциллятора,
как известно из механики, среднее
значение кинетической и потенциальной
энергии равны между собой. Поэтому на
одну колебательную степень свободы
будет приходиться энергия равная
![]() .
Обычно при расчете кинетической энергии
молекул предполагают, что на все степени
свободы приходиться одна и та же энергия
.
Обычно при расчете кинетической энергии
молекул предполагают, что на все степени
свободы приходиться одна и та же энергия
![]() ,
но число колебательных степеней свободы
удваиваются. Если число степеней свободы
молекулы i,
то её средняя кинетическая энергия
равна
,
но число колебательных степеней свободы
удваиваются. Если число степеней свободы
молекулы i,
то её средняя кинетическая энергия
равна
![]() .
.
Пусть данный идеальный газ содержит N молекул, которые имеют i степени свободы. Внутренняя энергия такого газа будет равна
![]() .
.
Если же имеем один моль идеального газа, то N=NA, соответственно
![]() .
(3.26)
.
(3.26)
Из формулы (3.26) следует, что внутренняя энергия идеального газа зависит только от температуры. Это является теоретическим подтверждением закона Джоуля, который был установлен опытным путем.
