- •Часть 2 под редакцией
- •Иркутск
- •В. А. Кубышкин;
- •Клинические лекции по хирургии
- •Часть 2
- •664003, Г. Иркутск, бульвар Гагарина, 36; тел. (3952) 24–14–36.
- •Оглавление
- •Заболевания щитовидной железы в. А. Белобородов
- •Оценка тяжести тиреотоксикоза
- •Классификация тиреотоксикоза по степени тяжести
- •Классификация по степени увеличения щж
- •Классификация зоба (воз, 1994)
- •Токсический зоб
- •Узловой эутиреоидный зоб
- •Тиреоидиты
- •Клинические проявления тиреотоксикоза и гипотиреоза
- •Литература
- •Заболевания молочной железы а. В. Щербатых
- •Дисгормональные заболевания молочной железы
- •Этиология и патогенез
- •Мастодиния
- •Фиброзная мастопатия
- •Дифференциальный диагноз заболеваний молочной железы
- •Протокол ультразвукового исследования молочных желез
- •Комплексное лечение больных мастопатией
- •Хронический мастит
- •Трещины сосков
- •Как провести самообследование молочной железы?
- •Литература
- •Нагноительные заболевания легких е. Г. Григорьев Острый абсцесс и гангрена легкого
- •Классификация
- •Этиология и патогенез
- •Клиника и диагностика
- •Инструментальная диагностика
- •Дифференциальная диагностика
- •Осложнения
- •Лечение
- •Хирургическое лечение
- •Хронический абсцесс легкого
- •Клиника
- •Инструментальная диагностика
- •Лечение
- •Бронхоэктатическая болезнь
- •Этиология
- •Классификация бронхоэктазий
- •Осложнения
- •Диагностика
- •Инструментальная диагностика
- •Дифференциальный диагноз
- •Лечение
- •Хроническая эмпиема плевры
- •Литература
- •Врожденные и приобретенные пороки сердца ю. В. Желтовский
- •Недостаточность митрального клапана
- •Пороки трехстворчатого клапана
- •Многоклапанные пороки
- •Литература
- •Рубцовые стриктуры пищевода м. Б. Скворцов
- •История вопроса
- •I. По локализации:
- •II. По протяженности:
- •Клиника
- •Диагностика
- •Лечение рсп
- •Хирургическое лечение рубцовых сужений пищевода (рис. 5-10)
- •Иллюстрации р ис. 1. Рентгенограмма пищевода. Длинная стриктура грудного отд. Пищевода.
- •Литература
- •Хронический панкреатит с. П. Чикотеев
- •Диагностика
- •Клиника
- •Ультразвуковая диагностика хронических панкреатитов
- •Ультразвуковые признаки хп
- •Данные компьютерной томографии при хп
- •Эрхпг в диагностике хронического панкреатита
- •Эндоскопическое исследование
- •Непрямые
- •Тесты на выявление стеатореи
- •Литература
- •Хирургическое лечение хронического панкреатита с. П. Чикотеев
- •III. Паллиативные операции:
- •IV. Эндоскопические вмешательства на поджелудочной железе и ее протоках.
- •V. Закрытые хирургические вмешательства, выполняемые под контролем узи и кт.
- •Литература
- •Неспецифический язвенный колит а. А. Реут
- •Эпидемиология
- •Этиология и патогенез
- •Клиника
- •Классификация
- •Диагностика и дифференциальная диагностика
- •Клиническое течение
- •Лечение
- •Прогноз
- •Литература
- •Боль и Острый живот с позиций врача общей практики к. А. Апарцин
- •Неопухолевые заболевания прямой кишки с. М. Кузнецов
- •Особенности обследования проктологических больных
- •Острый и хронический геморрой
- •Н. П. Лужнов
- •Клиника
- •Литература
- •Заболевания вен ю. А. Бельков, а. Г. Макеев Острые тромбозы системы нижней полой вены
- •Варикозная болезнь нижних конечностей Введение
- •Основы анатомии венозной системы нижних конечностей
- •Гемодинамические механизмы хвн при варикозной болезни
- •Классификация хронической венозной недостаточности при варикозной болезни
- •Диагностика Клиническая диагностика
- •Инструментальная диагностика варикозной болезни
- •Лечение
- •Эластическая компрессионная терапия
- •Топические средства
- •Фармакотерапия
- •Склеротерапия
- •Показания к применению различных концентраций склерозирующих веществ
- •Хирургическое лечение варикозной болезни
- •Литература
- •Окклюзионно-стенотические заболевания терминального отдела брюшной аорты и магистральных артерий нижних конечностей (ю. А. Бельков, а. Г. Макеев, с. А. Кыштымов)
- •Анатомия брюшного отдела аорты и магистральных артерий нижних конечностей
- •Отдаленные результаты
- •Международная статистическая классификация болезней и проблем, связанных со здоровьем (десятый пересмотр)
- •Болезни системы кровообращения
- •Литература
- •Сведения об авторах
- •Чикотеев Сергей Павлович – Заслуженный деятель науки рф, профессор кафедры госпитальной хирургии Иркутского государственного медицинского университета.
Литература
Амбулаторная хирургия, Справочник практического врача / под ред. В. В. Гриценко, Ю. Д. Игнатова. – СПб. : Нева; М. : Олма-пресс Звездный мир, 2002. – 448 с.
Варикозная болезнь. Компрессионная склеротерапия : Сборник трудов. – М. : Издательство НЦССХ им. А. Н. Бакулева. – 1999. – 100 с.
Техника хирургических операций на сосудах / В. А. Долин, Л. В. Лебедев, И. Г. Перегудов и др. – СПб. : Гиппократ, 2004. – 176 с.
Лекции по сердечно-сосудистой хирургии. – 2-е изд., перераб. и доп. : в 2 т. / под ред. Л. А. Бокерия. – М. : Изд-во НЦССХ им. А. Н. Бакулева РАМН, 2001. – 400 с.
Флебология: руководство для врачей / В. С. Савельев, В. А. Гологорский, А. И. Кириенко и др.: под ред. В. С. Савельева. – М. : Медицина, 2001. – 664 с.
Хирургические болезни: учебник / М. И. Кузин, О. С. Шкроб, Н. М. Кузин и др.; под ред. М. И. Кузина. – 2-е изд., перераб. и допол. – М. : Медицина, 1995. – 640 с.
Частная хирургия : учебник для медицинских ВУЗов : 2 т. / под ред. Ю. Л. Шевченко. – СПб. : Специальная литература, 1998. – 517 с.
Яблоков Г. Г. Хроническая венозная недостаточность / Г. Г. Яблоков, А. И Кириенко, А. Ю. Богачев. – М. : Берег, 1999. – 128 с.
ЛЕКЦИЯ 13
Окклюзионно-стенотические заболевания терминального отдела брюшной аорты и магистральных артерий нижних конечностей (ю. А. Бельков, а. Г. Макеев, с. А. Кыштымов)
M. De Bakey делит окклюзионно-стенотические поражения аорты на 4 категории:
Категория 1 – коронарные артерии.
Категория 2 – основные ветви дуги аорты.
Категория3 – висцеральные ветви брюшной аорты (чревный ствол, верхняя брыжеечная и почечные артерии).
Категория 4 – терминальная аорта и ее основные ветви.
В этой лекции будут рассмотрены аспекты тактики лечения больных четвертой категории.
Анатомия брюшного отдела аорты и магистральных артерий нижних конечностей
Брюшная аорта (aorta abdominalis) расположена на предпозвоночной фасции спереди и слева от позвоночного столба. Ее длина у взрослого человека составляет приблизительно 13-14 см. С хирургической точки зрения абдоминальную аорту принято делить на три отдела:
Верхний – супраренальный.
Средний – ренальный.
Нижний – инфраренальный.
Все ветви аорты делят на париетальные и висцеральные. К париетальным ветвям относятся правая и левая нижние диафрагмальные артерии, поясничные артерии, срединная крестцовая артерия. К висцеральным – чревный ствол, верхняя брыжеечная артерия, правая и левая почечные артерии, нижняя брыжеечная артерия.
На уровне IV-V поясничных позвонков брюшная аорта делится на общие подвздошные артерии, которые в свою очередь – на наружные и внутренние. Внутренние подвздошные артерии кровоснабжают органы малого таза. Наружные – выйдя из под пупартовой связки на бедро, переходят в общие бедренные артерии. В верхней трети от общей бедренной артерии отходит глубокая бедренная артерия, после чего она называется поверхностной бедренной. Далее она располагается в Гунтеровом канале и, выйдя в подколенную ямку, именуется подколенной артерией. Последняя, в верхней трети голени, делится (трифуркация подколенной артерии) на переднюю и заднюю большеберцовые, межостную артерии.
История вопроса
Окклюзия брюшной аорты как секционная находка впервые была описана Larcheus в 1643 г. и Fontani в 1700 г. Graham (1814) впервые указал на окклюзию бифуркации аорты как причину хронической ишемии нижних конечностей. Goodison в 1818 году обратил внимание на хорошее развитие при этой патологии артериальных коллатералей. В 1923 году R. Leriche описал клинические проявления и уровень обструкции при поражении аорто-подвздошного сегмента, которое назвал aortitis terminalis. Им было выделено 5 клинических признаков:
диффузная мышечная атрофия нижних конечностей;
выраженная утомляемость ног;
отсутствие трофических расстройств;
нестабильная и неполная эрекция;
бледность голеней и стоп, не исчезающая даже в вертикальном положении больного.
О
Рис.
1. Rene
Leriche
(1879-1955 г.)
Около 90 % всех ампутаций выполняется по поводу выраженной ишемии нижних конечностей, у 25 % пациентов с критической ишемией требуется ампутация голени или бедра.
Этиология
По данным различных авторов до 90 % случаев этиологическим фактором в развитии хронической ишемии нижних конечностей является атеросклероз. На втором месте по частоте встречаемости (4-5 %) стоят различные неспецифические воспалительные заболевания аорты и магистральных артерий нижних конечностей (неспецифический аортоартериит, тромбангиит, эндартериит). 2-3 % приходится на постэмболические и посттравматические окклюзии. Чрезвычайно редко хроническая ишемия нижних конечностей развивается вследствие аплазии сосудов, деформирующего ретроперитонеального фиброза, фиброзно-мышечной дисплазии.
По материалам нашей клиники причиной хронической ишемии нижних конечностей в 97 % является атеросклероз, в 2 % – неспецифические воспалительные заболевания артерий, в 1 % – посттравматические артериальные окклюзии. Средний возраст пациентов составляет 52,2±7,5 лет, преобладают лица мужского пола.
Патологическая анатомия
Чаще всего окклюзия возникает в области бифуркации брюшной аорты и общей подвздошной артерии. Проксимальное развитие тромбоза приостанавливается на уровне бифуркации до тех пор, пока не произойдет резкое стенозирование и снижение кровотока по контрлатеральной подвздошной артерии. Лишь при тромбозе противоположной подвздошной артерии создаются условия для окклюзии бифуркации брюшной аорты и восходящего тромбоза аорты по мере редукции кровотока в поясничных артериях. Считается, что «излюбленная» локализация атеросклероза в области бифуркации брюшной аорты и подвздошных артерий обусловлена значительным уменьшением кровотока дистальнее почечных артерий, а также хронической травмой артериальных стенок из-за «систолических ударов» о близко расположенные жесткие ткани (promontorium) и в местах разветвления сосудов при артериальной гипертензии с повреждением vasa vasorum, ишемией стенок аорты и артерий и дегенеративными изменениями в них.
Для тромбангиита в отличие от атеросклероза характерен восходящий тип окклюзионного поражения от дистальных отделов к более проксимальным. Морфологическая картина характеризуется тромбами в просвете сосудов и полинуклеарной инфильтрацией стенок артерий и вен, а также околососудистой клетчатки. Вокруг тромба обычно выявляются разрастания эндотелия и милиарные гранулемы. Макроскопически тромбы имеют вид плотного тяжа, далеко распространяющегося в коллатеральные ветви.
По виду поражения артерий различают окклюзии, то есть полную их непроходимость и стенозы. А. В Покровский выделяет три типа окклюзии брюшной аорты, в зависимости от ее локалиации:
низкая окклюзия – окклюзия бифуркации брюшной аорты ниже уровня отхождения нижней брыжеечной артерии;
средняя окклюзия – окклюзия аорты проксимальнее уровня отхождения нижней брыжеечной артерии;
высокая окклюзия – окклюзия аорты тот час ниже уровня почечных артерий или в пределах 2 см. дистальнее.
Патологическая физиология
Изменение характера кровообращения у больных с хронической ишемией нижних конечностей, как правило, наступает при стенозе 60–70 %. При менее выраженном стенозе гемодинамически значимых нарушений не возникает и заболевание может протекать асимптомно.
При окклюзии магистральной артерии главную роль в компенсации кровотока играют мышечные коллатерали, которые должны не только увеличивать фильтрационную поверхность, но и обеспечивать переток крови к более дистально расположенным тканям. Считается, что одним из наиболее важных факторов прогрессирования ишемии является снижение объёмной скорости кровотока. Обмен между капиллярами и клетками происходит только при «надкритическом» давлении в магистральных артериях (более 60 мм рт. ст.).
При снижении перфузионного давления, способного преодолеть периферическое сопротивление, исчезает градиент давления между артериальным и венозным руслами и нарушается процесс микроциркуляции. При снижении перфузионного давления ниже 20–30 мм рт. ст. обменные процессы между кровью и тканями прекращаются, развивается атония капилляров, в мышечных тканях накапливаются продукты метаболизма и развивается ацидоз, что оказывает раздражающее действие на нервные окончания и обусловливает болевой симптомокомплекс, а затем и трофические нарушения. Просвет большинства капилляров становится неровным, с участками облитерации, развивается гипертрофия эндотелия капилляров, утолщение базальной мембраны, что нарушает проницаемость сосудистой стенки. Однако, нарушения микроциркуляции вызваны не только поражением капиллярного русла, но и выраженными нарушениями гидродинамики крови. Снижается деформирующая способность эритроцитов. Их жесткость наряду с замедлением скорости тока крови приводит к динамической агрегации, увеличению периферического сопротивления, уменьшению снабжения тканей кислородом. Компенсация местной ишемии за счет усиления анаэробного гликолиза, увеличения образования лактата и пирувата в сочетании с местными тканевым ацидозом и гиперосмолярностью еще больше усиливает жесткость мембраны эритроцитов. Таким образом, нарушение регионарного кровообращения конечностей представляет собой суммарную величину, определяемую степенью нарушения магистрального, коллатерального кровотока и состоянием микроциркуляции.
Классификация
Окклюзионно-стенотические заболевания терминального отдела аорты и магистральных артерий нижних конечностей подразделяются по многим признакам.
По виду поражения они делятся на:
окклюзии (полная непроходимость сосуда);
стенозы (частичная непроходимость сосуда).
По характеру патологического процесса на:
сегментарные поражения;
диффузные поражения;
дистальные поражения;
многоэтажные поражения.
В зависимости уровня поражения артериального русла нижних конечностей различают поражения:
проксимального отдела (аорто-подвздошного сегмента),
среднего отдела (поверхностной бедренной артерии);
дистального сегмента с вовлечением ветвей подколенной артерии.
Окклюзионно-стенотические заболевания терминального отдела аорты и магистральных артерий нижних конечностей сопровождаются хроническим нарушением артериального кровоснабжением нижних конечностей. Для его оценки применяется классификация Р. Фонтена, А. В. Покровского. По Р. Фантену (1969) выделяют четыре стадии хронической ишемии нижних конечностей:
I стадия (начальных проявлений) – характеризуется зябкостью, чувством похолодания, парестезиями, бледностью кожных покровов, повышением потливости, утомляемостью ног.
II стадия (недостаточность кровообращения при функциональной нагрузке) – появление симптомов перемежающейся хромоты (claudicacio intermitens).
III стадия (недостаточность кровообращения в покое) – основным симптомом является постоянная боль в конечностях, в том числе и в ночное время.
IV стадия – язвенно-некротические изменения в тканях дистальных отделов конечностей.
В нашей стране принято пользоваться классификацией А. В. Покровского (1979). Эта классификация также предусматривает наличие четырех стадий заболевания, однако создана на основании более тщательного анализа клинических проявлений:
I стадия – появление болей в конечности при ходьбе на расстояние более 1 км.
IIA стадия – перемежающаяся хромота, возникающая при ходьбе на расстояние более 200 м;
II Б стадия – перемежающаяся хромота, возникающая при ходьбе на расстояние менее чем 200 м.
III стадия – боли в покое и «ночные» боли.
IV стадия – трофические изменения и гангрена нижних конечностей.
В дальнейшем, говоря о выраженности ишемии нижних конечностей, мы будем пользоваться именно этой классификацией.
Кроме того, существует термин критическая хроническая ишемия нижних конечностей, предложенный P. R. F. Beel в 1982 году для выделения группы больных с болями покоя и трофическими изменениями тканей конечностей, указывающий на стадию заболевания в переходной фазе от жизнеспособности к гибели. Группа ангиологов ряда европейских стран на заседании Европейской рабочей группы по критической ишемии нижних конечностей (Berlin, 1989 г.) строго огранила данное состояние III и IV степенями по классификации Фонтейна и определила критическую ишемию как:
постоянные боли покоя, требующие не менее чем двухнедельной регулярной аналгезии;
язва или гангрена стопы при систолическом давлении у лодыжки менее 50 мм. рт. ст.
В. С. Савельев, В. М. Кошкин (2002) предлагают для лучшего понимания патогенетических расстройств при критической хронической ишемии нижних конечностей ориентироваться на наличие ишемического, лимфатического отека голени и стопы. Они предлагают делить третью и четвертую стадии на две подстадии. При III А степени имеется «боль покоя» при отсутствии ишемического отека, больной может держать ногу в горизонтальном положении больше двух часов. При III Б степени – на фоне боли покоя имеется ишемический отек, возможность держать ногу в горизонтальном положении менее двух часов. IV А степень хронической ишемии характеризуется наличием гангрены пальцев или части стопы с перспективой сохранения опорной функции конечности. При IV Б степени – показана ампутация конечности. Таким образом, к критической – относится III Б,VI А, IV Б степени ишемии.
Клиника
Складывается из симптомов недостаточности артериального кровоснабжения нижних конечностей, органов таза и ягодичных мышц; перемежающейся хромоты, импотенции, трофических расстройств тканей дистальных отделов конечностей. Выраженность указанных симптомов будет зависеть от степени окклюзионно-стенотических поражений аорты и магистральных артерий нижних конечностей, степени развитости коллатерального кровоснабжения. У подавляющего числа пациентов эти признаки появляются постепенно и носят волнообразный характер.
Первым симптомом заболевания, как правило, являются боли в икроножных мышцах при форсированной физической нагрузке (быстрая ходьба, бег, подъем по лестнице). Больной вынужден останавливаться, чтобы компенсировать в покое ишемию мышц. Этот симптом получил название симптома перемежающийся хромоты и имеет исключительную важность для оценки степени недостаточности артериального кровообращения конечностей. Симптом впервые описан французским студентом-ветеринаром G. Boley (1831) у лошади с повреждением бедренной артерии, вынужденной при беге переходить на медленную ходьбу и начинающей при этом хромать. Объяснение этого симптома следующее. Во время ходьбы мышцы, сокращаясь, «откачивают» кровь по венозной системе от конечности. Приток же по суженной артерии является недостаточным. Таким образом, возникает обескровливание – ишемия конечности. Поскольку с артериальной кровью поступает нужный для оксигенации тканей кислород, то его недостаток приводит к включению анаэробного пути метаболизма с накоплением недоокисленных продуктов, что и вызывает возникновение ишемических болей. В момент, когда больной останавливается, потребность мышц в кислороде уменьшается – боли успокаиваются, и он может продолжить ходьбу дальше.
При окклюзии аорты ишемическая боль локализуется в ягодичных мышцах и латеральной поверхности бедер – это так называемая высокая перемежающаяся хромота. В ряде случаев наблюдается артериальная недостаточность мышц тазового дна, что проявляется нарушением функции сфинктеров (перемежающаяся хромота сфинктеров) прямой кишки в виде недержания кала, газов, а так же функции мочевого пузыря в виде недержания мочи. Одновременно при высокой окклюзии отмечаются явления хронического колита, вазоренальной гипертензии, хронической абдоминальной ишемии.
Импотенция встречается у 50-60 % больных. Ее проявления обусловлены тремя факторами: недостаточностью притока крови, что исключает полноценное кровенаполнение кавернозных тел во время эрекции, хронической артериальной спинальной ишемией, отражающейся на функции спинальных половых центров, снижением гормональной активности, в связи с ишемией яичек, предстательной железы.
Трофические нарушения кожи проявляются выпадением волос, сухостью, шелушением кожи, гиперкеравтозом подошвенной поверхности стоп. Ногтевые пластинки становятся толстыми и приобретают бурую окраску. Атрофируются подкожная клетчатка и мелкие мышцы стоп. Кожа истончается, становится легкоранимой. Длительно не заживают трещины и раны. При декомпенсации кровообращения появляется отек стоп, голени. В дистальных отделах конечностей, чаще пальцев, возникают язвы. Дно их покрыто налетом грязно-серого цвета. В окружности язв определяется воспалительная инфильтрация.
Диагностика
Правильный диагноз окклюзионно-стенотических поражений терминального отдела брюшной аорты и магистральных артерий нижних конечностей более чем в 90 % случаев может быть поставлен на основании результатов объективного осмотра и физикального исследования пациентов.
При осмотре можно обнаружить различной степени выраженности трофические нарушения тканей нижних конечностей, снижение сфинктера прямой кишки.
Пальпаторно определяют пульсацию артерий:
бедренной – в скарповом треугольнике, непосредственно ниже середины паховой связки;
подколенной – в медиальной половине подколенной ямки в положении лежа при слегка согнутой в коленном суставе и расслабленной ноге;
задней большеберцовой – позади внутренней лодыжки голеностопного сустава;
артерии тыла стопы – между I и II плюсневыми костями.
Следует помнить, что из-за аномального расположения артерий тыла стопы пульс в типичном для a. dorsalis pedis месте не определяется в 6-24 % случаев. Местоположение задней большеберцовой артерии анатомически более постоянно.
Исследование пульса необходимо производить одновременно на симметричных точках обеих конечностей. Это позволяет сравнить и наиболее четко представить силу пульсовой волны, ослабление или полное отсутствие пульсации.
При аускультации над магистральными артериями можно выслушать проводной тон удара пульсовой волны. При поражении артерии (чаще всего сужении) возникает систолический шум. Систолический шум с терминального отдела аорты определяется по средней линии живота под мечевидным отростком. В этой же точке выслушивается шум чревного ствола при сдавлении и стенозе. По средней линии выше и ниже уровня пупка локализуются шумы с бифуркации аорты. Отсюда по направлению к точке между внутренней и средней третью пупартовой связки идет проекция подвздошных артерии, по которой выслушиваются их шумы. В той же точке паховой связки, где определяется пульсация бедренной артерии, аускультируются и ее шумы.
О нарушении артериального кровообращения в конечности свидетельствуют и функциональные пробы:
Симптом прижатия пальца («белого пятна»). При сдавлении подошвенной поверхности дистальной фаланги I пальца стопы в течение 5-10 секунд у здоровых людей образовавшиеся побледнение кожи сменяется нормальной окраской через 2-4 секунды. При нарушении кровообращения конечности побледнение держится дольше, и нормализации окраски кожи происходит с задержкой.
Симптом Оппеля-Бюргера (1911 г.). У больного в положении лежа поднимают нижние конечности вверх. Через 1-2 минуты стопа пораженной ноги становится бледной. После опускания ног в горизонтальное положение бледность медленно исчезает и сменяется гиперемией. Лучше эту пробу проводить в положении больного лежа на животе, при согнутых в коленных суставах под прямым углом ногах, так как это положение легче переносится.
Проба Самуэльса сходна с пробой Опеля: в указанном положении больной совершает сгибательные и разгибательные движения в голеностопных суставах. При нарушениях кровообращения в конечности наступает бледность стопы и боль в икроножной мышце.
Проба Гольдфлама производится так же, но отмечается, что усталость в пораженной конечности наступает раньше.
Проба Н. Н. Бурденко. Больной становится босыми ногами на пол, затем садится и поднимает ноги. На подошвенной поверхности больной ноги длительное время остаются бледные пятна.
Инструментальные методы исследования позволяют уточнить характер нарушения кровотока. Различают исследования макро- и микрогемодинамики. Среди методов исследования макрогемодинамики выделяют неинвазивные и инвазивные вмешательства. К неинвазивным относятся:
Ультразвуковая доплерография с измерением лодыжечно-плечевого индкса.
Определение сегментарного давления на разных уровнях.
Измерение пальцевого артериального давления.
Дуплексное сканирование аорты, подвздошных артерий и артерий нижних конечностей, в том числе артерий голени и стопы.
Магнитно-резонансная ангиография аорты, подвздошных артерий и артерий нижних конечностей, в том числе артерий голени и стопы.
К инвазивным исследованиям макрогемодинамики относится рентгенконтрастная ангиография аорты, подвздошных артерий и артерий нижних конечностей, в том числе артерий голени и стопы.
Исследование микрогемодинамики включает:
Транскутанную оксиметрию.
Лазерную флоуметрию.
Видеокапиляроскопию.
Сцинтиграфию пораженной конечности с Таллием 201.
Наиболее простыми и показательными являются ультразвуковые методы исследования. Ультразвуковая доплерография позволяет установить характер кровотока (магистральный, магистрально-измененный, коллатеральный) и определить лодыжечно-плечевой индекс (ЛПИ) – отношение систолического давления на лодыжке к давлению на плече. На основании ЛПИ судят о степени нарушения кровообращения в конечности. В норме его величина составляет около 1,1. При ишемии II Б степени ЛПИ падает ниже 0,7, при III степени – ниже 0,5, при IV степени – ниже 0,3.
Д
 уплексное
сканирование, как доказала сотрудница
нашей клиники Л. В. Алексеева (2000),
позволяет у ряда больных отказаться от
проведения ангиографического исследования.
Так, этот
метод с высокой точностью дает возможность
оценить степень и характер
окклюзионно-стенотического процесса.
уплексное
сканирование, как доказала сотрудница
нашей клиники Л. В. Алексеева (2000),
позволяет у ряда больных отказаться от
проведения ангиографического исследования.
Так, этот
метод с высокой точностью дает возможность
оценить степень и характер
окклюзионно-стенотического процесса.
У
Рис.
2. Дуплекс-сонографическая картина
окклюзии дистального отдела брюшной
аорты
П
Рис.
3. Ангиографическое изображение стеноза
дистального отдела брюшной аорты,
окклюзии подвздошных артерий справа
и критического стеноза общей подвздошной
артерии слева.
(Наблюдение госпитальной хирургической
клиники)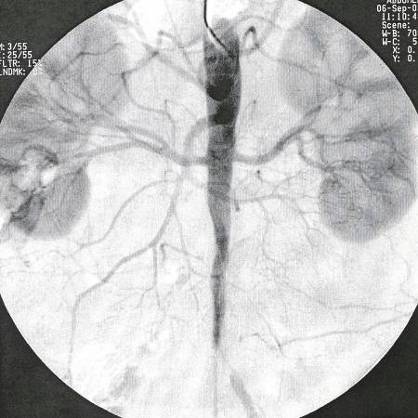
Исследование магистральных артерий таким методом позволяет определить уровень окклюзионно-стенотического поражения, наличие или отсутвие заполнения дистальных сегментов (подколенная и берцовые артерии), наличие кальцинированных блящек в проксимальном и дистальном артериальном русле.
Таким образом, инструментальные методы исследования позволяют уточнить характер нарушения кровотока.
Лечение
Лечение пациентов с оккклюзионно-стенотических поражениями терминального отдела брюшной аорты и магистральных артерий нижних конечностей должно быть комплексным и индивидуальным.
Консервативная терапия у таких больных базируется на:
Устранении действия неблагоприятных факторов внешней и внутренней среды (отказ от курения и употребления спиртных напитков, недопущение переохлаждений).
Купировании болевого синдрома – назначение ненаркотических и наркотических анальгетиков.
Активации обменных процессов в тканях (витамины В1, В6, В12, В15. никотиновая кислота, аскорбиновая кислота, компламин, солкосерил).
Улучшении реологических свойств крови, нормализации адгезивно-агрегационной функции тромбоцитов, состояния свертывающей системы крови (малые дозы аспирина, гепарин, трентал, реополигюкин, курантил, простагландины).
Десенсибилизирующей терапии (димедрол, супрастин, тавегил и др.).
Седативной терапии (седуксен, элениум и др.).
Назначении антиатеросклеротических препаратов (липримар).
Применении методов экстракорпоральной детокикации (УФО крови, плазмаферез).
Физиотерапевтические и бальнеологические процедуры (магнитотерапия, ДДТ, радоновые, сероводородные ванны).
Санаторно-курортном лечении.
Наиболее эффективным методом лечения больных с окклюзионно-стенотическими поражениями терминального отдела аорты и магистральных артерий нижних конечностей является хирургическая коррекция кровообращения, так как через 2–3 года после появления клинических проявлений большинство больных становятся нетрудоспособными. Показанием к оперативному вмешательству является II Б – IV степени хронической ишемии нижних конечностей. Противопоказаниями к операции служат: инфаркт миокарда (давностью менее 3 месяцев), недостаточность кровообращения III степени, выраженная легочная недостаточность, цирроз печени, почечно-печеночная недостаточность. Возраст больных не может служить противопоказанием.
Оперативные вмешательства можно разделить на четыре большие группы:
Реконструктивные – открытые операции, выполняемые с целью замещения, удаления или шунтирования окклюзированного (стенозированного) сегмента артерии с восстановлением пульсирующего кровотока ниже пораженного сегмента.
Восстановительные – операции, при которых удаляют окклюзирующий субстрат (тромб, атеросклеротическая бляшка, эмбол) из артериального русла.
Непрямые реваскуляризирующие или паллиативные – операции, позволяющие улучшить кровоток без прямой сосудистой операции.
Абляционные – операции, позволяющие удалить инородный, инфицированный материал, прекратить кровоток по сосуду. К этим же операциям относятся органоуносящие операции.
К первой группе операций относятся резекция с протезированием и шунтирование артерий.
Резекция с протезированием выполняется при окклюзии и особенно кальцинозе терминального отдела брюшной аорты и подвздошных артерий; при отсутствии коллатеральной сети; при аневризматическом расширении бифуркации аорты. Сущность операции заключается в полном пересечении аорты (подвздошной артерии) и наложении анастомоза – протез-сосуд способом «конец в конец» или «конец в бок», проведении дистального анастомоза с общей бедренной артерией. При непроходимости поверхностной бедренной артерии соустье формируется с глубокой бедренной артерией. В случаях, когда аорта не пересекается и проксимальный анастомоз накладывается «конец в бок», такие операции называются шунтирующими. Положительным моментом таких операций является то, что остаются функционально активными коллатерали шунтируемой артерии; при тромбозе сосуда кровоток будет осуществляться по протезу, а при тромбозе шунта – по шунтируемой артерии. Отрицательным фактом – то, что в месте проксимального анастомоза изменяется характер кровотока из-за того, что шунт отходит от артерии под углом.
|
|
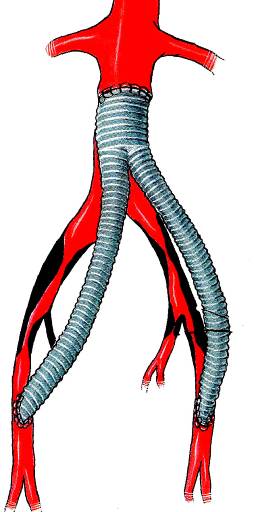
Рис. 4. Бифуркационное аорто-бедренное протезировние. |
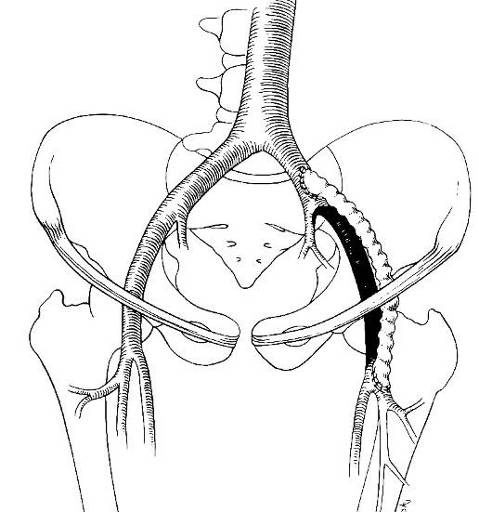
Рис. 5. Линейное подвздошно-бедренное шунтирование |
Шунтирование (протезирование) в аортоподвздошной зоне может быть выполнено линейным или бифуркационным протезом. Линейные операции показаны при одностороннем поражении общей и наружной подвздошной артерии с проходимыми сосудами с противоположной стороны. Бифуркационные реконструкции выполняются при двустороннем стенозе или окклюзии (и их сочетании) аорто-подвздошного сегмента, при сочетании окклюзий подвздошных артерий с одной стороны с клинически компенсированным стенозом противоположной стороны. Возможны различные сочетания реконструктивных операций.
Реконструктивные вмешательства проводят в условиях комбинированной многокомпонентной анестезии (тотальная внутривенная анестезия с миоплегией и искуственной вентиляцией легких в сочетании с эпидуральной анестезией).
При проведении бифуркационных реконструкций двумя хирургическими бригадами выполняют доступ на обеих бедрах с обнажением общей, поверхностной и глубокой бедренных артерий, затем путем осмотра и пальпации устанавливют степень их поражения. После этого производят тотальныю срединную лапаротомию. Далее выполняют ревизию органов брюшной полости (желудок, печень, желчный пузырь) для выявления сопутствующей патологии. Затем кишечник отводят вправо, а сигмовидную кишку оставляют слева, вскрывают задний листок брюшины. Выделют аорту. Пальпаторно определют границу кальциноза и тромбоза аорты. После внутривенного введения 5000 ЕД гепарина аорту пережимают выше окклюзиии, пересекают при протезировании, либо выполнют продольную аортотомию при шунтировании. Накладывют анастомоз конец в конец (протезирование) либо конец в бок (шунтирование) обвивным швом. После окончания анастомоза на короткое время ослаблют зажим на аорте и проверют герметичность анастомоза. При необходимости накладывают дополнительные швы. На следующем этапе корцанг с тупфером со стороны разреза на бедре подводят под пупартову связку и далее забрюшинно к бифуркации брюшной аорты. Проведенным в брюшную полость корцангом захватывют браншу протеза и выводят на бедро. Протез хорошо натягивали и проверяют его ход, чтобы не было изгибов и перекрутов. Если наружная подвздошная артерия окклюзирована, то бедренную артерию пересекают и накладывают анастомоз конец в конец. При непроходимости бедренной артерии последнюю резецируют и за счет общей бедренной артерии формируют площадку с устьем глубокой артерии бедра, затем накладывают анастомоз конец в конец. При сохраненной проходимости наружной подвздошной артерии анастомоз накладывют конец в бок, так как при этом сохранялся кровоток по всем коллатеральным ветвям. Перед окончанием операции проводят контроль центрального и дистального кровотока. Операцию заканчивают дренированием брюшной полости и паропротезного пространства. При выполненни линейных реконструкций выполняют доступ к бедренным артериям с одной стороны. После чего внебрюшинно выделялют аорту и общую подвздошную артерию. При проведении аорто-бедренных реконструкций проксимальный анастомоз накладывалют конец протеза в бок аорты, при подвздошно-бедренных реконструкций – конец протеза в конец подвздошной артерии. Дистальный анастомоз выполняют аналогично бифуркационным реконструкциям.
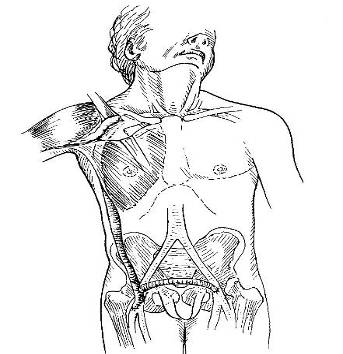
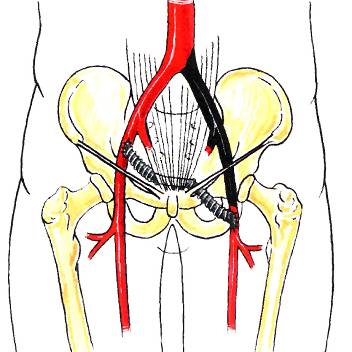
К группе реконструкций относятся внеанатомические шунтирования. Показаниями к ним служат тотальный кальциноз аорты и подвздошных артерий; проксимальный тромбоз аорты, когда ее выделение и затруднено и рискованно; гнойно-воспалительные процессы в брюшной полости, забрюшинном пространстве, в коже передней брюшной стенки. К таким операциям относятся подключично-общеглубокобедренное, подмышечно-общеглубокобедренное и различные варианты бедренно-бедренного шунтирования. При выполнении соустья между подключичной (подмышечной) и бедренными артериями протез проводится между большой и малой грудными мышцами подкожно на боковой поверхности грудной клетки и живота по средней подмышечной линии. При бедренно-бедренном шунтировании эксплантат может распологаться подкожно или в залобковом пространстве (пространство Ретциуса).
|
|
Рис. 6. Подключично-бедренное шунтирование. |
Рис. 7. Перекрестное подвздошно-бедренное шунтирование. |
К восстановительным операциям относятся эндартерэктомия, тромбэктомия. Эти операции могут быть прямыми или открытми и непрямыми или полузакрытыми. В первом случае атеросклеротическая бляшка, тромб удаляются из артерии через артериотомическое отверстие. Во втором – удаление вышеназванных структур осуществляется на протяжении с помощью катетера Фогарти либо петли для эндартерэктомии. Такие хирургические вмешательства производятся при ограниченном стенозе или окклюзии артерии и зачастую сочетаются с реконструктивными операциями.
Показанием для выполнения непрямых реваскуляризирующих (паллиативных) операций является наличие форм поражения артерий нижних конечностей, не подлежащих реконструктивно–восстановительным вмешательствам. К ним относятся диффузные поражения артериального русла, либо дистальные окклюзионно-стенотические поражения, не позволяющие адекватно восстановить магистральный кровоток.
Предложенная в 1924 г. J. Diez поясничная симпатэктомия направлена на ликвидацию влияния симпатической иннервации на сосуды нижних конечностей, в результате чего ликвидируется ангиоспазм дистального артериального русла, а так же стимулируется коллатеральное кровообращение. Суть хирургического вмешательства заключается в резекции симпатического ствола на уровне L2-L4 позвонков из забрюшинного доступа. Эта операция сопровождается повышением температуры кожи в связи с улучшением мышечного кровотока в конечностях, особенно на стопе.
|
Рис. 8. Поясничная симпатэктомия |
Ю. А. Бельков в своей кандидатской диссертации (1987) определил показания к поясничной симпатэктомии, как самостоятельной операции, так и в комплексном лечении больных окклюзионно-стенотическими заболеваниями терминального отдела брюшной аорты и магистральных артерий нижних конечностей. Ими явились:
наличие противопоказаний общего и локального характера к реконструктивным операции на сосудах;
клиническая эффективность спазмолической терапии;
функциональная достаточность мышечного кровотока;
ангиографически доказанное наличие коллатералей;
величина лодышчно-плечевого индекса больше 0,4.
К малотравматичным паллиативным вмешательствам на костях нижних конечностей относится реваскуляризирующая остеотрепанация. Механизм положительного влияния данной операции остается до конца неясным. В последние годы в литературе описываются возможные основные механизмы ее эффекта. Главными из них считают стимуляцию раскрытия коллатералей с увеличением кровотока по ним. Непосредственно сама перфорация запускает два патофизиологических звена: декомпрессия костномозговой полости и субпороговое раздражение нервных окончаний костной ткани. Субпороговое болевое раздражение вызывает рефлекторную вазодилатацию и активный приток крови к костям голени, что благотворно влияет на купирование ишемического синдрома. Эффект остеотрепанации более выражен и дольше сохраняется у больных с дистальными формами окклюзий. Сотрудник нашей клиники С. А. Кыштымов (2004) в своей работе доказал, что применение реваскуляризирующей остеотрепанации в лечении больных с критической хронической ишемией нижних конечностей, при отсутствии возможности восстановления магистрального кровотока в дистальное русло, позволяет повысить частоту сохранения конечности в ближайшие сроки послеоперационного периода, что определяет улучшение непосредственных и отдаленных результатов комплексного хирургического лечения.
Сосудистые реконструктивно-восстановительные операции не всегда приводят к реваскуляризации конечности. В 6-15 % случаев не удается купировать явления критической ишемии, и хирурги вынуждены выполнять ампутацию конечности. Это вынужденная мера, которая позволяет спасти жизнь больному. Различают:
Ампутацию конечности – травматическое или хирургическое отсечение периферической части конечности на протяжении какой-либо кости (или костей).
Экзартикуляцию (вычленение) – травматическое или хирургическое отсечение периферической части конечности на уровне какого-либосустава.
Резекцию стопы – хирургическое иссечение сегмента стопы с одним или несколькими пальцами в продольном направлении.
Показанием к первичной ампутации конечности при окклюзионно-стенотических заболеваниях терминального отдела аорты и магистральных артерий нижних конечностей являются сухая и влажная гангрена периферического сегмента (или сегментов) конечности.
К вторичным ампутациям относятся ампутации, выполняемые по вторичным показаниям. К ним относятся длительная безуспешная консервативная терапия при невозможности проведения сосудистых реконструктивных операций, неудачная хирургическая коррекция магистрального кровотока у больных с выраженным болевым синдромом.
Относительно новым методом лечения больных с окклюзионно-стенотическими заболеваниями терминального отдела аорты и магистральных артерий нижних конечностей является рентгеноэдоваскулярная хирургия. К ней относятся лазерная, ротерная, ультразвуковая реканализация, рентгенэндоваскулярная баллонная дилатация и стентирование. При выполнении баллонной дилатации в область стеноза вводится баллон, который раздувают под определенным давлении, тем самым, восстанавливая просвет артерии. Данную процедуру обычно сочетают со стентированием.
Сущность стентирования состоит во введении в просвет артерии вытянутой проволоки (стента) из медицинского сплава, обладающего эффектом «памяти формы». При отливе проволоки в заводских условиях ей придается форма спирали, которую она теряет при температуре 0–10 ○С. В случае введения проволоки в артерию, где температура равна 37 ○С, она восстанавливает спиралевидную форму, равномерно расширяя просвет артерии изнутри.
Лазерное и ротерное восстановление проходимости артерий основано на разрушении атероматозных бляшек лазерным излучением и действием ротера.
Ультразвуковая реканализация артерий базируется на использовании эффекта ультразвуковых механических колебаний. При этом методе к зоне окклюзии подводится волновод, представляющий собой металлический стержень из титанового сплава длиной 15-40 см с рабочей частью в виде лопаточек, полуколей и колец. При возбуждении в волноводе продольных ультразвуковых колебаний с частотой 26,5 кГц и амплитудой 35–40 мкм атеросклеротические бляшки разрушаются.
В послеоперационном периоде больные должны постоянно принимать дезагреганты (аспирин 0,25 г в сутки), один раз в шесть месяцев проходить курсы стационарного консервативного лечения. Им рекомендуется рациональное трудоустройство.