
- •1.Функції печінки
- •2. Панкреатичне і кишкове травлення. Роль жовчі в механізмі травлення
- •3.Синтез гема
- •4. Вторинні месенджери та їх роль в механізмах гормонального впливу на клітини-мішені
- •5. Нормальні і патологічні складові сечі
- •6.Катаболізм пуринових нуклеотидів
- •1.Види жовтяниць. Причини виникнення
- •2. Блокування біосинтезу білка дифтерійним токсином (адф-рибозилювання факторів трансляції)
- •3. Джерело енергії для м’язового скорочення. Атф, креатинфорфат. Особливості обміну в серцевому м’язі.
- •4. Всмоктування вуглеводів. Порушення травлення і всмоктування. Недостатність лактази
- •5. Орнітиновий цикл сечоутворення. Послідовність реакцій
- •6. Порушення обміну медіаторів і модуляторів головного мозку при психічних розладах. Нейрохімічні механізми дії психотропних препаратів
- •Розпад гема
- •Паренхіматозна жовтяниця. Причини. Біохімічні показники
- •Молекулярні механізми дії тиреоїдних гормонів.
- •Молекулярні механізми м’язового скорочення та розслаблення м’язів
- •Нейромедіатори. Рецептори для нейромедіаторів та фізіологічно активних сполук
- •Білковосинтезуюча система. Особливості генетичного коду
- •Орнітиновий цикл сечоутворення.
- •Обтураційна жовтяниця
- •Білки плазми крові. Альбуміни. Глобуліни. Фібриноген.
- •Біологічний ефект альдостерону.
- •Особливості метаболізму нервової тканини
- •Значення обміну мінеральних солей.
- •Механізм активації й функціонування каскадної системи згортання крові.
- •Види жовтяниць
- •Молекулярні механізми м’язового скорочення та розслаблення м’язів
- •Енергетичний обмін в головному мозку людини. Значення аеробного окислення глюкози.
- •Мікросомальне окислення і реакції кон’югації в печінці. Компоненти окислення. Роль цитохрома р-450
- •Розпад гема. Жовчні пігменти.
- •Молекулярні механізми м’язового скорочення та розслаблення м’язів
- •Всмоктування вуглеводів. Порушення травлення і всмоктування.
- •Класифікація гормонів: за місцем синтезу, хімічною природою, механізмом дії.
- •Біосинтез піримідинових нуклеотидів
- •Жіночі статеві гормони. Механізм дії
- •Загальна схема біосинтезу днк. Ферменти реплікації днк у прокаріотів та еукаріотів.
- •Розпад гема.
- •Біохімія нейромедіаторів та фізіологічно активних сполук.
- •Роль печінки в обміні білків, жирів та вуглеводів
- •Потреба в ліпідах, роль лейкотрієпів, простагландинів, тромбоксанів. Ліпіди і захворювання.
- •Етапи та механізми трансляції. Ініціація. Елонгація. Термі нація.
- •Гормони гіпофіза
- •2.Технологія трансплантації генів.
- •Дія стероїдних та тиреоїдних гормонів.
- •Дія гормонів білково-пептидної природи та катехоламінів
- •Транспортні рнк. Активація ак, Аміноацил-тРнк-синтетази. Кодони рнк
- •Гормони на обмін кальцію та фосфатів
- •Єдиний нейрогуморальний механізм регуляції
- •Цтк і механізми, що контролюють його у мозку
- •Катаболізм піримідинових нуклеотидів
- •Порушення гомеостазу кальцію
- •Хімічний склад поперечно-смугастих мязів.
- •3. Експресія генів на рівні транскрипції.
- •Гормони підшлункової. Цукровий діабет.
- •Травлення в шлунку.
- •Антибіотики
- •Сполучна тканина
Мікросомальне окислення і реакції кон’югації в печінці. Компоненти окислення. Роль цитохрома р-450
1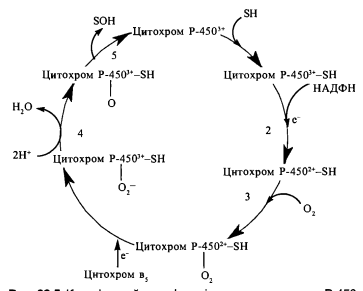 фаза — окислювально-відновлювальні та
гідролітичні реакції, що каталізуються
мембранозв'язаними ферментами
ендоплазматичного ретикулуму гєпатоцитів
("мікро- сомальними ферментами").
У результаті реакцій першої фази у
складі субстратів біотрансформації
утворюються функціональні групи -ОН,
-СООН, -SH, -NH2; таким чином, ці реакції
(функціоналізації, або прекон 'югації)
призводять до збільшення полярності
молекули ксенобіотика або ендогенного
субстрату (наприклад, стероїду).
фаза — окислювально-відновлювальні та
гідролітичні реакції, що каталізуються
мембранозв'язаними ферментами
ендоплазматичного ретикулуму гєпатоцитів
("мікро- сомальними ферментами").
У результаті реакцій першої фази у
складі субстратів біотрансформації
утворюються функціональні групи -ОН,
-СООН, -SH, -NH2; таким чином, ці реакції
(функціоналізації, або прекон 'югації)
призводять до збільшення полярності
молекули ксенобіотика або ендогенного
субстрату (наприклад, стероїду).
2 фаза — реакції синтезу, або кон'югації, що ґрунтуються на приєднанні до молекулярних продуктів 1-ї фази (або вихідних субстратів, що вже мали у своєму складі полярні функціональні групи) залишків глюкуронової, сірчаної кислот, гліцину, глутаміну, глутатіону, метильного або ацетильного радикалів.
1) окислювальне гідроксилування аліфатичних сполук: 1а - алканів та алкенів:
R-CH3 »-R-CH2OH
1 б - алкільних бічних ланцюгів циклічних сполук, наприклад:
С,Н,-СН, ►С,Н,-СН,ОН
2) окислювальне гідроксилування циклічних сполук
3) окислювальне дезалкілування,
4) реакції відновлення
Цитохром Р-450 гемопротеїн залежно від ізоформи, який має спектр поглинання СО-комплексу при 450 нм. виявлено близько 500 ізоформ цитохрому-450, що розрізняються за своєю субстратною специфічністю, особливостями первинної структури та фізико-хімічних властивостей. каталізі реакцій окислювального гідроксилування, що мають місце при синтезі і біотрансформації ендогенних гідрофобних сполук ліпідної природи, а саме - холестерину, фізіологічно активних стероїдів, жовчних кислот та деяких інших природних ліпідів, зокрема метаболізмі ейкозаноїдів.
Реакції кон 'югації в гепатоцитах
Реакції кон'югації з утворенням "парних" сполук - шлях детоксикації більшості ксенобіотиків, що мають функціональні групи -ОН, -СООН, -NH2, -SH. 1. Реакціїглюкуронування (УДФ), УДФ-глюкуронілтрансфераза, 2. Реакції сульфування, донором NH2
сульфатних радикалів у яких є біологічно активна форма сірчаної кислоти - 3'-фосфоаденозин-5'-фосфосульфат (ФАФС). 3. Реакції метилування та ацетилування - поширений тип кон'югації, якому підлягають як ксенобіотики, так і ендогенні субстрати; в цих реакціях беруть участь S-аденозилметіонін (О-метилування) та ацетил-КоА (N-ацетилування): 4. Реакції кон 'югації з гліцином. Поширеною реакцією є утворення гіпурової кислоти при взаємодії ендогенної амінокислоти гліцину із введеною в організм бензойною кислотою:
Розпад гема. Жовчні пігменти.
1. Розрив тетрапірольного кільця гему (у складі гемоглобіну) шляхом окислювального розщеплення метинового містка між І та II кільцями протопорфіринового циклу; в результаті реакції червоний пігмент еритроцитів гемоглобін перетворюється на зелений кров'яний пігмент вердоглобін (холеглобін). Реакція каталізується ферментом НАДФН-залежною гемоксигеназою і
супроводжується виділенням монооксиду вуглецю. Перетворення гемоглобіну на вердоглобін внаслідок окислення гему спричиняє послідовну зміну забарвлення в ділянках гематом, що утворюють "синці"
2. Розпад вердоглобіну з відщепленням білкової частини, вивільненням іона заліза та утворенням тетрапірольної молекули білівердину.
3. Перетворення білівердину на білірубін шляхом відновлення метинового зв'язку між піроламиIII, IV. Реакція каталізується ферментом НАДФН-залежною білівер- динредуктазою
4. Зазначені етапи утворення жовчних пігментів (1-3) відбуваються в клітинах ретикулоендотеліальної системи, з яких білірубін надходить у кров, де адсорбується молекулами сироваткового альбуміну. Комплекс "сироватковий альбумін - білірубін" транспортується в печінку, де пігмент поглинається гепатоцитами і підлягає подальшим перетворенням.
5. Білірубін є ліпідорозчинною речовиною і у високих концентраціях проявляє мембранотоксичність, особливо щодо клітин головного мозку. Детоксикація білірубіну, яка полягає в перетворенні пігменту у водорозчинну (і менш токсичну) форму - глю- куронід білірубіну, відбувається в мембранах ендоплазматичного ретикулуму гепатоцитів. У процесі взаємодії білірубіну з УДФ-глюкуроновою кислотою (УДФГК) утворюються моно- та диглюкуроніди білірубіну: Реакція каталізується УДФ-глюкуронілтрансферазою. Основна частина білірубіну екскретується в жовч у формі диглюкуронідів;
