
- •F 68. Принцип Ферма
- •§ 69. Плоске і сферичне дзеркало
- •§ 70. Повне відбивання
- •§ 71. Лінза. Формула тонкої лінзи. Збільшення лінзи
- •Предмет з відстанівід лінзи наблизили до неї в* від станьОптична сила лінзадатр. На скільки ир« щиту шіатшмлш зображення предмета?
- •Зашийка свічка знаходиться на відстанівід екрана. Де треба помістити збнрву лінзу, щоб дістати 20-кратне збільшення свічки? Якою мав бути оптична сила лінзи?
- •При відстані предмета від лінзивисота зображення
- •§ 72. Побудова зображень у лінзах
- •§ 73. Сферична і хроматична аберація
- •§ 74. Оптичні системи
- •§ 75. Око як оптична система
- •§ 7 В. Дефекти зору. Окуляри
- •§ 77. Світловий потік. Сила світла
- •Як треба змінити час експозиції під час друкування фотографії за допомогою фотозбільшувача при переході від збільшення 6x9 до збільшення 9x12?
- •§ 79. Суб'єктивні і об'єктивні характеристики випромінювання
- •§ 80. Оптичні прилади
- •§ 81. Роздільна здатність оптичних приладів
- •§ 82. Принцип відносності Ейнштейна
- •§ 83. Релятивістський закон додавання швидкостей
- •§ 84. Маса й імпульс в теорії відносності
- •§ 85. Закон взаємозв'язку маси й енергії
- •§ 87. Фотоелектричний ефект і його закони
- •§ 88. Рівняння Ейнштейна. Кванти світла
- •§ 89. Фотоелементи та їх застосування
- •§ 90. Фотон
- •§ 92. Дослід Боте
- •§ 93. Тиск світла
- •§ 94. Хімічна дія світла та її застосування
- •§ 95. Корпускулярно-хвильовий дуалізм
- •§ 95. Корпускулярно-хвильовий дуалізм
- •§ 97. Закономірності в атомному спектрі водню
- •§ 98. Квантові постулати Бора
- •§ 99. Експериментальне підтвердження
- •1 1. У чому полягала ідея досліду Франка і Герца? Який висновок можна було зробити на основі його результатів? 2. Які істотні недоліки теорії Бора?
- •§ 100. Гіпотеза де Бройля. Хвильові властивості електрона
- •§ 101. Корпускулярно-хвильовий дуалізм у природі
- •§ 102. Поняття про квантову механіку. Співвідношення неозначеностей
- •§ 103. Вимушене випромінювання. Лазери та їх застосування
- •§ 104 Поняття про нелінійну оптику
- •§ 105. Склад атомного ядра. Ізотопи. Ядерні сили
- •§ 106. Енергія зв'язку атомних ядер
- •§ 107. Спектр енергетичних станів атомного ядра. Ядерні спектри
- •§ 108. Ефект Мессбауера
- •§ 109. Радіоактивність
- •§ 110. Загадки бета-розпаду. Нейтрино
- •§ 111. Штучна радіоактивність. Позитрон
- •§ 112. Експериментальні методи реєстрації заряджених частинок
- •§ 113. Закон радіоактивного розпаду
- •§ 114. Штучне перетворення атомних ядер. Відкриття нейтрона
- •§ 115. Ядерні реакції
- •Під час бомбардування ізотопу азоту нейтронами одер жується бета-радіоактивний ізотоп вуглецю Записати рівняння обох реакцій.
- •§ 116. Енергетичний вихід ядерних реакцій
- •§ 117. Поділ ядер урану
- •§ 118. Ланцюгова ядерна реакція
- •Що таке коефіцієнт розмноження нейтронів і від чого він залежить?
- •У чому труднощі практичного здійснення ланцюгової ядерної реакції? Які існують шляхи їх подолання?
- •§ 119. Ядерний реактор
- •§ 120. Атомні (ядерні) електростанції
- •§ 121. Термоядерні реакції. Токамак
- •§ 122. Одержання радіоактивних ізотопів
- •§ 123. Використання радіоактивних ізотопів у науці й техніці
- •§ 124. Поглинута доза випромінювання та її біологічна дія. Захист від випромінювань
- •§ 126. Античастинки і антиречовина
- •§ 127. Взаємні перетворення частинок і квантів електромагнітного випромінювання
- •§ 128. Класифікація елементарних частинок
- •§ 129. Кварки
- •§ 130. Типи фізичних взаємодій у природі
- •§ 131. Закони збереження в мікросвіті
- •§ 132. Сучасна фізична картина світу
- •§ 133. Фізика і науково-технічний прогрес
§ 113. Закон радіоактивного розпаду
Альфа-, бета- і гамма-промені випускаються атомними ядрами радіоактивних елементів. Виникає запитання: що ж відбувається з ядром хімічного елемента під час радіоактивного випромінювання?
Для відповіді на це запитання скористаємося законами збереження електричного заряду і маси. Альфа-частинка є ядром атома гелію, її заряд дорівнює 2 елементарним електричним зарядам і масове число дорівнює 4 одиницям. Отже, в результаті вилітання альфа-частинки ядро даного радіоактивного елемента перетворюється в ядро нового хімічного елемента з меншим на дві одиниці зарядом і на чотири одиниці масовим числом. Таким чином, новий елемент міститься в таблиці Менделєєва на дві клітинки ближче до її початку, ніж даний радіоактивний елемент. Наприклад, під час альфа-розпаду радію маємо:
![]()
Тут зліва, внизу, вказані порядкові номери елементів у таблиці Менделєєва, тобто заряди їх ядер, а вгорі — масові числа.
Rn — благородний газ радон. У загальному вигляді схему радіоактивного альфа-розпаду ядер можна записати :
Літерою
X
позначено![]() хімічний
символ ядра, яке розпадається
(часто його називають материнським),
літерою У
— хімічний символ ядра, яке утворюється
(дочірнього).
хімічний
символ ядра, яке розпадається
(часто його називають материнським),
літерою У
— хімічний символ ядра, яке утворюється
(дочірнього).
У
випадку бета-розпаду ядро радіоактивного
елемента самодовільно випускає
електрони
![]() і
перетворюється
і
перетворюється
при цьому в нове атомне ядро, атомний номер якого на одиницю більший (легко зрозуміти, що віднімання від'ємної одиниці означав додавання одиниці), але з тим самим масовим числом А, оскільки маса електрона в 1840 раз менша за масу протона. Таким чином, у результаті бета-розпаду виникає елемент, який розміщується в таблиці Менделєєва в наступній клітинці за даним радіоактивним елементом. Наприклад:
![]()
Схематично рівняння бета-розпаду ядер записується:
Розглянуті
вище![]() правила,
за допомогою яких можна встановити
масове число і заряд нового елемента,
що
правила,
за допомогою яких можна встановити
масове число і заряд нового елемента,
що
виникає внаслідок альфа- або бета-перетворення, дісти... яазву правил зміщення.
Явище гамма-випромінювання ядер полягає у випусканні ядром гамма-кванта без зміни заряду ядра (порядкового номера елемента в таблиці Менделєєва Z) і масового числа А.
Легко зрозуміти, що коли за одним альфа-перетворен-вям відбувається підряд два бета-перетворення, то кінцевий продукт їх повинен повернутися в те саме місце таблиці Менделєєва, де був вихідний елемент, маючи на 4 одиниці менше масове число. Хімічні елементи, які відрізняються масовими числами, але мають один і той самий заряд атомних ядер і тому займають одне й те саме місце в таблиці Менделєєва, називаються ізотопами. З курсу хімії 9-го класу ви знаєте, що ядерні властивості ізотопів одного й того самого елемента різні. Однак їх хімічні властивості майже однакові. Зараз установлено, що більшість елементів у природі є сумішшю ізотопів. Пізніше ви ознайомитесь з методами створення штучних радіоактивних ізотопів, з їх властивостями й використанням.
Досить
часто елемент, який виникає в результаті
радіоактивного перетворення, теж є
радіоактивним. Наприклад, ізотоп
урану![]() в
результаті альфа-розпаду перетворює-
в
результаті альфа-розпаду перетворює-
ться
в ізотоп торію![]() який,
у свою чергу, внаслідок
який,
у свою чергу, внаслідок
альфа-розпаду
перетворюється в ізотоп![]() Радій
в
Радій
в
бета-радіоактивним,
і, випустивши бета-частинку, перетворюється
в ізотоп актинію![]() .
Актиній також бета-радіоактивний
і внаслідок бета-розпаду перетворюється
в
ізотоп торію
.
Актиній також бета-радіоактивний
і внаслідок бета-розпаду перетворюється
в
ізотоп торію![]() і
т. д. Завершується цей ланцюжок
радіоактивних
перетворень утворенням ядра стабільного
(нерадіоактивного)
ізотопу.
і
т. д. Завершується цей ланцюжок
радіоактивних
перетворень утворенням ядра стабільного
(нерадіоактивного)
ізотопу.
На
малюнку 226 приведена схема послідовних
перетворень
ізотопу урану![]() Закінчується
цей радіоактивний
ряд стабільним ізотопом свинцю
Закінчується
цей радіоактивний
ряд стабільним ізотопом свинцю![]() На
схемі в
кружках вказано символ ізотопу, його
масове число й
атомний номер. Літери а
і
р біля стрілок чи над ними вказують
характер радіоактивного перетворення.
Сукупність
усіх ізотопів, які виникають внаслідок
послідовних радіоактивних
перетворень з однієї материнської
речовини (на
схемі такою речовиною є ізотоп урану
На
схемі в
кружках вказано символ ізотопу, його
масове число й
атомний номер. Літери а
і
р біля стрілок чи над ними вказують
характер радіоактивного перетворення.
Сукупність
усіх ізотопів, які виникають внаслідок
послідовних радіоактивних
перетворень з однієї материнської
речовини (на
схемі такою речовиною є ізотоп урану![]() ),
прийнято називати радіоактивним рядом,
або сім'єю. Дослідження показали,
що всі природні радіоактивні елементи
в членами
чотирьох радіоактивних рядів:
),
прийнято називати радіоактивним рядом,
або сім'єю. Дослідження показали,
що всі природні радіоактивні елементи
в членами
чотирьох радіоактивних рядів:
-
ряд
-
ряд
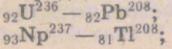
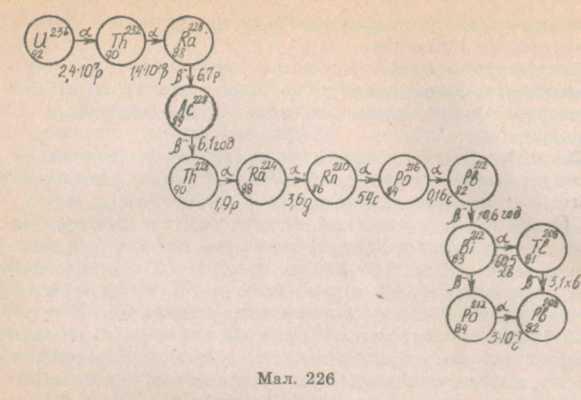
-
ряд
-
ряд

Радіоактивний
альфа- чи бета-розпад веде до неперервного
зменшення числа атомів вихідного
елемента. Для одних
елементів це зменшення відбувається
дуже швидко
— протягом хвилин і навіть секунд, для
інших на це
йдуть сотні років. Мірою швидкості
радіоактивного перетворення
може служити час, за який розпадається
половина
атомів будь-якої кількості елемента.
Цей час називають періодом гаврозпаду
Т.
Наприклад,
період пів-розпаду полонію![]() дорівнює
Т=
140
днів. Значить,
дорівнює
Т=
140
днів. Значить,
від 1 г полонію через 140 днів залишиться 1/2 г. Яка буде швидкість подальшого розпаду? Досліди показали, що вона залишиться незмінною, тобто від 1/2 г полонію залишиться половина, тобто 1/4 г: рівно через 140 днів. Це означає, що 1/16 г полонію, яка залишиться через 560 днів від вихідного грама, не відрізняється абсолютно нічим від 1/16 вихідного грама полонію. Це надзвичайно важливий факт. Він свідчить про те, що розпад не є результатом зміни властивостей ядра (своєрідного ♦старіння»). Властивості радіоактивних ядер з часом не змінюються, ядра не «старіють» у процесі свого існування. Так, наприклад, ядра атома актинію, що виникають при розпаді протактинію, мають однакові шанси зазнати радіоактивного розпаду як відразу ж після свого утворення, так і через добу чи через кілька років після цього. Розпад будь-якого атом-
ного ядра — це, так би мовити, не «смерть від старості», а «нещасний випадок» в його житті.
Розпад того чи іншого ядра в певний момент часу є випадковою подією. Ми не можемо сказати, що станеться саме з даним ядром. Воно може однаковою мірою як розпастися, так і залишитися цілим, незалежно від того, скільки часу воно взагалі існує. Можна лише твердити, що є певна ймовірність розпаду кожного ядра радіоактивного елемента за певний час.
Сформулюємо тепер основний закон радіоактивного розпаду. За одиницю часу з наявної кількості радіоактивних ядер завжди розпадається певна їх частина, яку позначають через к і називають сталою розпаду даного радіоактивного елемента. Якщо є N атомних ядер, то очевидно, що за 1 с розпадається з них WV ядер, а за час dt:
(113.1)
![]()
Знак мінус взято тому, що загальна кількість радіоактивних ядер зменшується у процесі розпаду.
![]()
(113.2)
З курсу математики ви знаєте, що це рівняння легко інтегрується:
де No — початкова кількість ядер атомів даного радіоактивного ізотопу, а N — кількість, ядер, яка збереглася до моменту часу t.
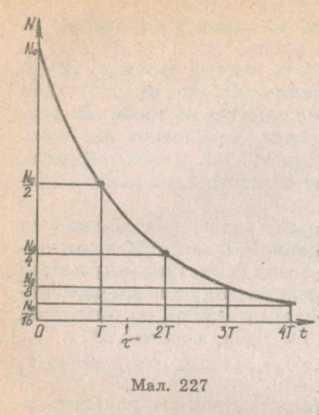
Кількість радіоактивних ядер даного сорту N(t) зменшується з часом за експоненціальним законом (мал. 227). Кількість розпадів за одиницю часу
![]() (113.3)
(113.3)
називають активністю даного препарату. Активність характеризує інтенсивність випромінювання препарату в цілому, а не окремого ядра. Одиниця активності в СІ — б є к-керель (Бк): 1 Бк — активність препарату, при якій за 1 с відбувається 1 розпад. В ядерній фізиці часто застосовується позасистемна одиниця активності — кюрі (Кі): 1 Кі=3,7 10'°Бк.
Важливо підкреслити, що одиниці активності відповідають певній кількості розпадів за секунду, а не певній масі радіоактивної речовини. Так, кюрі приблизно відповідає активності 1 г радію або 3 т урану-238. Чим менший період піврозпаду, тим менша кількість речовини необхідна для одержання одиниці активності.
![]() ,
тобто стала
,
тобто стала
розпаду є відношенням кількості ядер, що розпадаються
за
одну секунду![]() ,
до кількості
ядер атомів радіоактивної
речовини N,
які
містяться в
ній у даний момент часу, або,
іншими словами, ймовірність розпаду
ядер атома радіоактивного елемента
протягом
секунди.
,
до кількості
ядер атомів радіоактивної
речовини N,
які
містяться в
ній у даний момент часу, або,
іншими словами, ймовірність розпаду
ядер атома радіоактивного елемента
протягом
секунди.
Знайдемо
зв'язок сталої розпаду
л з періодом півроз-паду Т.
За
умовою з No
наявних
ядер через час Т
залишається
половина, тобто![]() Отже,,
тобто
Отже,,
тобто![]()
![]() (113.4)
(113.4)
Може
виникнути питання, чому визначається
період піврозпаду, а не час повного
розпаду радіоактивного елемента.
Визначення часу розпаду радіоактивної
речовини позбавлене смислу, оскільки
згідно з формулою (113.2) повний
розпад елемента відбувається за
нескінченно великий
час![]()
На закінчення ще раз звернемо увагу» що радіоактивний розпад є статистичним процесом. Не можна передбачити, коли саме розпадеться те чи інше ядро радіоактивного елемента, але відомо, що в середньому за одиницю часу в будь-якій радіоактивній речовині розпадається цілком певна, характерна для даної радіоактивної речовини частка атомних ядер. Так, з їв1" атомів радію щосекунди розпадається приблизно 14 атомних ядер.
? 1. Що станеться з ядром при випромінюванні альфа-часлпвеи, бета-частинки і гамма-кванта? 2. Записати схему радіоактивного альфа- і бета-розпаду. 3. Які елементи називають ізотопами? 4. Що таке радіоактивний ряд (сім'я)? Навести приклад радкмітшвого ряду. 5. Що розуміють під періодом піврозпаду? Чому не визначають час повного розпаду всіх ядер? в. Чи вірно, що чим довше атом існує, тим більша ймовірність його розпаду?
