
- •1. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- •1.1. Квазистатические процессы
- •1.3. Первое начало термодинамики для системы в адиабатической оболочке
- •1.4. Количество тепла. математическая формулировка первого начала термодинамики
- •1.5.Закон Гесса
- •1.6. Теплоемкость
- •1.7.Внутренняя энергия идеального газа. закон Джоуля
- •1.8. Уравнение Роберта Майера
- •1.9.Адиабатический процесс. Уравнение Пуассона
- •1.10. Определение СР/СV методом Клемана и Дезорма
- •1.11. Скорость звука в газах
- •1.12.Уравнение Бернулли
- •2. II НАЧАЛО ТЕРМОДИНАМИКИ
- •2.1. Различные формулировки основного постулата, выражающего второе начало термодинамики
- •Второе начало термодинамики в формулировках Кельвина и Клаузиуса
- •2.2. Обратимые и необратимые процессы
- •2.3. Цикл Карно и теорема Карно
- •2.3. Термодинамическая шкала температур
- •2.4.Тождественность термодинамической шкалы температур со шкалой идеально-газового термометра
- •2.5. Преобразование теплоты в механическую работу при изотермическом процессе. Вторая теорема Карно
- •2.6. Энтропия
- •2.7. Закон Возрастания Энтропии
- •2.8. Парадокс Гиббса при диффузии газов
- •2.9.Термодинамические функции
- •2.10. Cоотношения Максвелла.
- •2.11.Соотношения между термодинамическими производными. Правила Якобианов
- •2.12. Уравнения Гиббса — Гельмгольца
- •2.13.Максимальная работа и свободная энергия
- •3. УСТОЙЧИВОСТЬ ТЕРМОДИНАМИЧЕСКИХ СИСТЕМ.
- •3.1.Основные критерии устойчивости
- •3.2.Принцип Ле-Шателье — Брауна и устойчивость термодинамического равновесия
- •4. ТЕПЛОПРОВОДНОСТЬ
- •4.1. Уравнение теплопроводности
- •, то (1) можно переписать в виде:
- •4.2.Стационарные задачи на теплопроводность
- •4.3.Температурные волны
- •5. Фазовые переходы
- •5.1. Условия равновесия фаз
- •5.2. Правило фаз Гиббса
- •5.3. Фазовые переходы первого рода
- •5.4. Фазовые переходы второго рода
- •6.Основные положения молекулярно-кинетической теории.
- •6.1.Введение
- •6.3. Молекулярно-кинетический смысл температуры. Теорема о равнораспределение энергии по степеням свободы.
- •6.4. Броуновское движение
- •6.5. Барометрическая формула. Закон Больцмана
- •6.6. Понятие о вероятности
- •6.7. Распределение молекул по скоростям
- •Поскольку вместо r мы используем v, тогда интеграл представим в виде:
- •6.8.Распределение Максвелла. Наиболее вероятная, средняя и среднеквадратичная скорости молекул
- •6.9. Границы применимости классических распределений. Температура вырождения
- •7. ЭНТРОПИЯ И ВЕРОЯТНОСТЬ
- •7.1.Энтропия
- •Плотность функции распределения
- •Свойства плотности функции распределения
- •Можно показать: Плотность вероятности остается постоянной при движении системы по своей фазовой траектории.
- •7.3.Связь энтропии с функцией распределения. Классический случай
- •8. ИДЕАЛЬНЫЕ ГАЗЫ
- •8.1 Распределение Больцмана
- •8.2 Термодинамические функции и уравнение состояния идеального газа
- •8.4 Распределение Ферми-Дирака и Бозе-Энштейна
- •8.5 Вырожденный электронный газ
- •9. Третий закон термодинамики и его следствия
- •9.1.Теорема Нернста
- •10.СВОЙСТВА ЖИДКОСТЕЙ
- •10.1.Введение. Сопоставление газа и жидкости
- •10.2.Изотермы Ван-дер-Ваальса. Критические точки. Фазовые переходы. Правило рычага
- •10.3.Объемные свойства жидкостей
- •10.4.Соотношение между коэффициентами сжимаемости и объемного теплового расширения
- •10.5.Теплоемкость жидкостей
- •10.6. Явления на границе жидкости
- •10.7.Условия равновесия на границе двух сред. Краевой угол
- •10.9.Силы, возникающие на кривой поверхности жидкости
- •10.9.Капиллярные явления

136 Молекулярная физика
то это соотношение можно переписать в виде
(тж + mГ) NM = mжNL + mГNG.
Отсюда |
|
|
|
|
||
|
mж |
= |
NG−NM |
|||
|
mГ |
|
NM −NL |
|||
|
|
|
||||
или |
|
|
|
|
||
|
|
mж |
= |
MG |
||
|
|
mГ |
LM |
|||
|
|
|
||||
Таким образом, точка M делит отрезок LG на части LM и MG, обратно пропорциональные массам жидкости и газа. Этот результат называется правилом рычага.
10.3.Объемные свойства жидкостей
Рассмотрим сначала те свойства жидкостей, которые могут быть изучены |
|
непосредственно из уравнения состояния: сжимаемость и тепловое расширение. |
|
Сжимаемость жидкостей: Коэффициентом сжимаемости χ тела называется |
|
относительное изменение объема dV при изменении давления р на единицу, т. е. величина |
|
χ= 1 dV |
(1) |
V dp |
|
Для идеальных газов
χ=− 1p
так что, например, при р = 1 атм имеем χ = —1 атм-1: при увеличении давления от одной до двух атмосфер объем газа уменьшается вдвое.
У жидкостей, в отличие от газов, сжимаемость очень мала. Это сразу видно из кривой уравнения Ван-дер-Ваальса (рис. 1), на которой жидкому состоянию соответствует участок АВ. Крутизна этого участка свидетельствует о том, что
производная dV dp
незначительного изменения объема требуется очень большое изменение давления.
Опыт показывает, что коэффициент сжимаемости жидкостей в самом деле очень мал и у большинства из них лежит в пределах от 10-4 до 10-6 атм-1. Он, следовательно, в десятки, и сотни тысяч раз меньше, чем в газах. Среди всех жидкостей наибольшей сжимаемостью
обладает жидкий гелий, у которого при давлении в несколько атмосфер коэффициент χ равен 8-10-3 атм-1. Коэффициент сжимаемости воды равен 4,53 10-5, ртути — 3,95 10-6 атм-1.
Коэффициент сжимаемости зависит от давления, уменьшаясь с его ростом. Это вполне естественно, так как по мере того, как жидкость сжимается, уменьшаются расстояния между ее частицами и увеличиваются силы отталкивания между ними. При обычных давлениях сжимаемости различных жидкостей могут сильно отличаться друг от друга, а при очень высоких давлениях коэффициенты сжимаемости всех жидкостей оказываются почти одинаковыми.
Коэффициент сжимаемости жидкости зависит от температуры. Ведь при нагревании

137 |
Молекулярная физика |
вследствие теплового расширения объем жидкости увеличивается и расстояния между молекулами возрастают. Из-за этого силы отталкивания между частицами уменьшаются и сжатие жидкости облегчается. Поэтому коэффициент сжимаемости с повышением температуры возрастает. Описанные особенности явления сжимаемости могут быть получены непосредственно из уравнения Ван-дер-Ваальса. При расчете необходимо только учитывать, что постоянные а и b, входящие в уравнение состояния, на самом деле не являются постоянными, а зависят от температуры (постоянная b зависит, кроме того, от удельного объема вещества), причем вид этой зависимости можно определить только из опыта.
Совокупность опытных данных позволила получить следующую эмпирическую формулу для коэффициента сжимаемости жидкости:
 (2) где А — некоторая функция, возрастающая с температурой, р — внешнее давление и рт — давление, связанное с силами Ван-дер- Ваальса (a/V2) при температуре Т.
(2) где А — некоторая функция, возрастающая с температурой, р — внешнее давление и рт — давление, связанное с силами Ван-дер- Ваальса (a/V2) при температуре Т.
Формула (2) показывает, что коэффициент сжимаемости растет с повышением температуры и уменьшается с ростом давления. Формула (2) является приближенной формулой, пригодной для сравнительно ограниченной области давлений.
Опытное определение сжимаемости жидкости. Приборы и установки, служащие для измерения сжимаемости, называются пьезометрами. Один из простейших пьезометров, пригодный для измерения коэффициента сжимаемости жидкости при не очень больших давлениях, схематически представлен на рис. 2. Исследуемая жидкость заполняет сосуд А так, что она входит и в тонкую трубку (капилляр) а. Последний в свою очередь помещается
в камеру В, в которой может, быть создано повышенное давление, измеряемое манометром М. Так как на стенки сосуда А с жидкостью снаружи и изнутри действует одинаковое давление, то объем сосуда от приложенного внешнего давления не изменяется (об этом необходимо заботиться при измерениях сжимаемости). Под действием приложенного давления объем жидкости в сосуде А несколько уменьшается и это уменьшение становится заметным по понижению уровня в капилляре а. Ввиду малости коэффициента сжимаемости жидкости заметить изменение объема в сосуде без капилляра нельзя было бы. Если площадь
сечения капилляра равна S, а уровень жидкости в нем понизился на величину h, то
изменение объема равно S h. Зная начальный объем жидкости и отсчитав по манометру изменение давления, можно вычислить коэффициент, сжимаемости по формуле (1).
Тепловое расширение жидкости. Тепловое расширение вещества характеризуется коэффициентом объемного расширения
 (3) т. е. относительным изменением объема V при изменении температуры на 1 К.
(3) т. е. относительным изменением объема V при изменении температуры на 1 К.
Для идеальных газов
α=1/Т .
При температуре таяния льда (Т = 273К), следовательно, α = = 1/273 (3,66 10-3 К-1). У жидкостей коэффициент объемного расширения значительно меньше по своему численному значению и несколько слабее зависит от температуры.

138 |
Молекулярная физика |
Ниже приведены значения α для некоторых жидкостей при комнатной температуре. Спирт этиловый α=1,1 10-1 К-1 Ртуть α=1,8 10-4 К-1 Вода (15оС) α=1,5 10-4 К-1 Вода (90оС) α=7 10-4 К-1
Т.о. коэффициент объемного теплового расширения должен уменьшаться с повышением давления и расти с повышением температуры.
10.4.Соотношение между коэффициентами сжимаемости и объемного теплового расширения
Из самых общих соображений, даже не зная вида уравнения состояния вещества, можно установить соотношения между следующими величинами:
1) ( |
∂ V |
)p |
— изменение объема тела, приходящееся на единицу изменения |
∂T |
температуры при постоянном давлении (тепловое расширение);
2) ( |
∂ V |
)T |
— изменение объема тела, приходящееся на единицу изменения |
∂ P |
давления, испытываемого телом при постоянной температуре (сжимаемость);
3) ( |
∂ P |
)V |
— изменение давления, приходящееся на единицу изменения |
∂T |
температуры при постоянном объеме тела (тепловое напряжение).
Что между этими величинами должна существовать связь, ясно из следующих соображений. Если тело, подвергнутое нагреванию, расширяется, т. е. увеличивает свои объем V, то, увеличив внешнее давление р, можно сжать его до первоначального объема.
Значит, одновременным повышением температуры и давления можно сохранить объем постоянным. Легко понять, что увеличение давления, приходящееся на единицу увеличения температуры, потребное для компенсации увеличения объема, вызванного этим изменением температуры, тем больше, чем больше тепловое расширение и чем меньше сжимаемость тела этим условием и определяется связь между указанными тремя величинами.
Чтобы установить эту связь количественно воспользуемся тождеством:
Перепишем это равенство так, чтобы в него входили измеряемые на опыте коэффициент объемного расширения а и коэффициент сжимаемости (изотермический)
(4)
тогда
или
(5)
Это уравнение показывает, что если изменять температуру жидкости (это также
139 |
Молекулярная физика |
справедливо для любого вещества) при неизменном объеме, то изменение давления, вызванное изменением температуры на один градус, равно отношению коэффициентов объемного теплового расширения и сжимаемости.
Если, например, запаянная трубка целиком заполнена ртутью, то при изменении
температуры на 1 К давление изменится на величину р, равную α/χ (коэффициент теплового расширения твердого материала трубки значительно меньше, чем у ртути, так что
изменением объема трубки можно пренебречь). Для ртути α = 1,8 10-4, a χ = -3,9-10-6.
Следовательно, р = 46,5 атм, т. е. при этом возникает весьма значительное давление. Этим, в частности, объясняется, почему нельзя перегревать ртутный термометр
настолько, чтобы ртуть, расширяясь, заполнила весь объем капилляра; при дальнейшем даже незначительном повышении температуры капилляр разрушается.
Из (5) следует, что если известен коэффициент объемного теплового расширения жидкости, то можно определить и коэффициент сжимаемости.
Приборы, предназначенные для измерения коэффициента теплового расширения тел, называются дилатометрами. Самый простой из методов, применяемых в дилатометрии, состоит в следующем. Исследуемую жидкость помещают в сосуд с термометрической трубкой так, чтобы жидкость заполняла и часть трубки. Если с помощью нагревателя, в котором помещен сосуд, повысить температуру жидкости, то уровень ее вследствие
теплового расширения повысится на h. Измерив термометром t изменение температуры t и зная начальный объем Vo жидкости, можно вычислить коэффициент объемного расширения по формуле
α= |
1 |
V |
= |
S |
h |
|
V |
V |
T |
||||
|
T |
|
где S — площадь сечения трубки.
Аномалия воды. Большинство жидкостей, как и других тел, при повышении температуры увеличивает свой объем, уменьшая при этом свою плотность. Вода отличается известной аномалией, состоящей в том, что в области температур от 0°С до 4°С повышение температуры вызывает не повышение, а уменьшение объема, так что при 4°С вода обладает максимальной плотностью.
Эта аномалия объясняется тем, что молекулы воды частично ассоциируют, т. е. собираются в группы из нескольких молекул, образуя своеобразные большие молекулы. По-видимому, вода состоит из трех видов молекул, соответствующих формулам Н2О, (Н2О)2 и (Н2О)3, удельный объем которых различен. При разных температурах соотношение концентраций этих групп молекул различное. Этим и объясняется, что при определенной температуре (4°С) удельный объем воды имеет минимальное значение.
Сходной по характеру аномалией обладает и жидкий гелий, плотность которого максимальна при 2,186 К. Однако здесь аномалия объясняется тем, что при температуре максимума плотности жидкий гелий претерпевает фазовое превращение, так что выше и ниже этой температуры мы имеем две различные фазы жидкого гелия, которые называют Не I и Не II , свойства которых, разительным образом отличаются друг от друга. Интересно отметить, что жидкий гелий — единственная в природе жидкость, в которой происходит фазовый переход.
10.5.Теплоемкость жидкостей
Те простые закономерности, которые были получены для теплоемкостей идеальных газов из уравнений кинетической теории, не могут быть справедливы для жидкостей (как и
140 |
Молекулярная физика |
для реальных газов), так как их внутренняя энергия определяется не только кинетической энергией тепловых движений частиц, но и их потенциальной энергией взаимодействия.
Опыт показывает, что теплоемкость жидкостей зависит от температуры, причем вид зависимости у разных жидкостей различный. У одних (и таких большинство) жидкостей теплоемкость с повышением температуры увеличивается, у других, наоборот, уменьшается (ртуть). У некоторых жидкостей теплоемкость с повышением температуры сначала падает, а затем, пройдя через минимум, начинает расти, Такой именно ход теплоемкости наблюдается у воды (это еще одна из ее многочисленных аномалий).
Как и в газах, у жидкостей следует различать теплоемкость при постоянном объеме и при постоянном давлении. Разность молярных теплоемкостей Ср — Cv равна работе расширения pdV (p — молекулярное давление) моля жидкости при его нагревании на один градус, поэтому численное значение этой разности зависит от значения коэффициента объемного теплового расширения жидкости. В отличие от идеальных газов значение Ср—Cv у жидкостей не равно универсальной постоянной R, а может быть и больше и меньше в зависимости от значения а и от величины внутренних сил взаимодействия частиц жидкости, против которых и совершается работа расширения (давление р в выражении р dV связано именно с этими силами).
Так, например, у жидкого аргона при 140 К теплоемкость Ср = = 15,4 кал/моль-К, a Cv = 4,65 кал /моль -К и, следовательно, разность теплоемкостей Ср — Cv = 10,75 кал/моль К. У воды же при температуре около 0°С теплоемкость Ср = 18,1, a Cv = 18,09 кал/моль К, так что
Ср — Cv = 0,01 кал/моль К.
Таким образом, теплоемкость жидкостей не может быть выражена такими простыми формулами, как теплоемкость идеальных газов. Численные значения теплоемкостей могут быть самыми разнообразными. Исключение составляют жидкие металлы, у которых молярная теплоемкость обычно близка к значению 3R (~6 кал/моль К).
10.6.Явления переноса в жидкостях
В жидкостях, как и в газах, наблюдаются явления диффузии, теплопроводности и вязкости. Но механизм этих процессов в жидкостях иной, чем в газах. Явления переноса в газах определяются длиной свободного пробега молекул. Именно поэтому выражения для всех коэффициентов переноса содержат в качестве множителя длину свободного пробега. Но в жидкостях, как и в очень плотных газах, понятие длины свободного пробега теряет смысл. В жидкостях среднее расстояние между молекулами такого же порядка, как размеры самих молекул, поэтому и «свободного» пробега у молекул нет. Молекулы жидкости могут лишь совершать малые колебания в пределах, ограниченных межмолекулярными расстояниями. Однако время от времени колеблющаяся молекула в результате флуктуации может получить от соседних молекул избыточную энергию, достаточную для того, чтобы совершить скачок на некоторое расстояние δ. В новом месте частица проведет некоторое время, совершая колебания, пока снова не получит, опять в результате флуктуации, нужную для скачка энергию; она вновь совершит скачок, и т. д. Такие колебания, сменяющиеся скачками, — это и есть тепловые движения молекул жидкости.
Как часто происходят молекулярные скачки? Сколько времени проходит между скачками? Это зависит от свойств молекул, от сил взаимодействия между ними, от плотности жидкости. Хотя силы взаимодействия между молекулами имеют очень сложный характер, но все же некоторые соображения о движениях частиц и о связанных с этим явлениях переноса можно высказать.
Для явления диффузии в жидкости, как и в любом веществе, остается справедливым закон Фика:
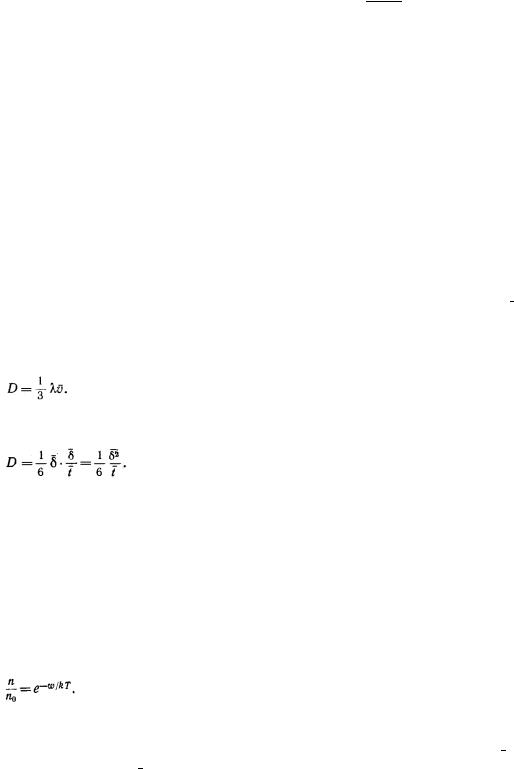
141 |
Молекулярная физика |
|
|
I =−D dq |
(*) |
|
dx |
|
где I —диффузионный поток (более верно плотность потока) интересующего нас компонента в направлении оси X. Плотность потока вещества можно определить как переносимая масс
через единичную площадку в единицу времени: I = dm dS dt
Знак минус в правой части уравнения показывает, что диффузионный поток направлен в сторону убывания концентрации q.
Коэффициент D в уравнении (*) называется коэффициентом диффузии. Смысл его заключается в том, что он численно равен диффузионному потоку при градиенте концентрации, равном 1.
Очевидно, что коэффициент диффузии измеряется в системе СИ в м2/с или в единицах см2/с в системе СГС. Диффузионный поток I измеряется в единицах кг/м2 • с или г/см2 • с; концентрация q измеряется в кг/м3 или г/см3, а градиент концентрации- в кг/м4 или г/см4. Отсюда следует, что
dq dx
измеряется в м2/с или см2/с.
Выражение для коэффициента диффузии D можно получить из следующих соображений. Если время между скачками молекул (его можно назвать временем «оседлой» жизни молекулы) обозначить через t, то величина δ/t представляет собой скорость молекулы. Это позволяет нам сравнить δ со средней длиной свободного пробега, а δ/t со
средней скоростью молекул. Тогда по аналогии с идеальными газами, у которых коэффициент диффузии определяется произведением длины свободного пробега на среднюю скорость молекул
,
мы можем и для жидкости написать, что коэффициент диффузии (точнее — самодиффузии) жидкости выражается равенством
Множитель 1/6 (а не 1/3) здесь появляется потому, что движения молекул носят характер случайных блужданий, для которых существует шесть равновозможных направлений (три оси координат и два направления вдоль каждой из них), так что в некотором избранном направлении движется 1/6 всех молекул.
Коэффициент самодиффузии D сильно зависит от температуры прежде всего потому, что с повышением температуры уменьшается длительность t «оседлой» жизни молекулы, что и приводит к резкому увеличению D с температурой. Длительность пребывания молекулы в данном месте жидкости определяется вероятностью для молекулы получить энергию w, достаточную для скачка. А вероятность эта, как всегда в таких случаях, выражается законом Больцмана:
Здесь n — число молекул в единице объема, энергия которых равна w, а n0 — число молекул в том же объеме, чья энергия порядка средней тепловой, т. е. kT. Чем больше вероятность получения молекулой энергии w, тем меньше будет время «оседлости» t . Поэтому для среднего времени t можно написать выражение:

142 |
Молекулярная физика |
Множитель А имеет ясный физический смысл. Ведь до того, как молекула совершает скачок, она колеблется с некоторой частотой v.' Каждое колебание можно рассматривать как «попытку» молекулы совершить скачок. Поэтому вероятность совершить его тем больше, а время оседлости молекулы тем меньше, чем больше частота колебаний v. Множитель А и связан с этой частотой: А = 1/v. Следовательно, множитель А имеет смысл периода колебаний молекулы.
Если подставить только что написанное выражение для t в формулу для коэффициента диффузии, мы получим:
D= B e−w/(kT )
Здесь |
B= |
1 |
|
ν |
, a w — энергия, необходимая для скачка молекулы, называемая энергией |
δ2 |
|||||
|
|
6 |
|
|
|
активации молекулы.
Численное значение коэффициента диффузии у жидкостей много меньше, чем у газов.. Так, например, коэффициент диффузии NaCl в воде при комнатной температуре равен 1,1 10-9 м2/с, в то время как для диффузии аргона в гелий он равен 7 10-5 м2/с.
Внутреннее трение (вязкость) жидкостей, как и газов, возникает при движении жидкости изза переноса импульса в направлении, перпендикулярном к направлению движения.
Вязкость газов и жидкостей — это свойство, благодаря которому выравниваются скорости движения различных слоев газа и жидкости. Этому свойству мы обязаны, например, тем, что ветер или буря с течением времени утихают. Выравнивание скоростей, соседних слоев газа, если эти скорости различны, происходит потому, что из слоя газа с большей скоростью движения переносится импульс (количество движения) к слою, движущемуся с меньшей скоростью.
Если внешними силами поддерживается постоянной разность скоростей движения различных слоев газа, то и поток импульса от слоя к слою будет постоянным (стационарным), причем этот поток будет направлен вдоль падения скорости. С таким случаем мы, например, встречаемся при медленном течении газа (или жидкости) между двумя пластинами или в трубе под действием постоянной внешней разности давлений, направленной вдоль движения.
Известно, что при течении газа вдоль трубы скорости разных слоев распределены так, как это показано на рис., где стрелки представляют векторы скорости движения газа и жидкости. Наибольшая скорость наблюдается в средней, прилегающей к оси части трубы; по мере приближения к стенкам скорость уменьшается, а слой, непосредственно прилегающий к стенкам трубы, покоится.
При таком течении происходит перенос импульса от центрального слоя газа, где скорость наибольшая, к слоям, движущимся с меньшей скоростью. Так как этот процесс связан с изменением количества движения, то газ ведет себя так, как если бы на него действовала некоторая сила (сила внутреннего трения).
Количественно перенос импульса может быть описан так же, как мы описали перенос энергии в процессе теплопроводности. Пусть изменение скорости движения газа происходит в направлении оси X, которое в данном случае перпендикулярно к направлению самой скорости движения газа (см. рис.).
143 |
Молекулярная физика |
В направлении, перпендикулярном к оси X, скорость движения во всех точках одинакова. Это значит, что скорость v является
функцией только х. Тогда, как показывает опыт, количество движения L, переносимое за 1 с через 1 см2 сечения, перпендикулярного к оси X, определится уравнением
L=− η dvdx
где dv/dx—градиент скорости вдоль оси X, характеризующий быстроту изменения скорости вдоль этой оси. Знак минус означает, что импульс переносится в направлении уменьшения скорости. Коэффициент η называется коэффициентом вязкости или коэффициентом внутреннего трения газа и так же, как коэффициенты диффузии и теплопроводности, зависит от свойств газа. Иногда коэффициент η, определенный этим уравнением, называют коэффициентом динамической вязкости, в отличие от коэффициента кинематической вязкости, равного отношению η /ρ, где ρ —плотность газа Сила эта есть не что иное, как сила трения между слоями газа, или жидкости, движущимися
с различными скоростями. Отсюда и название внутреннее трение. Уравнение можно поэтому записать и в виде
F=−η dvdx
где F —сила, действующая на единицу площади поверхности, разделяющей два соседних слоя газа. Коэффициент вязкости численно равен силе, действующей на единицу площади при градиенте скорости, равном единице.
Внутреннее трение является причиной того, что для протекания газа (или жидкости) через трубу требуется некоторая разность давлений. Чтобы скорость течения имела некоторое данное значение, эта разность давлений должна быть тем больше, чем больше коэффициент внутреннего трения η .
Перенос импульса из одного слоя жидкости в другой осуществляется при скачках молекул, о которых говорилось выше.
Коэффициент же вязкости η может быть получен на основе следующих соображений. Очевидно, что жидкость будет тем более текучей (с тем меньшей вязкостью), чем меньше время t «оседлости»' молекул и значит чем чаще происходят скачки. Эти соображения приводят к выражению для коэффициента вязкости, называемому уравнением Френкеля — Андраде:
η=C e−w/ kT
Множитель С, входящий в это уравнение, зависит от дальности скачка δ, частоты колебаний v и температуры. Однако температурный ход вязкости определяется больцмановским
множителем e−w/ kT . Как следует из этой формулы, с повышением температуры вязкость быстро уменьшается. Так, вязкость воды при изменении температуры от 0°С до 100°С уменьшается от 1,8 10-3 до 2,8 10-4 кг/(м с).
Теплопроводность в жидкостях, как и в газах, имеет место при наличии градиента температуры. Однако, если в газах передача энергии осуществляется при столкновениях частиц, совершающих поступательные движения, то в жидкостях энергия переносится в процессе столкновений колеблющихся частиц. Частицы, имеющие более высокую энергию, совершают колебания с большей амплитудой и при столкновениях с другими частицами как бы раскачивают их, передавая им энергию. Такой механизм передачи энергии, так же как и механизм, действующий в газах, не обеспечивает ее быстрого переноса, и поэтому
