
Nikolls_-_Ot_neyrona_k_mozgu
.pdfГлава 16. Вегетативная (автономная) нервная система |
343 |
Название «автономная» подразумевает независимую систему, которая действует самостоятельно. Отчасти это справедливо. Вегетативная нервная система контролирует кровеносные сосуды, сердце и гладкую мускулатуру кишечника, бронхов, мочевого пузыря и селезенки без участия нашего сознания. Простым усилием воли невозможно увеличить диаметр зрачка либо кровоток в собственном пальце. Можно, конечно, добиться этого обходным путем, используя некоторые уловки: так, волнение, возникающее в результате преднамеренного размышления о предстоящем экзамене, о визите к зубному врачу или о кинозвезде, может усилить частоту сердцебиений.
На практике функционирование вегетативной нервной системы тесно связано с произвольными движениями. Физическая нагрузка приводит к адекватному притоку крови к мышцам и к активации потовых желез; подъем из положения лежа требует такого перераспределения кровоснабжения, которое обеспечивает приток крови к головному мозгу. Потребление пищи перенаправляет кровь к желудку и кишечнику. Включая или выключая активность в повсеместно распределенных группах иннервируемых ею клеток, вегетативная нервная система выполняет работу по поддержанию и обеспечению функций тела. Приоритеты задаются головным мозгом, запускающим процессы пищеварения, размножения, мочеиспускания, дефекации или световой адаптации, которые, однако реализуются механизмами, не контролируемыми на уровне нашего сознания. Ключевыми проблемами, заботящими человечество, являются расстройства вегетативной нервной системы, приводящие к таким явлениям, как астма, кишечная непроходимость, диарея, язвенная болезнь, гипертония, сердечные заболевания, инсульт, задержка мочи (или ее недержание).
Недавние эксперименты и классические работы по вегетативной нервной системе представляют настолько широкую и разнообразную область, что ее всесторонний обзор невозможен в рамках данной главы. На самом деле, целые учебники 1)--3) и специализированные журналы4)--5) посвящены важным функциям вегетативной нервной системы. Имеется большое количество информации, касающейся механизмов, управляющих энтеральной нервной системой и мочевым пузырем, диаметром зрачка, секрецией желез и хромаффинных клеток надпочечников, центральной регуляцией дыхания, температуры, веса тела, аппетита и размножения6)--11). В этой главе, как и в других, основное внимание уделено выборочным примерам, которые иллюстрируют клеточные, молекулярные и интегративные механизмы.
Ниже будет показано, что хотя сейчас уже многое известно о вегетативной нервной системе, остается еще много открытых вопросов, в частности, по поводу интегративных механизмов в структурах, расположенных в ЦНС. Различия между вегетативной и соматической системами недостаточны для того, чтобы четко и строго разграничить их на уровне ЦНС. Поэтому удобнее начать с краткого описания основных свойств периферической вегетативной нервной системы.
§ 1. Непроизвольно управляемые функции
Симпатическая и парасимпатическая нервные системы
Основные анатомические особенности показаны на рис. 16.1. Фактически все органы тела снабжены вегетативной иннервацией. Даже волокна скелетной мускулатуры, которые не получают прямой иннервации, зависят от вегетативной нервной системы; их кровоснабжение регулируется в соответствии с потребностями. Симпатические преганглионарные нейроны расположены в интермедиолатеральном роге спинного мозга в сегментах с Т1 по L3. Их миелинизированные аксоны выходят через вентральные корешки, образуя синапсы в ганглиях, расположенных как рядом с позвоночным столбом, так и на большем удалении (рис. 16.1А). Из этих ганглиев к тканям идут уже немиелинизированные волокна. В противоположность этому, парасимпатический выход ограничен черепномозговыми нервами III, VII, IX и X пар и крестцовыми корешками S2, S3 и S4 (рис. 16.1В). Парасимпатические ганглии расположены вблизи от иннервируемых тканей либо непосредственно в них самих. Следовательно, парасимпатический миелинизированный преганглионарный аксон длинный, тогда как немиелинизированный постганглионарный аксон — короткий. Результаты действия двух систем часто, хотя и не всегда, антагонистичны (табл. 16.1). Например, возбуждение симпатических нейронов приводит к расширению зрачка, повышению сердечного ритма и ослаблению

344 |
Раздел III. Интегративные механизмы |
Рис. 16.1. Вегетативная нервная система и ин нервируемые ею органы-- мишени. (А) Основные особенности симпатической нервной системы, включая паравертебр ль ные ганглии, периферические ганглии и мозговой слой надпочечников. (В) Более ограниченный выход парасимпатической нервной системы и иннервируемые ею органы.
Fig. 16.1. The |
Autonomie |
||
Nervous |
System |
and |
the |
target |
organs |
that |
it |
innervates. |
(A) |
Principal |
||
features |
|
of |
|
the |
sympathetic |
|
nervous |
||
system, |
|
including |
the |
|
paravertebral |
ganglia, |
|||
peripheral |
ganglia, |
and |
||
adrenal |
medulla. |
(B) |
The |
|
more restricted output |
from |
|||
the |
parasym-pathetic |
|||
nervous |
system |
and |
the |
|
targets |
that |
it |
innervates. |
|
Solid lines are myelinated preganglionic axons; dashed lines are un myelinated postganglionic axons.
кишечной моторики. Парасимпатическая активация вызывает противоположные эффекты: сужение зрачка, замедление ритма сердца и усиление моторики кишечника. С другой стороны, секреция желез может быть усилена при активации каждой из этих систем. Обе системы могут вызвать сокращение или расслабление гладких мышц, в зависимости от того, какой медиатор при этом высвобождается, и от того, какого типа рецепторы присутствуют в мышце.
Главное различие между двумя отделами вегетативной системы состоит в том, что симпатическая нервная система имеет тенденцию активироваться как единое целое, вызывая диффузные генерализованные реакции по всему телу. Она характерным образом активируется в условиях испуга, нападения или бегства, а также в процессе интенсивной физической нагрузки. Симптомы хорошо известны: расширенные зрачки, сухость во рту, колотящееся сердце, потение, сильные переживания. Системные эффекты симпатической нейронной активности усиливаются в дальнейшем хромаффинными клетками мозгового слоя надпочечников12). Эти клетки являются видоизмененными ганглионарными нейронами. Хромаффинные клетки получают холинергический вход от преганглионарных аксонов и секретируют адреналин, норадреналин, пептиды и АТФ в качестве гормонов, переносимых током крови. Адреналин, циркулирующий в крови, поддерживает и продлевает симпатическую активность. Адреналин, поступающий из симпатических нервных окончаний, может достигать рецепторов гладкой мускулатуры бронхов и связываться с ними; адреналин также связывается с рецепторами
Глава 16. Вегетативная (автономная) нервная система |
345 |
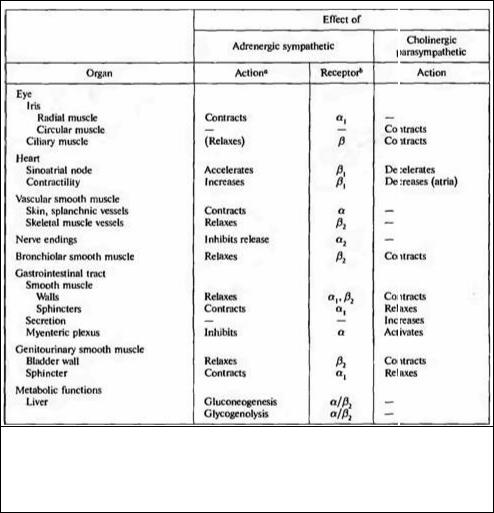
Таблица 16.1. Типичные эффекты адренергической симпатической и холинергической парасимпатической нервных систем.
Table 16.1. Characteristic actions of adrenergic sympathetic and chohnergic parasympathetic nervous systems.
° Accounts of the actions of the autonomie nervous system on target organs listed in this table that are not dealt with in this chapter are given in reviews and textbooks of physiology and pharmacology (see references in text). * Not all the adrenergic receptors or effector cells are included; purinergic, peptidergic, and cholinergic mechanisms are dealt with in the text. Whereas epinephrine acts on all the adrenergic receptors, norepinephrine is effective on α,, α, , and /3, receptors, but not /J2. The various types of adrenergic and muscarinic receptors are characterized by the specific agonists and antagonists that bind to them, and by their molecular structures.
кровеносных сосудов, которые нечувствительны к норадреналину. В отличие от норадреналина, адреналин может вызывать как расширение, так и сокращение кровеносных сосудов.
В противоположность этому, парасимпатическая нервная система является более избирательной в своей деятельности. Есть существенная выгода в том, что зрачок может сокращаться при ярком освещении, а хрусталик глаза — аккомодироваться для рассматривания соседствующих объектов избирательно, без сопутствующих и весьма несвоевременных сокращений мочевого пузыря либо еще менее уместных парасимпатических эффектов.
Синаптическая передача в симпатических ганглиях
Некоторые механизмы синаптической передачи в вегетативной нервной системе уже были описаны в предыдущих главах (10, 12 и 13). Они включают совместное высвобождение
346 |
Раздел III. Интегративные механизмы |
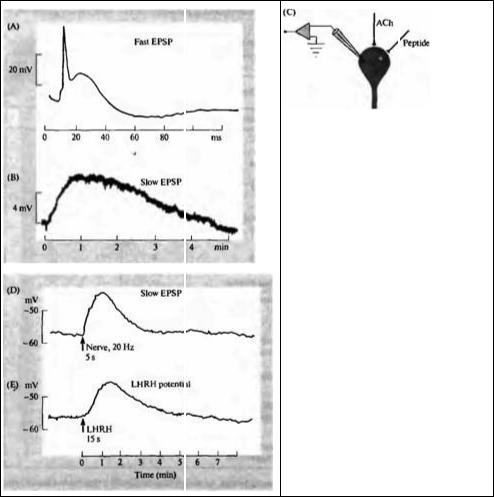
Рис. 16.2. Быстрый и медленный постсинаптические потенциалы в симпатическом ганглии лягушки-быка.
Fig. 16.2. Fast and Slow Synaptic Potentials in Sympathetic Ganglion Cells in a bullfrog. (A) A single stimulus to the preganglionic inputs evokes a large, fast EPSP and an action potential. (B) Trains of stimuli (10/s for 5 s) are required to elicit slow synaptic potentials. Note that the timescale is in minutes instead of milliseconds. (C) Cells in ganglia receive cholinergic and peptidergic inputs, which can be stimulated selectively. (D) Slow excitatory potential evoked by stimulating peptidergic input (20/s for 5 s). As in A, the depolarization lasts several minutes. (E) Application of LHRH to the same neuron by pressure from a micropipette. The peptide mimics the action of the naturally released transmitter.
(After Kuffler, 1980.)
многих медиаторов из нервных окончаний, модулирующее действие вегетативных медиаторов, свойства рецепторов, использующих вторичные посредники, и эффекты ацетилхолина и адреналина на сердечную мышцу. Путь, которым такие механизмы взаимодействуют, чтобы обеспечить сигнализацию, наглядно иллюстрируется экспериментами по изучению синаптической передачи в вегетативных ганглиях.
Вегетативные ганглии представляют собой релейные станции, функциональное значение которых не сразу стало очевидным13). На первый взгляд механизм прямой передачи поразительно сходен с таковым в скелетном нервно-мышечном соединении. Каждый пресинаптический импульс освобождает ацетилхолин, который действует на никотиновые рецепторы постсинаптической клетки, открывая каналы и вызывая быструю деполяризацию (глава 9)14, 15). Как и в нервно--мышечном соединении, одиночный пресинаптический потенциал действия сопровождается аналогичным событием в постсинаптической клетке (рис. 16.2).
Передача в синапсе между преганглионарным аксоном и постсинаптической клеткой, однако, организована значительно сложнее, чем это представлялось по первым результатам. Так, совершенно иная картина возникает при ритмической стимуляции пресинаптических аксонов с частотой, возникающей обыч-
Глава 16. Вегетативная (автономная) нервная система |
347 |
но в живом организме. При этих условиях ганглий уже не является простой передающей станцией, а становится местом сложных взаимодействий. При пачечной активности и продолжительной деполяризации и гиперполяризации в ганглионарных клетках возникают длиннолатентные синаптические потенциалы. Суммируясь, они производят устойчивую подпороговую деполяризацию, сохраняющуюся в течение секунд, минут или даже часов. В процессе деполяризации одиночный пресинаптический потенциал действия может вызвать множественные постсинаптические импульсы. Как быстрые, так и медленные синаптические потенциалы возникают при высвобождении ацетилхолина из пресинаптических нервных окончаний. Как уже упоминалось, быстрый синаптический потенциал является результатом активации никотиновых ацетилхолиновых рецепторов. Медленный потенциал обусловлен активацией мускариновых АХ рецепторов, которые связаны с G-белками (глава 10).
Куффлер и коллеги показали, что в возникновении медленного синаптического потенциала участвует второй передатчик16, 17). Некоторые пресинаптические аксоны высвобождают декапептид, сходный с релизинг-фактором лютеинизирующего гормона (LHRH). (LHRH известен также под названием GnRH, релизинг-фактор гонадотропина; см. рис. 16.9.) Следовательно, в вегетативных ганглиях нейрональная импульсная активность и возбудимость контролируются как АХ, так и LHRH, секретируемыми пресинаптическими нейронами. Сложное взаимодействие между передатчиками и рецепторами наблюдается также в хромаффинных клетках надпочечников. Эти модифицированные ганглионарные клетки
возбуждаются преганглионарными аксонами брыжеечного нерва, который высвобождает АХ и АТФ 18).
Несмотря на кажущуюся сложность, это описание ганглионарной передачи является слишком упрощенным. Интеграция в симпатических и парасимпатических ганглиях модулируется в той или иной степени интернейронами, называемыми SIF-клетками (small intensely fluorescent cells, мелкие интенсивно флюоресцирующие клетки), содержащими катехоламины, а также пресинаптическими окончаниями, которые высвобождают вазоактивный интестинальный пептид (VIP) иэнкефалины19· 20).
М-токи в вегетативных ганглиях
Каков механизм, ответственный за медленную деполяризацию, вызываемую ацетилхолином и LHRH? Этот вопрос был решен Брауном, Адамсом и их коллегами, которые впервые описали необычные калиевые токи, протекающие через «М-каналы» (получившие свое название благодаря взаимодействию с мускариновыми рецепторами)2)--23). М-каналы открываются часто на уровне потенциала покоя, внося существенный вклад в калиевую проводимость в состоянии покоя, и вероятность их открывания возрастает при деполяризации. Активация мускариновых рецепторов приводит к закрыванию каналов (рис. 16.3, 16.4). Вследствие этого нарушается баланс, существующий при потенциале покоя между входом натрия и выходом калия, и клетка деполяризуется.
М-каналы оказывают сильное влияние на синаптические ответы, вызванные АХ24). Одиночный пресинаптический потенциал действия приводит к активации никотиновых рецепторов, вызывая ВПСП, который характеризуется малой длительностью и генерирует не более одного постсинаптического потенциала действия. Длительность ВПСП невелика потому, что синаптическая деполяризация приводит к активации М-каналов, увеличивая таким образом степень реполяризации (см. рис. 16.2). Если при этом активируются также мускариновые рецепторы, то возникающее в результате снижение калиевой проводимости приводит к двум последствиям: во-первых, клетка деполяризуется; во-вторых, существенно возрастает длительность ВПСП, вызванных активацией никотиновых рецепторов. В результате каждый непосредственно вызванный ВПСП остается надпороговым в течение многих миллисекунд и вызывает пачку импульсов (см. рис. 16.4). Возникновение медленных потенциалов, вызванных пептидами, также обусловлено закрыванием М-каналов и оказывает сходное воздействие на синаптическую активность.
После открытия М-каналов в вегетативных ганглиях они были обнаружены также в спинном мозге, гиппокампе и коре головного мозга25). МакКиннон, Браун и коллеги клонировали гены субъединиц, входящих в состав калиевых М-каналов26· 27). Механизм, обеспечивающий закрывание М-каналов, до конца не изучен, хотя показано, что в нем участвует повышение внутриклеточного уровня

348 |
Раздел III. Интегративные механизмы |
Рис. 16.3. Свойства М-каналов, закрывающихся при аппликации мускарина. Пэтч-отведение от клеток нейробластомы в культуре. Мускарин существенно снижает вероятность открывания каналов.
Fig. 16.3. Properties of M-Channels, which are closed by application of muscarine. The records were made by cell-attached patch recording from a transformed neuroblastoma cell in culture that expressed M-receptors and M- chan-nels. When muscarine was applied, the probability of channel opening was drastically decreased. (After Brown et al. 1993.)
кальция, вовлеченное в систему вторичных посредников28) .
М-каналы оказывают решающее влияние на паттерн импульсной активности в вегетативной нервной системе29). В клетках с большим M-током, в частности, в тех, которые ответственны за расширение зрачка, пресинаптический вход не обладает тонической импульсной активностью, и на выходе частота входящих импульсов воспроизводится приблизительно один к одному. Ответы ганглионарных клеток, таким образом, имеют фазный характер, т. е. импульсы в них возникают лишь в случае поступления внешней команды. Напротив, клетки поясничных ганглиев, которые обеспечивают сокращение сосудов, находятся под постоянным активирующим воздействием пресинаптических входов. Это воздействие подавляет М-токи через мускариновые АХ рецепторы. В результате эти клетки проявляют тоническую активность, частота которой зависит от входа, и производят повышение или снижение тонуса сосудов. Эти результаты соответствуют требованиям прерывистого, эпизодического расширения зрачка в случае необходимости, с одной стороны, и поддержанию регуляции диаметра кровеносных сосудов, с другой. Тонические и фазные разряды вызывают и дополнительные эффекты; они определяют, возможно, какой тип передатчика будет высвобождаться терминалями ганглионарной клетки на ее мишени.
§ 2. Синаптичесиая передача от постганглионарных аксонов
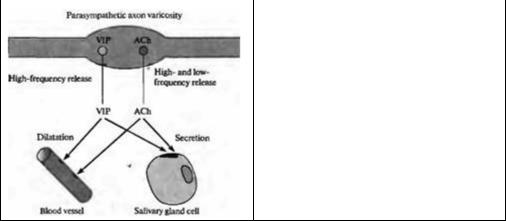
Хотя АХ является основным медиатором, используемым посттанглионарными парасимпатическими аксонами, они одновременно выделяют пептиды (рис. 16.5). Например, АХ, высвобождаемый парасимпатическими аксонами, вызывает секрецию слюнных желез, действуя через мускариновые рецепторы. При высокочастотной стимуляции те же аксоны высвобождают также пептид, называемый вазоактивным интестинальным пептидом (VIP). VIP, изначально открытый в кишечнике и мозге, вызывает вазодилятацию, повышает внутриклеточную концентрацию кальция и усиливает секрецию слюны, причем эти эффекты не блокируются антагонистом мускариновых

Глава 16. Вегетативная (автономная) нервная система |
349 |
Рис. 16.4. Торможение калиевых токов в клетках симпатического ганглия модулирует ответы на пресинаптическое раздражение. (А) АХ и LHRH, действуя через соответствующие рецепторы, оба тормозят M токи калиевых каналов. (В) Результатом снижения М-токов во время медленного синаптического потенциала является повышение возбудимости ганглионарной клетки. Деполяризующие стимулы до и после медленного ВПСП вызывают одиночный ПД, а во время медленного ВПСП — серию ПД. Сходная с медленным ВПСП деполяризация клетки, вызванная инъекцией поддерживающего тока, не вызывает такого эффекта.
Fig. |
16.4. |
Inhibition |
of |
|
|
Potassium |
Currents |
in |
|
||
Sympathetic Ganglion Cells |
|
||||
modulates |
responses |
to |
|
||
presynaptic |
stimulation. |
(A) |
(B) The effect of the decrease in the M-current during the slow synaptic potential is to |
||
Binding |
of |
ACh |
to |
||
muscarinic |
|
receptors |
increase the excitability of the ganglion cell. Depolarizing current pulses applied through |
||
(mAChR) and |
binding |
of |
the microelectrode (lower traces) before and after a slow synaptic potential produce a |
||
LHRH to its receptor both |
single action potential. During the slow potential the same current pulse elicits a burst of |
||||
inhibit |
M-current |
potassium |
action potentials. Depolarizing the ganglion cell (to the same extent as occurs during |
||
channels. |
|
|
|
closure of M-channels) by injecting a maintained current has no such effect on the |
|
|
|
|
responsiveness of the cell. (After Jones and Adams, 1987.) |
||
|
|
|
|
|
|
рецепторов атропином30· 31). Такая передача известна также как неадренергическая и нехолинергическая, или как NANC32).
Основным медиатором для симпатических постганглионарных нейронов является норадреналин. Однако симпатические аксоны, иннервирующие потовые железы и кровеносные сосуды в скелетной мышце, вместо норадреналина секретируют ацетилхолин33). Симпатические нервные волокна также секретируют АТФ и пептиды, высвобождаемые совместно с основными медиаторами. Пространственное распределение некоторых медиаторов, используемых в интестинальных рефлексах, показано на рис. 16.6.
В табл. 16.1 приведены основные области локализации адренергических рецепторов в организме и механизмы их действия. С развитием молекулярной биологии стало ясно, что все адренергические рецепторы, содержащие субъединицы α?, α2, β, и β2, так же как и мускариновые АХ рецепторы, сходны по аминокислотной последовательности. Все эти рецепторы состоят из семи трансмембранных сегментов, связаны с G-белками и используют вторичные посредники (главы 10 и 13).
Пуринергическая передача
В серии выдающихся экспериментов Бернсток и его коллеги открыли и описали один из важных классов симпатических медиаторов, включающих производные пуринов — АТФ и аденозин34). Терминали некоторых симпатических нервных волокон высвобождают АТФ либо как основной медиатор, либо совместно с норадреналином или ацетилхо-
350 |
Раздел III. Интегративные механизмы |
|
|
|
|
|||
|
Рис. |
16.5. |
|
Совместная |
|
передача |
с |
|
|
парасимпатического |
постганглионарного |
нейрона, |
|||||
|
высвобождающего |
наряду |
с |
ацетилхолином |
||||
|
вазоактивный |
интестинальный |
пептид |
|
(VIP). |
|||
|
Парасимпатические |
нервные |
|
волокна, |
||||
|
иннервирующие слюнные железы, секретируют оба |
|||||||
|
медиатора, которые запасаются в разных везикулах. |
|||||||
|
При |
низкочастотной стимуляции |
высвобождается |
|||||
|
только АХ, а при высокочастотной — оба, вызывая и |
|||||||
|
вазодилятацию, и слюноотделение. |
|
|
|
||||
Fig. 16.5. Cotransmission by Parasympathetic Postganglionic Neurons that release both acetylchohne and vasoactive intestinal peptide (VIP). Parasympathetic nerve fibers supplying the salivary gland secrete both transmitters, which are stored in separate vesicles. Stimulation at low frequencies releases acetylchohne but not VIP, while at higher frequencies both transmitters are released, causing vasodilatation and secretion of saliva. (After Burnstock, 1995.)
лином. Эксперименты, в которых было показано, что АТФ является медиатором в симпатической системе, изначально планировались с совершенно иной целью. Бернсток и Холман35) осуществляли внутриклеточное отведение от гладкомышечных волокон репродуктивных органов для изучения синаптической передачи в симпатической нервной системе, медиатором которой в то время считался норадреналин. Отведение ими спонтанных миниатюрных потенциалов представляло важное открытие, поскольку до этого квантовое освобождение наблюдали лишь в нервно-мышечном соединении на скелетной мышце. Позже, однако, Бернсток и его коллеги36) показали, что норадреналин является не единственным медиатором и что симпатические нейроны совместно с норадреналином высвобождают пурин (АТФ) и пептид (нейропептид Y). Миниатюрные потенциалы, обнаруженные в гладкой мышце, были в действительности вызваны не норадреналином, а АТФ, действующим прямо на рецепторы ионных каналов.
Существует два основных семейства пуринергических рецепторов, которые были идентифицированы, секвенированы и клонированы (глава 3). Семейство Р1 включает восемь или более рецепторов, расположенных в пре--и постсинаптических структурах периферии и мозга. Они активируются преимущественно аденозином и сопряжены с G- белками. Хотя передатчиком, высвобождаемым из пресинаптических окончаний, является АТФ, он быстро разрушается ферментами до аденозина, который и является естественным агонистом для Р1 рецепторов. Сам по себе, АТФ действует напрямую на рецепторы37) семейства Р2 в центральной и периферической нервной системе, где он регулирует эндокринную секрецию и сократимость гладкой мускулатуры.
Сенсорные входы вегетативной нервной системы
К приведенному описанию вегетативной нервной системы необходимо добавить два важных компонента: сенсорные входы и рефлекторную регуляцию. На самом деле, в учебниках по физиологии и фармакологии вегетативная нервная система часто рассматривается как чисто моторная система, управляющая гладкой мускулатурой, сердечной мышцей и железами. Одной из причин, по которым вегетативной регуляции не уделяется должного внимания, является недостаточность наших знаний. Механизмы сокращения гладкой мускулатуры, такие как сокращение и расслабление кровеносных сосудов, поступательное перемещение пищи по кишечнику и опорожнение мочевого пузыря, кажутся более простыми, чем, скажем, игра в теннис. В действительности, они требуют весьма сложной интеграции. Со стороны афферентных входов, от сенсорных рецепторов глаза, легких, кровеносных сосудов, внутренностей и других тканей-мишеней постоянно поступает информация о состоянии управляемых органов (рис. 16.6). В число этих рецепторов входят и ноцицепторы, способные передавать ощущение сильной боли.
Простым, на первый взгляд, и хорошо изученным рефлексом является ответ системы кровообращения на изменение положения тела. Когда тело человека находится в горизонтальном положении, мозг снабжается кровью в отсутствие различий кровяного давле-
Глава 16. Вегетативная (автономная) нервная система |
351 |
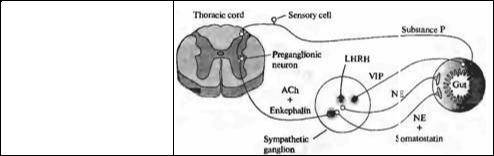
Рис. 16.6. Локализация медиаторов и нейропептидов в нейронах симпатической нервной системы.
Fig. 16.6. Localization of Transmitters and neuropeptides in neurons of the sympathetic nervous system. All known transmitters are found in the intestine. NE = norepinephrine. (After Hukfelt et al., 1980.)
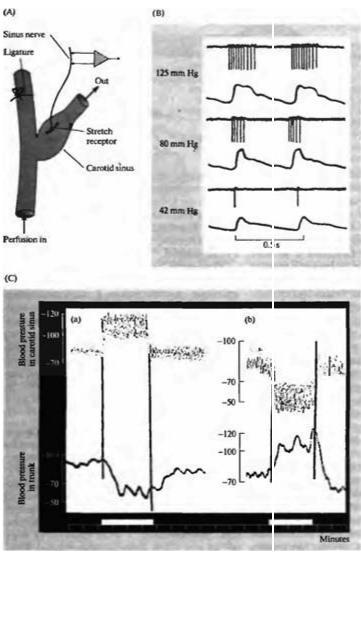
ния между ногами и головой. Переход в вертикальное положение приводит к снижению кровяного давления в участках тела, расположенных выше уровня сердца, и к одновременному накоплению крови в кишечнике и в ногах. При отсутствии автономной регуляции возможна потеря сознания в момент вставания, обусловленная снижением притока крови к мозгу. Рецепторы, которые сигнализируют о необходимости изменения паттерна циркуляции крови, расположены в крупной артерии шеи, называемой сонной артерией. Нервные окончания представляют собой рецепторы растяжения, встроенные в утолщение артериальной стенки, называемое каротидным синусом. Растяжение сосудистой стенки приводит к усилению импульсации, как показано на рис. 16.7.
Сенсорные аксоны направляются в ствол мозга и оканчиваются в строго определенных ядрах (ядра одиночного пучка, или солитарного тракта). Нейроны этих ядер, в свою очередь, проецируются в ретикулярную формацию ствола мозга, откуда осуществляется проекция на преганглионарные нейроны. В горизонтальном положении высокая частота сенсорной импульсации приводит к торможению кардиоваскулярных симпатических выходов (рис. 16.7). Когда человек лежит, его кровяное давление, частота сердечных сокращений и сердечный выброс снижены, а кровеносные сосуды кожи и кишечника расширены. При вставании давление в артерии падает, и частота импульсации в аксонах каротидного синуса резко снижается, снимая центральное торможение. В результате происходит увеличение симпатической активности, приводящее к сужению кровеносных сосудов в коже и кишечнике, а сердечный выброс и частота сердечных сокращений повышаются. Повышение давления поддерживает кровоснабжение мозга. Записи на кимографе (вращающемся закопченном барабане), сделанные несколько десятилетий назад Анрепом и Стерлингом, хорошо иллюстрируют вышеизложенное38). (Это именно тот Стерлинг, который вместе с Бейлисом в 1902 году впервые ввел термин «гормон» и предложил концепцию гормонального воздействия, контролирующего секрецию в кишечнике.)
Описание рефлекса, представленное на рис. 16.7, кажется простым. Однако центральные симпатические и парасимпатические интегративные механизмы перенаправления крови туда, где она срочно необходима, до сих пор неизвестны39). Вышесказанное справедливо и для других вегетативных рефлексов, сенсорные и моторные звенья которых известны, — например, энтеральных, эвакуаторных и респираторных рефлексов40)--42).
Энтеральная нервная система
Местные регуляторные рефлексы в кишечнике (рис. 16.6) в высшей степени сложны и обеспечиваются огромным числом нейронов. Энтеральная нервная система содержит более 10 миллионов нервных клеток, расположенных в стенке кишечника и выполняющих функции сенсорных нейронов, интернейронов и мотонейронов. Все известные медиаторы присутствуют в этой системе (а многие из них были впервые обнаружены в кишечнике). Анализ внутренних рефлекторных цепей существенно затруднен тем, что эти рефлексы очень сложны и включают множество связей43). Функциональный анализ представляет серьезную проблему даже в таких простых системах, как кишечник лангуста. Когда Сельверстон и коллеги44) начинали изучение стоматогастрических ганглиев, состоящих всего из 30 нейронов, то казалось, что им удастся полностью в них разобраться. Однако несмотря на значительные успехи, достигнутые путем электрического отведения от идентифицированных нейронов, и даже на открытие некоторых основополагаю-
352 |
Раздел III. Интегративные механизмы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. |
|
16.7. |
|
|
Разряды |
|||||
|
|
|
рецепторов |
|
растяжения |
||||||||
|
|
|
каротидного |
|
синуса |
|
в |
||||||
|
|
|
ответ |
|
на |
|
повышение |
||||||
|
|
|
кровяного давления. (А) |
||||||||||
|
|
|
Схема |
эксперимента |
для |
||||||||
|
|
|
отведения |
|
активности |
||||||||
|
|
|
чувствительных |
|
волокон |
||||||||
|
|
|
каротидного |
|
|
синуса, |
|||||||
|
|
|
растягиваемого |
|
|
при |
|||||||
|
|
|
естественной |
циркуляции, |
|||||||||
|
|
|
или при перфузии. (В) |
||||||||||
|
|
|
Взаимоотношения |
между |
|||||||||
|
|
|
кровяным |
давлением |
и |
||||||||
|
|
|
импульсацией |
|
|
|
|
в |
|||||
|
|
|
одиночном |
|
|
|
|
|
|
||||
|
|
|
афферентном |
|
волокне. |
||||||||
|
|
|
(С) |
Классическая |
запись |
||||||||
|
|
|
системного |
|
|
кровяного |
|||||||
|
|
|
давления (нижние кривые) |
||||||||||
|
|
|
и |
|
|
экспериментально |
|||||||
|
|
|
изменяемого |
|
давления |
в |
|||||||
|
|
|
сосудах |
|
изолированной |
||||||||
|
|
|
головы, |
|
|
|
снабжаемой |
||||||
|
|
|
кровью другого |
животного |
|||||||||
|
|
|
(верхние |
|
|
|
|
кривые), |
|||||
|
|
|
сделанная |
в |
1924 |
году |
|||||||
|
|
|
с |
помощью |
ртутного |
||||||||
|
|
|
манометра на закопченном |
||||||||||
|
|
|
барабане. |
|
|
|
|
|
|
||||
|
|
|
Fig. 16.7. Firing of Carotid |
||||||||||
|
|
|
Sinus |
|
Stretch |
Receptors |
in |
||||||
|
|
|
response |
|
to |
|
raised |
blood |
|||||
|
|
|
pressure. |
|
(A) |
Experimental |
|||||||
|
|
|
arrangement |
|
for |
recording |
|||||||
|
|
|
from sensory nerve fibers in |
||||||||||
|
|
|
the carotid sinus while it is |
||||||||||
|
|
|
distended |
by |
the |
circulation |
|||||||
|
|
|
or, as in the diagram, |
||||||||||
|
|
|
artificially |
|
perfused. |
|
(B) |
||||||
|
|
|
Relationship |
between |
blood |
||||||||
|
|
|
pressure |
|
(lower |
trace) and |
|||||||
|
|
|
the firing of a single afferent |
||||||||||
|
|
|
fiber from the carotid sinus |
||||||||||
|
|
|
at different levels of mean |
||||||||||
|
|
|
arterial |
pressure |
(from |
top |
|||||||
|
|
|
down: 125, 80, and 45 mm |
||||||||||
|
|
|
of mercury, measured with a |
||||||||||
|
|
|
manometer). (C) A classic |
||||||||||
|
|
|
record made in 1924. The |
||||||||||
(a) Increased pressure in the head caused a fall in systemic blood |
pressure in the trunk |
head |
|
of |
|
this |
animal |
was |
|||||
supplied |
with |
blood |
from a |
||||||||||
of the animal. (b) Decreased pressure in the head caused an |
increase in systemic |
different animal so that blood |
|||||||||||
pressure. Such records were made before electrical recordings were possible; |
pressure in the head arteries |
||||||||||||
experimenters determined blood pressure using a mercury manometer and registered |
could |
|
|
|
be |
|
|
controlled |
|||||
the movements with a fine pointer on a smoked drum. (B redrawn from Neil, 1954; С |
separately |
|
|
by |
|
|
the |
||||||
after Starling, 1941.) |
|
|
experimenters. |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
||||||
щих принципов нейробиологии, полного понимания по-прежнему нет. То, что казалось на первый взгляд простой системой регуляции работы кишечника, оказалось не жесткой и статичной, а пластичной и изменчивой структурой.
