
- •Міністерство освіти і науки України
- •Передмова
- •Робоча програма
- •Приклади виконання завдань
- •Контрольні завдання
- •Основні класи неорганічних сполук основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Термохімія та термохімічні розрахунки основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Ентропія, енергія гіббса та напрямленість процесів основні поняття та визначення
- •Приклади виконання завдань
- •Визначити можливість перебігу реакції
- •Визначити, за якої температури настане рівновага в системі
- •Контрольні завдання
- •Хімічна кінетика основні поняття та визначення
- •Приклади виконання завдань
- •Визначити швидкість реакції
- •Контрольні завдання
- •Хімічна рівновага основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •II модуль розчини. Концентрації розчинів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Властивості розчинів неелектролітів. Основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електролітична дисоціація ступінь та константа дисоціації основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Іонний добуток води. Водневий показник основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Іонна рівновага в гетерогенних системах добуток розчинності основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Реакції в розчинах електролітів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Гідроліз солей основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Колоїдні розчини основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Будова атома основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •III модуль окисно-відновні реакції основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Гальванічні елементи основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Корозія металів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Электроліз розплавів і водних розчинів електролітів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Твердість води основні поняття та визначення
- •Приклади виконання завдань
- •Приклад 2. Визначення маси солі, розчиненої в певному об’ємі води, за величиною твердості води.
- •Контрольні завдання
- •Карбонатна рівновага. Форми існування со2 у воді. Основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Список рекомендованої літератури Основна література
- •Додаткова література
- •Додаток абудова речовини а1.Будова атома
- •А2.Періодична система елементів д. І.Менделєєва та електронна теорія будови атомів
- •Головна підгрупа Побічна група
- •Двох періодів.
- •Відносні електронегативності елементів(за шкалою Полінга)
- •А3. Хімічний зв’язок і будова молекул
- •2 Відштовхування rзв.Е, кДж/моль
- •Елементів д.І.Менделєєва
- •Навчальне видання
Контрольні завдання
81.
Визначити кількість теплоти, яка
виділяється при вибуху 1 л водню та 2 л
хлору (н.у.), якщо теплота утворення
хлороводню становить
![]() кДж/моль.
кДж/моль.
Відповідь: 8,2 кДж.
82.
Визначити кількість теплоти, яка
виділяється, якщо під час реакції
![]() кДж
кДж
прореагує 60 г алюмінію:
Відповідь: 921,1 кДж.
83.Визначити об’єми (н.у.) фосфіну і кисню, необхідних для реакції
![]() кДж,
кДж,
якщо при цьому виділяється 5000 кДж теплоти.
Відповідь: 94,9 л; 189,8 л.
84. Визначити кількість теплоти, яка поглинається при розкладі 1 кг магній карбонату, виходячи з рівняння
![]() кДж.
кДж.
Відповідь: 1207,86 кДж.
85.
При взаємодії азоту з воднем з утворенням
амоніаку виділилось 100 кДж теплоти.
Визначити які об’єми (н.у.) газів
прореагували, якщо теплота утворення
газоподібного амоніаку дорівнює
![]() кДж/моль.
кДж/моль.
Відповідь: 24,2 л; 72,7 л.
86. Визначити теплоту утворення нітроген(II) оксиду, якщо при взаємодії 28 г азоту з киснем за стандартних умов поглинулося 180 кДж теплоти. Записати відповідне термохімічне рівняння.
Відповідь:
![]() кДж/моль.
кДж/моль.
87. Визначити об’єм (н.у.) і масу кисню, необхідного для реакції
![]() кДж,
кДж,
якщо при цьому виділяється 500 кДж теплоти.
Відповідь: 54,1 г; 37,8 л.
88. Визначити теплоту утворення сірководню, якщо при взаємодії водню з 500 г сірки виділилось 314,8 кДж теплоти. Записати термохімічне рівняння процесу.
Відповідь:
![]() кДж/моль.
кДж/моль.
89. Визначити кількість теплоти, яка поглинається при взаємодії 80 л (н.у.) водню з ферум(III) оксидом, якщо термохімічне рівняння має вигляд:
![]() кДж.
кДж.
Відповідь: 115 кДж.
90. Процес відновлення Fe2O3 воднем відбувається за рівнянням:
![]() кДж.
кДж.
Визначити масу заліза, що утворилося під час цієї реакції з поглинанням 1725,2 кДж теплоти.
Відповідь: 2 кг.
91.
При взаємодії водню з киснем з утворенням
рідкої води виділилось 1500 кДж теплоти
(н.у.). Які об’єми газів прореагували?
Теплота утворення рідкої води дорівнює
![]() кДж/моль.
кДж/моль.
Відповідь: 117,55 л; 58,77 л.
92. На основі термохімічного рівняння реакції
![]() кДж
кДж
визначити масу гашеного вапна, яке утворюється при виділенні 1323,65 кДж теплоти.
Відповідь: 1,5 кг
93. Визначити теплоту утворення газоподібного метану СН4(г), якщо при взаємодії з вуглецем прореагувало 40 л водню і при цьому виділилось 66,8 кДж теплоти. Записати відповідне термохімічне рівняння.
Відповідь:
![]() кДж/моль.
кДж/моль.
94. Визначити кількість теплоти, яка виділяється при утворенні 30 г кальцій силікату, виходячи з термохімічного рівняння
![]() кДж.
кДж.
Відповідь: 22,66 кДж.
95. Визначити маси ферум(II) оксиду і карбон(II) оксиду, необхідні для реакції
![]() кДж,
кДж,
якщо при цьому виділяється 5,5 кДж теплоти.
Відповідь: 20,49 г, 7,97 г.
96. Визначити кількість теплоти, яка виділяється при утворенні 3 кг кристалогідрату цинк сульфату, виходячи з термохімічного рівняння:
![]() кДж.
кДж.
Відповідь: 902,9 кДж.
97. Термохімічне рівняння згоряння бензену з утворенням рідкої води має вигляд
![]() кДж.
кДж.
Визначити кількість молів кисню і бензену, при взаємодії яких виділиться 27795 кДж теплоти.
Відповідь: 63,6 молів, 8,5 молів.
98. Визначити кількість грамів фосфору, який згорів у надлишку кисню, якщо при цьому виділилось 746 кДж теплоти.
Відповідь: 30,97 г.
99. Визначити кількість теплоти, яка виділяється при взаємодії трьох молів алюмінію з надлишком сірки, якщо внаслідок реагування 13,49 г алюмінію виділилось 127,2 кДж теплоти.
Відповідь: 763,2 кДж.
100. Визначити об’єми азоту та водню (н.у.), які прореагували з виділенням 184,8 кДж теплоти.
Відповідь: 44,8 л, 134,4 л.
101. Визначити тепловий ефект реакції відновлення ферум(II) оксиду воднем, виходячи з термохімічних рівнянь:

Відповідь: 28 кДж.
102 Визначити тепловий ефект процесу перетворення графіту на алмаз, виходячи з термохімічних рівнянь:
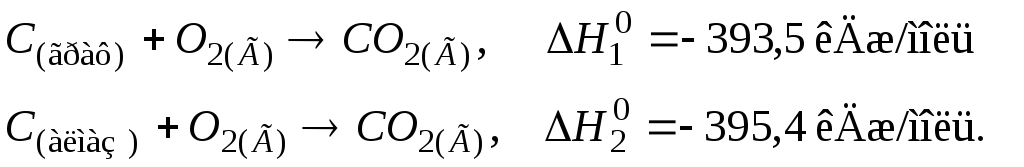
Відповідь: 1,9 кДж.
103. Визначити теплоту утворення кальцій гідроксиду, виходячи з термохімічних рівнянь:
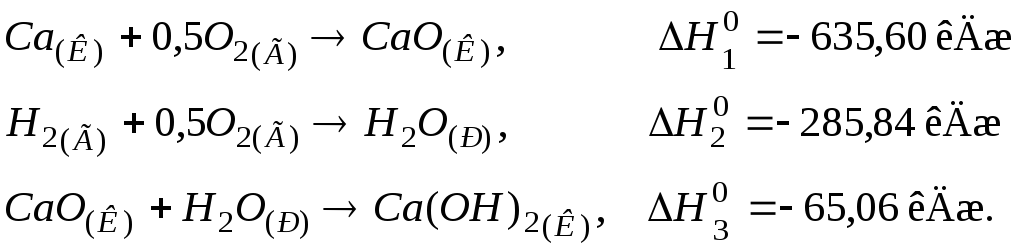
Відповідь: –986,50 кДж/моль.
104. Визначити тепловий ефект реакції відновлення Fe3O4(К)воднем, виходячи з термохімічних рівнянь:
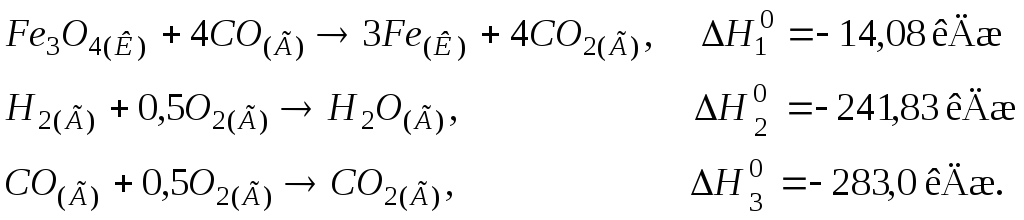
Відповідь: 150,6 кДж.
105. Визначити теплоту утворення етилену С2Н4(Г), виходячи з термохімічних рівнянь:
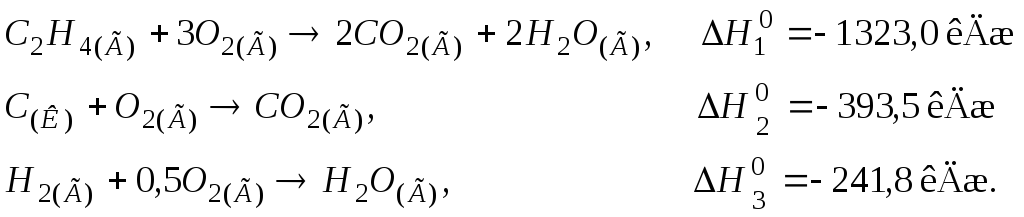
Відповідь: 52,4 кДж/моль.
106. Визначити теплоту утворення NO(Г), виходячи з термохімічних рівнянь:
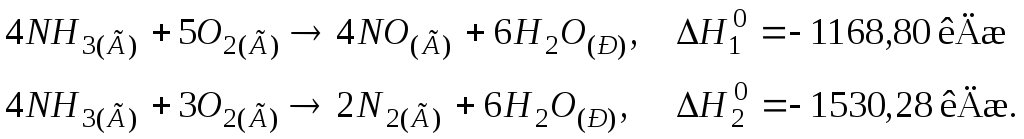
Відповідь: 90,37 кДж/моль.
107. Визначити теплоту утворення вуглекислого газу СО2(Г), виходячи з термохімічних рівнянь:
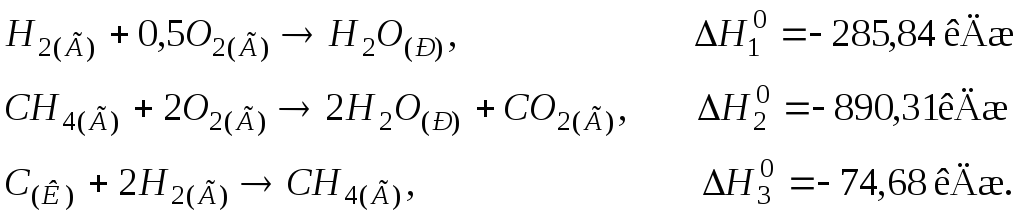
Відповідь: –393,31 кДж/моль.
108. Визначити теплоту утворення Н2О(Р), виходячи з термохімічних рівнянь:
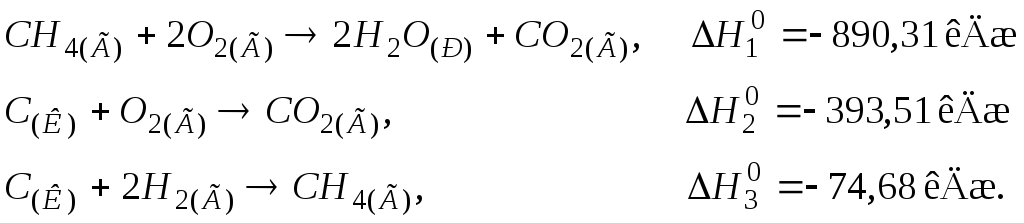
Відповідь: –285,8 кДж/моль.
109. Визначити теплоту утворення ферум(II) оксиду FeO(К), виходячи з термохімічних рівнянь:
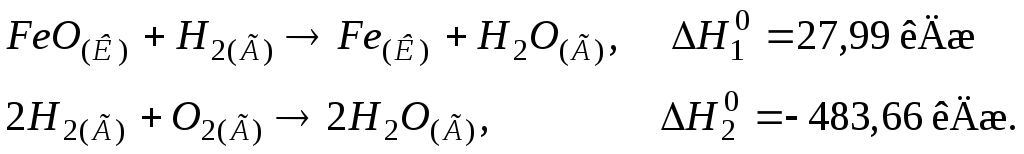
Відповідь: –269,82 кДж/моль.
110. Визначити теплоту утворення етану С2Н6(Г), виходячи з термохімічних рівнянь:
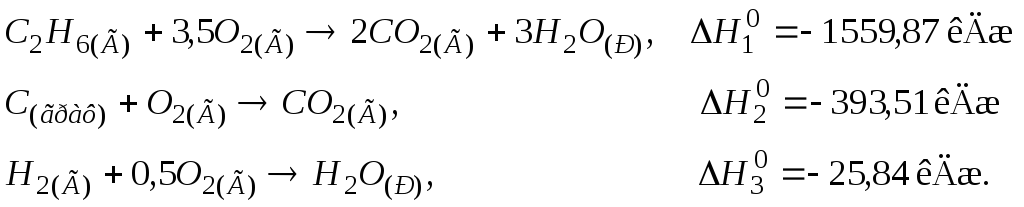
Відповідь: –84,67 кДж/моль.
111. Визначити теплоту утворення N2O(Г), виходячи з термохімічних рівнянь:

Відповідь: 82 кДж/моль.
112. Скільки треба витратити теплоти, щоб розкласти 200 г Na2CO3 до натрій
оксиду та вуглекислого газу, якщо теплові ефекти реакцій дорівнюють:
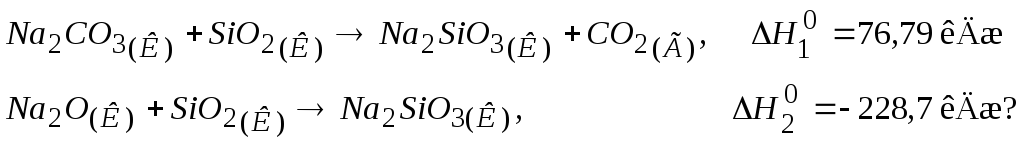
Відповідь: 576,4 кДж.
113. Розрахувати тепловий ефект реакції утворення цинк сульфату ZnSO4(К) шляхом окиснення цинк сульфіду ZnS(К), виходячи з термохімічних рівнянь:
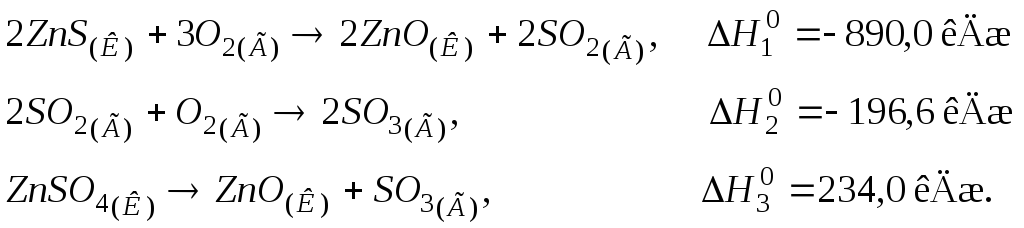
Відповідь: 777,3 кДж.
114. Визначити кількість теплоти, що виділяється під час взаємодії 50 г фосфорного ангідриду Р2О5(К)з водою за реакцією
![]() ,
,
якщо відомі теплові ефекти реакцій:
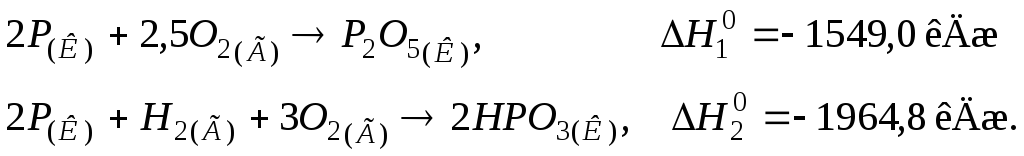
Відповідь: –146,41 кДж
115. Визначити стандартну теплоту утворення етилового спирту С2Н5ОН(Р), виходячи з термохімічних рівнянь:
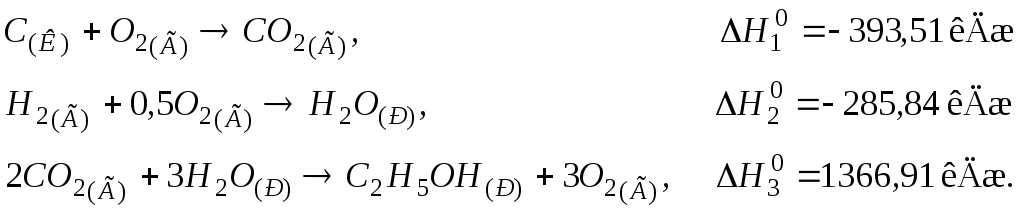
Відповідь: –277,63 кДж/моль.
116. Визначити стандартну теплоту утворення Fe2O3(К), виходячи з термохімічних рівнянь:
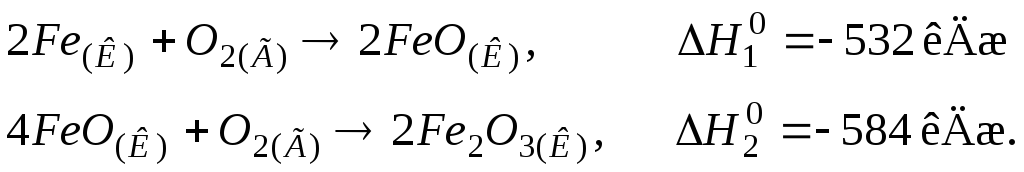
Відповідь: –824 кДж/моль.
117. Визначити стандартну теплоту утворення MgCO3(К), виходячи з термохімічних рівнянь:
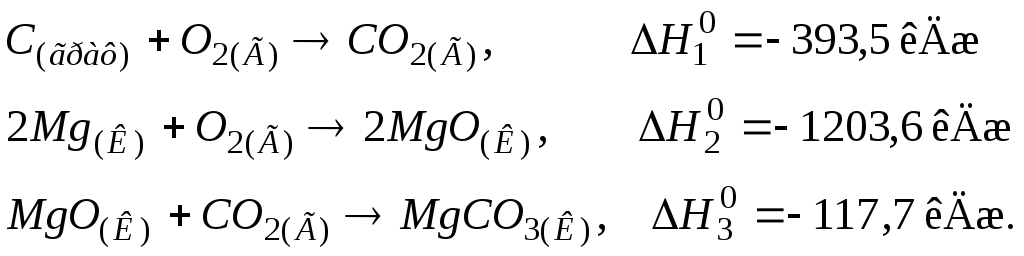
Відповідь: –1113 кДж/моль.
118. Розрахувати тепловий
ефект реакції
![]() ,
,
виходячи з термохімічних рівнянь:
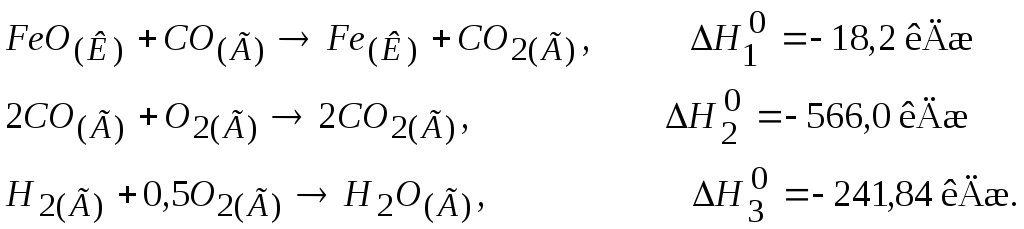
Відповідь: 22,96 кДж/моль.
119. Визначити тепловий ефект реакцій горіння метану СН4(Г)з утворенням вуглекислого газу СО2(Г)та води Н2О(Г)за такими даними:

Відповідь: –802,28 кДж.
120. Визначити стандартну теплоту утворення амоніаку NH3(Г), виходячи з термохімічних рівнянь:
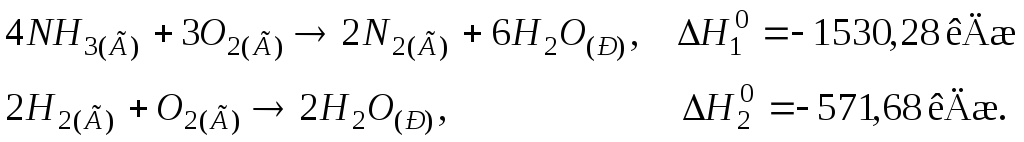
Відповідь: –46,19 кДж/моль.
121. Теплота утворення кальцій гідроксиду з оксидів СаО(Т) та Н2О(Р) становить –65,1 кДж/моль. Визначити стандартну теплоту утворення кальцій оксиду, виходячи з термохімічного рівняння
![]()
Відповідь: -635,6 кДж/моль.
122. Визначити тепловий ефект реакції
![]()
за відомими величинами стандартних теплот утворення вихідних речовин та продуктів реакції.
Відповідь: 233,2 кДж
123. Визначити стандартну теплоту утворення фосфіну РН3, використовуючи термохімічне рівняння
![]() ,
,
якщо відомі стандартні теплоти утворення Р2О5(Т) і Н2О(Р).
Відповідь: 5,3 кДж/моль.
124. Визначити тепловий ефект реакції
![]()
за відомими величинами стандартних теплот утворення вихідних речовин та продуктів реакції.
Відповідь: -115,5 кДж.
125. Визначити тепловий ефект реакції
![]()
за відомими величинами стандартних теплот утворення вихідних речовин та продуктів реакції.
Відповідь: -853,7 кДж.
126. Визначити тепловий ефект реакції за відомими величинами стандартних теплот утворення вихідних речовин та продуктів реакції
![]()
Відповідь: -566 кДж
127. Визначити тепловий ефект реакції за відомими величинами стандартних теплот утворення вихідних речовин та продуктів реакції
![]()
Відповідь: -198 кДж
128. Знайти стандартну теплоту утворення CaSiO3(Т), використовуючи стандартні теплоти утворення SiO2(Т), СаО(Т) і тепловий ефект реакції
![]()
Відповідь: -1579,0 кДж/моль.
129. Використовуючи термохімічне рівняння
![]() ,
,
розрахувати стандартну теплоту утворення СаО, якщо відомі стандартні теплоти утворення SiO2(Т) і CaSiO3(Т).
Відповідь: -635,1 кДж/моль.
130. Визначити стандартну теплоту утворення SiO2(Т), використовуючи термохімічне рівняння
![]() ,
,
якщо відомі стандартні теплоти утворення CaO(Т) і CaSiO3(Т).
Відповідь: -859,3 кДж/моль.
131. Використовуючи термохімічне рівняння
![]() ,
,
розрахувати стандартну теплоту утворення СО, якщо відомі стандартні теплоти утворення Fe2O3(Т) і CO2(Г)
Відповідь: -110,5 кДж/моль.
132. Використовуючи термохімічне рівняння
![]() ,
,
розрахувати стандартну теплоту утворення СО2(г), якщо відомі стандартні теплоти утворення СО(Г) і Fe2O3(Т).
Відповідь: -393,51 кДж/моль
133. Використовуючи термохімічне рівняння
![]() ,
,
розрахувати стандартну теплоту утворення Fe2O3(Т), якщо відомі стандартні теплоти утворення СО(Г) і СО2(Г).
Відповідь: -821,32 кДж/моль.
134. Визначити тепловий ефект гасіння вапна водою при 250С, якщо відомі величини стандартних теплот утворення вихідних речовин та продуктів реакції.
Відповідь: -65,1 кДж.
135. Знайти стандартну теплоту утворення Na2CO3, використовуючи термохімічне рівняння
![]() ,
,
якщо відомі стандартні теплоти утворення SiO2(Т), Na2SiO3(Т) і СО2(Г).
Відповідь: -1129,0 кДж/моль.
136. Визначити стандартну теплоту утворення NH4Cl(Т) використовуючи термохімічне рівняння
![]()
якщо відомі стандартні теплоти утворення NH3(Г) і HСl(Г).
Відповідь: -315,39 кДж/моль.
137. Визначити тепловий ефект реакції розкладу MgCO3
![]()
за величинами стандартних теплот утворення MgCO3(Т), MgO(Т) і СО2(Г).
Відповідь: 100,9 кДж.
138. Визначити стандартну теплоту утворення MgCO3, використовуючи термохімічне рівняння
![]() ,
,
якщо відомі стандартні теплоти утворення MgO(m) і CO2(г).
Відповідь: -1096 кДж/моль.
139. Знайти тепловий ефект реакції
![]()
за відомими величинами стандартних теплот утворення вихідних речовин та продуктів реакції.
Відповідь: 490,54 кДж.
140. Визначити стандартну теплоту утворення пентахлориду фосфору, використовуючи термохімічне рівняння
![]()
якщо відома стандартна теплота утворення РСl3.
Відповідь: -374,9 кДж/моль.
